Первичный колоректальный анастомоз при субкомпенсированном и декомпенсированном обтурирующем раке дистальных отделов толстой кишки: альтернатива абдоминальной колостомии, риск несостоятельности, непосредственные результаты
Автор: Соляников А.С., Захарченко А.А., Винник Ю.С.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 6 (40), 2014 года.
Бесплатный доступ
В статье представлены результаты хирургического лечения 121 пациента с обтурационной толстокишечной непроходимостью (ОТкН) на фоне обтурирующего рака дистальных отделов толстой кишки (Тк) II и III стадии.
Рак толстой кишки, кишечная непроходимость, хирургическое лечение, интраоперационная декомпрессия, первичный колоректальный анастомоз
Короткий адрес: https://sciup.org/142211189
IDR: 142211189 | УДК: 616.24-616.36:006.6-07-08
Текст научной статьи Первичный колоректальный анастомоз при субкомпенсированном и декомпенсированном обтурирующем раке дистальных отделов толстой кишки: альтернатива абдоминальной колостомии, риск несостоятельности, непосредственные результаты
До 40% больных раком толстой кишки поступают в стационары по срочным и экстренным показаниям с клиническими явлениями субкомпенсированной и декомпенсированной обтурационной толстокишечной непроходимости (ОТКН) [2].
Одной из актуальных задач современной абдоминальной хирургии, в том числе и онкологической колопрок-тологии, является улучшение качества жизни пациентов, определяющееся возможностью выполнения сфинктеро- и функционально-сохраняющих операций на толстой кишке (без абдоминальной колостомии) не в ущерб онкологическому радикализму [4].
Основной проблемой при этом является несостоятельность швов толстокишечных анастомозов [5]. Проблема значительно усугубляется у пациентов с резекциями дистальных отделов толстой кишки (ТК), выполняемых по поводу суб- и декомпенсированной ОТКН по срочным и экстренным показаниям, когда ведущими причинами этого грозного осложнения становятся: повышение внутрибрюш- ного давления (ВБД), синдром интраабдоминальной гипертензии (СИАГ), раковая интоксикация, прогрессирующий парез кишечника, эндотоксикоз, биологическая проницаемость анастомоза и т.д. [1, 3].
К настоящему времени существует 4 вида хирургических вмешательств при обтурирующем раке дистальных отделов толстой кишки: 1 – реканализация опухолевого стеноза; 2 – формирование проксимальной разгрузочной колосто-мы; 3 – обструктивная резекция толстой кишки с формированием колостомы (операции Гартмана и типа Гартмана); 4 – резекция толстой кишки с формированием первичного колоректального анастомоза (КРА).
Первые два вида операций относятся к паллиативным (симптоматическим) вмешательствам и направлены на купирование таких осложнений ОТКН, как повышение ВБД и СИАГ, пареза кишечника и эндотоксикоза, что позволяет после их купирования выполнить резекцию толстой кишки с опухолью в плановом порядке с возможностью формирования КРА (второй этап хирургического лечения).
Третий вид вмешательств на первом этапе предполагает удаление опухоли, устранение раковой интоксикации и снижение риска других вышеописанных осложнений ОТКН. При этом варианте хирургического лечения реабилитация пациента возможна на втором этапе (реконструктивновосстановительная операция).
Наиболее интересным для хирурга и мотивированным для больного вариантом лечения обтурирующего рака дистальных отделов ТК является четвертый вид хирургических вмешательств (одноэтапный). Однако до сих пор окончательно не решен вопрос о возможности формирования первичных толстокишечных анастомозов с минимальным риском их несостоятельности в срочных и экстренных ситуациях.
С целью профилактики несостоятельности швов кишечных анастомозов (в т.ч. и первичных) предложены различные технологии и средства, такие как укрепление кишечных швов фибрин-коллагеновой субстанцией «ТахоКомб», применение аутофибринового клея, биоклея «ЛАБ», интубационная декомпрессия, декомпрессионный санационый лаваж толстой кишки и др. [1].
Нами разработан и используется в клинике (с 1999 г.) метод профилактики несостоятельности первичных колоректальных анастомозов в условиях ОТКН на фоне обтурирующего рака дистальных отделов толстой кишки [4, 6, 7].
Цель исследования
Определить возможность первичной хирургической реабилитации больных при обтурационной толстокишечной непроходимости (ОТКН), обусловленной опухолевым стенозом дистальных отделов толстой кишки (ТК) и оценить течение раннего послеоперационного периода при формировании первичного бесшовного позадипрямокишечного (ППК) колоректального анастомоза (КРА).
Пациенты и методы
Анализированы результаты хирургического лечения 121 пациента с ОТКН на фоне обтурирующего рака дистальных отделов ТК (сигмовидная кишка, средний и в/ампулярный отдел ПК) II (T3–4 N0M0) и III (T3–4 N1–2M0) стадии.
Мужчин было в 1,5 раза больше, чем женщин. Средний возраст составил 56,0±4,1 года. Субкомпенсированная ОТКН имела место у 88 (72,7%) больных, декомпенсированная – у 33 (27,3%). Сроки непроходимости: субкомпенси-рованной – 4,2±0,8 месяца, декомпенсированной – 1,9±0,7 суток. У всех больных, после обструктивного этапа и проведения интраоперационной декомпрессии ТК, сформированы первичные КРА. Клиническая характеристика пациентов представлена в таблице 1.
В зависимости от характера декомпрессии и вида анастомоза пациенты разделены на 3 группы. В группе клинического сравнения (ГКС, n=35) проводили интраоперационный лаваж ТК гиперосмолярным раствором NaCl (450 осмоль/л) и формировали прямой КРА однорядным непрерывным швом викрилом № 3/0 с протекцией ТахоКомбом. В исследуемой группе 1 (ИГ 1, n=31) – мануальная декомпрессия ТК и бесшовный ППК КРА с избытком низведенной ободочной кишки. В исследуемой группе 2 (ИГ 2, n=55) – интраоперационный лаваж ТК (аналогично, как в ГКС) и бесшовный ППК КРА (как в ИГ 1).
Предоперационная подготовка включала проведение соответствующей корригирующей терапии волемических, электролитных и белковых нарушений, сопутствующих заболеваний, коррекцию анемии. При наличии явлений субкомпенсированной обтурационной толстокишечной непроходимости (72,7% случаев) в предоперационном периоде подготовку толстой кишки к операции (механическая очистка) проводили традиционным способом: бесшлако-вая диета, прием слабительных средств, очистительные клизмы. В остальных случаях (27,3%), при декомпенсированной непроходимости проведение механической очистки – нецелесообразно. Оперировали больных, в первом случае по срочным показаниям (через 3–4 суток с момента госпитализации), во втором – через 4–6 часов после проведения интенсивной инфузионной терапии, направленной на нивелирование явлений гиповолемии, электролитных, белковых нарушений и эндотоксикоза.
Обследование пациентов включало: сбор жалоб, уточнение анамнеза, физикальное обследование, оценку тяжести состояния больного по шкале ECOG. Лабораторный метод предусматривал рутинные исследования унифицированными методами: общего анализа крови и мочи, определение группы крови, Rh-фактора, уровня общего белка, мочевины, креатинина, билирубина, глюкозы крови, электролитов, исследование крови на RW, ВИЧ, гепатиты, показателей коагулограммы (АЧТВ, МНО, содержание фибриногена, ВСК).
Таблица 1
Клиническая характеристика пациентов (n=121)
|
Группы сравнения |
ГКС (n = 35) |
ИГ 1 (n = 31) |
ИГ 2 (n = 55) |
|||
|
кол-во |
% |
кол-во |
% |
кол-во |
% |
|
|
Стадия заболевания |
||||||
|
T3-4N0M0 (II стадия) |
13 |
37,1 (1) |
12 |
38,7 (2) |
21 |
38,2 (3) |
|
T3-4N1-2M0 (III стадия) |
22 |
62,9 (1) |
19 |
61,3 (2) |
34 |
61,8 (3) |
|
Локализация опухоли |
||||||
|
Сигмовидная кишка |
12 |
34,3 (1) |
11 |
35,5 (2) |
19 |
34,5 (3) |
|
Верхнеампулярный отдел прямой кишки |
15 |
42,8 (1) |
13 |
41,9 (2) |
23 |
41,8 (3) |
|
Среднеампулярный отдел прямой кишки |
8 |
22,9 (1) |
7 |
22,6 (2) |
13 |
23,7 (3) |
|
Стадия толстокишечной непроходимости |
||||||
|
Субкомпенсированная |
25 |
71,4 (1) |
23 |
74,2 (2) |
40 |
72,7 (3) |
|
Декомпенсированная |
10 |
28,6 (1) |
8 |
25,8 (2) |
15 |
27,3 (3) |
|
Показатели ВБД и степень СИАГ |
||||||
|
Субкомпенсированная толстокишечная непроходимость |
ВБД (мм рт. ст.) 12,4±1,3 (1) СИАГ – I степень 25 (71,4%) (1) |
ВБД (мм рт. ст.) 12,8±1,2 (2) СИАГ – I степень 23 (74,2%) (2) |
ВБД (мм рт. ст.) 13,7±1,5 (3) СИАГ – I степень 40 (72,7%) (3) |
|||
|
Декоменсированная толстокишечная непроходимость |
ВБД (мм рт. ст.) 16,7±1,4 (1) СИАГ – II степень 6 (17,1%) (1) |
ВБД (мм рт. ст.) 16,4±1,1 (2) СИАГ – II степень 5 (16,1%) (2) |
ВБД (мм рт. ст.) 17,6±1,3 (3) СИАГ – II степень 9 (16,4%) (3) |
|||
|
ВБД (мм рт. ст.) 21,9±1,8 (1) СИАГ – III степень 4 (11,4%) (1) |
ВБД (мм рт. ст.) 22,8±1,9 (2) СИАГ – III степень 3 (9,7%) (2) |
ВБД (мм рт. ст.) 23,4±2,4 (3) СИАГ – III степень 6 (10,9%) (3) |
||||
Примечание: - недостоверные различия показателей между ГКС, ИГ 1, ИГ 2, p 1, 2, 3 > 0,05.
Инструментальные методы: эндоскопические исследования прямой и сигмовидной кишки осуществляли при помощи ректосигмоидоскопа или фиброколоноскопа. По данным эндоскопии предварительно определяли локализацию, протяженность опухолевого процесса, степень обтурации просвета кишки, предварительно оценивали стадию заболевания, выполняли биопсию.
Техника вмешательств. Интубационный наркоз + пери-дуральная анестезия. Срединная лапаротомия. Сигмовидную кишку и мезоколон и/или прямую кишку и мезоректум (по технологии ТМЭ) чрезбрюшинно наданально мобилизовали, резецировали.
Интраоперационную декомпрессию ободочной кишки проводили по трем методикам. Пациентам в группе клинического сравнения (ГКС) (n=24/35; 68,6%) и в исследуемой гуппе (ИГ) 2 (n=38/55; 69,1%) – антеградный лаваж ОК гиперосмолярным раствором через аппендикостому. Дистальный конец ободочной кишки (ОК) интубировали трубчатым дренажом в замкнутый контейнер (рис. 1а).
У больных, которым ранее была выполнена аппендэктомия, соответсвенно в ГКС (n=11/35; 31,4%) и в ИГ 2 (n=17/55; 30,9%), дистальные отделы ОК интубировали двухпросвет-
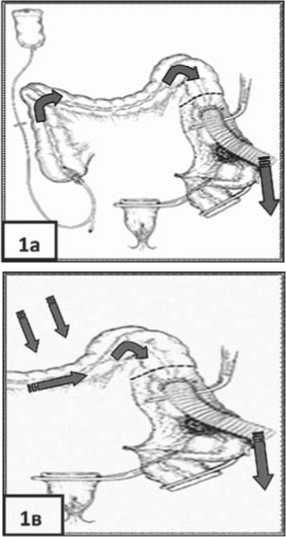
Рис. 1. Схемы интраоперационной декомпрессии ободочной кишки: а – антеградный лаваж ОК через аппендикостому, б – ретроградный лаваж ОК, в – мануальная декомпрессия
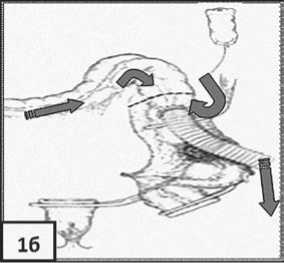
ным трубчатым дренажом и проводили ретроградный лаваж (рис. 1б). В ИГ 1 (n=31/31; 100%) – мануальная декомпрессия ОК через трубчатый дренаж в замкнутый контейнер (рис. 1в). Вышележащие (левые) отделы ободочной кишки после декомпрессии мобилизовали (колотрансплантат).
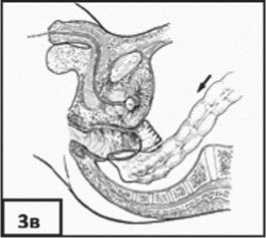
У пациентов всех групп культю прямой кишки (нижнеампулярный отдел) ушивали наглухо, ретроградно санировали. Позади культи в процессе мобилизации ПК по технологии ТМЭ формировался «тоннель» (рис. 2а). Транс-анально в культе (по задней стенке) на 2–3 см выше зубчатой линии создавали отверстие (адекватного диаметра) для низведения на промежность мобилизованных левых отделов ОК (рис. 2б). Через это отверстие и культю ПК коло-трансплантат низводили на промежность за пределы анального канала с избытком (рис. 2в).
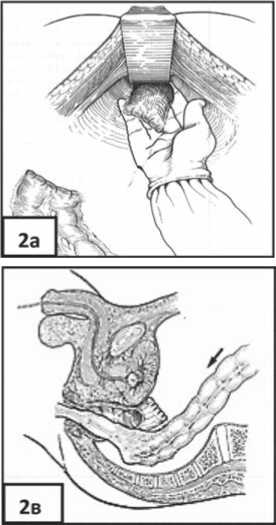
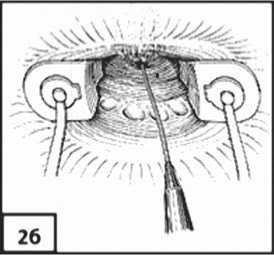
Рис. 2. Схемы этапов операции: а – ушитая культя ПК и сформированный «тоннель» позади культи ПК, б – создание отверстия в культе для низведения на промежность мобилизованных левых отделов ОК, в – низведение колотранспла-тата через культю ПК на промежность за пределы анального канала с избытком
Избыток кишки, выведенный через анальный канал сначала фиксировали отдельными швами в проекции белой линии Хилтона (рис. 3а) и окончательно (с разбортовкой) к коже промежности, без наложения швов между краями отверстия в культе ПК и колотрансплантатом (рис. 3б).
Отсечение избытка низведенной ОК на уровне позади-прямокишечного колоректального соустья в культе прямой кишки выполняли на 10–13 сутки (в среднем 11,4±1,3 суток) после основного этапа (срок естественного формирования бесшовного анастомоза). Краевой сосуд брыжейки колотрансплантата лигировали, а избыток кишки отсекали электроскальпелем над анастомозом на высоте до 0,5 см, что нивелировало риск кровотечения и способствовало адекватной адаптации слизистых оболочек культи ПК и коло-трансплантата в области межкишечного соустья (рис. 3в).
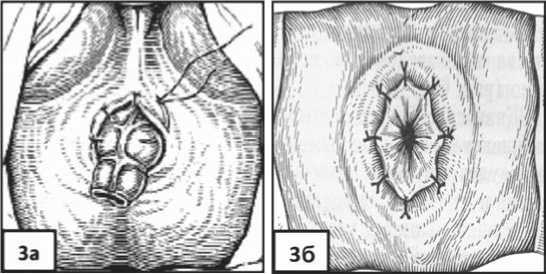
Рис. 3. Схемы этапов операции: а – фиксация избытка низведенной ОК в проекции белой линии Хилтона, б – фиксация избытка низведенной ОК к перианальной коже (с разбортовкой), в – окончательный вид сформированного по-задипрямокишечного бесшовного колоректального анастомоза
Для оценки непосредственных результатов хирургического лечения учитывали частоту и характер послеоперационных гнойных осложнений, показатели летальности. Клиническая оценка течения послеоперационного периода основывалась на общих и местных признаках. Особенности течения раннего послеоперационного периода контролировали стандартными клиническими, биохимическими методами, показателями лейкоцитарного индекса интоксикации (ЛИИ) и уровнем молекул средней массы (МСМ) – критерии объективной оценки тяжести эндотоксикоза.
Для определения величины ВБД с целью диагностики СИАГ использовали непрямую методику измерения давления в мочевом пузыре, предложенную I. Kron с соавторами, которая считается «золотым стандартом» измерения давления в брюшной полости [7].
Описательные статистики для количественных нормально распределенных учетных признаков были представлены средними значениями и стандартной ошибкой среднего (М±m). Определение достоверности различий для параметрически распределенных вариационных рядов определяли по критерию Стьюдента для связанных и не связанных признаков с учетом равенства дисперсий и поправкой Бон-феррони. Различия считали статистически значимыми при p<0,05. Обработку полученных результатов осуществляли c помощью программного обеспечения STATISTIKA 6.1 (StatSoft Inc., USA).
Результаты
Продолжительность интраоперационной механической очистки ободочной кишки в ИГ 1 (мануальная декомпрессия) составила 17,2±2,1 мин. и была в 2,4 раза короче, чем при проведении лаважа в ГКС и ИГ 2 (40,5±5,7 мин.) (p<0,05). Клиническая картина неосложненного течения раннего послеоперационного периода в группах сравнения достоверно не различалась, как при срочных, так и экстренных ситуациях (табл. 2). Сроки купирования болевого синдрома на фоне пролонгированной перидуральной анестезии в группах сравнения: ГКС, ИГ 1 и ИГ 2, соответственно – в течение 3,5±0,5, 3,4±0,4 и 3,6±0,5 суток (p>0,05).
Клинические параметры неосложненного течения раннего послеоперационного периода (n=121)
|
Группы сравнения Параметры |
ГКС (n = 35) |
ИГ 1 (n = 31) |
ИГ 2 (n = 55) |
|
Сроки купирования болевого синдрома (сутки) |
3,5±0,5 (1) |
3,4±0,4 (2) |
3,6±0,5 (3) |
|
Сроки восстановления перистальтики кишечника (часы) |
34,2±12,3 (1) |
33,8±11,7 (2) |
33,5±11,9 (3) |
|
Сроки полной активизации пациентов (сутки) |
3,6±0,4 (1) |
3,5±0,5 (2) |
3,6±0,3 (3) |
|
Послеоперационный койко-день |
8,2±0,5 (1) |
8,1±0,4 (2) |
7,9±0,2 (3) |
Примечание: - недостоверные различия показателей между ГКС, ИГ 1, ИГ 2, p 1, 2, 3 > 0,05.
Сроки восстановления полноценной перистальтики кишечника также не имели достоверных отличий в группах, соответственно – через 34,2±12,3, 33,8±11,7 и 33,5±11,9 часа. Сроки полной активизации пациентов – через 3,6±0,4, 3,5±0,5 и 3,6±0,3 суток (p>0,05), обычно совпадали с моментом удаления дренажных трубок.
Показатели эндотоксикоза (ЛИИ и МСМ) (табл. 3), обусловленные транслокацией эндогенной микрофлоры и эндогенным инфицированием имели недостоверную тенденцию к росту в первые 28,8±4,3 часа послеоперационного периода (соответственно – 1,30±0,08 ед. и 0,266±0,04 у.е.) по сравнению с предоперационными показателями (1,27±0,6 ед. и 0,264±0,05 у.е.), как при суб-, так и при декомпенсированной толстокишечной непроходимости и достоверно не отличались в группах сравнения. Нормализовались к 3–4 суткам после операции.
Динамика показателей ВБД представлена в таблице 4. У 88 пациентов (72,7%) с явлениями субкомпенсированной ОТКН уровень ВБД составил в среднем 12,8±1,2 мм рт. ст. (I степени СИАГ). У 23 больных (19,0%) с декомпеси-рованной непроходимостью – 17,6±1,3 мм рт. ст. (II степень). У 10 пациентов (8,3%) в той же группе – 23,4±2,4 мм рт. ст. (III степень).
В раннем послеоперационном периоде (1–2 сутки) у больных (88) при субкомпенсирован- ной ОТКН уровень ВБД составил в среднем 3,8±0,5 мм рт. ст., что находилось в рамках физиологической нормы. У пациентов (33) при явлениях декомпенсации нормализация ВБД после операции наступала позже – к 3–4 суткам (в среднем – 5,1±0,2 мм рт. ст., по мере восстановления полноценной перистальтики).
На основании полученных данных о динамике показателей ВБД и эндотоксикоза можно считать, что интраопе-Таблица 2 рационный лаваж и интенсивная терапия до- и после операции оказывают положительное влияния на течение послеоперационного периода.
Подтверждением целесообразности и безопасности использования разработанной технологии хирургического лечения больных с суб- и декомпенсированной ОТКН на фоне обтурирующего рака дистальных отделов толстой кишки являются непосредственные результаты оперативных вмешательств (табл. 5).
Послеоперационные осложнения в ГКС, ИГ 1 и ИГ 2, соответственно – 4/35 (11,5%), 1/31 (3,2%) и 3/55 (5,4%). Несостоятельности бесшовного ППК КРА, про тяженного некроза низведенной ОК (проксимальнее зоны бесшовного соустья) в ИГ 1 и ИГ 2 (86 пациентов) не наблюдали.
У 4/86 пациентов (4,6%) – дистальный некроз избытка низведенной ОК до уровня наружной границы анального канала (разбортованный участок). Эти случаи мы не вклю-
Таблица 3
Динамика показателей ЛИИ и МСМ в раннем послеоперационном периоде (n=121)
|
Показатели |
До операции |
Сутки послеоперационного периода |
||
|
1 |
3 |
6 |
||
|
ГКС (n = 35) |
||||
|
ЛИИ (ед.) |
1,25±0,03 (1) |
1,29±0,05 (2) |
1,05±0,04 (3) |
0,81±0,07 (4) |
|
МСМ (у.е.) |
0,262±0,03 (1) |
0,264±0,04 (2) |
0,258±0,02 (3) |
0,239±0,01 (4) |
|
ИГ 1 (n = 31) |
||||
|
ЛИИ (ед.) |
1,27±0,05 (1) |
1,30±0,06 (2) |
1,04±0,03 (3) |
0,82±0,06 (4) |
|
МСМ (у.е.) |
0,264±0,04 (1) |
0,266±0,02 (2) |
0,261±0,03 (3) |
0,242±0,03 (4) |
|
ИГ 2 (n = 55) |
||||
|
ЛИИ (ед.) |
1,28±0,04 (1) |
1,31±0,05 (2) |
1,02±0,01 (3) |
0,80±0,09 (4) |
|
МСМ (у.е.) |
0,266±0,02 (1) |
0,268±0,03 (2) |
0,260±0,03 (3) |
0,242±0,06 (4) |
Примечание: - недостоверные различия показателей ЛИИ и МСМ между ГКС, ИГ 1, ИГ 2, p > 0,05; - достоверные различия показателей ЛИИ в группах сравнения, p 1, 2 и 3, 4 < 0,05; - достоверные различия показателей МСМ в группах сравнения, p 1, 2, 3 и 4 < 0,05.
Таблица 4
|
Показатели (мм рт. ст.) Группы сравнения |
До операции |
Сутки послеоперационного периода |
|||
|
1 |
2 |
4 |
7 |
||
|
Субкомпенсированная непроходимость (СИАГ I ст., n = 88) |
|||||
|
ГКС (n = 25) |
12,4±1,3 (1) |
5,2±0,9 (2) |
3,8±0,4 (3) |
3,7±0,3 (4) |
3,5±0,2 (5) |
|
ИГ 1 (n = 23) |
12,8±1,2 (1) |
6,5±0,3 (2) |
4,3±0,3 (3) |
4,1±0,1 (4) |
3,8±0,3 (5) |
|
ИГ 2 (n = 40) |
13,4±2,5 (1) |
5,8±0,7 (2) |
3,4±0,5 (3) |
3,5±0,4 (4) |
3,6±0,5 (5) |
|
Декомпенсированная непроходимость (СИАГ II ст., n = 20) |
|||||
|
ГКС (n = 6) |
16,7±1,4 (1) |
10,4±0,8 (2) |
5,4±0,7 (3) |
4,2±0,2 (4) |
3,6±0,3 (5) |
|
ИГ 1 (n = 5) |
16,4±1,1 (1) |
11,2±0,4 (2) |
6,3±0,5 (3) |
4,5±0,4 (4) |
3,8±0,2 (5) |
|
ИГ 2 (n = 9) |
17,6±1,3 (1) |
10,6±0,7 (2) |
5,7±0,7 (3) |
4,1±0,5 (4) |
3,5±0,4 (5) |
|
Декомпенсированная непроходимость (СИАГ III ст., n = 13) |
|||||
|
ГКС (n = 4) |
21,9±1,8 (1) |
13,2±0,9 (2) |
10,2±0,8 (3) |
5,1±0,1 (4) |
4,2±0,3 (5) |
|
ИГ 1 (n = 3) |
22,8±1,9 (1) |
14,9±0,3 (2) |
11,4±0,3 (3) |
5,3±0,2 (4) |
4,4±0,2 (5) |
|
ИГ 2 (n = 6) |
23,4±1,5 (1) |
13,5±0,7 (2) |
10,5±0,5 (3) |
4,9±0,3 (4) |
4,3±0,4 (5) |
Динамика показателей ВБД в раннем послеоперационном периоде (n=121)
Примечание: - недостоверные различия показателей ВБД между ГКС, ИГ 1, ИГ 2, p > 0,05; - достоверные различия показателей ВБД в группах сравнения, p 1 и 2, 3, 4, 5 < 0,05.
Заключение
Таблица 5
Частота и характер послеоперационных осложнений (n=121)
Технология формирования первичного бес-
|
Группы сравнения Вид осложнения |
ГКС (n = 35) |
ИГ 1 (n = 31) |
ИГ 2 (n = 55) |
|
Нагноение лапаротомной раны |
1 (2,9%) |
1 (3,2%) |
2 (3,6%) |
|
Эвентрация |
1 (2,9%) |
0 |
0 |
|
Гематома в области таза |
0 |
0 |
1 (1,8%) |
|
Несостоятельность анастомоза |
2 (5,7%) |
0 |
0 |
|
Всего |
4 (11,5%) (1) |
1 (3,2%) (2) |
3 (5,4%) (3) |
Примечание: - недостоверные различия показателей между ИГ 1 и ИГ 2, p 2, 3 > 0,05, - достоверные различия показателей между ГКС и ИГ 1, ИГ 2, p 1 и 2, 3 < 0,05.
чили в структуру ранних послеоперационных осложнений потому, что отрицательного влияния на положительный исход операции они не оказывают. Причиной такого вида некроза было нарушение микроциркуляции в избытке на фоне сдавления кишки в анальном канале. Избыток низведенной ОК иссекали на 10–12-е сутки после операции. В ГКС несостоятельность прямого КРА – у 2/35 больных (5,7%). Летальности в группах сравнения не зарегистрировано. Послеоперационный койко-день составил в среднем 8,1±0,3.
шовного позадипрямокишечного колоректального анастомоза с избытком низведенной ободочной кишки при суб- и декомпенсированной ОТКН, обусловленной колоректальным раком дистальных отделов толстой кишки (сигмовидная кишка, средний и в/ампулярный отдел прямой кишки), минимизирует риск его несостоятельности, избавляет больного от колостомы и отсроченного реконструктивно-восстановительного вмешательства.
Интраоперационная декомпрессия ободочной кишки (лаваж/мануальная декомпрессия) приводит к быстрому устранению синдрома ин-траабдоминальной гипертензии и способствует сокращению сроков купирования явлений эндотоксикоза.
Список литературы Первичный колоректальный анастомоз при субкомпенсированном и декомпенсированном обтурирующем раке дистальных отделов толстой кишки: альтернатива абдоминальной колостомии, риск несостоятельности, непосредственные результаты
- Агаев Э.К. Профилактика несостоятельности швов кишечных анастомозов методом перманентной внутрибрыжеечной блокады и лимфотропной терапии//Вестник хирургии. 2013. № 7. С. 81-84.
- Алекперов С.Ф., Пугаев А.В., Калачев О.А. и др. Диагностика и хирургической лечение опухолевой толстокишечной непроходимости//Хирургия. Журнал им. Н.И. Пирогова. 2012. №11. С. 38-44.
- Алиев С.А. Синдром интраабдоминальной гипертензии у больных осложненным раком ободочной кишки и его хирургическая коррекция//Хирургия. Журнал им. Н.И. Пирогова. 2012. №11. С. 45-52.
- Захарченко А.А., Винник Ю.С., Штоппель А.Э. и др. Рак прямой кишки: современные аспекты комбинированного лечения. Новосибирск: Наука, 2013. 132 с.
- Попов Д.Е. Факторы риска несостоятельности колоректаль-ных анастомозов у больных раком прямой кишки (обзор литературы)//Колопроктология. 2014. № 2 (48). С. 48-56.
- Штоппель А.Э., Захарченко А.А. Наложение первичного колоректального анастомоза при низкой обтурационной толстокишечной непроходимости//Проблемы колопроктологии. Сборник научных трудов. М.: ГНЦК. 2000. № 17. С. 237-241.
- Винник Ю.С, Маркелова Н.М., Куз Нецов М.Н., Соляни-ков А.С. К вопросу о применении биополимеров для профилактики несостоятельности кишечных анастомозов//Хирургическая практика. 2013. № 1. С. 30-35.
- Kron I.L., Hartman P.K., Nolan S.P. The measurement of intraabdominal pressur as a criterion for abdominal reexploracion//Ann. Surg. 1984. Vol. 199. P. 28-30.


