Первичный скрининг коллекционных грибных штаммов антагонистов к возбудителю фомоза рапса озимого
Автор: Маслиенко Л.В., Дейнега Л.А., Заверюха Е.А., Кузнецова А.В.
Рубрика: Агрохимия, агропочвоведение, защита и карантин растений
Статья в выпуске: 4 (200), 2024 года.
Бесплатный доступ
В лаборатории биометода агро-технологического отдела ФГБНУ ФНЦ ВНИИМК с целью разработки микробиологического метода снижения вредоносности наиболее опасной болезни рапса озимого - фомоза (Leptosphaeria maculans (Desm.) Ces. et de Not, анаморфная стадия Phoma lingam (Tode) Desm.), в 2024 г. из рабочей коллекции проводили поиск перспективных штаммов-продуцентов микробиопрепаратов. В результате первичного скрининга выделено 26 перспективных грибных штаммов с разными типами антагонистической активности (конкуренция за площадь питания, гиперпаразитизм и антибиоз) против возбудителя фомоза: шесть штаммов из рода Trichoderma, семь - из рода Penicillium, четыре - из рода Chaetomium, три - из рода Aspergillus, два - из класса Basidiomycota, а также по одному из родов Sordaria, Metarhizium, Trichothecium и Talaromyces.
Фомоз, рапс озимый, первичный скрининг, грибные штаммы антагонисты, микробиологический метод
Короткий адрес: https://sciup.org/142243372
IDR: 142243372 | УДК: 633.853.494:632.937 | DOI: 10.25230/2412-608X-2024-4-200-107-113
Primary screening of collection of fungal antagonist strains against phoma rot pathogen on winter rapeseed
In 2024, in order to develop a microbiological method to reduce the harmfulness of the most dangerous disease of winter rapeseed - Phoma rot (Leptosphaeria maculans (Desm.) Ces. et de Not, anamorphic stage Phoma lingam (Tode) Desm.), promising strains-producers of microbiopreparations were searched for in the working collection at V.S. Pustovoit All-Russian Research Institute of Oil Crops. As a result of the primary screening, 26 promising fungal strains with different types of antagonistic activity (competition for feeding area, hyperparasitism and antibiosis) against the Phoma rot pathogen were identified: six strains of the genus Trichoderma, seven of the genus Penicillium, four of the genus Chaetomium, three of the genus Aspergillus, two of the class Basidiomycota and one each of the genera Sordaria, Metarhizium, Trichothecium, and Talaromyces.
Текст научной статьи Первичный скрининг коллекционных грибных штаммов антагонистов к возбудителю фомоза рапса озимого
Введение. Для снижения вредоносности одной из наиболее распространенных и опасных болезней рапса озимого – фо-моза (возбудитель Leptosphaeria maculans (Desm.) Ces. et de Not, анаморфная стадия Phoma lingam (Tode) Desm.) [1], актуальной задачей является разработка микробиологического метода. В условиях центральной зоны Краснодарского края, а в последние годы и в южных областях Нечерноземья, фомоз является одной из наиболее вредоносных болезней озимых культур семейства капустные, в том числе и рапса озимого, поражение которой может привести к снижению урожая до 40,0 %, а при раннем заражении – и к преждевременной гибели растений [2–5]. В качестве основных мер ее контроля рекомендуются: устойчивые сорта, уборка растительных остатков, соблюдение севооборота (срок возврата рапса на прежнее поле не ранее чем через 3–4 года), оптимальные сроки посева, пространственная изоляция, протравливание семян и применение фунгицидов во время вегетации культуры [6].
Зарегистрированных биопрепаратов от фомоза на рапсе в России нет. В лаборатории биометода агротехнологического отдела ФГБНУ ФНЦ ВНИИМК, одной из немногих в России, многие годы ведутся исследования по разработке микробиологических средств защиты масличных культур от болезней. В основе разработанной в лаборатории концепции целенаправленного создания микробиопрепаратов для защиты масличных и других сельскохозяйственных культур от болезней лежит поиск штаммов антагонистов, безопасных для человека, нефитотоксичных, проявляющих высокую активность в широко варьируемых погодных условиях против комплекса патогенов, обладающих полифунк-циональным типом действия [7]. Начальным этапом этих исследований является ступенчатый скрининг вновь выделенных или коллекционных штаммов в лабораторных условиях in vitro.
Настоящая работа посвящена первому этапу ступенчатого скрининга – первичному скринингу коллекционных грибных штаммов к агрессивному изоляту возбудителя фомоза рапса озимого Phoma lingam in vitro.
Материалы и методы. Исследования проводили в лаборатории биометода агро-технологического отдела ФГБНУ ФНЦ ВНИИМК в 2024 г. Объектом исследований служили: конидиальная стадия агрессивного изолята возбудителя фомоза рапса озимого Phoma lingam , выделенного в центральной зоне Краснодарского края; коллекционные штаммы грибных антагонистов возбудителей болезней масличных культур – 26 штаммов, представленных родами Trichoderma , Penicillium , Chaetomium , Sordaria , Metarhizium , Trichothecium, Talaromyces , Aspergillus , а также классом Basidiomycota.
Оценку антагонистической активности штаммов in vitro к агрессивному изоляту возбудителя фомоза рапса озимого проводили методом двойных или встречных культур [8]. Метод позволяет определить антагонистическую активность выделенных или коллекционных штаммов при совместном культивировании с возбудителем болезни (агрессивным изолятом) в одной чашке Петри.
Культуры грибных антагонистов и возбудителя болезни выращивали отдельно в течение пяти–семи суток на агаризирован-ной питательной среде. Стерильным сверлом размером 0,7 см вырезали блоки с мицелием антагониста и патогена и помещали в одну чашку Петри на расстоянии 6,0 см. Контролем служили культуры антагонистов и патогена, посеянные порознь. Антагонистов и патоген выращивали на картофельно-сахарозном агаре (КСА) [9] и на специализированной для грибов среде Рудакова [10]. Учёты взаимодействия патогена с антагонистами проводили на 20 сутки культивирования, отмечали:
-
- рост патогена и антагониста в % от площади чашки Петри (конкуренция за площадь питания);
-
- наличие или отсутствие зон задержки роста патогена в результате синтеза антагонистами гидролитических ферментов или веществ антибиотической природы (стерильная зона);
-
- нарастание антагониста на колонию патогена (гиперпаразитическая зона).
Результаты и обсуждения. Результаты первичной оценки коллекционных грибных штаммов к возбудителю фомоза рапса озимого Phoma lingam методом двойных или встречных культур на питательных средах КСА и Рудакова показали, что все штаммы проявили антагонистическую активность, при этом механизм антагонистического действия грибов представлен тремя типами: конкуренция за площадь питания, гиперпаразитизм и антибиоз.
Из 26 испытанных коллекционных штаммов грибов к возбудителю фомоза на среде КСА пять штаммов из рода Trichoderma (Т-1, Т-2, Т-3, Т-4 и Т-5 Trichoderma sp.) проявили тройной тип механизма антагонистической активности, заняв 100 % поверхности питательной среды, со стерильной зоной 4,5–5,5 мм и с гиперпаразитической зоной 0,5–3,7 см2 (табл. 1, рис. 1).
Таблица 1
Антагонистическая активность грибных штаммов к возбудителю фомоза рапса озимого Phoma lingam при температуре 25 °С на 20-е сутки культивирования на среде КСА
ФГБНУ ФНЦ ВНИИМК, 2024 г.
|
Штамм антагонист |
Площадь зарастания поверхности питательной среды |
Размер стерильной зоны, мм |
Размер гиперпаразитической зоны, см2 |
|||
|
антагонистом |
патогеном |
|||||
|
% |
см2 |
% |
см2 |
|||
|
Phoma lingam |
- |
- |
27,6 |
17,5 ± 1,3 |
- |
- |
|
конкуренция за площадь питания + антибиоз + гиперпаразитизм |
||||||
|
T-1 Trichoderma sp . |
100 |
63,6 ± 0 |
5,8 |
3,7 ± 0,1 |
4,5 ± 0,5 |
3,7 ± 0,1 |
|
T-2 Trichoderma sp . |
100 |
63,6 ± 0 |
1,3 |
0,8 ± 0,2 |
5,0 ± 0 |
0,8 ± 0,2 |
|
T-3 Trichoderma sp . |
100 |
63,6 ± 0 |
2,1 |
1,4 ± 0,2 |
5,5 ± 0,5 |
1,4 ± 0,2 |
|
T-4 Trichoderma sp . |
100 |
63,6 ± 0 |
0,8 |
0,5 ± 0,3 |
5,0 ± 0 |
0,5 ± 0,3 |
|
T-5 Trichoderma sp . |
100 |
63,6 ± 0 |
1,2 |
0,8 ± 0 |
5,5 ± 0,5 |
0,8 ± 0 |
|
конкуренция за площадь питания + антибиоз |
||||||
|
Pv-3 Penicillium verrucosum |
53,7 |
34,2 ± 1,8 |
18,5 |
11,8 ± 2,0 |
10,0 ± 0 |
0 |
|
Pk-1 Penicillium vermiculatum |
56,1 |
35,7 ± 5,3 |
27,2 |
17,3 ± 2,0 |
8,0 ± 1,0 |
0 |
|
Pbc-1 Penicillium brevi-compactum |
46,7 |
29,7 ± 0,7 |
35,2 |
22,4 ± 0,5 |
7,5 ± 0,5 |
0 |
|
Pp-1 Penicillium purpurescens |
69,5 |
44,2 ± 3,9 |
12,4 |
7,9 ± 1,2 |
7,5 ± 2,5 |
0 |
|
Av-1 Aspergillus versicolor |
64,8 |
41,3 ± 5,9 |
15,6 |
9,9 ± 1,1 |
7,5 ± 0,5 |
0 |
|
An-1 Aspergillus niger |
66,3 |
41,2 ± 4,9 |
12,7 |
8,1 ± 4,0 |
7,5 ± 0,5 |
0 |
|
Af-1 Aspergillus flavus |
53,9 |
34,3 ± 1,1 |
17,7 |
11,2 ± 1,9 |
6,5 ± 0,5 |
0 |
|
М-1 Metarhizium sp . |
53,4 |
33,9 ± 1,5 |
15,2 |
9,7 ± 1,1 |
6,5 ± 0,5 |
0 |
|
Xk-1 Chaetomium olivaceum |
61,6 |
39,3 ± 0,5 |
23,7 |
15,1 ± 1,5 |
6,0 ± 0 |
0 |
|
Pr-1 Penicillium rugulosum |
25,8 |
16,5 ± 1,8 |
16,4 |
10,4 ± 0,6 |
5,5 ± 0,5 |
0 |
|
Xk-2 Chaetomium globosum |
66,1 |
42,1 ± 3,2 |
18,7 |
11,8 ± 1,9 |
5,5 ± 0,5 |
0 |
|
Tt-1 Talaramyces trachispermus |
25,8 |
16,4 ± 0,2 |
40,0 |
25,5 ± 0,3 |
5,5 ± 2,5 |
0 |
|
Хk-4 Chaetomium sp . |
65,8 |
41,9 ± 1,3 |
21,3 |
13,5 ± 2,2 |
5,0 ± 0 |
0 |
|
Sm-1 Sordaria macrospora |
80,3 |
51,1 ± 6,3 |
7,0 |
4,4 ± 2,4 |
5,0 ± 0 |
0 |
|
Pf-1 Penicillium funiculosum |
58,7 |
37,4 ± 1,5 |
11,6 |
7,5 ± 0,2 |
4,5 ± 0,5 |
0 |
|
Tr-1 Trichothecium roseum |
82,7 |
53,6 ± 0 |
10,4 |
6,6 ± 1,7 |
4,0 ± 1,0 |
0 |
|
A-1 Basidiomycota |
86,9 |
55,3 ± 2,1 |
11,1 |
7,1 ± 1,8 |
3,5 ± 0,5 |
0 |
|
Хk-3 Chaetomium globosum |
63,5 |
44,4 ± 0,2 |
16,4 |
10,4 ± 0,2 |
2,5 ± 0,5 |
0 |
|
M-24 Penicillium vermiculatum |
53,7 |
34,2 ± 0,1 |
9,9 |
6,3 ± 4,7 |
1,5 ± 0,5 |
0 |
|
конкуренция за площадь питания + гиперпаразитизм |
||||||
|
Tk-1 Trichoderma koningii |
87,4 |
55,6 ± 0 |
25,2 |
16,0 ± 2,0 |
0 |
8,1 ± 3,5 |
|
И-3 Basidiomycota |
53,5 |
34,0 ± 2,9 |
31,1 |
19,8 ± 2,7 |
0 |
3,1 ± 1,2 |
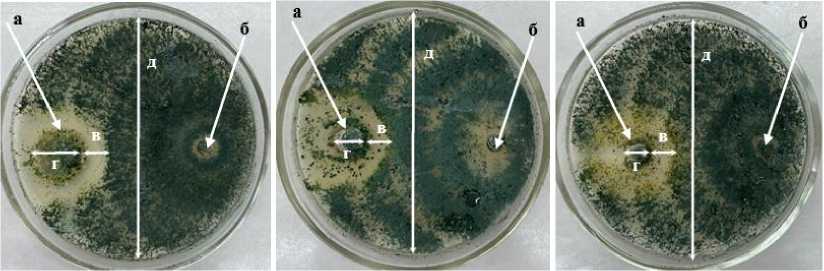
T-1 Trichoderma sp . T-3 Trichoderma sp . T-4 Trichoderma sp .
Рисунок 1 – Антагонистическая активность грибов рода Trichoderma к возбудителю фомоза рапса озимого Phoma lingam через 20 суток совместного культивирования на среде КСА при температуре 25 °С (ориг.) (ФГБНУ ФНЦ ВНИИМК, 2024 г.): а – колония патогена; б – колония антагониста; в – стерильная зона; г – гиперпаразитизм; д – конкуренция за площадь питания
Двойной тип механизма антагонистической активности (конкуренция за площадь питания и антибиоз) проявили семь штаммов из рода Penicillium (Pv-3 Penicillium verrucosum , Pk-1 Penicillium vermiculatum , Pbc-1 Penicillium brevi-compactum , Pp-1 Penicillium purpurescens , Pr-1 Penicillium rugulosum , Pf-1 Penicillium funiculosum и M-24 Penicillium vermiculatum ), четыре из рода Chaetomium (Xk-1 Chaetomium oliva-ceum , Xk-2 и Хk-3 Chaetomium globosum и Хk-4 Chaetomium sp . ), три из рода Aspergillus (Av-1 Aspergillus versicolor , An-1 Aspergillus niger и Af-1 Aspergillus flavus ), а также штаммы М-1 Metarhizium sp . , Tt-1
Talaramyces trachispermus , Sm-1 Sordaria macrospora , Tr-1 Trichothecium roseum и A-1 Basidiomycota . Вышеуказанные штаммы на 20 сутки заняли от 25,8 до 86,9 % площади поверхности питательной среды при таковой у патогена 7,0–40,0 %, а также образовали стерильную зону задержки роста патогена размером от 1,5 до 10,0 мм. Максимальная стерильная зона установлена у штаммов Pv-3 Penicillium verrucosum , Pk-1 Penicillium vermiculatum , Pbc-1 Penicillium brevi-compactum , Pp-1 Penicillium pur-purescens , Av-1 Aspergillus versicolor и An-1 Aspergillus niger – 7,5–10,0 мм (рис. 2).
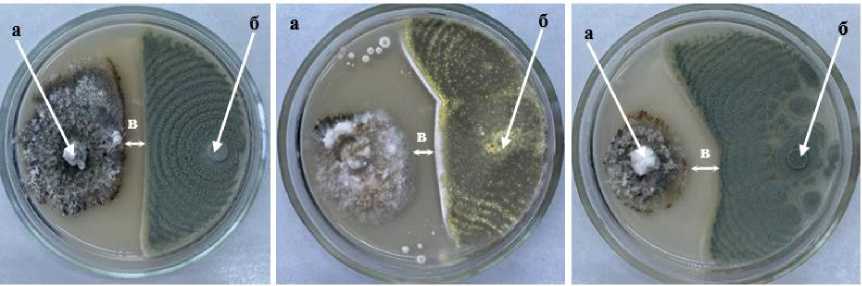
Pv-3 Penicillium
Pk-1 Penicillium
Pbc-1 Penicillium
verrucosum vermiculatum brevi-compactum
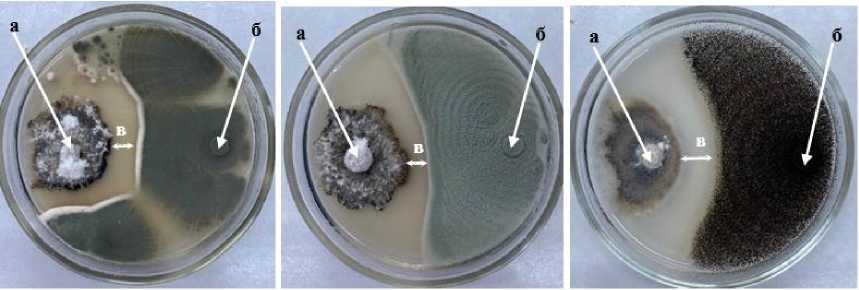
Pp-1 Penicillium Av-1 Aspergillus An-1 Aspergillus purpurescens versicolor niger
Рисунок 2 – Антибиотическая активность грибных штаммов к возбудителю фомоза рапса озимого Phoma lingam через 20 суток совместного культивирования на среде КСА при температуре 25 °С (ориг.) (ФГБНУ ФНЦ ВНИИМК, 2024 г.): а – колония патогена; б – колония антагониста; в – стерильная зона
Штаммы И-3 Basidiomycota и Tk-1 Trichoderma koningii на среде КСА проявили двойной тип механизма антагонистической активности (конкуренция за площадь питания и гиперпаразитизм), заняв 53,5–87,4 % поверхности питательной среды при гиперпаразитической зоне 3,1– 8,1 см2 соответственно.
На специализированной для грибов питательной среде Рудакова у 12 штаммов (Т-1, Т-2, Т-3, Т-4 и Т-5 Trichoderma sp., Xk-1 Chaetomium olivaceum, Xk-2 и Хk-3 Chae-tomium globosum, и Хk-4 Chaetomium sp., И-3 и А-1 Basidiomycota и Tr-1 Trichothe-cium roseum) выявлен двойной тип антагонистической активности к возбудителю фо-моза рапса озимого Phoma lingam – конку- ренция за площадь питания и гиперпаразитизм (табл. 2). При этом максимальную конкуренцию за площадь питания проявили штаммы из рода Trichoderma (Т-1, Т-2, Т-3, Т-4 и Т-5), заняв 100 % поверхности питательной среды, а максимальная гиперпаразитическая зона выявлена у штаммов Xk-2 и Хk-3 Chaetomium glo-bosum, Tr-1 Trichothecium roseum и И-3 Ba-sidiomycota – 8,2–12,1 см2.
Таблица 2
Антагонистическая активность грибных штаммов к возбудителю фомоза рапса озимого Phoma lingam при температуре 25 °С на 20-е сутки культивирования на среде Рудакова
ФГБНУ ФНЦ ВНИИМК, 2024 г.
|
Штамм антагонист |
Площадь зарастания поверхности питательной среды |
Размер стерильной зоны, мм |
Размер гиперпаразитической зоны, см2 |
|||
|
антагонистом |
патогеном |
|||||
|
% |
см2 |
% |
см2 |
|||
|
Phoma lingam |
- |
- |
78,0 |
49,1 ± 0,6 |
- |
- |
|
конкуренция за площадь питания + гиперпаразитизм |
||||||
|
T-1 Trichoderma sp . |
100 |
63,6 ± 0 |
2,7 |
1,7 ± 0,2 |
0 |
1,7 ± 0,2 |
|
T-2 Trichoderma sp . |
100 |
63,6 ± 0 |
2,0 |
1,2 ± 0,5 |
0 |
1,2 ± 0,5 |
|
T-3 Trichoderma sp . |
100 |
63,6 ± 0 |
4,2 |
2,6 ± 0,2 |
0 |
2,6 ± 0,2 |
|
T-4 Trichoderma sp . |
100 |
63,6 ± 0 |
2,9 |
1,8 ± 0,1 |
0 |
1,8 ± 0,1 |
|
T-5 Trichoderma sp . |
100 |
63,6 ± 0 |
6,0 |
2,1 ± 1,0 |
0 |
2,1 ± 1,0 |
|
Tr-1 Trichothecium roseum |
100 |
63,6 ± 0 |
13,4 |
8,5 ± 1,7 |
0 |
8,5 ± 1,7 |
|
A-1 Basidiomycota |
90,7 |
57,7 ± 2,9 |
14,3 |
9,1 ± 1,1 |
0 |
7,1 ± 0,9 |
|
Xk-2 Chaetomium globosum |
81,4 |
51,7 ± 1,5 |
16,5 |
10,5 ± 2,1 |
0 |
8,2 ± 1,7 |
|
Xk-1 Chaetomium olivaceum |
77,9 |
49,6 ± 2,2 |
17,7 |
11,3 ± 1,2 |
0 |
1,9 ± 0,3 |
|
Хk-4 Chaetomium sp . |
75,3 |
47,9 ± 0 |
13,8 |
8,7 ± 0 |
0 |
6,8 ± 0 |
|
Хk-3 Chaetomium globosum |
71,8 |
45,6 ± 1,0 |
16,8 |
10,6 ± 0,7 |
0 |
8,3 ± 0,5 |
|
И-3 Basidiomycota |
58,9 |
37,4 ± 0,8 |
23,5 |
15,5 ± 0,5 |
0 |
12,1 ± 0,4 |
|
конкуренция за площадь питания + антибиоз |
||||||
|
Av-1 Aspergillus versicolor |
56,1 |
35,7 ± 0,4 |
33,1 |
21,0 ± 5,5 |
5,0 ± 1,0 |
0 |
|
Pr-1 Penicillium rugulosum |
36,3 |
23,0 ± 1,6 |
46,6 |
29,6 ± 2,2 |
3,5 ± 0,5 |
0 |
|
Tk-1 Trichoderma koningii |
100 |
63,6 ± 0 |
6,0 |
2,1 ± 0,7 |
2,5 ± 0,5 |
0 |
|
Pk-1 Penicillium vermiculatum |
59,5 |
37,8 ± 5,4 |
33,2 |
21,1 ± 1,9 |
2,5 ± 0,5 |
0 |
|
Pbc-1 Penicillium brevi-compactum |
54,9 |
34,9 ± 0,4 |
37,9 |
24,1 ± 0,6 |
2,5 ± 0,5 |
0 |
|
Pp-1 Penicillium purpurescens |
52,8 |
33,5 ± 0,4 |
29,6 |
18,8 ± 0,7 |
2,5 ± 0,5 |
0 |
|
Af-1 Aspergillus flavus |
58,3 |
37,1 ± 1,1 |
21,8 |
13,8 ± 0,7 |
2,5 ± 0,5 |
0 |
|
An-1 Aspergillus niger |
87,4 |
55,5 ± 4,9 |
10,6 |
6,7 ± 3,6 |
2,0 ± 1,0 |
0 |
|
M-24 Penicillium vermiculatum |
55,7 |
35,4 ± 0,1 |
35,0 |
22,2 ± 1,4 |
1,0 ± 0 |
0 |
|
Pv-3 Penicillium verrucosum |
58,3 |
37,2 ± 1,7 |
39,5 |
25,1 ± 3,2 |
1,0 ± 0 |
0 |
|
конкуренция за площадь питания |
||||||
|
Sm-1 Sordaria macrospora |
97,8 |
62,2 ± 0,1 |
2,1 |
1,3 ± 0,1 |
0 |
0 |
|
Pf-1 Penicillium funiculosum |
51,5 |
32,8 ± 1,0 |
47,8 |
30,4 ± 1,4 |
0 |
0 |
|
М-1 Metarhizium sp . |
42,0 |
26,7 ± 0,3 |
43,9 |
27,9 ± 1,6 |
0 |
0 |
Конкуренцию за площадь питания и антибиоз проявили три штамма из рода Aspergillus (Av-1 Aspergillus versicolor , An-1 Aspergillus niger и Af-1 Aspergillus flavus ), шесть – из рода Penicillium (Pv-3 Penicillium verrucosum , Pk-1 Penicillium vermiculatum , Pbc-1 Penicillium brevi-compactum , Pp-1 Penicillium purpurescens , Pr-1 Penicillium rugulosum и M-24 Penicillium vermicula-tum ), а также штамм Tk-1 Trichoderma kon-ingii . При этом максимальную конкуренцию за площадь питания показал штамм Tk-1 Trichoderma koningii , заняв 100 % площади среды, а максимальный антибиоз – штаммы Pr-1 Penicillium rugulosum и Av-1 Aspergillus versicolor при стерильной зоне 3,5 и 5,0 мм соответственно. Только конкуренция за площадь питания выявлена у штаммов SM-1 Sordaria macrospora , Pf-1 Penicillium funiculosum и М-1 Metarhizium sp . , которые заняли от 42,0 до 97,8 % поверхности питательной среды, когда патоген при этом зарос всего на 2,1–47,8 %.
Таким образом, на двух питательных средах: КСА и Рудакова, выделено 26 перспективных грибных штаммов, проявивших антагонистическую активность к возбудителю фомоза рапса озимого с разными типами действия, для проведения вторичного скрининга на фоне искусственного заражения в лабораторных условиях во влажной камере.
Заключение. В результате первичного скрининга грибных штаммов антагонистов из рабочей коллекции лаборатории биометода агротехнологического отдела ФГБНУ ФНЦ ВНИИМК в 2024 г. на средах КСА и Рудакова выделены перспективные штаммы грибов с разными типами антагонистической активности к возбудителю фомоза рапса озимого: конкуренция за площадь питания, гиперпаразитизм и антибиоз. При этом пять штаммов из рода Trichoderma (Т-1, Т-2, Т-3, Т-4 и Т-5 Trichoderma sp.) проявили тройной тип механизма антагонистической активности. Максимальный антибиоз установлен у штаммов Pv-3 Penicillium verrucosum, Pk-1 Penicillium vermiculatum, Pbc-1 Penicillium brevi-compactum, Pp-1 Penicillium pur-purescens, Av-1 Aspergillus versicolor, An-1 Aspergillus niger и Pr-1 Penicillium rugu-losum, максимальная гиперпаразитическая зона – у штаммов Xk-2 и Хk-3 Chaetomium globosum, Tr-1 Trichothecium roseum и И-3 Basidiomycota, а максимальная конкуренция за площадь питания – у штамма Tk-1 Trichoderma koningii. Только конкуренция за площадь питания выявлена у штаммов Sm-1 Sordaria macrospora, Pf-1 Penicillium funiculosum и М-1 Metarhizium sp. В дальнейшем выделенные штаммы будут оценены во вторичном скрининге на фоне искусственного заражения возбудителем фо-моза рапса озимого в лабораторных условиях во влажной камере и в грунте.
Список литературы Первичный скрининг коллекционных грибных штаммов антагонистов к возбудителю фомоза рапса озимого
- Index Fungorum Data Bases: [Электронный ресурс]. - Режим доступа: https://www.indexfungorum.org/names/Names_Record.asp?RecordID=230154 (дата обращения: 29.10.2024).
- Бочкарев Н.И., Пивень В.Т., Тишков Н.М. [и др.]. Защита рапса // Защита и карантин растений. - 2017. - № S1. - С. 3776. EDN: XQQWJV
- Сердюк О.А., Трубина В.С., Горлова Л.А. Влияние внутренней инфекции на всхожесть и масличность семян масличных культур семейства капустные // Масличные культуры. - 2019. - Вып. 3 (179). -С.119-123.
- Gomzhina M.M., Gasich E.L. Plenodomus species infecting oilseed rape in Russia // Plant Protection News. - 2022. -No. 105 (3). - P. 135-147.
- Костин Н.К., Кузнецова А.А., Дудченко И.П. [и др.]. Видовой состав микромицетов, ассоциированных с растениями рапса озимого некоторых регионов России // Сб. тезисов докладов конф. "Генетические технологии в микробиологии и микробное разнообразие", Пущино, 06-08 декабря 2022 г. - С. 56-59. EDN: HSIUQG
- Гасич Е.Д. Фомоз рапса (обзор литературы) // Вестник защиты растений. -2004. - № 1. - С. 11-24. EDN: YKUWZV
- Маслиенко Л.В. Лаборатория биологических средств защиты растений (вчера, сегодня, завтра) // История научных исследований во ВНИИМКе за 90 лет. - Краснодар, 2002. - С. 191-197.
- Егоров Н.С. Выделение микробов антагонистов и биологические методы учета их антибиотической активности. - М.: Изд-во Моск. ун-та, 1957. - 78 с.
- Лысак В.В., Желдакова Р.А., Фомина О.В. Микробиология. Практикум: пособие. - Минск: БГУ, 2015. - 115 с.
- Рудаков О.Л. Микофильные грибы, их биология и практическое значение. -М.: Наука, 1981. - 160 с. EDN: UAJMLR


