Первый отечественный опыт выполнения холедоходуоденостомии под контролем эндоскопической ультрасонографии редакционные статьи
Автор: Алексеев К.И., Васильев И.В., Осипов А.С., Маады А.С., Будзинский С.А., Шаповальянц С.Г., Федоров Е.Д., Галкова З.В., Чернякевич П.Л., Андреева О.Н.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 2 т.8, 2013 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140188182
IDR: 140188182
The first national experience of eus-guided choledochoduodenostomy in patients with malignant obstructive jaundice
Текст статьи Первый отечественный опыт выполнения холедоходуоденостомии под контролем эндоскопической ультрасонографии редакционные статьи
УДК: ?????????????????
THE FIRST NATIONAL
EXPERIENCE OF EUS-GUIDED
CHOLEDOCHODUODENOSTOMY
IN PATIENTS WITH MALIGNANT
OBSTRUCTIVE JAUNDICE
Ретроградное эндоскопическое дренирование билиарного тракта, выполняемое транспапиллярным доступом, является сегодня общепринятым подходом к разрешению опухолевой механической желтухи с дистальным уровнем блока. К сожалению, у подавляющего числа пациентов заболевание диагностируется на поздних стадиях, когда радикальное хирургическое лечение уже невозможно, и постоянное внутреннее желчеот-ведение является предпочтительным и окончательным методом паллиативного лечения. Тем не менее, по разным причинам (дуоденальный стеноз, выраженная опухолевая стриктура интрапанкреати-ческой части общего желчного протока, хирургически изменённая анатомия верхних отделов пищеварительного тракта и др.) эндоскопическое ретроградное дренирование не удается выполнить от 0,6 до 9,4% случаев.
Альтернативным способом декомпрессии билиарного тракта в таких случаях является антеградное чрескожночреспеченочное дренирование. Однако, наличие асцита, выраженной коагулопатии, вероятность инфекционных осложнений, существующая при длительном наружном или наружно-внутреннем дренировании, являются сдерживающи- ми факторами при выборе антеградного способа желчеотведения. Немаловажно отметить также и снижение качества жизни, отмечаемое пациентами с наружными дренажами. Хирургические же методы дренирования, связанные с созданием различных видов билиодигестивных соустий, сопряжены со значительно более высоким уровнем осложнений и летальности и по эффективности дренирования не имеют явных преимуществ перед миниинвазивными технологиями.
Последние 20 лет отмечается бурное развитие нового направления диагностической эндоскопии – эндоскопической ультрасонографии (ЭУС). Первые эхоэндоскопы оснащались радиальным датчиком и использовались для выявления небольших опухолей поджелудочной железы и, в последующем, для диагностики патологических изменений стенки желудочно-кишечного тракта. Появление линейных эхоэндоскопов существенно расширило возможности ЭУС, которая быстро эволюционировала из сугубо диагностического в лечебно-оперативный метод. Так, в 1996 году Wiersema M.J. доложил об успешном дренировании псевдокисты поджелудочной железы под ЭУС-контролем. Тем же автором в 1996 году представлены результаты первых холангиографий, выполняемых под ЭУС-контролем тем пациентам, у которых по тем или иным причинам не удалось осуществить эндоскопический ретроградный доступ. Уже через 5 лет, в 2001 году, Giovannini М. с соавт. сообщили о первой успешной холедоходуоденостомии, наложенной под эндосонографическим контролем. В зарубежной научной литературе последнего десятилетия имеются сообщения как о единичных наблюдениях, так и небольших сериях холедоходуо-деностомий под контролем ЭУС. В 2011 году мировой опыт насчитывал не более 250-280 таких вмешательств. В доступной нам отечественной медицинской литературе сообщений о наложении билиодиги-стивных соустий под контролем ЭУС до настоящего времени не встречалось.
В начале 2012 г. специалистами научно-организационного центра абдоминальной хирургии и эндоскопии РНИМУ им. Н.И. Пирогова на базе ГКБ №31 и отделения диагностической и оперативной эндоскопии НМХЦ им. Н.И. Пирогова выполнены первые в России холедоходу-оденостомии под контролем ЭУС. Всего оперировано 3 пациента.
Пациентка Ц., 73 лет госпитализирована в 31 ГКБ в экстренном порядке с клинической картиной механической желтухи. Уровень билирубина при поступлении 339 мкмоль/л. По данным проведенного инструментального обследования диагностирована опухоль головки поджелудочной железы IV стадии с компрессией дистального отдела общего желчного протока(ОЖП), выраженной панкреатической и билиарной гипертензией, метастатическое поражение печени, асцит (Рис. 1). По экстренным показаниям, дважды предприняты попытки выполнения ЭРХПГ с целью ретроградного билиарного дренирования, которые не удались из-за выраженной опухолевой окклюзии ОЖП. От выполнения антеградного вмешательства решено воздержаться из-за наличия выраженного асцита и значимых нарушений со стороны свертывающей системы крови. Решено выполнить холедоходуоденостомию под контролем ЭУС. Операция выполнено совместной операционной бригадой под общей анестезией с сохранением спонтанного дыхания 24 февраля 2012 г.
При ЭУС линейным датчиком подтверждено наличие опухоли головки поджелудочной железы размерами 35 X 40 мм, расширение ОЖП до 25 мм с конусовидным сужением в проекции интрапанкреатической части, метаста-статическое поражение печени, асцит (рис. 2). Установлена инвазия опухоли в интрапанкреатическую часть ОЖП и воротную вену (рис. 3, 4).
Под контролем ЭУС выбрана оптимальная точка для пункции на задненижней стенке луковицы двенадцатиперстной кишки, непосредственно прилежащая к расширенному (супра-стенотическому) отделу ОЖП. В режиме
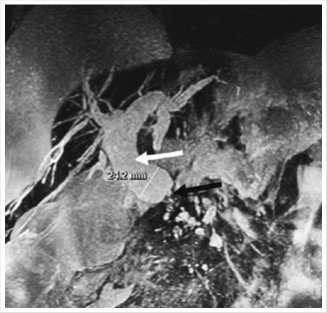
Рис. 1. МРТ в холангиогенном режиме: расширенный ОЖП, сужение интрапанкреати-ческой части.
Черная стрелка – опухолевая окклюзия интрапанкреатической части ОЖП;
Белая стрелка – расширенные супрасте-нотические отделы ОЖП

цветового допплеровского картирования подтверждено отсутствие значимых сосудистых структур в зоне намеченной пункции. Иглой для тонкоигольной биопсии 19G выполнена пункция ОЖП (Рис. 5). Через просвет иглы введено контрастное вещество и произведена холангиография (Рис. 6).
Через просвет иглы в общий желчный проток в проксимальном направлении проведена нитиноловая струна-проводник диаметром 0,035 дюйма (Рис. 7). Игла извлечена. По струне к пункционному отверстию низведен пластиковый конический дилататор и выполнено механическое расширение точечного соустья до диаметра 10 Fr (3,33 мм) (Рис. 8). Затем в просвет ОЖП по струне-проводнику введена система доставки покрытого са-морасширяющегося нитинолового стента, выполнено его позиционирование и раскрытие (Рис. 9а, 9б). После удаления доставочного устройства по сформированному соустью через стент отмечено обильное поступление желчи. Время оперативного вмешательства составило 1 час 15 мин. Интраоперационных осложнений не было.
Ближайший послеоперационный период также протекал гладко. Клинически отмечено быстрое разрешение явлений желтухи. При контрольном биохимическом анализе крови на 4 сутки констатировано снижение уровня билирубина до 80 мкмоль/л. На 7 сутки после вмешательства пациентка была выписана из стационара в относительно удовлетворительном состоянии.
Двое других пациентов, мужчина А. 65 лет и женщина М., 83 лет, госпитализированы НМХЦ им. Пирогова в плановом порядке для паллиативного лечения в объеме эндоскопического транспапиллярного стентирования общего желчного протока. Ранее с явлениями механической желтухи оба пациента госпитализировались в другие стационары, где был установлен диагноз рака головки поджелудочной железы и выполнено наложение микрохолецистостом под УЗИ-наведением. Оба пациента признаны неоперабель-
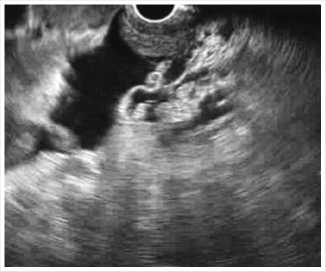
Рис. 2. ЭУС: асцит
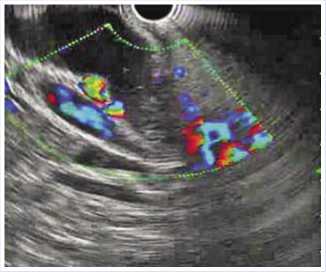
Рис. 4. ЭУС в режиме допплеровского сканирования. Инвазия опухоли в воротную вену ными. Пациент А. – из-за выраженного атеросклероза брахиоцефальных артерий с гемодинамически значимым стенозом, что расценено как высокий риск развития острой недостаточности мозгового кровообращения. Пациентка М. – из-за запущенности онкологического про-
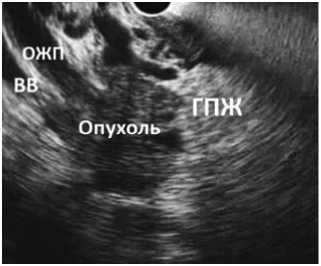
Рис. 3. ЭУС: опухоль головки поджелудочной железы с инвазией в желчный проток, воротную вену. ГПЖ – головка поджелудочной железы; ВВ – воротная вена; ОЖП – общий желчный проток
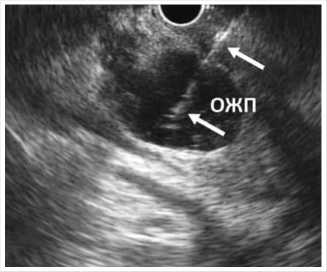
Рис. 5. Пункция общего желчного протока под контролем ЭУС. Белые стрелки – пункционная игла
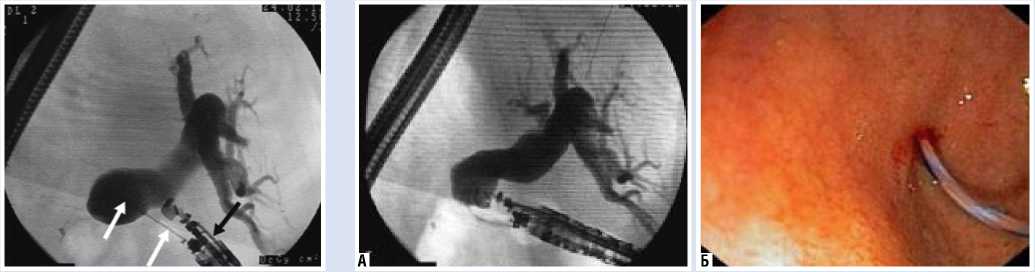
Рис. 7. Струна-проводник в просвете желчного дерева. (А – рентгенологическая картина, Б – эндоскопическая картина)
Рис .6. ЭУС-контролируемая холангиография.
Белые стрелки – пункционная игла.
Черная стрелка – дистальный конец операционного эхоэндоскопа

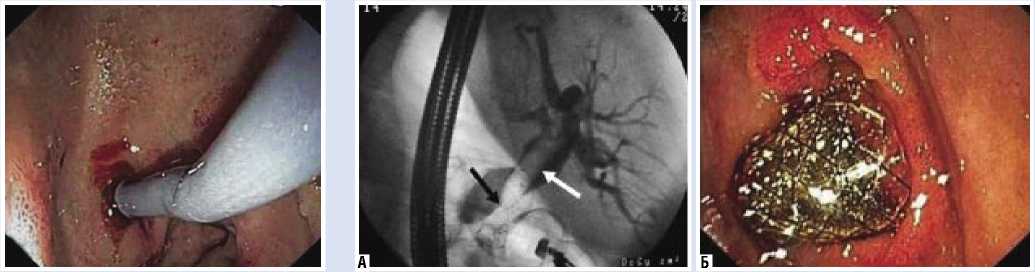
Рис. 8. Бужирование пункционного отверстия коническим дилататором
Рис. 9. Вид после раскрытия саморасширяющегося стента. (А – рентгенологическая картина, Б – эндоскопическая картина). Белая стрелка – раскрытый стент в просвете общего желчного протока. Черная стрелка – «талия» в области холедоходуоденостомы цесса. Однако, при попытке выполнения эндоскопического дренирования у обоих пациентов диагностирован субком-пенсированный дуоденальный стеноз из-за сдавления вертикального отдела двенадцатиперстной кишки опухолевым процессом. Поэтому в обоих случаях решено выполнить эндоскопическую холе-доходуоденостомию под контролем ЭУС. Вмешательства выполнялись под общей анестезией с сохранением спонтанного дыхания. За 3 часа до операции выполнено перекрытие дренажей микрохолеци-стом для формирования искусственной билиарной гипертензии, что значительно облегчило выполнение основных этапов вмешательства. Интраоперационных осложений не было. Послеоперацион- ный период протекал без осложнений. С первых суток отмечено прогрессивное снижение количества отделяемой желчи по микрохолецистостоме с 450–550 мл/ сут до 40–50 мл/сут к 5–6 сут. Микрохо-лецистостомы удалены на 6-е и 7-е сутки. Пациенты выписаны в относительно удовлетворительном состоянии на 7 сут. после операций под наблюдение хирургом и онкологом по месту жительства.
Заключение: первый опыт выполнения эндоскопических холедоходуодено-стомий под контролем эндосонографии контролем показал техническую выполнимость вмешательства, продемонстрировал его безопасность и клиническую эффективность в разрешении механической желтухи опухолевого генеза, а также в обеспечении постоянного внутреннего желчеотведения в случае неэффективности или невозможности применения других миниинвазивных методов. По мере набора опыта, данная операция может стать альтернативным методом декомпрессии желчных протоков при невозможности осуществления дренирования ретроградным доступом.
Национальный медико-хирургический Центр им. Н.И. Пирогова


