Пятилетний результат экстренного эндопротезирования аневризмы брюшной аорты при ее разрыве
Автор: Затевахин Игорь Иванович, Золкин Владимир Николаевич, Шиповский Владимир Николаевич, Матюшкин Андрей Валерьевич, Тищенко Иван Сергеевич, Бережной Кирилл Юрьевич
Журнал: Хирургическая практика @spractice
Рубрика: Клинические случаи, дискуссии
Статья в выпуске: 2, 2013 года.
Бесплатный доступ
В данной статье представлено клиническое наблюдение эндопротезирования аневризмы абдоминальной аорты при ее разрыве. Была произведена имплантация эндоваскулярной системы «Excluder, Gore». Также отслежены ближайшие и отдаленные результаты: через 5 лет по данным КТ-ангиографии аневризма не увеличивается в диаметре, стент-графт проходим, пристеночного тромбоза, эндоликов не определяется.
Аневризма аорты, эндопротезирование, эндоваскулярная хирургия
Короткий адрес: https://sciup.org/142211514
IDR: 142211514 | УДК: 616.136-089
Текст научной статьи Пятилетний результат экстренного эндопротезирования аневризмы брюшной аорты при ее разрыве
Разрыв аневризмы брюшной аорты – одна из главных трагедий современной сосудистой хирургии. Связано это с тем, что общая смертность при разрыве абдоминальной аорты крайне высока и составляет 80–90% [1]. Однако применение эндоваскулярной стратегии позволяет существенно снизить уровень смертности [2–5]. Основными преимуществами эндоваскулярной методики по сравнению с открытой операцией являются меньшая травматичность, снижение кровопотери, сокращение времени операции, отказ от общей анестезии [3]. Первые сообщения о применении стент-графтов при разрыве аневризм датируются 1994 годом [6]. Спустя еще 5 лет, Ohki et al. опубликовали первую серию из 12 пациентов перенесших эндопротезирование при разрывах аневризмы [7]. На сегодняшний день доля эндоваскулярных вмешательств в развитых западных странах составляет от 10 до 30% [2–5]. Мы встретили всего лишь одну публикацию о применении эндопротезирования при разрыве аневризмы в России: в 2010 г. Максимов А.В. и соавт. произвели имплантацию унилатерального стент-графта, перекрестное бедренно-бедренное шунтирование и перевязку контрлатеральной общей подвздошной артерии [11]. Приводим собственное клиническое наблюдение.
Клиническое наблюдение
Пациент Б., 71 года, находился в ЦКБ РАМН с 21 января 2008 года с обострением язвенной болезни 12-ти перстной кишки, состоявшемся кровотечением из хронической язвы. Больному проводилась противоязвенная терапия, однако сохранялся болевой синдром, слабость. Боль в брюшной полости локализовалась в эпигастрии и мезогастрии. При дальнейшем обследовании по данным КТ от 07.02.08 была обнаружена аневризма брюшного отдела аорты до 42 мм в диаметре, парааортальная гематома справа от аорты. Аневризма была выявлена впервые. На основании данных КТ заподозрен разрыв, после консультации сосудистого хирурга, больной был переведен в городскую клиническую больницу № 57 г. Москвы. Из анамнеза известно, что у пациента с 30 декабря отмечается постоянный субфебрилитет. При поступлении состояние средней тяжести, эпизодов

потери сознания не отмечал. В легких ослабленное везикулярное дыхание, хрипов нет. ЧД 16 в мин. Сердечные тоны приглушены, ритмичные АД 120/70 мм рт. ст. пульс – 74 в мин. Живот мягкий, малоболезненный в мезогастрии, где пальпируется болезненное пульсирующее образование размерами 5 на 8 см. Перитонеальные симптомы отрицательные. Пульса- ция на нижних конечностях на всем протяжении, движения и чувствительность сохранены в полном объеме. Гемоглобин – 105 г/л, лейкоциты 5,1∙109 л. По данным УЗДС обнаружено аневризматическое расширение аорты на 3,5 см ниже почечных артерий, протяженностью 7,5 см, диаметром до 42 мм с пристеночными тромбами. Правая стенка с нечеткими контурами, нельзя исключить дефект стенки, в проекции лоцируются ткани сниженной эхогенности 5 на 3,5 см, нельзя исключить гематому. ОПА справа до 17 мм, слева ОПА до 10 мм. Сопутствующая патология: ИБС, атеросклероз. Язвенная болезнь 12-перстной кишки с периодическими обострениями. ХОБЛ. Дыхательная недостаточность 2 ст. в анамнезе – герниопласти-ка паховой грыжи слева (1970).
С учетом данных клиники, обследования больному был поставлен диагноз – осложненная аневризма брюшной аорты, разрыв (отграниченный) правой стенки аневризмы, забрюшинная гематома. Состояние больного стабильное, гемодина- мика нормальная. Проанализированы данные КТ, выявлено, что параметры аневризмы позволяют применить больному эндоваскулярное лечение. Исходя из параметров аневризмы, «шейки» и подвздошных артерий, было принято решение произвести пациенту имплантацию эндоваскулярной системы «Excluder, Gore». Под местным обезболиванием раствором новокаина 0,5% – 20,0 с обеих сторон из продольного разреза в верхней трети бедра выделены общие бедренные артерии в месте бифуркации. Установлены интродьюссеры 18 F. Произведена контрольная ангиография (рис. 1).
По жесткому проводнику 0,035 справа проведен Trunk Ipsilateral Endoprothesis (23 мм – 12 мм – 14 см) – основное тело эндопротеза, стент-графт раскрыт тот час ниже почечных арте- рий и установлен в позицию
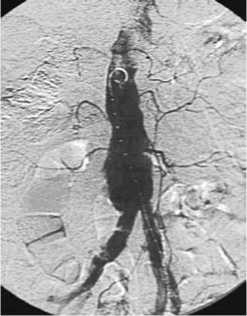
Рис. 1. Визуализация аневризмы – ангиограмма до проведения вмешательства
«аорта-правая ОПА». Раздувание проксимальной и дистальной порции баллоном низкого давления Z-MedII 23 мм – 3 см. Из левого интродьюссера в «окно» в аорту проведен жесткий проводник 0,035. По нему проведен Contralateral Leg Endoprothesis 16 мм – 11,5 см, установлен в позицию «аорта-левая ОПА». Раздувание проксимальной и дистальной порции баллоном низкого давления Z-MedII 23 мм – 3 см. При контрольной аорто-артериографии – полное исключение аневризмы из кровотока. Экстравазального контрастирования не выявлено (рис. 2).
Интродьюссеры удалены. Артериотомии ушиты отдельными швами Prolen 5,0 с обеих сторон. Швы на кожу. Асептические повязки. Интраоперационная кровопотеря составила 200 мл. Время операции составило 2 часа 35 мин. За время операции было перелито до 1500 мл растворов, диурез – 500 мл. Послеоперационный период протекал без осложнений. В реанимации проводилась инфузионная терапия, антибио-тикотерапия. На 2-е сутки был переведен в отделение. Швы сняты на 7 сутки после операции, пациент был выписан домой в удовлетворительном состоянии.
Отдаленный период
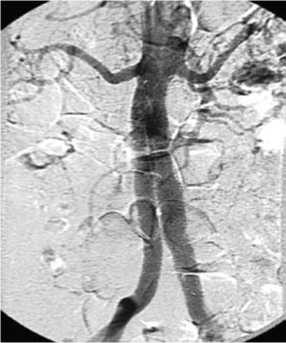
Рис. 2. Контрольная ангиограмма – после окончания эндоваскулярного этапа операции: полость аневризматическогомешкаисключена из кровообращения, почечные и подвздошные артерии проходимы, эндоликов не наблюдается
После проведенного лечения, пациент наблюдался каждые 6 месяцев первые 2 года, затем раз в год. При контрольных ультразвуковых исследованиях, КТ-ангиографии аневризма не увеличивается в размерах, стент-графт проходим, пристеночного тромбоза не определяется. Эндолики не выявлены (рис. 3, 4, 5). Абдоминальных болей больной не отмечает. Наблюдение за пациентом проводилось в течение 5 лет.
Обсуждение
Частота разрыва аневризмы брюшной аорты составляет 5,6–17,5 на 100 тыс. населения [8]. В западных странах этот
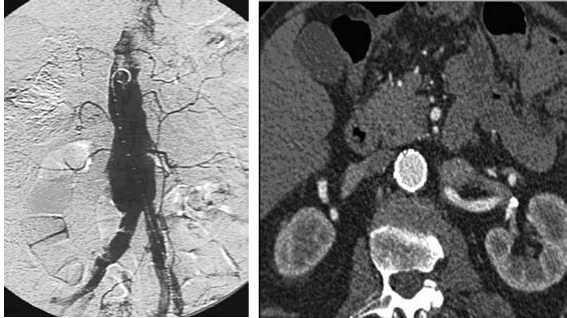
Рис. 4. Контрольная КТ (от 06.12.2012 – через 5 лет после вмешательства) – полость аневризматического мешка исключена из кровообращения, эндолики не наблюдаются
Рис. 3. Контрольная КТ (от 06.12.2012 – через 5 лет после вмешательства) – полость аневризматического мешка исключена из кровообращения, эндолики не наблюдаются

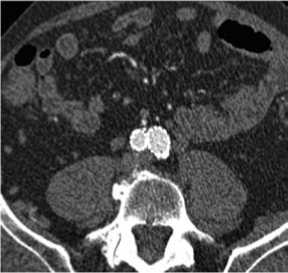
Рис. 5. Контрольная КТ (от 06.12.2012 – через 5 лет после вмешательства)– полость аневризматического мешка исключена из кровообращения, эндолики не наблюдаются
уровень снизился. Так, в США количество разрывов снизилась с 18,7/100 тыс. (в 1994 году) до 13,6/100 тыс. (в 2003) [1]. В первую очередь это связано с улучшением методов диагностики, а также с широким внедрением эндопротезирования, что позволило проводить вмешательства в плановом порядке больным с тяжелой сопутствующей патологией, которым ранее было отказано в проведении открытой операции. По данным
Kristina A. Giles, F. Pomposelli, в экстренных случаях доля эндоваскулярных вмешательств также растет. В 2000 году эндопротезирование выполнялось только в 1% от общего количества операций, к 2005 году эта процедура была выполнена уже в 15,5% случаев [9]. Однако применение этой методики при разрывах аневризм ограничивает ряд факторов, таких как наличие круглосуточной специализированной эндоваскулярной службы, расходного материала, определенные анатомические требования, предъявляемые к аневризме, а также организационными трудностями экстренной КТ-диагностики [5].
В нескольких исследованиях была достигнута более низкая смертность, чем при открытых операциях – от 12% до 53%. Самой низкой летальности смог добиться Veith. Его алгоритм проведения эндопротезирования заключается в следующем: поддержание гипотензивного гемостаза, при крайне тяжелом состоянии пациента установка стент-графта возможна без предварительного проведения КТ, операцию необходимо проводить в гибридной операционной, начинать под местной анестезией установкой интродьюсера трансфеморально, затем проводится установка окклюзионного баллона супраце-лиакально и его использование только при необходимости, предпочтение стоит отдавать унилатеральным конструкциям стент-графта, также необходимо следить за интраабдоминаль-ным давлением после операции, необходимо уделять внимание организации тренировки команды [10].
Заключение
На сегодняшний день имеют многочисленные данные о том, что в экстренных ситуациях количество осложнений и смертность при эндопротезировании аневризмы аорты значительно ниже, чем при открытой операции. Однако, для широкого вне- дрения эндопротезирования при разрывах аневризм необходимо множество предпосылок, в том числе наличие широкого выбора стент-графтов; специализированной, подготовленной, круглосуточной команды сосудистых и эндоваскулярных хирургов; анализ отдаленных результатов. Тем не менее у отдельных пациентов в хорошо оснащенных клиниках с достаточно квалифицированным и опытным персоналом эндоваскулярное протезирование при разрыве аневризмы брюшной аорты позволяет добиться хороших ближайших и отдаленных результатов.
Список литературы Пятилетний результат экстренного эндопротезирования аневризмы брюшной аорты при ее разрыве
- Dillavou E.D., Muluk S.C., Makaroun M.S. A decade of change in abdominal aortic aneurysm repair in the United States: have we improved outcomes equally between men and women?//J. Vasc. Surg. 2006. Vol. 43. P. 230-238.
- Antonopoulos C.N., Andrikopoulos V., Antoniadis et al. Rupture after EVAR and EVAR for Rupture: an Interactive Relation//J. Vasc. Surg. 2012. Vol. 4. P. 102.
- Azizzadeh A., Villa M.A., Miller 3rd C.C. et al. Endovascular repair of ruptured abdominal aortic aneurysms: systematic literature review//Vascular. 2008. Vol. 16(4). P. 219-224.
- Dillon M., Cardwell C., Blair P.H. et al. Endovascular treatment for ruptured abdominal aortic aneurysm//Cochrane Database Syst. Rev. 2007. Vol. 1. P. 1-134.
- Moll EL., J.T. Powell J.T., Fraedrich G. Management of Abdominal Aortic Aneurysms Clinical Practice Guidelines of the European Society for Vascular Surgery//J. Vasc. Surg. 2011. Vol. 41. P. 1-58.
- Yusuf S.W., Whitaker S.C., Chuter T.A. et al. Emergency endovascular repair of leaking aortic aneurysm//Lancet. 1994. Vol. 344. P. 1645.
- Ohki T., Veith F.J., Sanchez L.A. et al. Endovascular graft repair of ruptured aortoiliac aneurysms//J. Am. Coll. Surg. 1999. Vol. 189. P. 102113.
- Bengtsson H., Bergqvist D. Ruptured abdominal aortic aneurysm: a population-based study//J. Vasc. Surg. 1993. Vol. 18. P 74-80.
- Kristina A. Giles, Allen D. Hamdan. Population-Based Outcomes Following Endovascular and Open Repair of Ruptured Abdominal Aortic Aneurysms//J. Endovasc. Ther. 2009. Vol. 16. P 554-564.
- Veith F.J., Cayne N.S., Berland T.L. et al. Current role for endovascular treatment of ruptured abdominal aortic aneurysms//Semin. Vasc. Surg. 2012. Vol. 25(3). P 174-176.
- Максимов А.В., Хасанов Р.Н., Халилов И.Г. и соавт. Экстренное эндопротезирование при разрыве аневризмы брюшной аорты//Ангиология и сосудистая хирургия. 2011. Т. 17, №2. С. 65-68.


