Побочные эффекты длительной антиаритмической терапии амиодароном
Автор: Дорофеева Наталья Петровна, Иванченко Дарья Николаевна, Машталова Ольга Георгиевна, Куликова Ирина Евгеньевна, Чибинева Светлана Анатольевна, Тер-Акопян Александра Ованесовна, Скляров Федор Викторович, Кияшко Екатерина Евгеньевна
Журнал: Клиническая практика @clinpractice
Рубрика: Случай из практики
Статья в выпуске: 1 (29), 2017 года.
Бесплатный доступ
Распространенность фибрилляции предсердий подразумевает широкое применение антиаритмических препаратов, в частности, амиодарона. В качестве побочных эффектов применения данного препарата наиболее часто упоминается поражение щитовидной железы. В статье рассмотрен клинический случай развития у пациента с фибрилляцией предсердий фотосенсибилизации, которую редко можно наблюдать в клинической практике.
Фибрилляция предсердий, амиодарон, побочные эффекты, фотосенсибилизация, клинический случай
Короткий адрес: https://sciup.org/143164630
IDR: 143164630
Side effects of prolonged antiarrhythmic therapy with amiodarone
Atrial fibrillation is widespread in population. It determines extensive use of antiarrhythmic drugs such as amiodarone. Thyroid lesion is one of common side effects of this therapy. The article describes a clinical case of photosensitivity’s development in the application of amiodarone
Текст научной статьи Побочные эффекты длительной антиаритмической терапии амиодароном
Фибрилляция предсердий представляет собой наиболее часто встречаемое нарушение ритма сердца. Частота ее выявления в общей популяции составляет 1-2%. Распространенность фибрилляции предсердий предопределяет широкое назначение пациентам анти-аритмических препаратов. Одним из наиболее широко испольуемых антиаритмических препаратов является амиодарон, который назначается для профилактики и лечения желудочковых и наджелудочковых аритмий. Предпосылками применения амиодарона являются его способность оказывать влияние как на суправентрикулярные, так и на желудочковые тахиаритмии, а также тот факт, что он эффективен как при нормальной, так и при сниженной систолической функции ЛЖ [1, 2]. Амиодарон был открыт в 1961 году и первоначально был представлен как антиангинальный препарат. Лишь в 1970 году были открыты его антиаритмический и антифи-брилляторный эффекты.
Амиодарон относится к III классу анти-аритмических препаратов по классификации Vaughan Williams. Его уникальность обусловлена также способностью неконкурентно ингибировать альфа- и бета-адренорецепторы, инактивировать калиевые каналы, быстрые натриевые каналы в мембране кардиомиоцитов. Он обладает свойствами антагонистов кальция и периферических вазодилататоров. Особенностью фармакокинетики препарата является его кумуляция в жировой ткани и продолжительный период полувыведения, который также может варьировать в широких пределах и составлять от 25 до 110 суток. Следует отметить, что пациенты с нарушениями ритма сердца постоянно принимают несколько лекарственных препаратов. В связи с этим весьма актуаль- ной представляется проблема лекарственных взаимодействий. Так, известно, что повышение концентрации амиодарона в крови может быть вызвано приемом препаратов из группы статинов, дигоксина, варфарина, некоторых антагонистов кальция и ряда других, что обусловлено взаимодействием через систему цитохрома Р450. Среди побочных эффектов терапии амиодароном можно выделить поражение щитовидной железы (<35%), пневмопатию (1-17%), неврологические расстройства (3-35%), фото-токсические и аллергические кожные реакции.
Преимущественное поражение щитовидной железы обусловлено химической структурой препарата, содержащим 37% йода (в одной таблетке 200 мг содержится 75 мг йода), кроме того имеющего существенное структурное сходство с гормонами щитовидной железы. В процессе метаболической трансформации из каждых 200 мг амиодарона высвобождается примерно 6-9 мг неорганического йода, что в 50–100 раз превышает суточную потребность в элементе. Именно поэтому вероятность развития нежелательных реакций прогрессивно возрастает с увеличением дозы и продолжительности приема. Примерно 30% больных вынуждены прекращать прием антиаритмических препаратов из-за выраженных побочных эффектов. Это является особенно актуальным среди пациентов, получающих амиодарон с целью восстановления синусового ритма, а через годы вызывающее появление тяжелого тиреотоксикоза. И решение о дальнейшем восстановлении ритма откладывается до нормализации показателей гормонов щитовидной железы.
Под фототоксичностью понимают изменение цвета кожных покровов от серо-голубого до свинцового оттенка. Встречается она в 1% случаев применения терапии препаратом. Патоморфологически характеризуется отложением липофусцина в лизосомах дермы [3]. Может сохраняться продолжительное время [4].
В качестве иллюстрации представляем клинический случай, который демонстрируют описанные нежелательные эффекты амиодарона, а именно – изменение цвета кожных покровов с нормальных физиологических до сероголубого цвета и возникновение амиодарон-индуцированного тиреоидита.
Пациент Г. поступил в кардиологическое отделение Ростовской клинической больницы с основными жалобами на перебои в работе сердца, боли ноющего характера без четкой вза- имосвязи с физической нагрузкой. Кроме того, пациент обращал внимание на повышение артериального давления до 150/90 мм рт. ст., снижение массы тела на 6 кг в течение 3 месяцев.
Из анамнеза заболевания известно, что у больного в 2002 году впервые был зарегистрирован пароксизм фибрилляции предсердий (ФП). По данному факту он был госпитализирован в центральную районную больницу, где синусовый ритм удалось восстановить с использованием амиодарона в суточной дозе 600 мг, что соответствует среднетерапевтической дозировке. При выписке из стационара пациенту были даны рекомендации о последующем приеме амиодарона в дозе 200 мг по 1 таблетке 2 раза в день в течение 5 дней с последующим двухдневным перерывом и дальнейшим переходом на поддерживающую дозу 200 мг в сутки.
Однако полученные при выписке рекомендации пациент не выполнял и самостоятельно повысил дозу амиодарона до 8 таблеток в сутки (с достижением суточной дозы 1600 мг), которую принимал на протяжении последующих девяти лет. Впоследствии, к 2005 году появилось изменение окраски кожных покровов в местах контакта с солнечными лучами, начала уменьшаться масса тела. В 2011 году отметил ухудшение состояния, а именно – увеличились частота и интенсивность эпизодов сердцебиений, перебоев в работе сердца, болей за грудиной. На электрокардиограмме была снова зарегистрирована фибрилляция предсердий. Пациент продолжал прием амиодарона в той же дозе.
С октября 2015 года больной отменил препарат самостоятельно и начал принимать соталол в дозировке 40 мг в день. Помимо антиаритми-ческой терапии, регулярно принимал стандартную комбинацию кандесартана и гидрохлорти-азида в дозе 16/12,5 мг в сутки, варфарин 5 мг в сутки.
При поступлении объективно было выявлено, что кожные покровы лица, ушных раковин, верхней части шеи были серо-голубого цвета, окраска кожных покровов остальной поверхности тела без особенностей (рис. 1).
В легких дыхание везикулярное, хрипов, крепитаций не выслушивалось, частота дыхания составляла 18 в минуту. Со стороны сердечно-сосудистой системы было выявлено, что пульс на лучевой артерии слабого наполнения, аритмичен с частотой сердечных сокращений порядка 78 ударов в минуту, пульс – 72 удара в минуту. Дефицит пульса составил 6 уда-
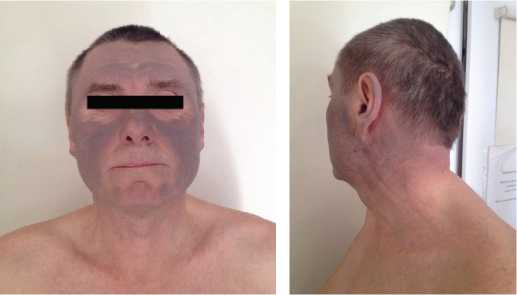
Рис. 1. Фотосенсибилизация кожных покровов у пациента Г. на фоне терапии амиодароном.
ров в минуту. Перкуторно границы сердца расширены влево на 1 см. Аускультативно тоны сердца аритмичны, приглушены. Артериальное давление было на уровне 125/80 мм рт. ст.
Лабораторно общий анализ крови без особенностей, рутинные биохимические показатели – в пределах нормальных значений. По данным коагулограммы дозировка принимаемого варфарина была адекватной, Международное нормализованное отношение было на уровне 2,3. Обращали на себя внимание лабораторные признаки нарушения функции щитовидной железы: уровень тиреотропного гормона составил 0,01 ММЕ/мл, свободного тироксина – 57,12 пмоль/л. Инструментально на электрокардиограмме определялись фибрилляция предсердий с частотой сердечных сокращений (ЧСС) 110-62 удара в минуту, нарушение внутрижелудочковой проводимости. В динамике было достигнуто снижение ЧСС до 92-50 ударов в минуту.
На эхокардиограмме были выявлены дилатация левого предсердия до 42 мм., повышение давления в легочной артерии до 37 мм рт. ст. с сохранной фракцией выброса левого желудочка (72%). При проведении УЗИ щитовидной железы обнаружены мелко-узловые образования обеих долей (максимально 7х6 мм).
На фоне проведенной в стационаре терапии состояние пациента улучшилось: уменьшились перебои в работе сердца, повысилась толерантность к физической нагрузке, гемодинамика стабилизировалась, пациент был выписан с рекомендациями по приему бисопролола 5 мг, инда-памида + периндоприла 2,5/0,625 мг, варфарина 5 мг, аторвастатина 20 мг.
При выписке из стационара пациенту была рекомендована терапия тиреостатиками (тиама-зол) в дозе 30 мг в сутки. Через 1 месяц амбула- торной тиреостатической терапии наблюдалась положительная динамика гормонов щитовидной железы: уровень свободного тироксина составил 23 пмоль/л, уровень тиреотропного гормона оставался 0,014 ММЕ/мл, свободный трийодти-ронин был на уровне 4,64 пмоль/л. Была уменьшена доза тиамазола до 20 мг/сутки. Проведен контроль гормонов щитовидной железы через 1 месяц: нормализация уровня тиреотропного гормона до 0,37 ММЕ/мл, общего тироксина до 106 нмоль/л, что соответствует нормативным значениям.
После стабилизации функции щитовидной железы пациент был госпитализирован в отделение сердечно-сосудистой хирургии Ростовской клинической больницы ЮОМЦ ФМБА России с целью проведения изоляции устьев легочных вен методом криодеструкции. При поступлении на электрокардиограмме определялись фибрилляция предсердий с ЧСС 75-85 ударов в минуту, нарушение внутрижелудочковой проводимости. На эхокардиограмме выявлялись дилатация левого предсердия до 45 мм, давление в легочной артерии 23 мм рт.ст. с сохранной фракцией выброса левого желудочка (59%). Повторное ультразвуковое исследование щитовидной железы не проводилось.
По данным мультиспиральной компьютерной томографии легочных вен и левого предсердия было выявлено увеличение размеров левого предсердия до 74х50х77 мм. Объем левого предсердия с учетом ушка превышал в 2 раза нормальные значения, составляя 180 мл. Правые верхняя и нижняя, а также левая верхняя легочные вены незначительной увеличены (до 19-20 мм).
Криовоздействие проводилось под общей анестезией. После выполнения двух криовоздействий в устье каждой легочной вены на электрокардиограмме был зарегистрирован синусовый ритм.
Учитывая, что интоксикация амиодароном у пациента происходила в течение девяти лет, а первые изменения со стороны кожных покровов появились уже спустя три года от начала использования антиаритмика, токсичный дозозависимый эффект в данном случае наступил при применении 1600 мг препарата на протяжении трех лет. Обращает также внимание тот факт, что, даже несмотря на имевшийся перерыв в приеме препарата в течение шести месяцев, предшествовавших первой госпитализации, интенсивность серого оттенка кожи сохранялась, что свидетельствовало о длительных фар- макодинамическом эффекте и периоде полувыведения.
Клинический интерес описанного нами случая состоит в том, что акцентирует внимание клинициста на риск фотосенсибилизации кожных покровов пациента и поиск амиодарон- индуцированных состояний. В данном случае они развилась вследствие отсутствия комплаент-ности к назначаемой антиаритмической терапии. Кроме того, наличие йода в составе амиодарона повышает вероятность поражения щитовидной железы, что также отмечалось у нашего больного.
Список литературы Побочные эффекты длительной антиаритмической терапии амиодароном
- Singh, B.N. Amiodarone as paradigm for developing new drugs for atrial fibrillation. J Cardiovasc Pharmacol 2008; 52: 300-305.
- Vassallo P. and Trohman R.G. Prescribing amiodarone: An evidence-based review of clinical indications. JAMA 2007; 298: 1312-1322.
- Harris L., McKenna W.J., Rowland E. et al. Side effects of long-term amiodarone therapy. Circulation 1983; 67:45-51.
- Blackshear J.L. Randle H.W. Reversibility of blue-gray cutaneous discoloration from amiodarone. Mayo Clin Proc 1991; 66:721-726.


