Подходы к получению и применению микробной трансглутаминазы в эмульгированных мясорастительных системах
Автор: Глотова И.А., Курчаева Е.Е., Ухина Е.Ю., Рязанцева А.О.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Биотехнология и бионанотехнология
Статья в выпуске: 4 (74), 2017 года.
Бесплатный доступ
В технологии традиционных и новых форм пищи модификацию структуры белков проводят в двух противоположных направлениях – гидролитическая деструкция высокомолекулярных полимеров и искусственное создание полимерных структур высокой молекулярной массы. Для реализации второго направления используют препараты трансглутаминазы (протеин-глутамин (-глутамилтрансфераза, НФ 2.3.2.13, ТГ). Основными механизмами воздействия являются реакции полимеризации, которые приводят к изменению гидрофобности белковых молекул. Основными катализируемыми реакциями являются ацильный перенос, связывание между глутаминовым и лизиновым остатками белков и дезаминирование. Авторами проанализированы подходы к получению, свойства и исследовано совместное влияние температуры и рН на активность коммерческого препарата Revada TG 11 с применением энзиматического колориметрического теста. Исследованы комбинированные фаршевые системы на основе говядины, свинины, мяса птицы механической обвалки, а также с заменой части сырья на белково-углеводные композиции с препаратом Revada TG 11. Результаты использованы для разработки имитирующих мясные системы биополимерных композиций (ИМСБК), приближенных по структуре и свойствам к гелям, формируемым актином и миозином при экстрагировании из миофибрилл в условиях традиционных технологических процессов производства мясопродуктов – созревание, посол, тонкое измельчение мяса. В состав ИМСБК включены биоактивированная проращиванием мука люпина, препараты пищевых волокон, препарат трансглутаминазы Revada TG 11. Для баланса аминокислотного состава пищевой композиции использовали белковые компоненты вторичных сырьевых ресурсов при переработке молока – казеинат натрия, а также молочную сыворотку. Для практического использования рекомендованы следующие варианты внесения ИМСБК в состав мясных фаршевых эмульсий: в виде гидратированной биополимерной дисперсии при куттеровании; в виде предварительно термообработанного геля
Трансглутаминаза, трансглутаминазная активность, культивирование, ферментация, мясо-растительные системы, биоактивированная люпиновая мука, белково-углеводные композиции
Короткий адрес: https://sciup.org/140229906
IDR: 140229906 | DOI: 10.20914/2310-1202-2017-4-210-219
Approaches to the production and use of microbial transglutaminase in emulsified meat and vegetable systems
In the technology of traditional and new forms of food, the modification of structure of proteins is carry out in two opposite directions: the hydrolytic destruction of high-molecular polymers and the artificial creation of polymeric structures of high molecular mass. The transglutaminase preparations (protein-glutamine (-glutamyltransferase, EC 2.3.2.13, TG) are used in practical work for realization of the second direction. The main mechanisms of action are polymerization reactions, which lead to a change in the hydrophobicity of protein molecules. The main catalyzed reactions are acyl transfer, binding between glutamine and lysine residues of proteins and deamination. The authors analyzed the approaches to the preparation, properties and studied the joint effect of temperature and pH on the activity of the commercial preparation Revada TG 11 with the application of an enzymatic colorimetric test. The authors studied combined stuffing systems based on beef, pork, poultry mechanical deboning, as well as replacing part of the raw material with protein-carbohydrate compositions with Revada TG 11. The results were used to develop simulated meat systems of biopolymer compositions (SMSBC), approximate in structure and properties to the gels formed by actin and myosin during extraction from myofibrils under the traditional technological processes of meat products production - maturation, salt curing, fine meat grinding. SMSBC includes lupine flour bio-activated by germination, a preparations of dietary fiber as well as a preparation of transglutaminase Revada TG 11. The protein components of the secondary raw materials during the processing of milk such as sodium caseinate, and also whey were used to balance the amino acid composition of the food systems. For practical use, the following options for SMSBC introducing into the composition of minced meat emulsions were recommended by the authors: in the form of hydrated biopolymer dispersion at cutting; in the form of a previously heat-treated gel.
Текст научной статьи Подходы к получению и применению микробной трансглутаминазы в эмульгированных мясорастительных системах
Работы в области модификации структуры белков с применением экзогенных ферментных препаратов применительно к технологии традиционных и новых форм пищи ведутся в двух противоположных направлениях. С одной стороны – гидролитическая деструкция высокомолекулярных биополимеров (тендеризация низкосортного мясного сырья, повышение переваримости и усвояемости белковых продуктов, в том числе
для специализированного питания); с другой – искусственное создание полимерных структур высокой молекулярной массы за счет использования препаратов трансглутаминазы (протеин-глутамин γ -глутамилтрансфераза, НФ 2.3.2.13, ТГ).
В связи с высокой трудоемкостью выделения и очистки ТГ из животных источников усилия зарубежных исследователей в предшествующее десятилетие были направлены на поиск продуцентов и разработку промышленной биотехнологии
получения микробных ТГ, удовлетворяющих требованиям пищевой промышленности по соотношению «степень очистки – себестоимость коммерческих препаратов».
Ассортимент препаратов ТГ на отечественном рынке комплексных пищевых добавок, в соответствии с терминологией Технического регламента Таможенного Союза ТР ТС 029/2012 «Требования безопасности пищевых добавок, ароматизаторов и технологических вспомогательных средств», представлен коммерческими марками фирм-производителей из Китая – BioBond («Shanghai Kinry Pharmaceutical Co., Ltd.»), Японии – ACTIVA («Аджиномото Ко. Инк.»), Западной Европы – Probind TX, Revada TG (BDF Natural Ingredients, Испания). В сопроводительных документах представлены краткие рекомендации по условиям использования препаратов ТГ при переработке разных видов сельскохозяйственного сырья, преимущественно животного происхождения, относительно температуры и рН среды. Сведения о продуцентах и биотехнологических процессах получения, выделения и очистки ТГ из микробных источников весьма ограничены, нуждаются в анализе и систематизации [1–3].
Цель работы – проанализировать подходы к получению, свойства и исследовать совместное влияние факторов внешней среды на активность коммерческого препарата Revada TG 11 с позиций последующей разработки имитирующих мясные системы биополимерных композиций
(ИМСБК), приближенных по структуре и свойствам к гелям, формируемым актином и миозином при экстрагировании из миофибрилл в условиях традиционных технологических процессов производства мясопродуктов – созревание, посол, тонкое измельчение мяса.
Материалы и методы исследования
Объектами исследования служили:
─ биосистемы растительного происхождения в виде комплексов биополимеров, макро-, микроэлементов, витаминов, других биологически активных веществ в их естественном соотношении (биоактивированная мука из семян люпина сорта Гамма), выбор которых обоснован рекомендациями [4, 5];
─ концентрированные формы балластных веществ при переработке растительного сырья в виде препаратов пищевых волокон с различными коммерческими названиями, характеристика которых, по данным [6], представлена в таблиц е 1;
─ коммерческие препараты вспомогательных технологических средств, обладающих протеин-глутамин γ -глутамилтрансферазной активностью, в частности, препарат Revada TG 11 (производитель BDF Natural Ingredients, Испания), при совместном использовании в составе гидратированных белково-углеводных композиций;
─ комбинированные фаршевые системы на основе говядины, свинины, мяса птицы механической обвалки и с заменой части сырья на белково-углеводные композиции с препаратом Revada TG 11.
Таблица 1.
Сравнительная характеристика различных видов клетчаток Витацель
Table 1.
Comparative characteristics of various types of fibers Vitacel
|
Показатель | Index |
Вид клетчатки Витацель Type of fiber Vitacel |
||||||
|
WF-200R пшеница wheat |
WF-400R пшеница wheat |
WF-600R пшеница wheat |
HF 401 овес oats |
PF 200 растительная vegetable |
AF 400 яблоко Apple |
AF 12 яблоко Apple |
|
|
Цвет | Colour |
белый | white |
бело-серый white-gray |
светло-коричный light cinnamon |
||||
|
Структура | Structure |
Волокно | Fiber |
Частицы волокон Fiber particles |
Частицы волокон грубого помола Fiber particles coarsely ground |
||||
|
Содержание балластных веществ, % The content of ballast substances, % |
≥97 |
≥97 |
≥97 |
≥90 |
≥88 |
≥60 |
≥60 |
|
Средняя длина волокон, мкм Average length of fibers, microns |
250 |
500 |
80 |
350 |
160 |
300 |
900 |
|
Насыпная масса, г/дм3 Bulk density, g/dm3 |
85 |
50 |
220 |
350 |
160 |
450 |
460 |
|
Водосвязывающая способность, % Water-binding capacity, % |
830 |
1050 |
550 |
350 |
1200 |
500 |
500 |
|
Жиросвязывающая способность, % Adhesive ability, % |
690 |
1100 |
370 |
250 |
450 |
- |
- |
|
Энергетическая ценность, кДж/100г Energy value, kJ/100g |
0.37 |
0.25 |
0.54 |
5.77 |
4.85 |
||
Активность ТГ определяли с помощью энзиматического колориметрического теста в соответствии с рекомендациями [7]. В основе метода лежит каталитическая реакция переноса глутаминовой кислоты на акцептор, подобный глицил-глицину, с образованием 5-амино-2-нит-робензоата в соответствии со схемой:
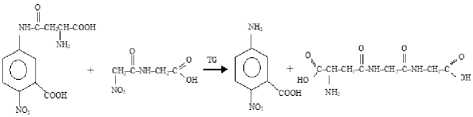
При этом скорость образования 5-амино- 2-нитробензоата прямо пропорциональна активности трансглутаминазы. Количественную идентификацию продукта реакции проводили на фотоэлектроколориметре КФК-2 при X = 405 нм. Для расчета использовали прямо пропорциональную зависимость между поглощением при указанной длине волны и активностью ТГ.
Для расчета целевой активности (ТГ, ед./г) использовали формулу:
ТГ = (А - А)хК, где А1 и А2 – оптическая плотность испытуемого раствора соответственно при первом измерении и проведенном через одну минуту после первого; К – коэффициент пересчета, зависящий от условий проведения измерений; при данных концентрациях реагентов К = 1158 ед./л).
Центральное композиционное ротата-бельное планирование эксперимента (ЦКРП) проводили по плану ПФЭ 22. В качестве основных факторов были выбраны: х 1 – температура, °С; х 2 – реакция среды, рН. Эти факторы совместимы и не коррелированы между собой. Критерием оценки влияния выбранных факторов была выбрана y – активность фермента, ед./г. Порядок опытов рандомизировали посредством таблицы случайных чисел, что исключает влияние неконтролируемых параметров на результаты эксперимента [8, 9].
При обработке экспериментальных данных использовали рекомендации, изложенные в ГОСТ 50779.21 [10]. В нем описаны основные способы и процедуры определения статистических характеристик нормально распределенных данных. Программным средством реализации обработки служил пакет «STATISTICA», включающий набор процедур построения плана многофакторного эксперимента, анализа полученных данных и выявления вида зависимости между входными факторами и выходными параметрами.
Для исследования микроструктуры мясных и мясо-растительных эмульсий использовали классические морфологические методы [11].
Образцы, предназначенные для исследования, фиксировали в растворе нейтрального формалина с объемной долей 10%. Обезвоживание образцов проводили в спиртах восходящей концентрации, затем образцы заливали в гомогенизированную парафиновую среду HISTOMIX. Для окрашивания использовали гематоксилин-эозин, в качестве ядерного красителя применяли квасцовый гематоксилин Бёмера, в качестве основного – спиртовой эозин. Изготовление срезов проводили на микротоме МПС-2, для просмотра и съемки полученных изображений использовали цифровую фотоустановку, смонтированную на базе отечественного микроскопа БИОМЕД-5 и цифровой фотокамеры CANON.
Результаты и обсуждение
Микробная трансглутаминаза (ТГ) – фермент класса трансфераз, популярный у производителей пищевой продукции как «биоинструмент», позволяющий целенаправленно изменять функциональные свойства белка в пищевых системах. Основными механизмами воздействия являются реакции полимеризации, которые приводят к изменению гидрофобности белковых молекул в соответствии с приведенными авторами [1, 2, 12] схемами реакций ацильного переноса, связывания между глутаминовым и лизиновым остатками белков и дезаминирования.
В качестве источника препарата микробной ТГ разными исследователями были апробированы штаммы-продуценты S. griseocarneum, S. cinnamoneum, S. mobaraense (табл. 2), однако в промышленных масштабах наиболее эффективно используется бактериальная экспресивная система S. mobaraense . Основными стадиями процесса промышленного получения моноферментного препарата микробной ТГ (рисунок 1) являются культивирование посевного материала в течение 48 ч, при этом в качестве источника углерода используют глюкозу, а в качестве источника азота – пептон; ферментация в условиях, представленных в таблице 2. Дозировка посевного материала составляет 1–2% к объему культуральной жидкости в ферментере. Жидкую фракцию культуральной жидкости отделяют центрифугированием с последующей очисткой, однако стадии ультрафильтрации, гельфильтрации и ионного обмена более применимы для препаративного выделения и исследования препаратов ферментов. В качестве наполнителя при получении коммерческих препаратов трансглутаминазы широко используется мальтодекстрин. Известное положительное действие мальтодекстрина в технологии мясопродуктов состоит в ускорении процесса диффузии соли в мышечную ткань, стимуляции процессов связывания влаги белковыми структурами и образовании ароматобразующих соединений [13].
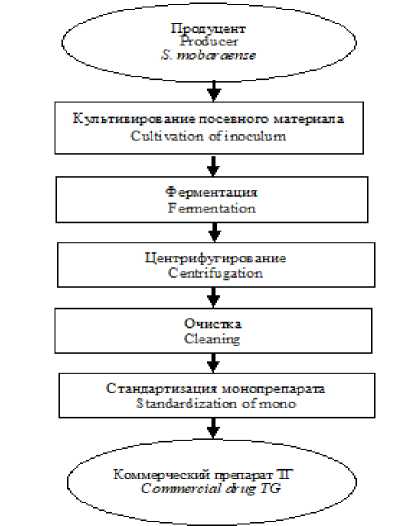
Рисунок 1. Схема получения коммерческого препарата трансглутаминазы
Figure 1. Scheme of preparation of a commercial preparation of trаnsglutаminаsе
С целью обоснования рекомендаций по использованию препарата ТГ для модифи-каци поликомпонентных мясо-растительных эмульгированных субстратов на первом этапе были проведены однофакторные эксперименты по исследованию влияния температуры и рН среды на активность ТГ в составе препарата Revada TG 11. Выбранная нижняя граница температурного интервала (рисунок) соответствует технологически целесообразным значениям данного параметра на этапе куттерования при получении фаршевых эмульсий.
Table 2.
|
Штаммы-продуценты Strains-producers |
Условия культивирования Conditions for cultivation |
Авторы и год публикации Authors and year of publication |
|
|
Температура, °С |
рН среды |
||
|
S. griseocarneum S. cinnamoneum S. mobaraense |
30 |
7,0* |
Gerber U., Jucknischke U., Putzien S., Fuchsbauer H.L., 1994 |
|
S. cinnamoneum |
28 |
7,0–7,4** |
Junqua M., Duran R., Gancet C., Goulas P., 1997 |
|
S. mobaraense |
28 |
6,5** |
Zhu Y., Tramper J., 2008 |
Примечание. * – стабильное значение; ** – регулирование во время биосинтеза Note. * – stable value; ** – regulation during biosynthesis
Таблица 2.
Данные о культивировании микробных источников ТГ
Data on the cultivation of microbial sources of TG
На рисунках 2–3 представлены зависимости активности трансглутаминазы от температуры и реакции среды, вид и выявленные экстремумы которых согласуются с более ранними результатами исследования физико-химических свойств микробной трансглутаминазы (Н.В. Мотина, 2007). Важное значение имеют условия инактивации ферментного препарата в процессе термической обработки продукта при доведении его до кулинарной готовности. Для определения условий инактивации трансглутаминазы раствор, содержащий ферментный препарат, инкубировали в течение 10 мин в термостате в интервале температур 50– 75 °C с шагом 5 °С. Установлено, что полная инактивация трансглутаминазы «REVADA TG 11» при температуре 70 °С происходит в течение 20 мин, при температуре 75 °С – в течение 7 мин.
Для исследования взаимодействия температуры и рН среды в качестве основных факторов, влияющих на активность трансглутаминазы, были применены математические методы планирования эксперимента. Результаты представлены в таблиц е 3.
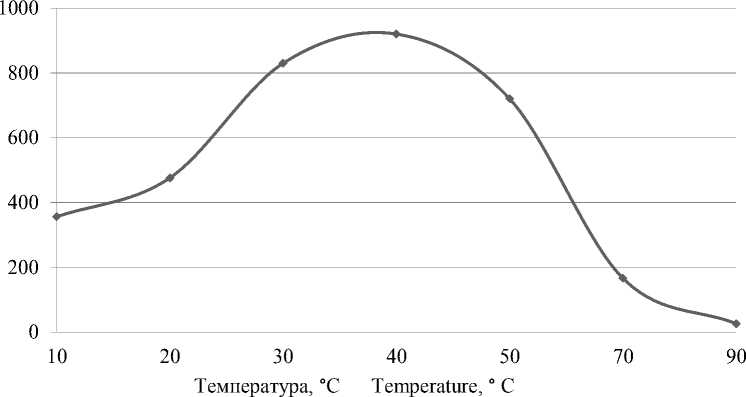
Рисунок 2. Зависимость активности трансглутаминазы от температуры
Figure 2. Dependence of the activity of transglutaminase on temperature
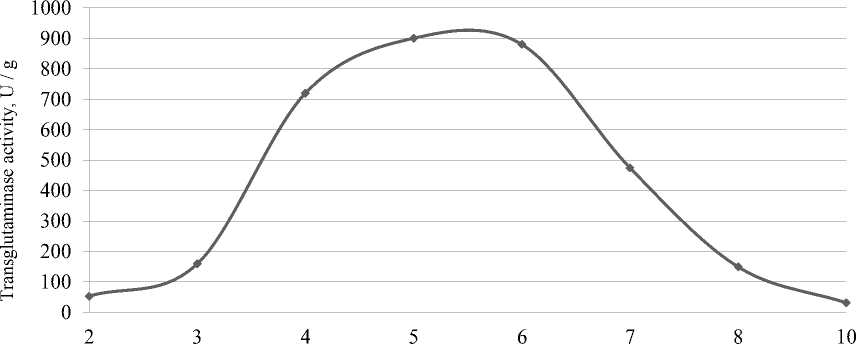
рН
Рисунок 3. Влияние реакции среды на активность трансглутаминазы
Figure 3. Influence of the reaction of the medium on the activity of trаnsglutаminаsе
Таблица 3.
Матрица Центрального Композиционного Ротатабельного Плана
Table 3.
Matrix of the Central Composite Rotatable Plan
|
Номер опыта Number of experience |
Кодированные значения факторов Coded factor values |
Натуральные значения факторов The natural values of factors |
Функция отклика Response function |
||
|
Х 1 |
Х 2 |
х 1 , С |
х 2 , рН |
y, ед./г |
|
|
1 |
+ |
+ |
60 |
8 |
112 |
|
2 |
- |
+ |
20 |
8 |
610 |
|
3 |
+ |
- |
60 |
4 |
504 |
|
4 |
- |
- |
20 |
4 |
640 |
|
5 |
+1,41 |
0 |
68,2 |
6 |
95 |
|
6 |
-1,41 |
0 |
11,8 |
6 |
65 |
|
7 |
0 |
+1,41 |
40 |
8,82 |
180 |
|
8 |
0 |
-1,41 |
40 |
3,18 |
830 |
|
9 |
0 |
0 |
40 |
6 |
886 |
|
10 |
0 |
0 |
40 |
6 |
890 |
|
11 |
0 |
0 |
40 |
6 |
891 |
|
12 |
0 |
0 |
40 |
6 |
890 |
|
13 |
0 |
0 |
40 |
6 |
887 |
В результате статистической обработки экспериментальных данных по известной методике получено уравнение регрессии, адекватно описывающие зависимость активности ферментного препарата от исследуемых факторов:
Y = 89,687 х + 618,966 х. - 2,263 хх -
1 2 12
-
- 0,905 х 2 - 37,045 х 2 2 - 3088,56
Анализируя полученное уравнение, приходим к выводу, что на ферментативную активность наибольшее влияние оказывает реакция среды, в 7 раз меньшее значение для изменения величины активности фермента имеет температуры среды. Причем, следует отметить, что оба входных фактора «положительно» влияют на увеличение активность фермента, т. к. коэффициенты уравнения регрессии – положительны, то с возрастанием значений температуры и реакции среды значение активности фермента будет увеличиваться, пока не достигнет своего максимального значения. Коэффициенты уравнения, находящиеся при произведении (х 1 ·х 2 ), имеют несколько меньшие значения по сравнению с коэффициентами при х 1 и х 2 , что свидетельствует о том, что совместное, влияние входных факторов на значение выходного параметра – ниже и носит «отрицательный» характер. А также, несмотря на то, что уравнение (1) является квадратичным полиномом, однако, коэффициенты при его членах во второй степени незначительны, что несущественно отражается на величине выходного параметра (оптимальное значение активности).
Поверхность отклика, описываемая уравнением (1), представлена на рисунке 4. Максимальное значение в области эксперимента имеет функция отклика при значениях х 1 = 0, х 2 = 0 в кодированных значениях переменных.
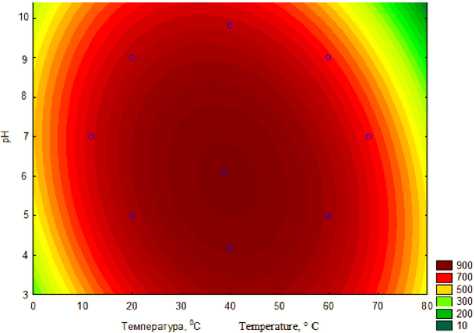
Рисунок 4. Области равных значений активности фермента в качестве функции отклика
Переходя от кодированных значений факторов к натуральным, получаем оптимальные условия для действия трансглутаминазы: х 1 = 40 °С; х 2 = 6,0 ед. рН. При этом функция отклика у приобретает значение 888,0 ед./г.
Полученные результаты использованы при обосновании способов внесения белково-углеводных композиций в состав мясорастительных эмульсий. С учетом современных тенденций развития отрасли животноводства в структуре АПК и популярности продуктов переработки мяса сельскохозяйственных животных и птицы у потребителей, в качестве модельной мясной системы использовали фаршевую эмульсию состава: говядина высшего сорта – свинина полужирная в соотношении 1:1. На следующем этапе в эмульсию вводили мясо птицы механической обвалки и имитирующую мясную систему биополимерную композицию (ИМСБК) с получением соотношения компонентов 1:1,5:1,75:0,75.
В состав ИМСБК входили биоактивиро-ванная проращиванием мука люпина при гидратации 1:1, гидратированные пищевые волокна Витацель WF-200R из перечня, приведенного в табл. 1, препарат трансглутаминазы Revada TG 11. Для баланса аминокислотного состава пищевой композиции использовали белковые компоненты вторичных сырьевых ресурсов при переработке молока – казеинат натрия, а также молочную сыворотку, перспективы которой как «универсального биоэкосырья» в комбинированных пищевых системах, по терминологии, введенной академиком А.Г. Храмцовым, доказаны рядом авторов [14, 15].
Для практической апробации использовали следующие варианты внесения ИМСБК в состав мясных фаршевых эмульсий:
-
1) в составе виде гидратированной биополимерной дисперсии при куттеровании;
-
2) в виде предварительно термообработанного при 40 °С геля.
При анализе структурной организации фаршевых систем применяли методы световой микроскопии в тонких срезах для выявления равномерности распределения составных частей фарша, их взаимоструктурированности, а также количественного соотношения. Специфические особенности микроструктуры фаршей представлены на рисунках 5 –6.
Figure 4. Areas of equal values of enzyme activity as an off-clique function
(a) (b)
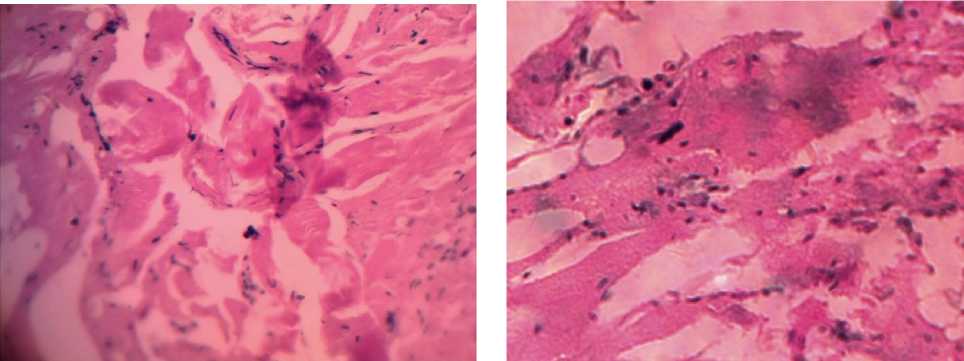
Рисунок 5. Гистоархитектоника контрольных образцов фаршевых систем; окраска гематоксилин-эозин, ув. x 100:
(a) – без внесения растительных компонентов; (b) – с гидратированной люпиновой мукой
Figure 5. Histoarchitectonics of control samples of farce systems; coloring of hematoxylin-eosin, uv. x 100: (a) – without the introduction of plant components; (b) – with hydrated lupine flour
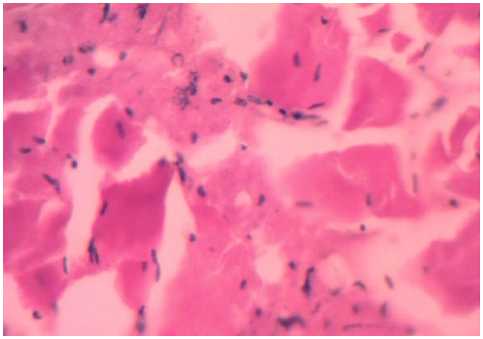
(b)
систем с белково-углеводной композицией; окраска
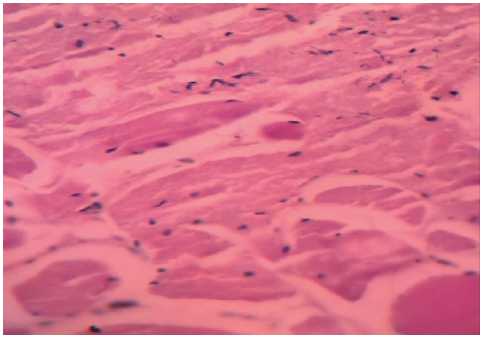
(а)
Рисунок 6. Гистоархитектоника образцов фаршевых
гематоксилин-эозин, ув. x 100: (а) – в виде гидратированной биополимерной дисперсии при куттеровании; (b) – в виде предварительно термообработанного при 40 °С геля
Figure 6. Histoarchitectonics of samples of minced systems with protein-carbohydrate composition; coloring of hematoxylin-eosin, uv. x 100: (a) – in the form of hydrated biopolymer dispersion at cuttering; (b) – in the form of preheat-treated at 40° C of the gel
В контрольном образце фарша (рисунок 5a) наблюдаются разрозненные частицы мышечной различных размеров, четко прослеживаются фрагменты соединительной ткани. В аморфном веществе комбинированного мясо-растительного фарша с гидратированной люпиновой мукой (рисунок 5b) присутствуют довольно крупные микропустоты удлиненной формы, которые придают фаршу рыхлую консистенцию, негативно влияющую на внешний вид готового продукта. В образцах мясного фарша с применением трансглутаминазы в составе ИМСБК (рисунок 6) наблюдается более уплотненная структура фаршевой системы. Объективно это выражается в уменьшении пространства между волокнами и фрагментами волокон мышечной такни, что свидетельствует о улучшении структуры мясной системы. В образце с применением гидратированной биополимерной системы (рисунок 6a) наблюдается явление адгезии между измельченными фрагментами мышечной ткани. Микропустоты между частицами фарша приняли сетчатую структуру, что, в свою очередь, по сравнению с контрольными образцами (рисунок 5) уменьшает рыхлость фаршевой эмульсии. При внесении ИМСБК в виде геля фаршевая система становится однородной, основная ее часть тонко измельчена. Отдельные фрагменты мышечной и рыхлой соединительной ткани достигают 0,3–0,4 мм.
Значительная часть мышечных волокон представлена в виде мелкозернистой белковой деструктивной массы. Прослеживаются небольшие включения измельченных фрагментов жировой ткани, не более 2%. Этот образец отличается от предыдущих улучшенной структурой, что позволяет прогнозировать улучшение функционально-технологических свойств фаршевой системы на последующих стадиях технологической обработки.
Заключение
Перспективным подходом в производстве традиционных и новых форм пищи является использование препаратов трансглутаминазы (ТГ) из микробных источников. На отечественном рынке представлены коммерческие марки ТГ фирм-производителей из Китая, Японии, Испании. Анализ сведений о продуцентах показывает, что в странах Европы преимущественно используют бактериальную экспрессивную систему S. mobaraense . Промышленный процесс получения коммерческих препаратов реализуется на стадиях: культивирование посевного материала – ферментация – отделение и очистка жидкой фракции культуральной жидкости –
Список литературы Подходы к получению и применению микробной трансглутаминазы в эмульгированных мясорастительных системах
- Kieliszek M., Misiewicz, A. Microbial transglutaminase and its application in the food industry. A review//Folia Microbiol. 2014. № 59. P. 241. URL: https://doi.org/10.1007/s12223-013-0287x
- Shleikin A.G., Danilov N.P. Evolutionary-biological peculiarities of transglutaminase. Structure, physiological functions, application//Journal of Evolutionary Biochemistry and Physiology. 2011. V. 47. № 1. P. 1-14.
- Shleikin A.G., Zhilinskaya N.T., Barakova N.V., Danilov N.P. et al. Structure properties of stirred yoghurt made with transglutaminase and amaranth//Carpathian Journal of Food Science and Technology. 2016. V. 8. № 2. P. 71-80.
- Khalid I. I., Elhardallou S. B., Gobouri A.A. Amino Acid Composition and Physicochemical Properties of Bitter Lupine (Lupinustermis) Seed Flour.//Orient. J. Chem. 2016. V. 32(6). URL: http://www.orientjchem.org/? p=26069.
- Bhardwaj H. L., Hamama A.A. Cultivar and Growing Location Effects on Fatty Acids and Minerals in White Lupin Sprouts//ISRN Agronomy. 2012. V. 2012. P. 5 DOI: 10.5402/2012/232349
- Прянишников В.В. Белки и пищевые волокна в технологии мясных продуктов//Мясная индустрия. 2013. № 5. С. 36-37.
- Мотина Н.В., Нефедова Н.В. Экспресс-метод определения активности трансглутаминазы//Материалы конф., посв. памяти П.Ф. Дьяченко. 2006. С. 87-89.
- Мастицкий С.Э. Методическое пособие по использованию программы STATISTICA при обработке данных биологических исследований. Минск: РУП "Институт рыбного хозяйства", 2009. 76 с.
- Дерканосова Н.М., Журавлев А.А., Сорокина И.А. Моделирование и оптимизация технологических процессов пищевых производств. Воронеж: Воронежский государственный технический университет, 2011. 196 с.
- ГОСТ 50779. 21 -2004 Статистические методы. Правила определения и методы расчета статистических характеристик по выборочным данным. Часть 1. Нормальное распределение. М.: ИПК Издательство стандартов, 2004. 35 с.
- Методы морфологических исследований / Л. П. Трояновская и др.: метод. пособие. Воронеж: ВГАУ, 2012. 103 с.
- Dimakopoulou-Papazoglou D., Katsanidis Е. Effect of Maltodextrin, Sodium Chloride, and Liquid Smoke on the Mass Transfer Kinetics and Storage Stability of Osmotically Dehydrated Beef Meat//Food and Bioprocess Technology. 2017. V. 10(4).
- Camolezi Gaspar A.L., G?es-Favoni S.P. Action of microbial transglutaminase (MTGase) in the modification of food proteins: A review//Food Chemistry. 2015. V. 171. P. 315-322. URL: https://doi.org/10.1016/J.FOODCHEM.2014.09.019.
- Evdokimov I.A., Titov S.A., Polyansky K.K., Saiko D.S. Ultrafiltration concentrating of curd whey after electroflotation treatment//Foods and Raw Materials. 2017. V. 5. № 1. P. 131-136.
- Gorlov I.F., Khramtsov A.G., Titov S.A., Glotova I.A. Нigh tech of controlled pumping into whole muscle meat food//Modern Applied Science. 2015. V. 9. № 10. P. 27-33.


