Поиск генов, ответственных за биосинтез токсинов гуанидинового ряда в бактериях Bacillus sp 1839 и Pseudoalteromonas sp 2138
Автор: Горобец Екатерина Алексеевна, Магарламов Тимур Юсифович, Мельникова Дарья Игоревна, Кузнецов Василий Геннадиевич, Власенко Анна Евгеньевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Общая биология
Статья в выпуске: 2-3 т.18, 2016 года.
Бесплатный доступ
В работе проведен биоинформационный анализ 32 открытых рамок считывания (ОРС) в плазмиде pNe-1, влияющей на синтез ТТХ в бактерии Aeromonas sp., выделенной из рыбы фугу. Также проведен поиск генов, локализованных в pNe-1, в плазмидной ДНК ТТХ-продуцирующих штаммов Bacillus sp. 1839, Pseudoalteromonas sp. 2138 и в общей бактериальной ДНК из рыбы-фугу Takifugu sp. В плазмиде pNe-1 были выявлены ОРС с высокой степенью консервативности, кодирующие аминокислотные последовательности «hypothetical proteins», вероятно участвующие в синтезе ТТХ и его аналогов. Эти ОРС могут быть рекомендованы для генетических исследований биосинтеза гуанидиновых токсинов.
Бактерии-продуценты, гуанидиновые токсины, тетродотоксин, анальгетики, анестетики, нейротоксины, плазмида pne-1
Короткий адрес: https://sciup.org/148204550
IDR: 148204550 | УДК: 579.6
Search of the genes responsible for biosynthesis of guanidine toxins in bacteria of Bacillus sp 1839 and Pseudoalteromonas sp 2138
In the current research the bioinformatic analysis of 32 open reading frames (ORF) in the plasmid pNe-1, involved in TTX synthesis in bacteria Aeromonas sp. isolated from puffer fish, was performed. The search of genes from pNe-1 in plasmid DNA of TTX-producing strains Bacillus sp. 1839, Pseudoalteromonas sp. 2138 and a total bacterial DNA from puffer fish Takifugu sp. was also carried out. ORFs with the high level of conservation were identified. These ORFs encode amino acid sequences identified to «hypothetical proteins», which can be involved in TTX and its analogs synthesis. The obtained results can be recommended for genetic studies of the guanidine toxins biosynthesis.
Текст научной статьи Поиск генов, ответственных за биосинтез токсинов гуанидинового ряда в бактериях Bacillus sp 1839 и Pseudoalteromonas sp 2138
Интенсивный рост антропогенной нагруз- Благодаря своей уникальной структуре
ки приводит к увеличению выброса промышленных, сельскохозяйственных, строительных, транспортных и бытовых отходов, загрязняющих окружающую среду. На фоне неблагоприятной экологической обстановки наблюдается устойчивая динамика роста острых респираторных, иммунных и аллергических заболеваний, сердечнососудистых патологий, а также онкологических заболеваний. Одним из симптомов этих болезней является боль. Боль является глобальной проблемой здравоохранения [1]. Было подсчитано, что диагноз «хронический болевой синдром» выявлен у 20% взрослого населения Земли и существенно ухудшает качество их жизни и условия труда. Становится очевидным необходимость в поиске и разработке новых лекарственных агентов анальгетического (анастетического) действия.
Наибольший интерес в поиске новых анестетиков представляют низкомолекулярные нейротоксины. Одним из таких токсинов бактериального происхождения являются гуанидиновые токсины - тетродотоксин (ТТХ) и его аналоги.
Горобец Екатерина Алексеевна, лаборант-
ТТХ-подобные токсины блокируют межмембранные токи в возбудимых тканях (мышечных и нервных), не нарушая гомеостаз окружающих тканей. Наиболее перспективным направлением применения ТТХ и его аналогов в терапевтической практике является купирование болей. Эти токсины могут использоваться в качестве анальгетиков общего или местного действия. Так, в Канаде на основе ТТХ и сакситоксина было создано лекарство-прототип для лечения болевого синдрома у больных с тяжелыми формами рака, оказывающее анальгетический эффект в течение 14 дней с момента приема [2]. Использование ТТХ-подобных токсинов в местной анестезии, представляет большой интерес, так как в отличие от других анестетиков, гуанидиновые токсины блокирует рефлекторные сокращения только в возбудимых тканях, не вызывает миокардиальную депрессию, а также не пересекает гематоэнцефалический барьер, что снижает риск развития судорог или повреждений центральной нервной системы [3]. Также есть попытки введения гуанидиновых токсинов в медицинскую практику в качестве препаратов для снятия абстинентного синдрома у наркотически зависимых пациентов [2].
Использование ТТХ-подобных токсинов в медицинской практике не представляется возможным из-за высокой стоимости производства токсинов. На сегодняшний день единственным сырьем для производства гуанидиновых ткоси-нов является рыба-фугу: из 1 тонны рыбы получают 1 грамм ТТХ. Отсутствие биотехнологического производства ТТХ и его аналогов связно с недостатком знаний о путях его биосинтеза в живых организмах. ТТХ и все его аналоги обладают необычной структурой, что является результатом сложных биосинтетических реакций. Для расшифровки биосинтетических путей в бактериях все большую популярность приобретают молекулярно-генетические методы, направленные на поиск генных кластеров ответственных за биосинтез токсинов у бактерий.
Впервые ТТХ-подобные токсины были обнаружены в рыбе-фугу, относящейся к семейству Tetraodontidae, а позже и в других организмах, принадлежащих к разным таксономическим группам [4]. Причем в большинстве токсин-содержащих организмов были найдены токсин-продуцирующие бактерии родов: Acinetobacter sp ., Aeromonas sp. , Bacillus sp ., Roseobacter sp ., Shewanella sp ., Tenacibaculum sp ., Vibrio sp. и др [5]. Учитывая, что столь филогенетически удаленные группы бактерий могут производить ТТХ-подобные токсины, можно предположить, что бактерии-продуценты могли освоить один и тот же путь биосинтеза токсина посредством горизонтального переноса генов, как это было показано для сакситоксина [6]. Так, бактерия Aeromonas sp ., выделенная из рыбы фугу Takifugu obscurus , способна продуцировать ТТХ и его аналоги, а их продукция прямо зависит от количества копий плазмиды pNe-1 [7]. Данный факт говорит о том, что среди белок-кодирующих последовательностей pNe-1 есть как минимум один ген-регулятор продукции токсинов. Полное секвенирование последовательности pNE-1 позволило идентифицировать 60 открытых рамок считывания (ОРС), кодирующих белки, причем 36 ОРС кодируют белки с неизвестными функциями [7]. Кроме того, в составе pNE-1 были идентифицированы последовательности мобильных генетических элементов секреторной системы 4 типа, ответственной за конъюгацию плазмид у грамм-положительных бактерий и транспозазы IS426 [4]. Исходя из данного факта, можно предположить, что эта плазмида попала в Aeromonas в результате горизонтального переноса генов [7].
Цель работы: провести биоинформаци-онный анализ 36 ОРС в плазмиде pNe-1 из ТТХ-продуцирующего штамма Aeromonas sp. Проверить наличие генов, локализованных в плазмиде pNe-1, в плазмидной ДНК токсин-продуци-рующего штаммов Bacillus sp. 1839, Pseudo-alteromonas sp. 2138 и в общей бактериальной ДНК из рыбы-фугу Takifugu sp..
Методика исследований. Штаммы, продуцирующие ТТХ-подобные токсины, Bacillus sp. 1839 (близкий к B. asahii ) и Pseudoalteromonas sp. 2138 (близкий к P. tetraodonis IAM 14160), были взяты из коллекции морских гетеротрофных микроорганизмов ИБМ ДВО РАН им. А.В Жирмунского. Для культивирования бактерий использовали питательную среду Йошимицу– Кимура следующего состава: пептон (5,0 г), дрожжевой экстракт (2,0 г), глюкоза (1 г), К 2 НРО 4 (0,2 г), MgSO 4 х7H 2 O (0,1 г), агар (12,0 г), дистиллированная вода (500 мл), и морская вода (500 мл);
рН среды 7,5–7,8. Для выделения ДНК бактерий культивировали в течение 7 сут в 5 мл среды. Для детекции ТТХ бактерий культивировали в 500 мл среды в течение 14 сут Pseudoalteromonas sp. 2138 и 30 сут Bacillus sp. 1839. Бактерий центрифугировали в течение 7 мин, при 4 ᵒ С и скорости 4000g, надосадочную жидкость сливали, а осадок помещали в холодильник на -80оС для последующих экспериментов.
Полимеразную цепную реакцию (ПЦР) проводили в реакционных объемах 10 мкл, содержащих 1 мкл Taq-полимеразного буфера, 0,2 мкл 2,5 мМ MgCl 2 , 0,8 мкл 2,5 mM дезоксинуклеотидтрифосфатов, по 0,5 мкл раствора прямого и обратного олигонуклеотидных праймеров в концентрации 10 пмоль/мкл (табл. 1), 1 мкл тотальной ДНК в концентрации 30 нг/мкл и 1U (единицы активности) в 0,2 мкл Taq-полимеразы. В качестве положительного контроля была составлена реакция с олигонуклеотидными праймерами B3/B4 на рибосомальные кластеры эубактерий. Негативным контролем служила реакция с оли-гонуклеотидными праймерами B3/B4, где матрицей являлась вода.
Термический цикл проводили в C1000 TouchTh Thermocycler (BioRad, США). Амплификация началась со стадии начальной денатурации при 95°С в течение 2 мин для ДНК, выделенной из тканей рыбы фугу, в течение 4 мин для бактериальных штаммов: Bacillus sp. 1839 и Pseudoalteromonas sp. 2138. Затем 33 цикла: денатурация при 95°С в течение 30 с, отжиг пары праймеров B1/B2 при температурах 60,8; 62,3 и 63°С, праймеров В3/В4 при 55°С и при 50, 52,6, 55,1°С для остальных праймеров в течение 30 с; элонгация при 72°С в течение 2 мин. Амплификация завершалась конечным этапом элонгации при 72°С в течение 5 мин. Далее 10 мкл ПЦР продукта смешивали с 4 мкл 6х загрузочного буфера (DNA Gel Loading Dye (6X) - Thermo Fisher Scientific) и разделяли с помощью электрофореза в 2% агарозном геле в ТАЕ-буфере 40 мин при 100В, затем 10 мин окрашивали бромистым этидием, промывали 3 раза по 7 мин дистиллированной водой. Визуализацию и документирование гелей ing System (BioRad, США). производили на системе ChemiDocTMTouch Imag-
Таблица 1. Праймеры, подобранные на консервативную последовательностьплазмиды pNE-1
|
Код |
Нуклеотидная последовательность праймера |
Участок в ДНК, на которую подобраны олигонуклеотидные праймеры |
|
B1 |
5’-tctctttcatgctgcggttcagc-3’ |
позиция 2252-2400 в плазмиде pNe-1 (праймеры взяты из статьи) -прямой |
|
B2 |
5’–gacaaggctcgg agacacgca– 3’ |
позиция 2252-2400 в плазмиде pNe-1 (праймеры взяты из статьи)- обратный |
|
B3 |
5’-gccagcagccgcggtaa-3’ |
на рибосомальные кластеры эубактерий - прямой |
|
B4 |
5’ggactaccagggtatctaat– 3’ |
на рибосомальные кластеры эубактерий - обратный |
|
B7 |
5′-gtactttgataattttggaata-3′ |
на гипотетический белок 2 (или на открытую рамку) прямой |
|
B8 |
5′- aaacatctagaattactact-3′ |
на гипотетический белок 2 (или на открытую рамку) обратный |
|
B9 |
5′-aagcttgacctttccctga-3′ |
на гипотетический белок 8 (или на открытую рамку) прямой |
|
B10 |
5′-gttcatggtacttcaagatg-3′ |
на гипотетический белок 8 (или на открытую рамку) обратный |
|
B11 |
5′-atcagcatggtgtaataa-3′ |
на гипотетический белок 5 (или на открытую рамку) прямой |
|
B12 |
5′-gctattcctgttaaagaa-3′ |
на гипотетический белок 5 (или на открытую рамку) обратный |
|
B13 |
5′-ggcgctttagctgaaaaat-3′ |
на гипотетический белок 10 (или на открытую рамку) прямой |
|
B14 |
5′-aagtgattcggtttattagc-3′ |
на гипотетический белок 10 (или на открытую рамку) обратный |
|
B15 |
5′-atcttgcacgctgatattgg-3′ |
на гипотетический белок 24 (или на открытую рамку) прямой |
|
B16 |
5′-atacttccaccaccatatac-3′ |
на гипотетический белок 24(или на открытую рамку) обратный |
|
B17 |
5′gaaaaaaatcttaaaaagaaaa-3′ |
на гипотетический белок 28 (или на открытую рамку) прямой |
|
B18 |
5′-attcgtctaaaacaaaatta-3′ |
на гипотетический белок 28(или на открытую рамку) обратный |
|
B19 |
5′-agaagtatttacattgtttgat-3′ |
на гипотетический белок 30 (или на открытую рамку) прямой |
|
B20 |
5′-ccaccaatatcctcataaa-3′ |
на гипотетический белок 30 (или на открытую рамку) обратный |
|
B21 |
5′-tatttaaaagag gatctagag-3′ |
на гипотетический белок 32 (или на открытую рамку) прямой |
|
B22 |
5′-atttaaatgtgcatatctagtt-3′ |
на гипотетический белок 32 (или на открытую рамку) обратный |
|
B23 |
5′-caaaagaaagcaagtttacaagg-3′ |
на гипотетический белок 31 (или на открытую рамку) прямой |
|
B24 |
5′-tatttgatccgctttataatgatg-3′ |
на гипотетический белок 31(или на открытую рамку) обратный |
|
B25 |
5′-ttacataggtactaaaaaaag-3′ |
на гипотетический белок 35 (или на открытую рамку) прямой |
|
B26 |
5′-cataaataatgtgtggatt-3′ |
на гипотетический белок 35 (или на открытую рамку) обратный |
Биоинформационный анализ. Анализ нуклеотидной последовательности и ОРС плазмиды pNe-1, выделенной из ТТХ-продуцирую-щего штамма Aeromonas sp., производили при помощи программы ApE (A plasmid Editor). Поиск гомологичных нуклеотидных последовательностей ОРС в других бактериях и их выравнивание выполнили с использованием программы BLAST (Basic Local Alignment Search Tool) и базы данных NCBI (ссылка на интернет ресурс). Дизайн праймеров составлялся на 10 ОРС, потенциально кодирующих белки с неизвестными функциями, плазмиды pNe-1 с использованием программы OligoCalc (Oligonucleotide Properties Calculator).
Бактериальный осадок, объемом около 2 мл, разбавляли 0,1% водным раствором уксусной кислоты до конечного объема 20 мл. Разрушение клеток проводили на ультразвуковом гомогенизаторе Sonopuls HD 2070 (Bandelin, Германия), в течение 3-х ч, с частотой 20 kHz, амплитудой 212 мкм, рабочим циклом 0,8 с и интервалом 0,2 с. Время обработки ультразвуком для бактерий Bacillus sp. 1839 составило 3 ч, а для Pseudo-alteromonas sp. 2138 – 30 мин. Полученный гомогенат центрифугировали при 13000g в течение 30 мин, супернатант отбирали и затем упаривали в вакуумном испарителе Centrivap Concentrator 2310905 (Labconco, Germany) при 500С. Получившийся после упаривания осадок растворяли в 2
мл водного раствора 0,1% уксусной кислоты. Раствор затем фильтровали с помощью 3кДа фильтров Microcon Ultarcel YM-3 (Millipore, США). Для удаления белковой фракции раствор нагревали до 85оС в течении 20 мин, затем коагулированные белки осаждали, а супернатант хранили при -80оС для дальнейших исследований.
Детекция и определение концентрации токсинов гуанидинового ряда. Клетки мышиной нейробластомы Neuro-2a (ATCC, CCL131) были взяты из коллекции культур университета Лозанны, Швейцария. Культивация велась в среде Игла в модификации Дюльбекко DMEM (Gibco) содержащей 4,5г/л D-глюкозы; глютамин, пируват и антибиотики – 1000 U/ml пенициллина и 10 mg/ml стрептомицина (Sigma, США), дополненной 10% эмбриональной сывороткой крупного рогатого скота FBS (Sigma, США). Культура клеток содержалась в СО 2 -инкубаторе при 37oC, 5% CO 2 и 80% важности. Пассирование клеток проводилось по достижению 80% конфлюэнтности раз в 2 дня.
Для проведения эксперимента клетки 2-х дневной культуры собирали из культурального флакона с помощью 0,25% раствора трипсина на фосфатном буфере (PBS) pH 7,4 и ресуспендиро-вали в культуральной среде (DMEM + 5% FBS) до плотности 4 х 105 клеток/мл. Посев клеток производили в 96-луночный планшет (Greiner Bio-One, Германия) по 50 мкл суспензии в каждую лунку, итоговое содержание клеток в каждой лунке составляло 2х104. Клетки преинкубировали 24 ч в СО2-инкубаторе при 37оС и 5% СО2. После 24 ч преинкубации в каждую лунку добавили по 100 мкл тестовых и контрольных растворов и инкубировали 24 ч в СО2-инкубаторе при 37оС и 5% СО2. Для приготовления тестовых растворов использовали среду DMEM с 5% FBS, содержащую различные разведения экстрактов Bacillus sp. 1839, и Pseudoalteromonas sp. 2138, а так же 133μМ вератридина (Sigma, США) в ДМСО и 0,4 мМ водного раствора уабаина (Sigma, США). Оценку жизнеспособности клеток проводили с помощью красителя МТТ (3-[4,5-dimethylthiazol-2-yl]-2,5-diphenyltetrazolium bromide; thiazolyl blue) (Sigma, США). Раствор красителя 5мг/мл в PBS pH 7,4 стерилизовали фильтрованием через 0.22 мкм фильтр (Millipore, США) и добавляли по 15 мкл в каждую лунку 96-луночного планшета. После инкубации в течение 4-х ч при 37оС и 5% СО2, образовавшиеся кристаллы формазана растворили добавлением 150 мкл изопропанола c 0,04М HCl, и перемешивали на шейкере (Biosan PST-60HL4, Латвия) при 37оС и 450 rpm в течение 10 мин. Измерение поглощения растворенного красителя, для каждой лунки, проводили на спектрофотометре ELx800uv (Bio-Tek Instruments Inc., США) при длине волны 595нм с референсной длинной волны 630 нм.
Результаты и их обсуждения. Согласно одной из гипотез, подтвержденной многочисленными исследованиями, первичными продуцентами ТТХ-подобными токсинами в морских экосистемах являются микроорганизмы. В качестве токсин-продуцирующих микроорганизмов были выбраны штаммы бактерий, относящиеся к разным систематическим группам: Firmicutes (штамм Bacillus sp. 1839) и Proteobacteria (штамм Pseudoalteromonas sp. 2138). Способность штамма Bacillus sp. 1839 продуцировать токсин была подтверждена иммуноцитохимическими методами с использованием антител против ТТХ [8]. Для штамма Pseudoalteromonas sp. 2138 способность к продукции ТТХ не была проверена, но было показано 100% сходство по рРНК со штаммом, продуцирующим ТТХ и его аналоги, Pseudoalteromonas tetraodonis IAM 14160 (не опубликованные данные). Для подтверждения способности продуцировать токсин штаммами Bacillus sp. 1839 и Pseudoalteromonas sp. 2138 был использован метод биотестирования на культуре клеток нейробластомы. Этот метод обладает высокой чувствительностью, определяет весь спектр ТТХ-подобных токсинов (ТТХ, сакситоксин, гуанотоксины I-IV и т.д.) и детектирует не только сам факт наличия токсинов, но и оценивает его концентрацию. Нами показано, что экстракты Bacillus sp. 1839 оказывали сильный токсический эффект на культуру клеток, эквивалентный концентрации чистого ТТХ - 28 нг. Так показатель оптической плотности в контроле в среднем составил 0,451 ОП (рис. 1А). При добавлении к культуре клеток ТТХ в концентрации от 2 нг/мл до 32 нг/мл показатель оптической плотности изменялся в диапазоне от 0,5 до 0,595 ОП. При добавлении к культуре клеток экстракта Bacillus sp. 1839 в разбавлении 1 к 50, оптическая плотность составила 0,585 ОП, что соответствует диапазону показателей оптической плотности для ТТХ в концентрации 16-32 нг/мл. Экстракты Pseudoalteromonas sp. 2138 оказывали токсичный эффект на культуру клеток, эквивалентный 1.8 нг ТТХ. При этом оптическая плотность в контроле в среднем составила 0,578 ОП (рис. 1Б). При добавлении к культуре клеток ТТХ в концентрации от 2 нг/мл до 8 нг/мл показатель оптической плотности изменялся в диапазоне от 0,655 до 0,621 ОП. При добавлении к культуре клеток экстракта Pseudoalteomonas sp. 2138 в разбавлении 1 к 50, оптическая плотность составила 0,615 ОП. Проведенные эксперименты доказывают способность коллекционных штаммов Bacillus sp. 1839 и Pseudoalteromonas sp. 2138 продуцировать ТТХ, а значит и правомочность их использования в качестве модельных объектов для поиска генетических основ биосинтеза ТТХ.
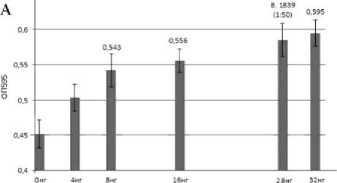
Рис. 1. Концентрация ТТХ-подобных токсинов в экстракте Bacillus sp. 1839 (А) и Pseudoalteomonas sp. 2138 (Б)
В настоящее время выявлено около 30 родов бактерий из разных систематических групп, способных продуцировать ТТХ и его аналоги. Существует гипотеза, что столь широкое распространение продуцентов токсинов гуанидинового ряда в филогинетически далёких систематических группах микроорганизмов связано с горизонтальным переносом генов. Известно, что горизонтальный перенос генов в бактериях осуществляется посредством плазмид. Исследователи Джинг и Лю [7] показали зависимость количества ТТХ, синтезируемого бактерией Aeromonas sp, от числа копий плазмиды pNE-1, т.е. как минимум один ген плазмиды pNE-1, влияет на синтез токсина. Возможно, благодаря горизонтальному переносу генов плазмида pNE-1 присутствует и в других ТТХ-продуцирующих бактериях, в том числе и Bacillus sp. 1839 и Pseudoalteromonas sp. 2138. Предварительные исследования показали, что оба исследуемых штамма Bacillus sp. 1839 и Pseudoalteromonas sp. 2138 содержали плазмид-ную ДНК (не опубликованные данные). На консервативный участок плазмиды pNE-1 были получены олигонуклеотидные праймеры B1/B2 (см. табл. 1). Однако ПЦР анализ не выявил наличие консервативных участков, соответствующих плазмиде pNE-1, в тотальной ДНК Bacillus sp. 1839 и Pseudoalteromonas sp. 2138.
Нами был проведен поиск плазмиды pNE-1 в ассоциативной микрофлоре рыбы-фугу, виды которой являются «богатым поставщиком» ток-син-синтезирующих бактерий [9]. С помощью ПЦР анализа был проведен скрининг микрофлоры из разных органов Takifugu sp. на наличие плазмиды pNE-1. ПЦР анализ не выявил наличие плазмиды pNE-1 в микрофлоре Takifugu sp. Отсутствие плазмиды в исследованных бактериальных образцах может быть связано с мутациями в составе консервативных участков, что сделало невозможным выявление плазмиды pNE-1, при помощи разработанных олигонуклеотидных праймеров (B1/B2, B7-B26). Для окончательного ответа о распространении плазмиды pNE-1 среди продуцентов ТТХ и его аналогов необходимо провести полный сиквенс плазмидной ДНК в токсин-продуцирующих бактериях.
Плазмида pNE-1 содержит 36 ОРС, кодирующих аминокислотные последовательности, которые фигурируют в базах данных NCBI как «белки с неопределенной функцией». Вероятно, один или несколько генов этой плазмиды могут принимать участие в биосинтезе ТТХ-подобных токсинов. При сравнении ОРС из pNE-1 с бактериальными нуклеотидными последовательностями из баз данных NCBI было обнаружено 10 последовательностей, с 60% уровнем гомологии в составе последовательности ДНК и выше, а в составе аминокислотной последовательности – более 90% (табл. 2). Все эти участки ДНК с высокой степенью гомологии были локализованы только в плазмидной ДНК бактерий. Наличие таких консервативных последовательностей в плазмидах разных видов бактерий говорит о важности этих генов в жизнедеятельности клетки. Можно предположить, что один или несколько белков, кодируемых этими консервативными ОРС, могут играть роль в синтезе токсинов гуанидинового ряда.
Таблица 2. Гомология ОРС плазмиды pNE-1 с базой данных BLAST
|
Организм |
OP C2 |
OP C5 |
OP C8 |
OP C10 |
OP C24 |
OP C28 |
OP C30 |
OP C31 |
OP C32 |
OP C35 |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
Bacillus thuringiensis serovar indiana strain HD521 plasmid pBTHD521-4, complete sequence |
66 |
53 |
70 |
58 |
38 |
56 |
57 |
87 |
87 |
- |
|
Bacillus thuringiensis strain Bc601 plasmid pBTBC5, complete sequence |
79 |
53 |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
- |
|
Bacillus thuringiensis strain YWC2-8 plasmid pYWC2-8-3, complete sequence |
79 |
- |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
- |
|
Bacillus thuringiensis strain YC-10 plasmid pYC20, complete sequence |
79 |
- |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
|
|
Bacillus thuringiensis serovar morrisoni strain BGSC 4AA1 plasmid pBMB76 |
79 |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
||
|
Bacillus thuringiensis serovar kurstaki strain HD 1 plasmid unnamed3 |
79 |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
||
|
Bacillus thuringiensis serovar galleriae strain HD-29 plasmid pBMB126 |
66 |
70 |
58 |
44 |
56 |
57 |
87 |
87 |
||
|
Bacillus thuringiensis serovar kurstaki str. YBT-1520 plasmid pBMB95 |
79 |
70 |
58 |
38 |
56 |
59 |
87 |
34 |
||
|
Bacillus thuringiensis serovar kurstaki str. HD-1 plasmid pBMB95 |
79 |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
||
|
Bacillus thuringiensis serovar kurstaki str. YBT-1520 plasmid pBMB94 |
79 |
70 |
58 |
38 |
56 |
59 |
87 |
34 |
||
|
Bacillus thuringiensis serovar thurin-giensis str. IS5056 plasmid pIS56-107 |
79 |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
||
|
Bacillus thuringiensis serovar kurstaki str. HD73 plasmid pHT77 |
79 |
70 |
58 |
38 |
56 |
59 |
87 |
87 |
||
|
Bacillus thuringiensis serovar chinensis CT-43 plasmid pCT127 |
79 |
63 |
58 |
38 |
56 |
59 |
87 |
87 |
||
|
Bacillus thuringiensis CT43 plasmid pBMB0558 |
53 |
44 |
58 |
38 |
59 |
87 |
87 |
|
Bacillus cereus H3081.97 plasmid pH308197_73 |
79 |
63 |
58 |
44 |
56 |
59 |
87 |
87 |
||
|
Bacillus thuringiensis HD1002 plasmid 7 |
85 |
|||||||||
|
Bacillus thuringiensis HD-789 plasmid pBTHD789-6 |
85 |
|||||||||
|
Bacillus thuringiensis strain 4Q2 plasmid pTX14-2 |
85 |
|||||||||
|
Bacillus thuringiensis serovar israelensis strain AM65-52 plasmid pAM65-52-8-7K |
85 |
|||||||||
|
Bacillus thuringiensis strain Al Hakam plasmid pBTZ_6 |
64 |
|||||||||
|
Bacillus mycoides strain 219298 plasmid |
64 |
|||||||||
|
Bacillus thuringiensis strain HS18-1 plasmid pHS18-7 |
56 |
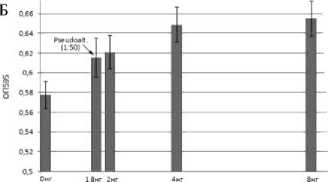
Примечание: 1,2,3 - праймеры B1/B2; 4,5,6 – праймеры B7/B8; 7,8,9 – праймеры B9/B10; 10,11,12 – праймеры B11/B12; 13,14,15 – праймеры B13/B14; 16,17,18 – праймеры B15/B16; 19,20,21 – праймеры B17/B18; 22,23,24 – праймеры B19/B20; 25,26,27 – праймеры B21/B22; 28,29,30 – праймеры B23/B24; 31,32,33 – праймеры B25/B26; К - - негативный контроль; К+ - положительный контроль, Ст. – синтетические маркеры молекулярного веса

Рис. 2. Электрофорез ПЦР фрагментов ДНК рыбы-фугу Takifugu sp. (А – печень, Б – кожа, В – кишечник), Bacillus sp. 1839 (Г) и Pseudoalteromonas sp. 2138 (Д)
В текущей работе был осуществлен ПЦР анализ на предмет наличия 10 консервативных плазмидных ОРС в Bacillus sp. 1839, Pseudo-alteromonas sp. 2138 и в общей бактериальной ДНК из рыбы-фугу Takifugu sp. С использованием программы OligoCalc были разработаны олиго-нуклеотидные праймеры, специфичные к наиболее консервативным участкам, исходя из допущения, что данные участки будут консервативны в бактериях рода Bacillus и Pseudoalteromonas (табл. 1, рис. 2). Ни один из подобранных праймеров не выявил ОРС из плазмиды pNE-1 в исследованных образцах тотальной и плазмидной ДНК бактерий. Отрицательный результат работы, возможно, связан с вырожденностью генетического кода, т.е. наличие в ДНК нуклеотидных замен, не влияющих на структуру белка. Продолжением работы станет подбор праймеров с учетом вырожденности кода 10 консервативных ОРС плазмиды pNE-1 и поиск «hypothetical proteins» в Bacillus sp. 1839 и Pseudoalteromonas sp. 2138.
Выводы: из 36 ОРС содержащиеся в плазмиде pNE-1, 10 обладают высокой степенью консервативности. Эти консервативные ОРС, кодирующие «белки с неустановленной функцией», могут быть рекомендованы в дальнейшем для поиска генетических основ синтеза токсина.
Исследование выполнено при поддержке ДВФУ, проект №14-08-06-19 и и программой фундаментальных научных исследований «Дальний Восток» №15-I-3-036.
-
1.
-
2.
-
3.
-
4.
-
5.
-
6.
-
7.
-
8.
-
9.
Список литературы Поиск генов, ответственных за биосинтез токсинов гуанидинового ряда в бактериях Bacillus sp 1839 и Pseudoalteromonas sp 2138
- Nieto, F.R. Tetrodotoxin (TTX) as a therapeutic agent for pain/F.R. Nieto, E.J. Cobos, M.Á. Tejada et al.//Mar Drugs. 2012. No10(2). P. 281-305.
- Lago, J. Tetrodotoxin, an Extremely Potent Marine Neurotoxin: Distribution, Toxicity, Origin and Therapeutical Uses/J. Lago, L. P. Rodríguez, L. Blanco et al.//Mar. Drugs. 2015. No 13. P. 6384-6406.
- Verde, C.B. Tetrodotoxin-Bupivacaine-Epinephrine Combinations for Prolonged Local Anesthesia/C.B. Berde, U. Athiraman, B. Yahalom et al.//Mar. Drugs. 2011. No 9. P. 2717-2728.
- Goessweiner-Mohr, N. Conjugative type IV secretion systems in Gram-positive bacteria/N. Goessweiner-Mohr, K. Arends, W. Keller, E. Grohmann//Plasmid. 2013. V. 70(3). P. 289-302.
- Chau, R. Diversity and biosynthetic potential of culturable microbes associated with toxic marine animals/R. Chau, J.A. Kalaitzis, S.A. Wood, B.A. Neilan//Mar. Drugs. 2013. No 11. P. 2695-2712.
- Kellmann, R. Identification of a saxitoxinbiosynthesis gene with a history of frequent horizontal gene transfers/R. Kellmann, T.K. Michali, B.A. Nielan//J. Mol. Evol. 2008. V. 67. P. 526-538.
- Liu, J. Production level of tetrodotoxin in Aeromonas is associated with the copy number of a plasmid/J. Liu, F. Wei, Y. Lu et al.//Toxicon. 2015. V. 101. P. 27-34.
- Magarlamov, T.Y. Tetrodotoxin-producing Bacillus sp. from the ribbon worm (Nemertea) Cephalothrix simula (Iwata, 1952)/T.Y. Magarlamov, I. Beleneva, A. Chernyshev, A. Kuhlevsky//Toxicon. 2014. V.85. P. 46-51.
- Chau, R. On the origins and biosynthesis of tetrodotoxin/R. Chau, J.A. Kalaitzis, B.A. Neilan//Aquatic Toxicology. 2011. V. 104. P. 61-72.


