Поиск молекулярно-генетических предикторов развития агрессивных лимфом
Автор: Березина Ольга Валерьевна, Поспелова Татьяна Ивановна, Филипенко Максим Леонидович, Воропаева Елена Николаевна, Овчинников Виктор Сергеевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.32, 2017 года.
Бесплатный доступ
Изучены полиморфные локусы генов фолатного обмена: C677T и A1298C MTHFR, A2756G MTR, A66G MTRR, G1958A MTHFD1 и 844ins68 CBS у больных агрессивными неходжкинскими злокачественными лимфомами. Обнаружена ассоциация редкого аллеля 1958A гена MTHFD1 со снижением риска развития диффузной В-крупноклеточной лимфомы (OR=0,429; C.I. [0.279-0.659], p
Генетический полиморфизм, фолаты, лимфома, предрасположенность
Короткий адрес: https://sciup.org/14920190
IDR: 14920190 | УДК: 616
Searching for molecular-genetic predictors of aggressive lymphomas
Polymorphic loci of genes of folate metabolism C677T and A1298C MTHFR, A2756G MTR, A66G MTRR, G1958A MTHFD1 and 844ins68 CBS have been studied in patients with aggressive malignant Non Hodgkin lymphomas. The association of a rare allele 1958A MTHFD1 with a reduced risk of enlargement of diffuse large B-cell lymphoma (OR=0.429; C.I. [0.279-0.659], p
Текст научной статьи Поиск молекулярно-генетических предикторов развития агрессивных лимфом
Выявление молекулярно-генетических маркеров развития и прогноза для опухолевых заболеваний крови составляет суть предиктивной онкогематологии, основной задачей которой является поиск доказательств диагностической ценности тех или иных генных полиморфизмов [3]. В качестве потенциальных маркеров исследуются гены различных систем клетки: метаболизма ксенобиотиков, апоптоза, цитокинов и др. Среди них большой интерес представляют гены фолатного обмена – важной биохимической системы клетки, влияющей на регуляцию экспрессии генов путем эпигенетической модификации ДНК (рис. 1). Метилирование CpG-островков в промоторе гена является нормальным процессом регуляции степени экспрессии генов в клетках. Гиперметилирование промоторов генов, которое связано с подавлением транскрипции, так же как и мутации, является механизмом инактивации классических генов-супрессоров опухолевого роста [12]. Аномальное метилирование генов-супрессоров опухолей встречается на ранних стадиях онкогенеза и прогрессивно увеличивается, что в конечном итоге приводит к злокачественной трансформации. Аберрантное метилирование ДНК и, как следствие, измененная экспрессия генов описаны при В-клеточных неходжкин-ских злокачественных лимфомах (НХЗЛ) [10]. Полимор- фные варианты генов фолатного цикла, которые влияют на метилирование ДНК, могут способствовать возникновению неходжкинских злокачественных лимфом, вызывая гипо- или гиперметилирование протоонкогенов и генов супрессоров опухолевого роста соответственно [11].
В связи с тем, что отмечается увеличение частоты агрессивных НХЗЛ в г. Новосибирске [5] актуально исследование однонуклеотидных замен (SNPs) в генах фолат-ного цикла как потенциальных молекулярно-генетических маркеров развития лимфоидных неоплазий.
Цель работы: изучить роль полиморфных локусов C677T и A1298C гена метилентетрагидрофолатредукта-зы ( MTHFR ), A2756G гена метионинсинтазы ( MTR ), A66G гена метионинсинтазыредуктазы ( MTRR ), G1958A гена метилентетрагидрофолатдегидрогеназы ( MTHFD1 ) и 844ins68 гена цистатион- β -синтазы ( CBS ) в формировании предрасположенности к развитию агрессивных НХЗЛ.
Материал и методы
Выборки. Группу обследованных составили 89 пациентов (46 мужчин и 43 женщины; средний возраст 49,4±14,2 года) Городского гематологического центра города Новосибирска с диагнозом агрессивной неходж-кинской лимфомы. Диагностика и лечение НХЗЛ прово-
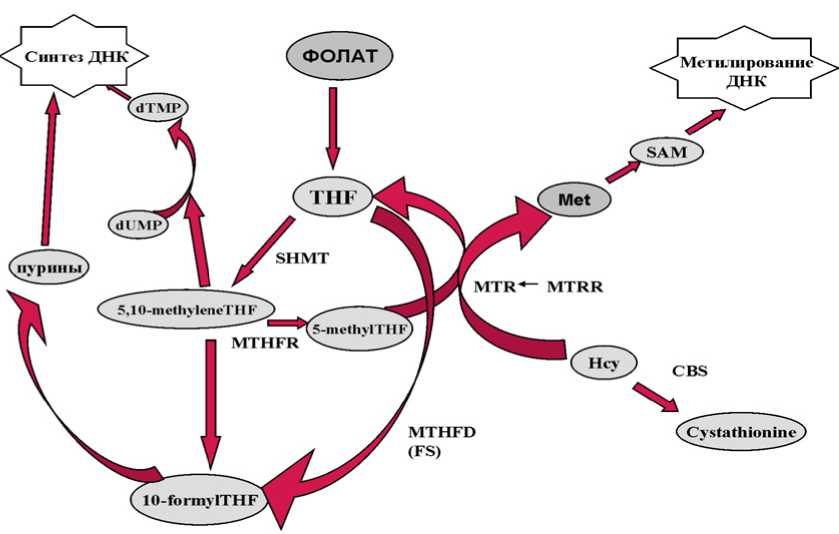
Рис. 1. (адаптировано из [15]) Фолатный цикл: dTMP – тимидин; dUMP – уридин; THF – тетрагидрофолат; 5,10-methyleneTHF – 5,10-метилентетрагидрофолат; 5-methylTHF – 5-метилтетрагидрофолат; 10-formylTHF – 10-формилтетрагидрофолат; Met – метионин; Hcy – гомоцистеин; SAM – S-аденозилметионин; MTHFR – метилентетрагидрофолатредуктаза; SHMT – серилгидрокси-метилтрансфераза; MTHFD – метилентетрагидрофолатдегидрогеназа; MTR – метионинсинтаза; MTRR – редуктаза метионинсин-тазы; SHMT – серингидроксиметилтрансфераза; CBS – цистатионин- β -синтаза; Cystathionine – цистатионин
дилось согласно Российским клиническим рекомендациям по диагностике и лечению лимфопролиферативных заболеваний [1]. Вариант НХЗЛ оценивался согласно классификации лимфоидных неоплазий ВОЗ 2008 года. В-клеточные лимфомы имели 79 (88,8%) человек. Диффузная В-крупноклеточная лимфома диагностирована у 56 (71%) пациентов, анапластическая и мантийноклеточная – у 8 (10,1%) человек каждая, лимфобластная и фолликулярная 3-го цитологического типа – у 3 (3,8%) человек каждая, беркиттоподобная у 1 (1,2%) пациента. Т-кле-точные лимфомы диагностированы у 10 (11,2%) больных.
Контрольную группу составили 549 доноров Новосибирского центра крови, средний возраст обследованных 33,0 ± 11,01 лет.
Все пациенты подписывали информированное согласие на участие в исследовании в соответствии с требованиями этического комитета.
Генотипирование. ДНК выделяли из венозной крови с использованием стандартной процедуры, включающей выделение и лизис клеток крови, гидролиз белков протеиназой К, очистку ДНК экстракцией примесей фенол-хло-роформом и осаждение ДНК этанолом; а также из буккального эпителия с использованием стандартной методики выделения ДНК на силике.
Определение генотипов полиморфных локусов G1958A гена MTHFD1 и 844ins68 гена CBS проводилось методом ПЦР-ПДРФ анализа. Определение полиморфных вариантов генов MTHFR, MTR, MTRR и SHMT1 проводилось методом ПЦР в режиме реального времени с использованием конкурирующих TaqMan-зондов, комплементар- ных полиморфной последовательности ДНК. Генотипирование осуществлялось по методике, описанной в [16].
Статистическая обработка данных. Частоты встречаемости аллелей и генотипов однонуклеотидных замен в генах фолатного цикла в выборке больных НХЗЛ сравнивали с таковыми в контрольной группе. Значимость различий оценивалась с помощью критерия χ2, статистически значимыми считались различия при р<0,05. Соответствие контрольной выборки равновесию Харди-Вайнберга также проверяли с помощью критерия χ2. Для оценки величины относительного риска использовали отношение шансов (OR) с его доверительным интервалом (C.I.) при уровне доверия 95%. Вычисления производились с помощью программы DeFinetti на сайте Института генетики человека (Мюнхен, Германия, . При оценке количественных признаков использовали вычисление средней арифметической (М) и ее ошибки (m).
Результаты
Исследованные SNPs имеют доказанное функциональное значение, т.е. изменяют активность, стабильность или количество соответствующих ферментов, что может привести к нарушению баланса между важнейшими метаболическими путями цикла фолиевой кислоты – синтезом dTMP и пуриновых нуклеотидов и метилированием ДНК, приводить к повреждению ДНК и, как следствие, инициировать онкогенез и обусловливать опухолевую прогрессию.
Таблица 1
Распределение аллелей и генотипов полиморфного локуса G1958A гена MTHFD1 в группе пациентов с агрессивными лимфомами
|
Аллели |
Контроль |
Больные ДВККЛ |
OR |
Больные ККЛ |
|
Генотипы |
1 |
2 |
С.I. |
3 |
|
Абс. % |
Абс. % |
P |
Абс. % |
|
|
n=539 |
n=54 |
ДВККЛ |
n=27 |
|
|
G |
544 50,5 |
76 70 |
2,331 |
24 44 |
|
p1–2< 0,0008 |
1,517–3,584 |
p1–3 > 0,05 |
||
|
p2–3< 0,001 |
0,0008 |
|||
|
A |
534 49,5 |
32 30 |
0,429 |
30 56 |
|
p1–2< 0,0008 |
0,279–0,659 |
p1–3 > 0,05 |
||
|
p2–3< 0,001 |
0,0008 |
|||
|
G/G |
141 26 |
27 50 |
5,209 |
3 11 |
|
p1–2< 0,003 |
1,949–13,918 |
p1–3 > 0,05 |
||
|
p2–3< 0,002 |
0,003 |
|||
|
G/A |
262 49 |
22 41 |
0,439 |
18 67 |
|
p1–2< 0,006 |
0,241–0,798 |
p1–3 > 0,05 |
||
|
0,006 |
||||
|
A/A |
136 25 |
59 |
0,192 |
6 22 |
|
p1–2< 0,003 |
0,072–0,513 |
p1–3 > 0,05 |
||
|
p2–3< 0,002 |
0,003 |
При анализе частот аллелей исследуемых полиморфных локусов в общей группе агрессивных лимфом отмечено увеличение частоты дикого 1958G-аллеля гена MTHFD1 (64%) по сравнению с контролем (50,5%, p < 0,001), тогда как редкий 1958A-аллель в группе агрессивных НХЗЛ встречался реже: 36% против 49,5% (p < 0,001).
Из группы агрессивных НХЗЛ, с учетом наибольшей представленности, были выделены пациенты с диффузной В-крупноклеточной лимфомой (ДВККЛ, n=56). Отдельному анализу также подверглись больные с другими вариантами агрессивных лимфом (Т- и В-анапластичес-кой, Т и В-лимфобластной, беркиттоподобной, мантийноклеточной, фолликулярной 3-го цитологического типа, плеоморфной, n=33), преимущественно крупноклеточными (ККЛ).
Дикий 1958G-аллель MTHFD1 в группе больных ДВККЛ встречался чаще как по сравнению с группой контроля: 70% против 50,5% (p < 0,0008), так и с группой больных ККЛ, в которой частота 1958G-аллеля составила 44% (p < 0,001). В свою очередь, частота редкого 1958A-аллеля MTHFD1 в группе больных ДВККЛ составила лишь 30%, тогда как в группе пациентов с ККЛ – 56%, а в популяции г. Новосибирска – 49,5% (табл. 1).
Учитывая различия в распределении аллелей и генотипов в группе ДВККЛ, была проведена оценка риска развития данной группы неоплазий.
Для полиморфного локуса G1958A гена MTHFD1 выявлена сильная ассоциация редкого 1958A-аллеля со сниженным риском развития ДВККЛ (OR=0,429 C.I. [0,279– 0,659], p<0,0008, табл. 1), в то время как связи данной однонуклеотидной замены с другими вариантами агрессивных лимфом не обнаружено.
Объяснением полученным данным может служить то, что однонуклеотидная замена G1958A приводит к замене Arg653Gln в формилтетрагидрафолатсинтетазном домене фермента MTHFD и уменьшает его термостабильность и метаболическую активность [7]. Поскольку субстратом данного фермента является тетрагидрофолат, потенциально его накопление способствует повышению концентрации 5,10-метилентетрагидрофолата, что, в свою очередь, может увеличивать эффективность синтеза тимидилата и метилирования ДНК, тем самым препятствуя злокачественной трансформации (рис. 1). Подтверждением этому служит ряд исследований, указывающих на протективный эффект фолата (предшественника тетрагидрофолата) в отношении НХЗЛ [6, 9].
Анализ остальных исследуемых локусов системы фо-латного цикла ассоциации с агрессивными НХЗЛ в выборке жителей г. Новосибирска не выявил.
Заключение
Проведенное исследование выявило ассоциацию полиморфного локуса G1958A гена MTHFD1 с предрасположенностью к развитию диффузной-В-крупноклеточ-ной лимфомы, что позволяет рассматривать данный локус как потенциальный маркер для включения в панель
SNPs, вклад которых в развитие и прогноз неходжкинс-ких злокачественных лимфом у жителей Западно-Сибирского региона был показан ранее [2, 4, 13]. Рискометрия НХЗЛ – это первый этап работы, направленный на выявление молекулярно-генетических предикторов, которые могут использоваться в рутинной диагностике лимфоидных неоплазий. В дальнейшем необходимо продолжить исследование на большем объеме выборки с изучением биохимических механизмов, определяющих действие полиморфных локусов генов фолатного обмена на лимфо-могенез.
Список литературы Поиск молекулярно-генетических предикторов развития агрессивных лимфом
- Аль-Ради Л.С., Барях Е.А., Белоусова И.Э. и др. Российские клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний//Современная онкология. -2014. -№S. -С. 6-126.
- Березина О.В., Поспелова Т.И., Овчинников В.С. и др. Полиморфизм глутатион-s-трансфераз m1 и т1 (GSTM1 и GSTT1) у больных неходжкинскими злокачественными лимфомами//Сибирский научный медицинский журнал. -2013. -Т. 33. -№1. -С. 40-46.
- Воропаева Е.Н., Березина О.В., Овчинников В.С. и др. Предиктивное значение тестирования полиморфного локуса Arg72Pro 4 экзона антионкогена TP53 у пациентов с неходжкинскими лимфомами//Сибирский научный медицинский журнал. -2013. -Т. 33, № 1. -С. 28-33.
- Воропаева Е.Н., Поспелова Т.И., Воевода М.И. Ассоциация полиморфизма Arg399Gln гена репарации ДНК XRCC1 с риском развития неходжкинских лимфом высокой степени злокачественности//Гематология и трансфузиология. -2013. -Т. 58, № 1. -С. 10-14.
- Ковынев И.Б., Поспелова Т.И., Агеева Т.А. и др. Частота и структура неходжкинских злокачественных лимфом в Новосибирске, НСО и городах Сибирского федерального округа//Сибирский научный медицинский журнал. -2006. -Т. 26, № 4. -С. 175-181.
- Christensen K.E., Rohlicek C.V., Andelfinger G.U. et al. The MTHFD1 p.Arg653Gln variant alters enzyme function and increases risk for congenital heart defects//Human Mutation. -2009. -Vol. 30, No. 2. -P. 212-220.
- Koutros S., Zhang Y., Zhu Y. et al. Nutrients contributing to one-carbon metabolism and risk of non-Hodgkin lymphoma subtypes//American Journal of Epidemiology. -2008. -Vol. 167, No. 3. -P. 287-294.
- Liu H., Jin G., Wang H. et al. Association of polymorphisms in one-carbon metabolizing genes and Lung Cancer risk: a case-control study in Chinese population//Lung Cancer. -2008. -Vol. 61, No. 1. -P. 21-29
- Polesel J., Dal Maso L., La Vecchia C. et al. Dietary folate, alcohol consumption and risk of non-Hodgkin lymphoma//Nutrition and Cancer. -2007. -Vol. 57, No. 2. -P. 146-150.
- Shaknovich R., Melnick A. Epigenetics and B-cell lymphoma//Curr. Opin. Hematol. -2011. -Vol. 18, No. 4. -P. 293-299.
- Skibola C.F., Curry J.D., Nieters A. Genetic susceptibility to lymphoma//Haematologica. -2007. -Vol. 92, No. 7. -P. 960-969.
- Tsou J.A., Hagen J.A. et al. DNA methylation analysis: a powerful new tool for lung cancer diagnosis//Oncogene. -2002. -Vol. 21, No. 35. -P. 5450-5461.
- Voropaeva E.N., Voevoda M.I., Maksimov V.N. et al. Prognostic impact of the tp53 rs1625895 polymorphism in dlbcl patients//British Journal of Haematology. -2015. -Vol. 169, No. 1. -P. 32-35.
- Wang L., Ke Q., Chen W. et al. Polymorphisms of MTHFD, plasma homocysteine levels, and risk of gastric cancer in a high-risk Chinese population//Clin. Cancer Res. -2007. -Vol. 13, No. 8. -P. 2526-2532.
- Weiner A.S., Gordeeva L.A., Voronina E.N. et al. Polymorphisms in folate-metabolizing genes and risk of having an offspring with congenital anomalies in the West Siberian region of Russia: a case-control study//Prenat. Diagn. -2012. -Vol. 32, No. 11. -P. 1041-1048
- Weiner A.S., Voronina E.N., Boyarskih U.A. et al. Polymorphisms in folate-metabolizing genes and risk of non-hodgkin’s lymphoma//Leukemia Research. -2011. -Vol. 35, No. 4. -P. 508-515.


