Показатели систолической функции и диссинхронии у больных инфарктом миокарда
Автор: Ярощук Наталия Андреевна, Кочмашева Валентина Викторовна, Дитятев Владимир Павлович, Кербиков Олег Борисович
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 2 (14), 2013 года.
Бесплатный доступ
С развитием трехмерной эхокардиографии в режиме реального времени, наряду с расчетом основных показателей систолической функции у больных острым инфарктом миокарда (ОИМ) сегодня появилась возможность определять дополнительные параметры, характеризующие состояние миокарда, в частности – степень диссинхронии.Цель данного исследования – выявить взаимосвязь степени диссинхронии миокарда с гемодинамическими показателями, показателями систолической функции, а также оценить ее влияние на развитие аритмических осложнений и возможное прогностическое значение.Материалы и методы: Обследовано 82 пациента с ОИМ и 65 человек контрольной группы(КГ) в возрасте 52 ±21 год. Для оценки степени диссинхронии использовался показатель Tmsv16-SD – индекс систолической диссинхронии (ИСД).Результаты: Между ИСД и СИ была отмечена умеренной силы отрицательная корреляционная связь (r = -0,58, p
Инфаркт миокарда, систолическая функция, индекс систолической диссинхронии, желудочковые аритмии
Короткий адрес: https://sciup.org/14338455
IDR: 14338455
Systolic function and dyssynchrony in patients with acute myocardial infarction
Echographic evaluation of systolic function plays an important role in examination of the patients with acute myocardial infarction (AMI). Recent developments in real-time 3D echocardiography (RT3DE) allow us to evaluate additional parameters such as the dyssynchrony.The aim of this study was to evaluate the relationship between myocardium dyssynchrony and systolic function and to assess the prognostic value of dyssynchrony and its influence on the development of arrhythmias and fatal event in post AMI period.Methods: Study population consisted of 82 (mean age 52±21) patients with AMI and 65 age and gender matched persons with similar cardiovascular risk factors, but without AMI (control group). Standard deviation of the time to the regional LV minimum systolic volume for all 16 segments Tmsv4 16-SD index was used for the assessment of dyssynchrony. The follow-up period was 6 months afterAMI.Results: Tmsv 16-SD values were significantly higher in patients with MI compared control group (6.8 ± 2.7% vs 2.9 ± 1.6 % respectively, р6.1 was associated with arrhythmic complications in post IM period (sensitivity 83.3%, specificity 87.5%, AUC=0.865, p6.1 correlates with increasing likelihood of fatal event (sensitivity 87.5%, specificity 71.6%, AUC=0.81, p
Текст научной статьи Показатели систолической функции и диссинхронии у больных инфарктом миокарда
Последнее десятилетие было отмечено рядом серьезных достижений в диагностике и лечении ишемической болезни. Но, несмотря на это, смертность от острого инфаркта миокарда (ОИМ) продолжает занимать значимое место в структуре смертности как в России, так и за рубежом. В связи с этим адекватная оценка систолической функции остается важной диагностической задачей, во многом определяющей тактику лечения больных ОИМ и дальнейший прогноз [1, 2].
Прогресс в развитии 3D эхокардиографии в режиме реального времени привел к тому, что помимо расчета основных показателей глобальной и локальной систолической функций, таких как конечно-диастолический объем (КДО), конечно-систолический объем (КСО), фракция выброса (ФВ), индекс локальной сократимости (ИЛС), сегодня появилась возможность определять дополнительные параметры, характеризующие состояние миокарда, в частности – степень диссинхронии [3-6].
До сих пор остаются открытыми вопросы, появляются ли практические преимущества в методиках трехмерной эхокардиографии и какие возможности открываются в использовании новых показателей.
Опыт применения параметров, полученных на основе использования 3D эхокардиографии, в клинической практике недостаточен [7-9].
В связи с этим представляется актуальным исследование возможности использования режима трехмерной визуализации в оценке показателей систолической функции у пациентов с ОИМ в рутинной практике лечебного учреждения и сравнение полученных результатов с данными традиционных визуализирующих методик.
Представляется важным исследование дис-синхронии левого желудочка, малоизученного феномена, существующего у здоровых лиц, возрастающей при увеличивающейся механической неоднородности миокарда. Методика определения индекса диссинхронии описана в совместных рекомендациях Американского общества эхокардиографии (ASE) и Европейского кардиологического общества (ESC) [10]. Но до сих пор отсутствуют данные о нормальных и патологических значениях данного показателя, и его изменении при ОИМ.
Одной из задач настоящего исследования была попытка найти возможную зависимость между внутрижелудочковой диссинхронией и гемодинамическими показателями у пациентов с ОИМ, а также проследить связь данного индекса с клиническим течением заболевания, в том числе с такими осложнениями, как развитие нарушений ритма в виде пароксизмов желудочковой тахикардии, фибрилляции желудочков, которые продолжают оставаться грозным осложнением ОИМ, увеличивающим риск летальности в этой группе больных.
Цель данного исследования: Изучить показатели диссинхронии у пациентов с ОИМ, сравнить их с показателями представителей контрольной группы. Выявить возможную взаимосвязь между степенью механической неоднородности миокарда с гемодинамическими показателями, а также оценить ее влияние на развитие аритмических осложнений и прогностическое значение.
Материалы и методы: Для оценки механической диссинхронии обследовано 147 человек (82 пациента с ОИМ и 65 человек контрольной группы). Возраст пациентов составил 52±21 г.
Помимо общеклинических и лабораторных исследований больным проводились электрокардиография и суточное мониторирование ЭКГ по Холтеру. Эхокардиография проводилась на аппарате IЕ 33 (Philips) c использованием матричного датчика Х-3.1 и выполнялась по стандартной методике, рекомендованной АСС и Американского общества эхокардиографии (АSE). Основные параметры систолической функции определялись в двухмерном и трехмерном режимах (КДО, КСО, ФВ). Оценка локальной сократительной функции проводилась с вычислением индекса локальной сократимости (ИЛС). Обработка данных выполнена c помощью программного обеспечения Qlab 3DQAdvanced (Philips).
Механическая диссинхрония оценивалась по степени дисперсии во времени достижения минимального объема на уровне каждого из 16 сегментов. Для оценки степени диссинхронии использовался показатель Tmsv 16-SD – величина, характеризующая стандартное отклонение времени систолического сокращения между сегментами левого желудочка (16 сегментов, за исключением апикального). Данный показатель определялся как индекс систолической диссинхронии (ИСД).
В исследование не включены больные с неудовлетворительной визуализацией сердца, с ХСН II и выше по классификации NYHA, с клапанными пороками сердца, нарушением проводимости, фибрилляцией предсердий и с имплантированными ЭКС.
Cтатистическая обработка данных проводилась с помощь программы "Statistica 6.1"
(StatSoft, USA). Для нормально распределенных показателей данные представлены в виде Mе±me, где Ме – медиана, me – стандартное отклонение. Количественные показатели с ненормальным распределением представлены в виде медианы (Mе) и процентилей (25-й и 75й процентиль). Для оценки различий между двумя выборками по уровню количественного признака использован U-критерий Манна-Уитни. При выявлении связей между сопоставляемыми показателями применялся метод рангового корреляционного анализа Спирмена. Статистически значимыми считались различия при р<0,05.
Результаты: Значения ИСД достоверно отличались у пациентов с ОИМ и контрольной группы и составили соответственно: 6,8 ± 2,7 % и 2,9 ± 1,6 % (р<0,001).
При вычислении гемодинамических показателей получены следующие данные: сердечный индекс (СИ) в группе с ОИМ составил 2,7 ± 0,26, в контрольной группе 3,6±0,35 (p<0,05). Была выявлена умеренной силы отрицательная корреляционная связь ИСД с СИ (r =-0,58, p<0,008).
Достоверной зависимости значений ИСД от уровня АД (р=0,82) и ЧСС (р=0,4) получено не было (табл 1).
При значениях ЧСС 60 - 90 мм рт. ст. ИСД составил 6,7 (4,7-8,7), при ЧСС от 90 до 125 мм рт. ст. – 6,8 (4,7-9,0) (р=0,4).
Значения критерия Манна-Уитни для ИСД при различных показателях САД и ДАД составили р=0,76 и р=0,82 соответственно.
Особый интерес могут представлять данные, полученные при анализе показателей диссихронии и значений, характеризующих легочную гипертензию, у исследуемой группы больных.
Величина ЛГ в исследовании определялась как максимальное систолическое давление в легочной артерии (СДЛА) и рассчитывалось по скорости трикуспидальной регургитации. Патологическим значением ЛГ было принято значение СДЛА выше 30 мм рт.ст.
В таблице 2 представлены данные ИСД 1, соответствующего высокому (СДЛА1) и ИСД 2, нормальному или умеренно повышенному давлению в легочной артерии (СДЛА2). Разница между значениями ИДС была достоверной (р=0,03).
Таблица 1
|
Параметры |
Me (max-min) |
25-й процентиль |
75-й процентиль |
Стандартное отклонение |
|
ИСЛСАД115-140 |
5,9 (4,6-7,9) |
4,7 |
7,9 |
2,7 |
|
ИСДСАД140-180 |
6,0 (4,8-8.1) |
4,9 |
8,0 |
2,8 |
|
ИСД ДАД 64 -90 |
6,5 (4,7-9,5) |
4,7 |
7,9 |
2,9 |
|
ИСДДАД 90-122 |
6,8 (4,6-10,1) |
4,9 |
7,6 |
2,8 |
Значения показателя ИСД при различных значениях СДЛА
Таблица 2
|
Параметры |
Me (max-min) |
25-й процентиль |
75-й процентиль |
Стандартное отклонение |
|
ИСД 1 |
4,9* (3,3-6,5) |
4,1 |
5,1 |
0,75 |
|
СДЛА 1 |
55,0 (46,0-67) |
50 |
56 |
5,58 |
|
ИСД 2 |
6,1* (3,9-10,2) |
5,0 |
7,7 |
1,88 |
|
СДЛА 2 |
33,0 (22-44) |
27 |
34 |
5,79 |
*Достоверная разница ИСД 1 и ИСД 2 р = 0,03
Значения ИСД при различных уровнях артериального давления у пациентов основной группы
Значения ИСД при легочной гипертензии (максимальное систолическое давление в легочной артерии (СДЛА) 55,0±5,58 мм рт. ст.) составило 4,9±0,75, при отсутствии легочной гипертензии (СДЛА 33±5,76 мм рт. ст.) – 6,1±1,88, (р=0,03); более низкие значения ИДС соответствуют более высоким значениям СДЛА (была зарегистрирована отрицательная умеренной силы корреляционная cвязь r = - 0,4, p<0,05) (рис.1).
При сопоставлении ИСД с основными показателями систолической функции отмечена cильная положительная корреляционная связь между ИСД и КДО (r=0,63; р<0,05) и отрицательная с ФВ (r = - 0,73; p<0,05).
При увеличении значений КДО и КСО пропорционально увеличивались значения ИСД. Значения ИСД также пропорционально повышались при снижении ФВ.
У 28 пациентов (34%) основной группы
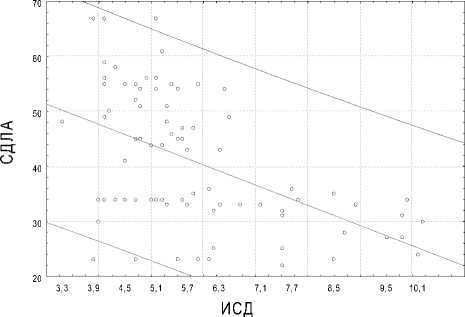
Рис. 1. Корреляция между ИСД и СДЛА.
увеличение ИСД отмечено при нормальных значениях КДО и ФВ.
У 68 (83%) пациентов была зарегистрирована желудочковая экстрасистолия высоких градаций, пробежки желудочковой тахикардии или эпизоды фибрилляции желудочков. Согласно данным ROC-анализа, значения индекса ИСДИМ, превышающие 6.1, связаны с развитием эпизодов нарушения ритма сердца, чувствительность 83,3%, специфичность 87,5%, площадь под кривой (areaundercurve – AUC)= 0.865, p<0.0001.
Также по результатам ROC-анализа отмечена взаимосвязь между ИСДИМ и смертностью. Значения ИСДИМ, превышающие 5.8, указывают на повышенную вероятность развития фатального события, чувствительность 87.5%, специфичность 71,6%, площадь под кривой (area-undercurve – AUC)= 0.81, p<0.0001) (рис. 2).
исдим
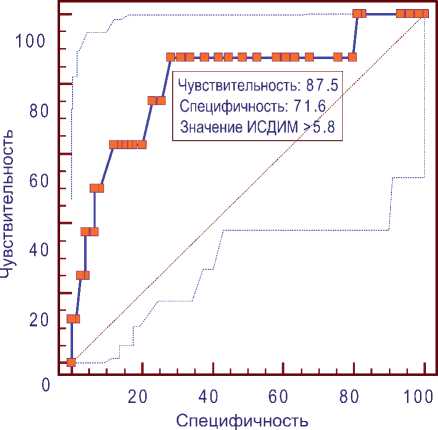
Рис. 2. ROC анализ. Взаимосвязь между ИСД и фатальными событиями.
Обсуждение результатов: В последнее десятилетие в повседневную клиническую практику вошли ультразвуковые приборы, позволяющие получать трехмерные изображения в режиме реального времени, что способствовало новому пониманию морфологии сердца, и также позволило производить более корректные расчеты показателей систолической функции [11-14] (рис. 3).
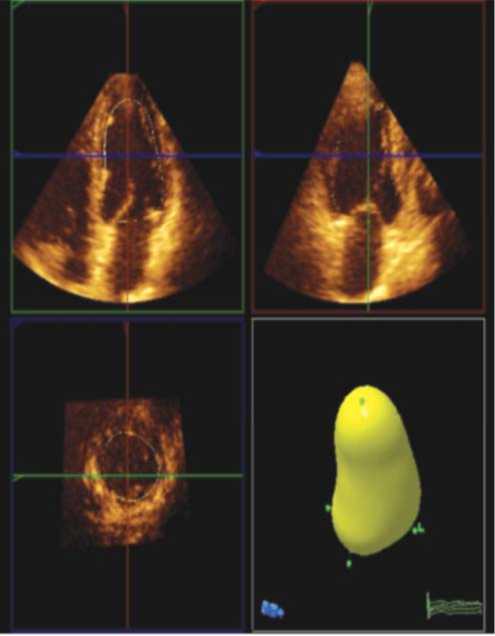
Рис 3. Определение систолического объема левого желудочка в режиме 3D.
Появление ультразвукового оборудования нового поколения позволяет надеяться на повышение диагностических возможностей в исследовании больных ИМ. [15]
Помимо изучения структуры, объемов и локальной сократимости ЛЖ, режим трехмерной визуализации позволяет оценить целый ряд важных параметров, таких как механическая диссинхрония миокарда. В настоящее время его используют для количественной оценки электромеханической диссинхронии больных с выраженной сердечной недостаточностью. Именно по нему предлагается определять степень успешности ресинхронизирующей терапии [16, 17].
Показатели механической неоднородности оцениваются автоматически после определения КДО и КСО и построения сегментарной модели ЛЖ. Они представляют собой величину, характеризующую стандартное отклонение времени систолического сокращения между сегментами левого желудочка. Показатели можно рассчитывать между 16 сегментами и 12 сегментами, оценивая базальные и средние сегменты, или только базальные сегменты. При этом возможно вычислять время отклонения сокращения самого быстрого и самого медленного сегментов ЛЖ. Вычисляются они в миллисекундах или в процентах к времени сердечного цикла.
Один из таких показателей, получивший название индекса систолической диссинхро-нии (ИСД) (sistolyc dissynchrony index – SDI), является наиболее употребляемым.
В рекомендациях по трехмерной эхокардиографии EAE и ASE 2012 года дано следующее определение ИСД: «Это индекс, рассчитанный как отклонение времени региональной фракции выброса (времени достижения минимального объема в каждом сегменте)».
Большинство проведенных на сегодняшний день исследований ИСД посвящено изучению степени диссинхронии у пациентов с различными степенями выраженности сердечной недостаточности, с имплантируемыми кардиостимуляторами. В работах ряда авторов ИСД демонстрировал корреляцию с КДО КСО и ФВ левого желудочка, и был способен отразить эффективность ресинхронизирующей терапии у пациентов со значительными проявлениями сердечной недостаточности. Отмечена высокая воспроизводимость данного показателя [18-20]. Но попытки оценить ИСД в аспекте нарушений при ОИМ немногочисленны.
В доступной нам литературе не было обнаружено работ, оценивающих связь этого показателя с клиническим течением заболевания и гемодинамическими параметрами.
Учитывая тот факт, что ИСД может нести информацию о контрактильной функции всех сегментов, представляется интересным изучение динамики изменения его значений при нарушении регионарной сократимости у пациентов ОИМ. Вполне вероятно, что использование ИСД позволит получить дополнительный количественный показатель, характеризующий изменения сегментарной кинетики миокарда.
ИМ в ранние сроки нередко протекают на фоне легочной гипертензии (ЛГ). В механизме возникновения ЛГ в данном случае ведущую роль играет снижение систолической функции, которое приводит к повышению давления в левых камерах. Гипертензия из левого предсердия передается на легочные сосуды и далее на правые отделы сердца [21].
При сопоставлении значений ИСД с показателями легочной гипертензии обнаружена следующая закономерность: более низкие значения ИДС соответствуют более высоким значениям СДЛА (была зарегистрирована отрицательная умеренной силы корреляционная cвязь r = - 0,4).
Данная особенность может быть вызвана следующими процессами: повышение давления в правых камерах оказывает дополнительное влияние на характер движения межжелудочковой перегородки, приводя к уменьшению ее подвижности, уплощению, что приводит, в свою очередь, к уменьшению степени дис-синхронии.
В доступной литературе нами не было обнаружено сравнения показателей механической неоднородности миокарда в зависимости от степени легочной гипертензии. Этот важный аспект, оказывающий влияние на клиническое течение ОИМ, безусловно требует дальнейшего изучения.
Развитие осложнений, в том числе целого ряда нарушений ритма сердца, значительно ухудшает прогноз больных ОИМ и приводит к увеличению количества летальных случаев [22, 23]. Согласно современным данным, развитие тех или иных аритмий зарегистрировано у 90% больных ОИМ. Это суправентрикулярная экстрасистолия, тахикардия, фибрилляция и трепетание предсердий, нарушение атрио-вентриокулярной проводимости. Одним из наиболее опасных аритмогенных осложнений является желудочковая тахикардия (ЖТ), так как именно у этих больных высок риск внезапной смерти [24, 25]. Патогенез развития ЖТ на фоне ишемии и некроза заключается в следующем: ишемия влияет на формирование потенциала действия, преодолевает рефрактерность, нарушает распространение возбуждения. При ОИМ некроз кардиомиоцитов развивается неравномерно: в области ИМ рубцовая ткань соседствует с работающим миокардом. Это служит морфологическим субстратом для повторного входа возбуждения (два пути с разной скоростью проведения и однонаправленной блокадой проведения в одном из них). ЖТ при
ОИМ, как правило, полиморфная [26-28].
Полученные результаты продемонстрировали, что ИСД ассоциирован с осложненным течением ИМ. Величина ИСД имела более сильную положительную корреляционную связь с желудочковыми нарушениями ритма, которые продолжают рассматриваться как предиктор внезапной смерти у больных в ранние сроки ИМ.
Согласно данным ROC анализа получена связь ИСД с летальным исходом в течение первых шести месяцев у пациентов, перенесших ОИМ, что позволяет надеяться на будущую возможность применения этого параметра в прогностических шкалах у таких больных в случае подтверждения наших выводов. Однако для более точной оценки прогностической информативности индекса необходимы дополнительные более масштабные исследова- ния, сопоставленные с клинической экспертной оценкой.
Выводы:
-
1. Значения ИСД у пациентов с ОИМ достоверно выше, чем у представителей контрольной группы. У 34% основной группы повышенный ИСД был зарегистрирован при нормальных значениях КДО и ФВ, что позволяет расценивать его как дополнительный показатель, характеризующий патологические изменения миокарда при инфаркте.
-
2. ИСД связан с такими гемодинамическими показателями как СИ и легочная гипертензия.
-
3. Согласно данным ROC анализа, высокие значения ИСД могут быть связаны с развитием аритмических осложнений и, возможно, указывают на повышенную вероятность развития фатального события.
Список литературы Показатели систолической функции и диссинхронии у больных инфарктом миокарда
- Алехин М.Н., Сидоренко Б.А. Современные подходы к эхокардиографической оценке систолической функции сердца. Кардиология. 2007;7: 4 12.
- Беленков Ю.Н. Терновой С.К. Функциональная диагностика сердечно-сосудистых заболеваний. М.: ГЭОТАР-Медиа; 2007; с. 355-412.
- Corsi C., Lang R.M.,Veronesi F. [et al.] Volumetric quantification of global and regional left ventricular function from real-time three-dimensional echocardiographic images. Circulation. 2005;112:1161-70.
- Sugeng L., Mor-Avi V., Lang R.M. Three-dimensional echocardiography: coming оf age. Heart. 2008 Sep; 94(9):1123-5.
- Muraru D., Badano L.P., Piccoli G. Validation of a novel automated border-detection algorithm for rapid and accurate quantitation of left ventricular volumes based on three-dimensional echocardiography. Eur J Echocardiogr. 2010 May;11(4):359-68.
- Кapetanakis S., Kearney M.Т., Siva А. [et al.] Real-Time three-dimensional echocardiography: a novel technique to quantify global left ventricular mechanical dyssynchrony. Circulation. 2005 Aug 16; 112(7): 992-1000.
- Hare J.L., Jenkins C., Nakatani S. [et al.] Feasibility and clinical decision-making with 3D echocardiography in routine practice. Heart. 2008 Apr; 94(4):440-5.
- Lang RM, Mor-Avi V, Dent JM, Kramer CM. Three-dimensional echocardiography: is it ready for Everyday Clinical Use? JACC Cardiovasc Imaging. 2009 Jan;2(1):114-7.
- Soliman O.I.I., Van Dalen B.M., Geleijnse ML. Semi-automated left ventricular function assessment by real-time three-dimensional echocardiography is ready for prime time. Eur Heart J. 2009; 30(18): (Suppl 1) р.342.
- 10/ASERECOMMEND
- Jenkins C., Chan J, Hanekom L, Marwick TH. Accuracy and feasibility of online 3-dimensional echocardiography for measurement of left ventricular parameters. J Am Soc Echocardiogr. 2006; 19(9): 1119-28.
- Jaochim Nesser H, Sugeng L, Corsi C. [et al.] Volumetric analysis of regional left ventricular function with real-time three-dimensional echocardiography: validation by magnetic resonance and clinical utility testing. Heart. May;93(5):572-8.
- Leung KY, Bosch JG. Automated border detection in three-dimensional echocardiography: principles and promises. Eur J Echocardiogr. 2010 Mar; 11(2): 97-108.
- Iskandrian A.E., Hage F.G. Imaging Acute MI in the 21st Century. JACC Cardiovasc Imaging. 2013 Mar; 6(3): 370-2.
- Аlonso L. Hari P., Pidlaoan V. Acute myocarditis: can novel echocardiographic techniques assist with diagnosis? Eur J Echocardiogr. 2010 Apr;11(3):E5.
- Zhang Q, Yu C,M. Clinical Implication of Mechanical Dyssynchrony in Heart Failure. J Cardiovasc Ultrasound. 2012 Sep;20(3):117-23.
- De Castro S, Faletra F, Di Angelantonio E. [et al.]. Tomographic left ventricular volumetric emptying analysis by real-time 3-dimensional echocardiography: influence of left ventricular dysfunction with and without electrical dyssynchrony. Circ Cardiovasc Imaging. 2008 Jul;1(1):41-9.
- Smiseth OA, Russell K, Skulstad H. The role of echocardiography in quantification of left ventricular dyssynchrony: state of the art and future directions. Eur Heart J Cardiovasc Imaging. 2012 Jan;13(1):61-8.
- Lamia B. Tanabe М., et al. Quantifying the role of regional dyssynchrony on global left ventricular performance. JACC Cardiovasc Imaging; 2009; 2(12): 1350-6.
- Mollema S.A., Liem S.S. Left ventricular dyssynchrony acutely after myocardial infarction predicts left ventricular remodeling. Am J Coll Cardiol. 2007, Oct 16; 50(16):1532-72.
- Weir R.A., McMurray J.J. Epidemiology of heart failure and left ventricular systolic dysfunction after acute myocardial infarction: prevalence, clinical characteristics and prognostic importance. Am J Cardiol; 2006, May 22;97(10A):13-25.
- Бойцов С.А. Никулина Н.Н. Внезапная сердечная смерть у больных ишемической болезнью сердца. (По результатам Российского многоцентрового качества диагностики и лечения острых форм ИБС (РЕЗОНАНС)/Бойцов С.А.,//Российский кардиологический журнал. 2011, 2 (88) стр. 59-64.
- Costal F. Ferreiral J. Impact of ESC/ACCF/AHA/WHF universal definition of myocardial infarction on mortality at 10 years. Eur Heart J; 2012, Vol. 33(20): 2544-50.
- Marijon E. Puymirat E. [et al.], Ventricular fibrillation is a major determinant of in-hospital mortality but does not impact long-term mortality after myocardial infarction: the FAST-MI registry. Eur Heart J. 2011 Aug; Vol. 32 (Suppl 1): 869.
- deKam P.J., Nicolosi G.L. [et al.] Prediction of 6 months left ventricular dilatation after myocardial infarction in relation to cardiac morbidity and mortality. Application of a new dilatation model to GISSI-3 data. Eur Heart J. 2002,Vol.23(7):536-42.
- Gajarsa J.J., Kloner R.A. Left ventricular remodeling in the post-infarction heart: a review of cellular, molecular mechanisms, and therapeutic modalities. Heart Fail Rev. 2011 Jan;16(1): 13-21.
- French B.A., Kramer C.M. Mechanisms of PostInfarct Left Ventricular Remodeling. Drug Discov Today Dis Mech. 2007;4(3):185-196.
- Yousef Z.R., Redwood S.R., Marber M.S. Postinfarction left ventricular remodeling: a pathophysiological and therapeutic review. Cardiovasc Drugs Ther. 2000; Vol.14(3): 243-52.


