Полный лечебный патоморфоз рака желудка после одного цикла неоадъювантной химиотерапии по схеме FLOT (клиническое наблюдение)
Автор: Скоропад В.Ю., Кудрявцев Д.Д., Шитарева В.Н., Жаворонкова Е.С.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 6 т.21, 2022 года.
Бесплатный доступ
Актуальность. Среди злокачественных новообразований рак желудка занимает пятое место по заболеваемости и третье место по смертности в мире. По показателю смертности в России он занимает второе место (10,7 %). В России и многих зарубежных странах стандартом лечения местнораспространенного рака желудка является применение хирургического метода в комбинации с адъювантной или перио-перационной химиотерапией. Наиболее часто применяется трехкомпонентная схема химиотерапии FLOT, назначаются по четыре цикла пред- и послеоперационно. Основанием для широкого внедрения данной методики химиотерапии послужили результаты крупного рандомизированного исследования FLOT4, согласно которому периоперационная схема FLOT показала большую эффективность в сравнении со схемой ECF. Цель исследования - демонстрация возможности достижения полного лечебного патоморфоза и длительной ремиссии в лечении пациента с местнораспространенным раком желудка после одного курса неоадъювантной полихимиотерапии по схеме FLOT. Описание клинического случая. Пациент В., 69 лет, обратился в МРНЦ им. А.Ф. Цыба с жалобами на общую слабость, умеренные боли в эпигастрии в течение 2 мес. При обследовании установлен диагноз: рак тела желудка сТ31\10М0 iiA стадии. Был проведен один цикл неоадъювантной химиотерапии по схеме FLOT. Вследствие того что у больного развилось массивное кровотечение из опухоли, было принято решение прекратить проведение неоадъювантной терапии и выполнить хирургическое лечение. Операция была выполнена в объеме дистальной субтотальной резекции желудка с лимфодиссекцией D2. При морфологическом исследовании удаленного препарата была зарегистрирована 1а степень лечебного патоморфоза (по классификации K. Becker, 2003). На момент анализа пациент жив без признаков прогрессирования опухоли в течение более 36 мес, находится под динамическим наблюдением. Заключение. В представленном клиническом наблюдении продемонстрировано достижение полного лечебного патоморфоза после одного цикла неоадъювантной химиотерапии, а также 3-летняя безрецидивная выживаемость пациента.
Рак желудка, периоперационная химиотерапия flot, хирургическое лечение, гастрэктомия, лечебный патоморфоз, динамическое наблюдение
Короткий адрес: https://sciup.org/140296638
IDR: 140296638 | УДК: 616.33-006.6-08:615.28 | DOI: 10.21294/1814-4861-2022-21-6-164-169
Clinical case of pathological complete response of gastric cancer after one cycle of neoadjuvant chemotherapy with FLOT regimen
Background. Gastric cancer is the 5th most common cancer and the 3rd leading cause of cancer death globally. In Russia, gastric cancer is the 2-nd leading cause of death (10.7 %). Surgery in combination with perioperative/adjuvant chemotherapy is the standard treatment for locally advanced gastric cancer. Four cycles of neoadjuvant chemotherapy and 4 cycles of adjuvant chemotherapy with the FLOT regimen is the most widely used treatment modality. The basis for the widespread use of this chemotherapy regimen was the results of a large randomized FLOT4 trial, according to which the perioperative FLOT regimen showed greater efficacy compared to the ECF regimen. The aim of the study was to demonstrate the feasibility of achieving patholopgical complete response and long-term remission after one course of neoadjuvant chemotherapy with FLOT regimen in a patient with locally advanced gastric cancer. Case description. A 69-year-old patient presented to A. Tsyb Medical Radiological Research Centre with complaints of general weakness, moderate epigastric pain for 2 months. The examination revealed stage T3N0M0 IIA gastric cancer. The patient received one cycle of neoadjuvant chemotherapy with the FLOT regimen. Given the fact, that the patient developed massive bleeding from the tumor, it was decided to stop neoadjuvant treatment. Subtotal gastrectomy with D2 lymph node dissection was performed. Histological examination of the surgical specimen revealed pathological complete response (grade 1a according to the classification of K.Becker et al., 2003). The patient is alive with no signs of disease progression for more than 36 months after starting the treatment. Conclusion. This clinical case demonstrated personalized approach to the treatment of patients with locally advanced gastric cancer. Pathological complete response was achieved after one cycle of neoadjuvant chemotherapy.
Текст научной статьи Полный лечебный патоморфоз рака желудка после одного цикла неоадъювантной химиотерапии по схеме FLOT (клиническое наблюдение)
Послеоперационный период протекал без осложнений. Выписан на 7-е сут после операции в удовлетворительном состоянии. На данный момент пациент жив без признаков прогрессирования в течение более 36 мес.
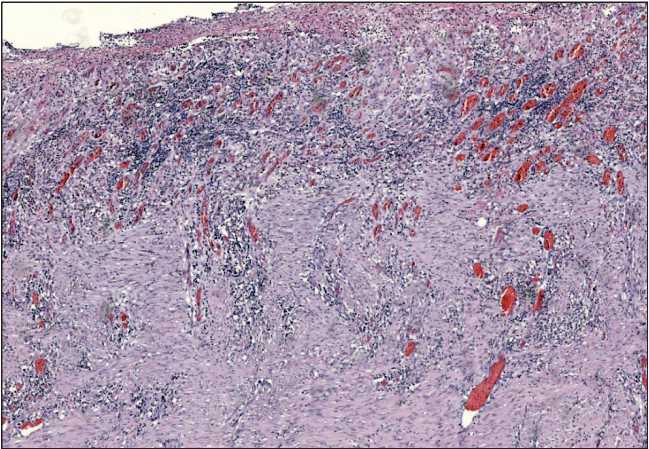
Fig. 1. Microphoto. The growth of granulation tissue covered with detritus and fibrin, the proliferation of loose fibrous connective tissue with focal lymphocytic infiltration, full-blooded thin-walled capillary vessels in the stomach wall. Morphological picture of pathological complete response of grade 1a by Becker. Staining hematoxylin-eosin, ×40
Обсуждение
-
H. Cho et al. [4] проанализировали данные о 22 пациентах с полной морфологической регрессией первичной опухоли и регионарных лимфатических узлов после неоадъювантной химиотерапии. Преобладали клиническая III/IV стадия (86 %), низкая степень дифференцировки (62 %) и инфильтративные формы (64 %) опухоли. Во всех случаях выполнена радикальная операция с лимфаденэктомией D2/D3. При медиане наблюдения 76 мес метастазы выявлены у 3 пациентов; 5-летняя общая и безре-цидивная выживаемость составили 85 и 75 % соответственно. Таким образом, авторы заключили, что в случае полной морфологической регрессии опухоли после неоадъювантной терапии больные имеют очень высокие показатели выживаемости.
Список литературы Полный лечебный патоморфоз рака желудка после одного цикла неоадъювантной химиотерапии по схеме FLOT (клиническое наблюдение)
- I. Sung H., Ferlay J., Siegel R.L., Laversanne M., Soerjomataram I., Jemal A., Bray F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021; 71(3): 209-49.
- Злокачественные новообразования в России в 2020 году (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М., 2021. 252 с.
- Al-Batran S.E., Homann N., Pauligk C., Goetze T.O., Meiler J., Kasper S., Kopp H.G., Mayer F., Haag G.M., Luley K., Lindig U., Schmiegel W., Pohl M., Stoehlmacher J., Folprecht G., Probst S., Prasnikar N., Fischbach W., Mahlberg R., Trojan J., Koenigsmann M., Martens U.M., Thuss-Patience P., Egger M., Block A., Heinemann V., Illerhaus G., Moehler M., Schenk M., Kullmann F., Behringer D.M., Heike M., Pink D., Teschendorf C., Lohr C., Bernhard H., Schuch G., Rethwisch V., von Weikersthal L.F., Hartmann J.T., Kneba M., Daum S., Schulmann K., Weniger J., Belle S., Gaiser T., Oduncu F.S., Guntner M., Hozaeel W., Reichart A., Jager E., Kraus T., Monig S., Bechstein W.O., Schuler M., Schmalenberg H., Hofheinz R.D.; FLOT4-AIO Investigators. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarci-noma (FLOT4): a randomised, phase 2/3 trial. Lancet. 2019; 393(10184): 1948-57.
- Cho H., Nakamura J., Asaumi Y., Yabusaki H., Sakon M., Takasu N., Kobayashi T., Aoki T., Shiraishi O., Kishimoto H., Nunobe S., Yanagisawa S., Suda T., Ueshima S., Matono S., Maruyama H., Tatsumi M., Seya T., Tanizawa Y., Yoshikawa T. Long-term survival outcomes of advanced gastric cancer patients who achieved a pathological complete response with neoadjuvant chemotherapy: a systematic review of the literature. Ann Surg Oncol. 2015; 22(3): 787-92.
- Hu Q., Wang J., Xu W-G., Shao P., Li G. Survival outcomes of locally advanced gastric cancer cases with pathological complete response received neoadjuvant chemotherapy. Precision Medical Sciences. 2021; 10(2): 78-82.
- Трусилова Е.В., Бесова Н.С., Горбунова B.A., Глухов Е.В., Неред С.Н., Стилиди И.В., Меликов С.А., Перфильев И.Б., Бондаренко Ю.В. Полная патоморфологическая регрессия опухоли желудка после проведения неоадъювантной химиотерапии у больного местнораспространенным раком желудка. Клинический случай. Вестник РОНЦ им. Н. Н. Блохина РАМН. 2013; 24(1).
- Mc Laren P.J., Barnes A.P., Terrell W.Z., Vaccaro G.M., Wiedrick J., Hunter J.G., Dolan J.P. Specific gene expression profiles are associated with a pathologic complete response to neoadjuvant therapy in esophageal adenocarcinoma. Am J Surg. 2017; 213(5): 915-20. 10.1016/j. amjsurg.2017.03.024.
- Мозеров С.А., Скоропад В.Ю., Новиков Н.Ю., Михайлова Г. Ф., Силантьева Н.К., Агабабян Т.А., Бекетова О.Г., Комин Ю.А., Чаиркин И.Н., Пашкин С.Б.,Мозерова Е.С. Гистологическая и молекулярно-генетическая оценка ответа опухоли на химио-лучевую терапию при раке желудка. Современные проблемы науки и образования. 2017; (4): 76.
- Sun J., Wang X., Zhang Z., Zeng Z., Ouyang S., Kang W. The Sensitivity Prediction of Neoadjuvant Chemotherapy for Gastric Cancer. Front Oncol. 2021; 11.


