Получение и свойства аминиевых солей (1-гидроксиэтилиден)дифосфоновой кислоты
Автор: Семенов Владимир Викторович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 1 т.13, 2021 года.
Бесплатный доступ
Представлен обзор методов получения и свойств аминиевых солей (1-гидроксиэтилиден)дифосфоновой кислоты. (1-Гидроксиэтилиден)дифосфоновая кислота с моноэтаноламином образует кристаллическое соединение, которое по данным элементного анализа и РСА представляет собой тройную C(CH3)(OH)[P(O)O-NH3+CH2CH2OH]3[P(O)(OH)] аминную соль. Характерной особенностью производных (1-гидроксиэтилиден)дифосфоновой кислоты и трис(гидроксиметил)аминометана является образование стекловидных и смолообразных продуктов. Их состав Н4L∙4NH2C(CH2OH)3 соответствует 4 молекулам основания на 1 молекулу четырехосновной кислоты. Присоединение 4 молекул первичного амина происходит как при соотношении исходных реагентов 1 : 4, так и 1 : 3. Полимерное строение и наличие сильных водородных связей в соединении Н4L∙4NH2C(CH2OH)3 приводят к его очень малой растворимости в органических средах и хорошей растворимости в воде. Растворимость Н4L∙4NH2C(CH2OH)3 в метаноле составляет 1,8 г в 100 мл. Взаимодействие (1-гидроксиэтилиден)дифосфоновой кислоты с парааминобензойной кислотой приводит к образованию бис(4-карбоксифениламиний)(1-гидроксиэтилиден)дифосфоната C(CH3)(OH)[P(O)(OH)O-NH3+C6H4С(О)ОН]2. В кристалле это соединение состоит из аниона дважды депротонированной (1-гидроксиэтилиден)дифосфоновой кислоты C(CH3)(OH)[P(OH)(O)O-]2 и двух аминных катионов NH3+C6H4С(О)ОН. Четырехосновная кислота связывает 3 молекулы морфолина, давая трис(морфолиний)(1-гидроксиэтилиден)дифосфонат H4L·3HN(CH2CH2)2O в виде порошка белого цвета, хорошо растворяющегося в воде, метиловом и этиловом спиртах. Твердый комплекс морфолина с (1-гидроксиэтилиден)дифосфоновой кислотой не кристаллизуется из различных растворителей, что может быть вызвано олигомерной формой морфолина, входящего в молекулу комплекса с H4L.
Соли аминов, (1-гидроксиэтилиден)дифосфоновая кислота, моноэтаноламин, трис(гидроксиметил)аминометан, парааминобензойная кислота, морфолин
Короткий адрес: https://sciup.org/147234250
IDR: 147234250 | УДК: 547.233.1, | DOI: 10.14529/chem210109
Preparation and properties of (1-hydroxyethylidene) diphosphonic acid aminium salts
An overview of the preparation methods and properties of (1-hydroxyethylidene) diphosphonic acid aminium salts is presented. (1-Hydroxyethylidene) diphosphonic acid with monoethanolamine forms a crystalline compound, which, according to the elemental analysis and XRD data, is ternary C(CH3)(OH)[P(O)O-NH3+CH2CH2OH]3[P(O)(OH)] amine salt. A characteristic feature of the derivatives of (1-hydroxyethylidene) diphosphonic acid and tris (hydroxymethyl)aminomethane is the formation of glassy and resinous products. Their composition Н4L∙4NH2C(CH2OH)3 corresponds to 4 base molecules per 1 tetrabasic acid molecule. The addition of 4 molecules of the primary amine occurs both when the ratio of the initial reagents is 1: 4 and 1: 3. The polymer structure and the presence of strong hydrogen bonds in the Н4L∙4NH2C(CH2OH)3 compound lead to its very low solubility in organic media and good solubility in water. The solubility of Н4L∙4NH2C(CH2OH)3 in methanol is 1.8 g per 100 mL. The reaction of (1-hydroxyethylidene)diphosphonic acid with para-aminobenzoic acid leads to the formation of bis(4-carboxyphenylamine)(1-hydroxyethylidene)diphosphonate C(CH3)(OH)[P(O)(OH)O-NH3+C6H4С(О)ОН]2. In a crystal, this compound consists of the anion of the double-deprotonated (1-hydroxyethylidene)diphosphonic acid C(CH3)(OH)[P(OH)(O)O-]2 and two amine cations NH3+C6H4С(О)ОН. The tetrabasic acid binds 3 molecules of morpholine, giving tris(morpholinium)(1-hydroxyethylidene)diphosphonate H4L·3HN(CH2CH2)2O in the form of a white powder that dissolves well in water, methyl and ethyl alcohols. The solid complex of morpholine with (1-hydroxyethylidene)diphosphonic acid does not crystallize from various solvents, which may be caused by the oligomeric form of morpholine included in the molecule of the complex with H4L.
Текст научной статьи Получение и свойства аминиевых солей (1-гидроксиэтилиден)дифосфоновой кислоты
Органические амины различного строения широко представлены [1] в перечне фармацевтических препаратов. Переведение их в водорастворимое состояние достигается посредством реакций с протонными кислотами. Соли аминов широко используется в фармацевтической промышленности. N-Карбоксиметил-трис(гидроксиметил)аминометан (трицин) (HOCH2)3C-NH2+-CH2-COO-) известен [2] как буфер в биохимических исследованиях и комплексобразователь для многих катионов металлов, а также как эффективная ловушка [3] гидроксильных радикалов. Его аналог - N-карбоксиэтил-трис(гидроксиметил)аминометан (гомотрицин) (HOCH2)3C-NH2+-CH2CH2-COO-) используется [4] для связывания ионов TcO42- c целью последующего введения в живой организм в качестве радиоактивной метки. Аминиевые производные триэтаноламина и 2-метилфеноксиуксусной кислоты [HN(CH2CH2OH)3] +[CH3-C6H4-CH2COO]- «крезацин» и «трекре-зан» [5, 6] применяются в медицине и сельском хозяйстве. Известно несколько примеров приложений солей аминов в синтезе. Так, на основе 1-(3-аминопропил)силатрана и арил(гетарил)окси(сульфанил)уксусных кислот получены [7] ионные жидкости состава [N(CH2CH2O)3SiCH2CH2CH2NH3]+[RCOO]-. Ряд ионных жидкостей синтезирован из триэтаноламина и карбоновых кислот [8–10], из хлористоводородного диэтаноламина и хлоридов желе-за(Ш) и кобальта(И) [11]. Предложен [12] новый путь образования 1-хлорсилатрана N(CH2CH2O)3SiCl через взаимодействие хлористоводородного триэтаноламина
[HN(CH2CH2OH)3]+Cl- с тетрахлор-, винил- и фенилтрихлорсиланами. 1-Фторсилатран N(CH2CH2O)3SiF получен [13] из фтористоводородного триэтаноламина [HN(CH2CH2OH)3]+F- и тетраэтоксисилана Si(OEt)4. Фторхромат триэтиламиния предложен [14] в качестве мягкого, ста- бильного и дешевого окислителя на основе шестивалентного хрома. Синтезированы и изучены кристаллическая и молекулярная структура хлорида 1-(3-аминийпропил)силатрана [15] [N(CH2CH2O)3SiCH2CH2CH2NH3]+Cl–, сульфата трис(гидроксиметил)аминийметана [16] [(HOCH2)3C-NH3]2+[SO4]2–, моногидрата сульфита N-(гидроксиэтил)этилендиаминия [17] [HOCH2CH2NH2+CH2CH2NH3+][SO3]2–, трис(2-гидроксиэтил)аминиевой соли янтарной кислоты [18] 2[HN(CH2CH2OH)3]+[O(О)С-CH2CH2-C(O)O]2–.
Методы получения и свойства аминопроизводных простых протонных кислот хорошо изучены. В настоящей работе сделано обобщение полученных нами недавно результатов о способах получения и свойствах солей аминов (1-гидроксиэтилиден)дифосфоновой кислоты. Необходимость такого рода исследований была вызвана работами по нахождению способов увеличения растворимости в водной среде координационных соединений марганца, железа и кобальта, предназначенных к использованию в качестве микроудобрений.
Реакции (1-гидроксиэтилиден)дифосфоновой кислоты с аминами
Моноэтаноламин (МЭА), трис (гидроксиметил)аминометан (ТГМА) и морфолин (МФ) оказались удобными реагентами, резко увеличивающими растворимость малорастворимых комплек-сонатов металлов. Пара -аминобензойная кислота (ПАБК) показала меньшую эффективность (схема 1).
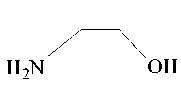
OH
H 2 N
МЭА
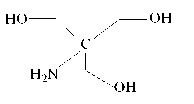
OH
HO
C
H 2 N
OH
ТГМА
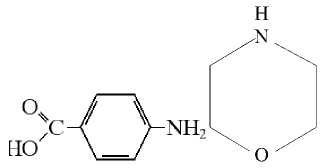
H
N
O
ПАБК
МФ
Схема 1. Водорастворимые органические амины – промоторы растворимости комплексов
В синтезах координационных соединений использовалась четырехосновная промышленно доступная [19] (1-гидроксиэтилиден)дифосфоновая кислота (ОЭДФ, H 4 L):
O
CH3
O
HO P
C
P OH
HO
OH OH
ОЭДФ (H 4 L)
Органический амин присоединяется к комплексонату металла прежде всего за счет образования координационной связи между положительно заряженным атомом азота и анионом фосфоновой кислоты -Р(О)О-…..+NH 3 CH 2 -. Находящиеся на противоположном конце молекулы гидрофильные группы –СОН способствуют переведению мало растворимого комплекса в водную фазу. Плохая растворимость координационных соединений, как известно [19], обусловлена прежде всего их полимерным строением. Увеличение растворимости может быть вызвано также сокращением молекулярной массы за счет разбиения молекул полимера промотором растворимости.
Органическая химия
Реакция с моноэтаноламином
В реакции ОЭДФ с МЭА выделено [20] кристаллическое соединение (рис. 1), которое по данным элементного анализа и РСА представляет собой тройную C(CH 3 )(OH)[P(O)O– NH 3 +CH 2 CH 2 OH] 3 [P(O)(OH)] (но не четверную) аминную соль.
0(41
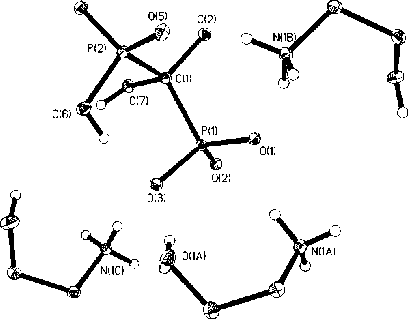
Рис. 1. Структура трис (моноэтаноламиниевой) соли 1-(гидроксиэтилиден)дифосфоновой кислоты
Полученный результат представляется вполне логичным. Известные данные по константам диссоциации (рК а (1) = 1,70; рК а (2) = 2,47) позволяют отнести (1-гидроксиэтилиден)дифосфо-новую кислоту в целом к сильным кислотам [19]. Однако это справедливо только для двух первых стадий диссоциации. Постепенное ослабление кислотности на последних стадиях (рК а (3) = 7,28; рК а (4) = 10,29) является общеизвестной закономерностью для многоосновных кислот и служит причиной отсутствия координации четвертой молекулы моноэтаноламина с молекулой (1-гидроксиэтилиден)дифосфоновой кислоты.
На примере тетрагидрата трис (оксиэтилидендифосфоната) дижелеза(III) Fe 2 (H 2 L) 3 ∙4H 2 O была выполнена [20] проверка на возможность присоединения максимального количества молекул амина в безводной среде. В этом соединении присутствуют 6 свободных кислотных групп –Р(О)ОН, которые в принципе могут образовать 6 фрагментов аминной соли –P(O)O–H 3 N+CH 2 CH 2 OH. Кроме того, МЭА, как более сильный нейтральный лиганд, может заместить 4 молекулы воды в координационном соединении железа. Таким образом, следовало ожидать, что максимальное количество его молекул, которое может присоединить одна молекула комплекса железа, составляет 10. Испытания показали, что при взаимодействии суспензии Fe 2 (H 2 L) 3 ∙4H 2 O с большим избытком МЭА (молярное соотношение 1:87) получается производное железа, содержащее 9 молекул амина Fe2(H2L)3∙9H2NCH2CH2OH. Недостающая до 10 одна молекула по-видимому отсутствует у одной из имеющихся шести групп –Р(О)ОН. Таким образом, органический амин может присоединиться (схема 2) и к катиону металла, и к оставшейся свободной группе кислоты –Р(О)ОН.
OCH
O Fe2+ O P C P OH + 2 H2NCH2CH2OH ►
HO OHOH
OCH
_2+ 3
O Fe2+ O P C P O H 3 NCH 2 CH 2 OH
HO OH OH
HOCH 2 CH 2 NH 2
Схема 2. Присоединение амина к комплексу железа
Реакция с трис(гидроксиметил)аминометаном
Характерной особенностью производных ОЭДФ и ТГМА является образование стекловидных и смолообразных продуктов. Взаимодействие этих реагентов [20] при молярном соотноше- нии 1:4 и 1:3 в различных органических растворителях (метиловом, этиловом спиртах, ацетоне, толуоле, диметилсульфоксиде) приводит к быстрому образованию белой суспензии соли ОЭДФ с ТГМА, которая уже в условиях реакции начинает превращаться в бесцветную вязкую смолу, оседающую на дно колбы. После отделения растворителя и нагревания до 70–80 °С вязкую смолообразную консистенцию сохраняет только продукт, выделенный из высококипящего ДМСО. В других растворителях получаются застывшие прочные твердые расплавы, с трудом отдирающиеся от стекла и размягчающиеся при нагревании до 100–120 °С. Нагревание в вакууме до 200 °С вызывает их плавление и вспучивание, однако отложения твердых или жидких продуктов на холодных стенках реактора не происходит. Это свидетельствует об отсутствии при данной температуре термической диссоциации соли до исходных соединений. После охлаждения получаются прозрачные стекловидные массы, которые разбиваются до мелких стекол и растираются в фарфоровой ступке до белых порошков. По данным элементного анализа их состав H4L^4NH2C(CH2OH)3 соответствует 4 молекулам основания на 1 молекулу четырехосновной кислоты. Присоединение 4 молекул первичного амина происходит при соотношении исходных реагентов как 1 : 4, так и 1 : 3 при проведении реакции в любом из вышеперечисленных растворителей. Растворимость H4LANH2C(CH2OH)3 в метаноле составляет 1,8 г в 100 мл.
Обращает на себя внимание существенное отличие в поведении продуктов реакции ОЭДФ с МЭА и ТГМА. Соль с МЭА легко кристаллизуется, в то время как взаимодействие с ТГМА приводит к образованию смол, превращающихся при нагревании в аморфные стекла. Причина этого может заключаться в образовании сильных межмолекулярных водородных связей между фрагментами Р=О5- и 5+Н-О-С, за счет чего соединение фактически представляет собой координационный полимер. В молекуле NH2C(CH2OH)3 три электроотрицательные гидроксильные группы (-ОН, а I = 0,25) [21] связаны с одним и тем же атомом углерода, в связи с чем их кислотные свойства взаимно усиливаются и существенно превосходят таковые для молекулы H2NCH2CH2OH (-СН2ОН, а I = 0,05). Присоединение к молекуле кислоты вызывает появление положительного заряда на атоме азота и дальнейшее возрастание кислотных свойств ТГМА. В молекуле МЭА атом азота отделен от гидроксильных групп дополнительным метиленовым мостиком, вследствие чего появляющийся на нем заряд компенсируется в большей степени. Полимерное строение и наличие сильных водородных связей в соединении H4L^4NH2C(CH2OH)3 приводят к его очень малой растворимости в органических средах и хорошей растворимости в воде.
Реакция с п-аминобензойной кислотой
Так же, как и МЭА, молекула п -аминобензойной кислоты NH2C6H4C(O)OH (ПАБК) содержит аминную группу. Однако вместо гидроксильного радикала в пара-положении бензольного кольца располагается не гидроксильная, а карбоксильная группа, способная к образованию с металлами более прочных карбоксилатов. ПАБК относится к слабым кислотам (рК а = 4,85), в то время как ОЭДФ - к сильным (рК а (1) = 1,7; рК а (2) = 2,47). Взаимодействие ОэДф с ПАБК [22] приводит к образованию бис (4-карбоксифениламиний)( 1 -гидроксиэтилиден)дифосфоната C(CH 3 )(OH)[P(O)(OH)O-NH 3 +C 6 H 4 C(O)OH] 2 (рис. 2).
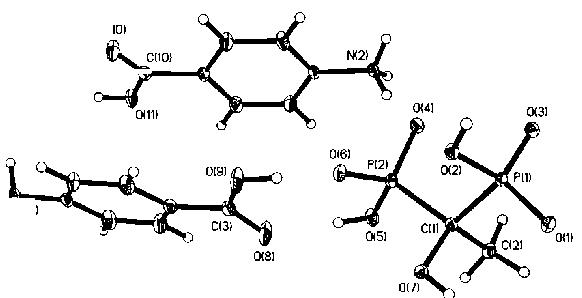
Рис. 2. Общий вид структуры бис (4-карбоксифениламиний)(1-гидроксиэтилиден)дифосфоната
Список литературы Получение и свойства аминиевых солей (1-гидроксиэтилиден)дифосфоновой кислоты
- Граник, В.Г. Основы медицинской химии / В.Г. Граник. - М.: Вузовская книга, 2006. -383 с.
- Первый пример кубаноподобного комплекса меди на основе N-карбоксиэтил-трис(гидроксиметил)аминометана: синтез и кристаллическая структура / А.В. Пестов, А.В. Вировец, Н.В. Подберезская и др. // Коорд. химия. - 2008. - Т. 34, № 1. - С. 3-10.
- N-[7>7's(hydroxymethyl)methyl]glytine (tricine) / M.R. Silva, J.A. Paixao, A.M. Beja et al. // Acta Cry st., Sect. C. - 2001. - V. 57. - P. 421-422.
- Пеплоу, М. Слепая медицина / М. Пеплоу // В мире науки. - 2017. - № 4. - С. 98-103.
- Взаимодействие 1-алкилсилатранов с 2-метилфеноксиуксусной кислотой / С.А. Адамович, А.И. Албанов, А.Н. Мирскова и др. // Журнал общей химии. - 2009. - Т. 79, № 6. - С. 10431044.
- Воронков, М.Г. Трекрезан - родоначальник нового класса адаптогенов и иммуномодуля-торов / М.Г. Воронков, М.М. Расулов // Химико-фармацевтический журнал. - 2007. - Т. 41, № 31. - С. 1-7.
- Адамович, С.Н. Ионные жидкости на основе биологически активных 1-(3-аминопропил)силатрана и арил(гетарил)окси(сульфанил)уксусных кислот / С.Н. Адамович, Р.Г. Мирсков, М.Г. Воронков // Известия АН. Сер. хим. - 2010. - № 10. - С. 1993-1994.
- Кондратенко, Ю.А. Протонные алканоламмониевые ионные жидкости на основе триэта-ноламмониевых солей карбоновых кислот / Ю.А. Кондратенко, Т.А. Кочина, В.С. Фундамен-ский // Физика и химия стекла. - 2016. - Т. 42, № 6. - С. 807-814. DOI: 10.1134/S1087659616060092.
- Характеристика протонных ионных жидкостей на основе триэтаноламмониевых солей биологически активных карбоновых кислот и их влияние на ростовые свойства гриба Rhizopus Oryzae / Ю.А. Кондратенко, Г.Г. Няникова, К.В. Молчанова и др. // Физика и химия стекла. -2017. - Т. 43, № 5. - С. 496-503.
- Кондратенко, Ю.А. Взаимодействие трис(гидроксиметил)аминометана с карбоновыми кислотами (бензойная, коричная, салициловая, никотиновая) / Ю.А. Кондратенко, А.А. Никано-рова, Т.А. Кочина // Физика и химия стекла. - 2018. - Т. 44, № 6. - С. S49-S52.
- Синтез, кристаллическое строение и термические свойства протонных металлосодержа-щих ионных жидкостей, галогенметаллатов диэтаноламмония: (HOCH2CH2)2NH2FeCl4, ((HOCH2CH2)2NH2)2CoCl4 / Захаров М.А., Филатова Ю.В., Быков М.А. и др. // Коорд. химия. -2020. - Т. 46, № 4. - С. 249-256. DOI: 10.31857/S0132344X20040076
- Воронков, М.Г. Новый путь образования 1-хлорсилатрана / М.Г. Воронков, Г.А. Кузнецова, В.П. Барышок // Журнал общей химии. - 2010. - Т. 80, № 10. - С. 1615-1617. DOI: 10.1134/S1070363210100075.
- Новый метод синтеза 1-фторсилатрана / М.Г. Воронков, Т.А. Кочина, Д.В. Вражнов и др. // Журнал общей химии. - 2008. - Т. 78, № 11. - С. 1924-1925. DOI: 10.1134/S1070363208110327.
- Ghammamy, Sh. Фторхромат триэтиламмония - новый, мягкий, стабильный и дешевый окислитель на основе шестивалентного хрома / Sh. Ghammamy, А. Hashemzadeh, М. Mazareey // Журнал органич. химии. - 2005. - Т. 41, № 12. - С. 1790-1792.
- Кристаллическая и молекулярная структура хлорида 1-(3-аммониопропил)силатрана / Воронков М.Г., Зельбст Э.А., Фундаменский В.С. и др. // Журнал структ. химии. - 2014. - Т. 55, № 2. - С. 392-394.
- Синтез, кристаллическая структура, колебательные спектры и термохимические превращения сульфата трис(оксиметил)аминометана / Р.Е. Хома, В.О. Гельмбольт, О.В. Шишкин и др. // Журнал неорг. химии. - 2014. - Т. 59, № 1. - С. 60-65. DOI: 10.7868/S0044457X14010061.
- Синтез и строение моногидрата сульфита ^(гидроксиэтил)этилендиаммония / Р.Е. Хома, В.О. Гельмбольт, О.В. Шишкин и др. // Журнал неорг. химии. - 2014. - Т. 59, № 6. - С. 716719. DOI: 10.1134/S0036023614060096.
- Структура трис(2-гидроксиэтил)аммонийных солей янтарной кислоты / С.В. Логинов, И.А. Даин, В.Б. Рыбаков и др. // Кристаллография. 2018. - Т. 63, № 1. - С. 65-71. DOI: 10.7868/S0023476118010125.
- Дятлова, Н.М. Комплексоны и комплексонаты металлов / Н.М. Дятлова, В.Я. Темкина, К.И. Попов. - М.: Химия, 1988. - 544 с.
- Получение аморфных водорастворимых комплексов биометаллов на основе (1-гидроксиэтилиден)дифосфоновой кислоты, 2-аминоэтанола и 2-амино-2-(гидроксиметил)пропан-1,3-диола / В.В. Семенов, Н.В. Золотарева, Б.И. Петров и др. // Журнал общей химии. - 2015. - Т. 85, № 5. - С. 822-830.
- Верещагин, А.Н. Индуктивный эффект. Константы заместителей для корреляционного анализа / А.Н. Верещагин. - М.: Наука, 1988. - 111 с.
- Семенов, В.В. Реакции тетрагидрата трис[(1-гидроксиэтилиден)дифосфоната] дижеле-за(Ш) и тетрагидрата трис[(1-гидроксиэтилиден)-дифосфоната] железа(Ш) с и-аминобензойной кислотой. Молекулярная структура бис(4-карбоксифениламиний)(1-гидроксиэтилиден)дифосфо-ната / В.В. Семенов, Н.В. Золотарева, Е.В. Баранов // Журнал общей химии. - 2017. - Т. 87, № 4.- С. 617-621.
- Гайле, А.А. Морфолин и его производные: Получение, свойства и применение в качестве селективных растворителей / А.А. Гайле, В.Е. Сомов, Г.Д. Залищевский. - СПб.: Химиздат, 2007. - 332 с.
- А.с. 967967 СССР. МПК C02F 5/14. Состав для предотвращения отложения минеральных солей / В.И. Гусев, В.С. Цивунин, А.В. Солодов, Н.В. Бикчантаева, Т.Н. Колтышева, Е.П. Семки-на, В.Г. Зарипова. - № 3221542; заявл. 12.1180, опубл. 23.10.82, Бюл. № 39.
- Козин, В. Г. Растворяющие и селективные свойства смешанных растворителей на основе морфолина / В.Г. Козин, А.А. Мухамадиев // Журнал прикладной химии. - 2001. - Т. 74, № 8. -С. 1252-1257.
- Присоединение морфолина и пирролидина к изопропенилфосфоновой кислоте in situ / А.Е. Бальцер, Д.А. Зайцев, Т.В. Иванова и др. // Журнал органической химии. - 2013. - Т. 49, № 4. - P. 642-643.
- Семенов, В.В. Действие морфолина на комплексы кобальта с (1-гидрокси-этилиден)дифосфоновой кислотой / В.В. Семенов, Н.В. Золотарева // Вестник ЮУрГУ. Серия «Химия». - 2017. - Т. 9, № 3. - С. 12-18. DOI: 10.14529/chem170302.
- Изучение спонтанной полимеризации морфолина с эпихлоргидрином / У.К. Уринов, О С. Максумова, А.Т. Джалилов, М.А. Аскаров // Докл. АН РУз. - 2015. - № 1. - С. 57-58.
- Кинетика и механизм реакций винил ацетата с диэтиламином, пиперидином и морфоли-ном / Г.С. Симонян, Н.М. Бейлерян, Э.Р. Саруханян и др. // Кинетика и катализ. - 1999. - Т. 40, № 4.- С. 578-582.


