Получение порошка оксида цинка из глубоких эвтектических растворителей
Автор: Сажнев Михаил Павлович, Харин Олег Игоревич, Макаров Николай Александрович
Журнал: Вестник Бурятского государственного университета. Химия. Физика @vestnik-bsu-chemistry-physics
Статья в выпуске: 1, 2025 года.
Бесплатный доступ
Порошок оксида цинка ZnO был осажден из систем хлорид - мочевина водой и натриевой щёлочью. Полученный материал обжигали при температурах 500-700 ℃ и исследовали методами РФА, БЭТ, РФЛа, СЭМ, ЭДС. Также для изучения структуры глубокого эвтектического растворителя применяли ИК-спектроскопию. По данным РФА расчитали параметры решётки для всех образцов. Оксид цинка кристаллизуется в гексагональной структуре вюрцита P63mc с параметрами решётки а = 3,24992 Å и с = 5,20658 Å. Для получения оксида цинка на основе проведённых анализов определены оптимальный состав исходного ГЭР и температура синтеза прекурсора.
Оксид цинка, глубокие эвтектические растворители, синтез, термообработка, структура
Короткий адрес: https://sciup.org/148331442
IDR: 148331442 | УДК: 543 | DOI: 10.18101/2306-2363-2025-1-36-48
Synthesis of zinc oxide powder from deep eutectic solvents
Zinc oxide (ZnO) powder was precipitated from chloride-urea systems using water and sodium hydroxide. The resulting material was calcined at temperatures ranging from 500 to 700 °C and analyzed using X-ray diffraction (XRD), Brunauer-Emmett-Teller (BET) surface area analysis, photoluminescence spectroscopy (PL), scanning electron microscopy (SEM), and energy-dispersive X-ray spectroscopy (EDS). Infrared (IR) spectroscopy was also used to study the structure of the deep eutectic solvent (DES). Lattice parameters for all samples were calculated based on XRD data. Zinc oxide crystallized in the hexagonal wurtzite structure (space group P6₃mc) with lattice constants a = 3.24992 Å and c = 5.20658 Å. Based on the analytical results, the optimal composition of the starting DES and the precursor synthesis temperature for obtaining zinc oxide were determined.
Текст научной статьи Получение порошка оксида цинка из глубоких эвтектических растворителей
Оксид цинка — полупроводниковое соединение типа AIIBVI, которое характеризуется широкой запрещенной зоной 3,3 эВ, сравнительно высокой энергией связи экситона 60 мэВ при комнатной температуре [1–4] и естественной электропроводностью n-типа [5]. Утверждается [6], что вакансии О2 (VO) являются донорами, могут быть ответственны за проводимость n-типа и междоузлия Zn (Zni) являются слабыми быстродиффундирующими донорами, поэтому они не стабильны. Вакансии цинка являются глубокими акцепторами с низкими энергиями образования химических связей в условиях, приводящих к росту проводимости n-типа. Кроме того, система склонна к самокомпенсации — при введении акцеп- торов автоматически увеличивается концентрация компенсирующих доноров. Глубокая валентная зона ZnO, обусловленная сильной связью Zn-O, также затрудняет генерацию свободных дырок. Оксид цинка представляет собой сложный полупроводник, который кристаллизуется в гексагональной структуре вюр-цита (P63mc) [7]. Близкая к тетраэдрической координации, она приводит к возникновению полярной симметрии в ZnO, что является причиной его сильной анизотропии, в том числе в процессе роста кристаллов [8]. Все эти свойства обусловливают применение оксида цинка в качестве материала для варисторной керамики [9], прозрачных проводящих оксидов (TCO) [10], биосенсоров, в том числе за счёт своей биосовместимости [11] и терморегулирующих покрытий ТРП [12,13], а также сорбентов для поглощения SO2 и H2S [14]. Из-за описанных выше особенностей структуры и свойств оксида цинка для его применения необходим чёткий контроль состава и морфологии кристаллов. В статье приводятся результаты исследования порошков оксида цинка, полученных путем осаждения из глубоких эвтектических растворителей (ГЭР) — систем, образованных из эвтектической смеси кислот Льюиса или Бренстеда, и оснований, которые могут содержать множество анионов и/или катионов [15].
Экспериментальная часть
В качестве исходной эвтектической системы для синтеза была выбрана смесь: хлорид цинка — мочевина (мольное соотношение 3 к 10). Осаждение из ГЭР проводили двумя способами: водой и натриевой щёлочью. Состав исходных смесей для получения ГЭР и чистота компонентов представлены в таблице 1.
Таблица 1
Составы смесей для получения ГЭР
|
Компонент 1 |
ZnCl2 (чистота — «Ч») |
|
Компонент 2 |
(NH2)2CO (чистота — «ЧДА») |
Смесь исходных порошков помещалась в водяную баню, где плавилась при температуре 80 ℃, после плавления и обесцвечивания перемешивалась магнитной мешалкой в течение 120 минут. После этого смесь осаждали охлаждённой до 5 ℃ водой объёмом 2,125 л. Полученную систему фильтровали и промывали дистиллированной водой.
Альтернативным было осаждение щёлочью. Твердый гранулированный NaOH добавляли в систему в мольном соотношении 2:1 к хлориду цинка и затем выдерживали 30 минут. Полученную систему фильтровали и промывали водой до достижения нейтральной среды (pH = 7).
После фильтрования порошки сушили при температуре 70 ℃ и далее синтезировали в печи на воздухе при температурах 500–700 ℃, со скоростью нагрева 2 ℃/мин и выдержкой 2 часа. Наименования образцов, полученных в ходе экспериментов, представлены в таблице 2.
Наименования образцов
Таблица 2
|
Температура синтеза, ℃ |
Способ осаждения |
|
|
Вода |
NaOH |
|
|
500 |
Zn-Cl-500 |
Na-Zn-Cl-500 |
|
600 |
Zn-Cl-600 |
Na-Zn-Cl-600 |
|
700 |
Zn-Cl-700 |
Na-Zn-Cl-700 |
Пос ле термообра бот ки для анализа порошков использовали ме тоды ре нтгенофазового а на л и за ( Р ФА), сканирующей электронной микроскоп и и (С ЭМ) , Брунауэра-Эммета-Те лле ра (Б ЭТ) и энергодисперсионной рентгеновской спек т ро скоп и и ( ЭДС) для контроля фазового и химического состава , а та кже оценк и м орф о лог и и к ри с т аллов . Дл я и з уче ни я ст руктуры ГЭР применялась ИК-с п ек троск опия ме т одом Н П ВО .
О бс уждени е р ез у л ь т ато в
Для п од тве р ж дени я фазового состава прекурсоров и прокаленных пор ошков прове дён ре нтге но фа зовый анализ. Результаты представлены на рис у нк а х 1 и 2. В с лу ча е прим е н е ния д и ст и ллированной воды в качестве осадителя в составе преку рсора наблюд а е т ся н а ли чи е ф аз симонколлеита и хлорида аммония, кото ры е об р а зу ю тся в ход е гидролиза ГЭР водой. Синтез при температурах 5 00–700 ℃ п озволяе т п олу ч ит ь е ди н ст ве нн у ю ф а зу — оксид цинка ZnO.
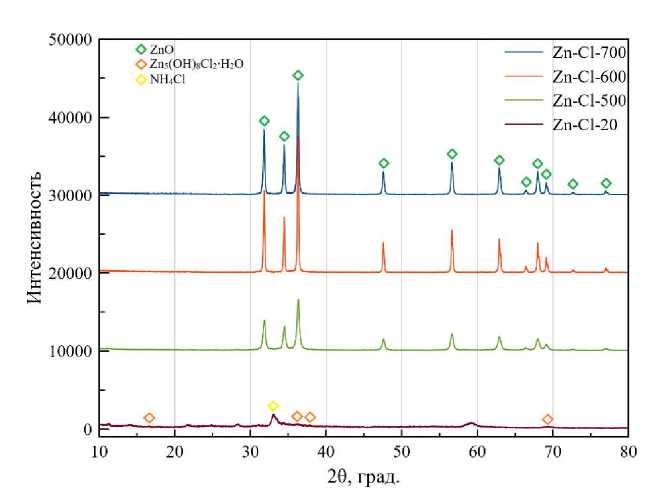
Рис. 1. Резуль т ат ы РФ А по ро шков, по л у ченны х при взаимодействии глу бо кого э в т е ктичес ко го р ас т в о р ит еля системы х ло р ид цинка — мочевина с дистиллированной водой
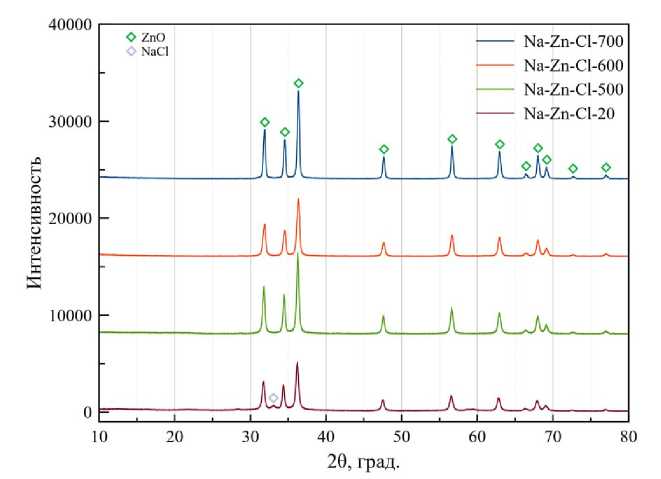
Рис. 2. Результаты РФА порошков, полученных при взаимодействии глубокого эвтектического растворителя системы хлорид цинка — мочевина с натриевой щёлочью
В случае осаждения гидроксидом натрия наблюдается вторая фаза — хлорид натрия с пиками слабой интенсивности.
Оценку химического состава полученных порошков проводили с помощью метода ЭДС. Соответствующие результаты представлены в таблицах 3 и 4.
Таблица 3
Результаты ЭДС порошков, полученных при взаимодействии глубокого эвтектического растворителя системы хлорид цинка — мочевина с дистиллированной водой
|
Температура синтеза, ℃ |
Zn-Cl |
||
|
Zn, атомн. % |
O, атомн. % |
Zn/O |
|
|
500 |
40,620 |
59,380 |
0,684 |
|
600 |
41,270 |
58,730 |
0,702 |
|
700 |
44,240 |
55,760 |
0,793 |
При увеличении температуры синтеза наблюдается стремление порошка к стехиометрическому составу, причём цинк находится в недостатке. Таким образом, с ростом температуры синтеза снижается количество вакансий по цинку, из-за чего соотношение становится более стехиометрическим. При этом не было обнаружено примесных элементов.
Таблица 4
Результаты ЭДС порошков, полученных при взаимодействии глубокого эвтектического растворителя системы хлорид цинка — мочевина с натриевой щёлочью
|
Температура синтеза, ℃ |
Na-Zn-Cl |
||
|
Zn, атомн. % |
Na, атомн. % |
Примеси, атомн. % |
|
|
500 |
58,429 |
38,426 |
3,145 |
|
600 |
64,608 |
28,034 |
7,358 |
|
700 |
64,433 |
30,674 |
4,893 |
По данным ЭДС, проведённого для порошков, полученных при осаждении NaOH, можно увидеть наличие натрия в образцах, а также наличие других элементов, например, хлора (статья «примеси»). Наличие натрия в любой форме крайне нежалательно и контроль его наличия на стадии синтеза затруднён. При повышении температуры синтеза также наблюдается увеличение содержания цинка.
Для оценки морфологии кристаллов, а также их размеров проведена сканирующая электронная микроскопия.
Результаты СЭМ представлены на рисунках 3–5.

Рис. 3. Микроструктуры порошков Zn-Cl-500 (а) и Na-Zn-Cl-500 (б)

Рис. 4. Микроструктуры порошков Zn-Cl-600 (а) и Na-Zn-Cl-600 (б)

Рис. 5. Микроструктуры порошков Zn-Cl-600 (а) и Na-Zn-Cl-600 (б)
В случае гидролиза водой частицы ZnO имеют преимущественно цилиндрическую форму со средней длиной 2,1 мкм и средним диаметром 0,6 мкм. При этом размер частиц с увеличением температуры синтеза уменьшается.
Аналогичной морфологией обладают порошки, полученные осаждением гидроксидом натрия. Размер частиц для Na-Zn-Cl — 0.8 мкм.
Температура прокаливания влияет на морфологию и размер частиц. Так, при 500 °C частицы ZnO в основном аморфные и агрегированные, при 600 °C в образце Zn-Cl-600 появляются стержнеобразные кристаллы, а при 700 °C формируются четко выраженные кристаллические структуры.
Для Zn-Cl-700 характерны цилиндрические частицы (длина 2,1 мкм, диаметр 0,6 мкм).
Тип осадителя влияет на размер частиц. Так, осаждение гидроксидом натрия приводит к уменьшению размера частиц (Na-Zn-Cl-700 — 0,8 мкм) по сравнению с аналогичным Zn-Cl-700, осаждённым водой — 2,1 мкм.
Для оценки удельной поверхности в таблице 5 представлены результаты БЭТ.
Таблица 5
Сравнение результатов БЭТ
|
Образец |
S уд , м2/г |
|
Na-Zn-Cl-500 |
18,5286 ± 0,03 |
|
Na-Zn-Cl-600 |
15,7685 ± 0,03 |
|
Na-Zn-Cl-700 |
8,8092 ± 0,03 |
|
Zn-Cl-500 |
17,52 ± 0,10 |
|
Zn-Cl-600 |
7,02 ± 0,05 |
|
Zn-Cl-700 |
2,00 ± 0,01 |
С ростом температуры синтеза закономерно снижается удельная поверхность частиц. При осаждении NaOH удельная поверхность частицы выше, а скорость седиментации ниже.
На основе РФА определены параметры решётки и ренгеновская плотность порошков. Эталонное значение рентгеновской плотности оксида цинка — 5,673 г/см3, а — 3,24992 Å, с — 5,20658 Å [16]. Результаты расчёта параметров решётки представлены в таблице 6.
Таблица 6
Рез у льт а ты рас чё та пара м е т ров решёт к и и ренгеновской плотности
|
Температура синтеза, °C |
Zn-Cl |
Na-Zn-Cl |
||||
|
a, Å |
c, Å |
Истинная плотность, г/см3 |
a, Å |
c, Å |
Истинная плотность, г/см3 |
|
|
500 |
3,2455 |
5,1981 |
5,689 |
3,2483 |
5,2017 |
5,689 |
|
600 |
3,2461 |
5,1999 |
5,683 |
3,2452 |
5,1959 |
5,684 |
|
700 |
3,2456 |
5,2005 |
5,680 |
3,2441 |
5,1936 |
5,693 |
Ренг е н ов ская плотност ь, к а к и па ра ме тры а и с , ве д ет себя нелинейно. Это с вя з ан о с и зм е н е н ием концентрации и вида дефектов кристаллическо й ре ше тки.
Для образцов Zn-Cl наблюдается тенденция к увеличению параметра с, что может быть связа но с изменением дефектов кристаллической решет к и , р о ст ом кри ст ал ли т ов или рел а кс ац ией нап ряж ен ий .
Ис ход я из с овок уп н ости всех приведённых результатов наибол е е оп ти ма л ь ны м образц ом д ля с ин тез а к е рамик и я вляе т ся Zn-Cl-500 за счёт чистоты, низкой температуры си нт еза и высок ой ак т и вн ос т и .
Одной из возможных переменных в процессе синтеза является время варки системы.
Таблица 7
Наименования образцов
|
Время синтеза, час |
Наименование |
|
0,5 |
Zii-Cl-0,5 |
|
1,0 |
Z11-C1-1 |
|
1,5 |
Zn-Cl-1,5 |
|
2,0 |
Zn-Cl-2 |
Дальнейши е и с с л едов а ни я направле ны н а оп ред еле н ие оп т им а л ьн ог о вре м ени варки сис те мы д о её ос а жд ени я.
В таб лиц е 7 предс т ав л е н ы н аим ен ования образ ц ов, с ин тезирова нн ы х в т ечение различ н ог о вре ме ни.
На рисунке 5 приведены результаты РФА для порошков, полученных из хло- рида цинка и осаждённых водой в зависимости от времени синтеза.
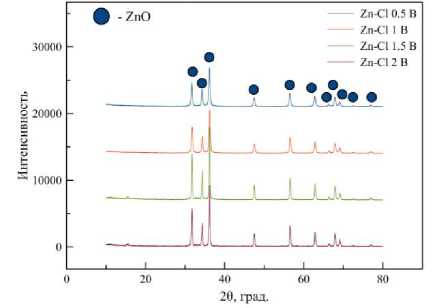
Рис. 6. Р ез у льт а ты рентгенофазового анализа для порошков, полу ч е нн ы х и з хлори д а цин к а после прокаливании при различном времени с и нт е з а
Как следует из результатов РФА, во всех случаях образуется целевая фаза ZnO. Энергодисперсионный анализ проведён в целях подтверждения химического состава полученных порошков. Результаты представлены в таблице 8.
Таблица 8
Результаты EDX для порошков, полученных из хлорида цинка при осаждении водой в зависимости от времени варки
|
Наименование образца |
Содержание элементов, атомн. % |
|||
|
Zn |
O |
Cl |
Примеси |
|
|
Zn-Cl-0.5 |
43,294 |
54,780 |
1,926 |
0,000 |
|
Zn-Cl-1 |
42.732 |
55,141 |
2,127 |
0,000 |
|
Zn-Cl-1.5 |
40,869 |
52,786 |
5,375 |
0,970 |
|
Zn-Cl-2 |
41,963 |
51,702 |
5,351 |
0,985 |
С увеличением времени варки наблюдается рост концентрации адсорбированного хлора, что может негативно сказаться на свойствах получаемого материала, особенно применяемого в биомедицинских целях. Наличие примесей в образцах Zn-Cl-1.5 и Zn-Cl-2 не связано с увеличением времени синтеза.
Для оценки наличия возможного содержания углерода в образцах, а также подтверждения количества примесей был проведён рентгенофлуоресцентный анализ (РфлА). Результаты представлены в таблице 9.
Таблица 9
Результаты РфлА для порошков, полученных из хлорида цинка после прокаливании при различном времени синтеза
|
Наименование образца |
Содержание элементов, мас. % |
||||
|
Zn |
C |
O |
Cl |
Zn/O |
|
|
Zn-Cl-0.5 |
55,90 |
20,75 |
22,43 |
0,92 |
71,36 |
|
Zn-Cl-1 |
55,80 |
21,27 |
21,92 |
1,01 |
71,80 |
|
Zn-Cl-1.5 |
53,15 |
22,74 |
22,11 |
1,99 |
70,62 |
|
Zn-Cl-2 |
59,00 |
16,31 |
22,20 |
2,49 |
72,66 |
С увеличением времени варки наблюдается снижение содержания углерода и увеличение количества хлора. Оптимальным образцом при этом является Zn-Cl-2 за счёт наименьшего количества примесей. Также при более длительной варке оксид цинка более стехиометричен (соотношение Zn/O — 72,66) и, следовательно, образец Zn-Cl-2 также предпочтителен.
На рисунках 7 и 8 представлены результаты исследования микроструктуры порошков.

Рис. 7. Результаты СЭМ для образцов Zn-Cl-0.5 (а) и Zn-Cl-1 (б)
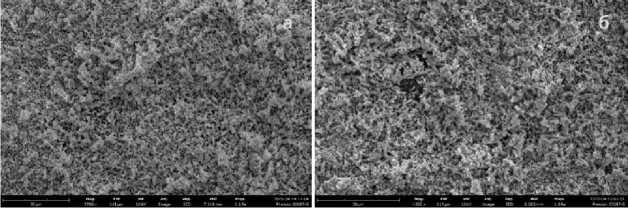
Рис. 8. Результаты СЭМ для образцов Zn-Cl-1.5 (а) и Zn-Cl-2 (б)
С увеличением времени варки системы наблюдается анизотропный рост кристаллов стержнеобразной формы, что характерно для оксида цинка. Средний размер частиц при этом остается на одном уровне. Анизотропия роста обсулов-лена гексагональной структурой вюрцита. Рост вдоль направления c происходит быстрее, чем в направлении а. Благодаря этому оксид цинка имеет игольчатые или стержневидные структуры. Соответственно, чем дольше длится процесс роста кристаллов, тем более выражены отличия в скоростях роста в различных направлениях.
Игольчатые структуры менее склонны к образованию крупных агрегатов. Однако несмотря на меньшую степень агрегации применение в синтезе керамики игольчатых структур не столь эффективно.
Имея более высокое сотношение длины к диаметру, игольчатые частицы сложно уплотняются, образуя большие поры. Также ввиду их анизотропии усадка в процессе спекания также становится анизотропной.
Рассчитаны параметры решётки ZnO в зависимости от времени варки на основе данных, полученных в ходе рентгенофазового анализа.
Результаты представлены в таблице 10.
Таблица 10
Результаты расчёта параметров решётки и ренгеновской плотности в зависимости от времени синтеза
|
Время синтеза, час. |
Zn-Cl-500 |
||
|
Параметр а, Å |
Параметр с, Å |
Плотность, г/см3 |
|
|
0,5 |
3,2554 |
5,2140 |
5,646 |
|
1,0 |
3,2512 |
5,2088 |
5,666 |
|
1,5 |
3,2515 |
5,2115 |
5,662 |
|
2,0 |
3,2517 |
5,2114 |
5,662 |
Наблюдается резкое падение обоих параметров при времени синтеза 1 час. При этом плотность образца Zn-Cl-1 ближе к рентгеновской, однако все образцы менее плотные по сравнению с эталоном — 5,673. Отличия вызваны дефектной структурой оксида цинка.
Для оценки структуры жидкого ГЭР была проведена ИК-спектроскопия методом НПВО. Результаты представлены на рисунке 9. Исследование проводилось на оборудовании ЦКП РХТУ им. Д. И. Менделеева.
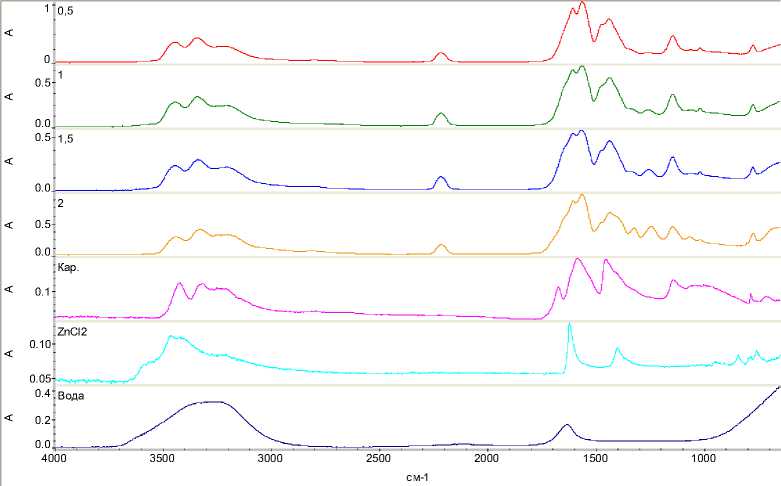
Рис. 9. Результаты ИК-спектроскопии для полученного ГЭР в зависимости от времени варки системы. Также проведены спектры воды, хлорида цинка и карбамида (Кар.)
Жидкая система хлорид цинка — мочевина образует тетраэдрические комплексы [Zn(urea)₄]²⁺, а также смешанные хлорид-карбамидные комплексы [Zn(urea)ₙClₘ](2-μ), где μ — заряд лигандов Cl-. При недостатке мочевины (возникающем в том числе в ходе варки системы) возможно появление полимерных структур типа [Zn(μ-Cl) 2 (urea) 2 ] n .
В ИК-спектре системы ZnCl₂ — мочевина наблюдаются характерные полосы поглощения, которые позволяют сделать выводы о взаимодействиях между компонентами. В области валентных колебаний N–H (3100–3500 см⁻¹) для свободной мочевины обычно видны две чёткие полосы: асимметричное колебание при ~3440 см⁻¹ и симметричное при ~3340 см⁻¹. В случае образования координационного комплекса эти полосы смещаются в низкочастотную область на 20–50 см⁻¹ и становятся более размытыми, что свидетельствует об участии групп N–H в образовании водородных связей с хлорид-ионами и соответственно об участии их в создании координационных соединений.
Важнейшим диагностическим признаком является поведение полосы карбонильной группы C=O мочевины. У свободной мочевины она проявляется как интенсивный пик около 1 680–1 700 см⁻¹. При координации мочевины к иону цинка через атом кислорода эта полоса смещается на 40 см⁻¹ в область 1 630–1 660 см⁻¹, что указывает на ослабление связи C=O вследствие донорно-акцепторного взаимодействия. Величина этого сдвига (~50 см⁻¹) подтверждает образование координационных связей Zn–O.
В низкочастотной области спектра (400–600 см⁻¹) также могли бы наблюдаться полосы, соответствующие колебаниям связей Zn–Cl и Zn–O. Для мостиковых хлоридных структур (μ-Cl) характерны полосы в районе 300–400 см⁻¹. Их наличие свидетельствует о возможном образовании полимерных цепочек [Zn(μ-Cl)₂(urea)₂] n в системе. Интенсивность этих полос зависит от соотношения компонентов: при избытке мочевины они менее выражены, так как доминируют тет-ракоординированные комплексы [Zn(urea)₄]²⁺. Однако оценка низкочастотного спектра затруднительная ввиду особенностей метода — возможна оценка спектра от 500 см⁻¹.
Образование полимерных структур подтверждает ускоренное затвердевание ГЭР при прекращении нагревания. При этом увеличение времени варки до 2,5 часа и более провоцирует ещё более активное затвердевание системы, а также её полимеризацию за счёт выкипания части мочевины.
Следовательно, оценка структуры посредством ИК-спектроскопии методом НПВО представляет трудности, поскольку ГЭР более не является жидкой фазой.
На основании приведённых анализов для различного времени варки были выбраны образцы Zn-Cl-2 за счёт наименьшего содержания углерода в порошке, а также стремления к стехиометрии (Zn/O — 72,66%).
Заключение
Проведённые исследования позволили установить ключевые закономерности синтеза оксида цинка из глубокого эвтектического растворителя системы ZnCl₂ — мочевина. Гидролиз дистиллированной водой приводит к образованию прекурсора на основе симонколлеита и хлорида аммония, который при прокаливании при 500–700 °C трансформируется в чистую фазу ZnO без примесей. В случае использования натриевой щёлочи в продукте сохраняется остаточный NaCl, что ограничивает его применение в высоко чистых процессах.
Установлено, что повышение температуры синтеза способствует приближению состава ZnO к стехиометрии за счёт уменьшения концентрации вакансий по цинку, при этом образцы, полученные гидролизом водой, демонстрируют более предсказуемый и воспроизводимый состав по сравнению с системами, содержащими натрий.
Морфология полученного ZnO характеризуется стержнеобразными частицами с выраженной анизотропией, обусловленной гексагональной структурой вюрци-та. Установлено, что увеличение времени варки системы усиливает анизотропию кристаллов, однако это негативно сказывается на их спекаемости из-за затруднённой упаковки и неоднородной усадки.
Наибольшую удельную поверхность демонстрируют образцы, синтезированные при 500 °C, что делает их перспективными для каталитических и сенсорных применений. При этом оптимальным с точки зрения чистоты и стехиометрии яв- 46
ляется образец Zn-Cl-2, полученный при двухчасовой варке системы, так как он содержит минимальное количество углеродных примесей и имеет наиболее сбалансированное соотношение Zn/O.
Инфракрасная спектроскопия подтвердила образование координационных комплексов [Zn(urea)₄]²⁺ и полимерных структур [Zn(μ-Cl)₂(urea)₂]n в ГЭР, что объясняет в том числе изменение реологических свойств системы при длительной варке. Таким образом, результаты работы позволяют заключить, что синтез ZnO посредством гидролиза ГЭР водой с последующим прокаливанием при 500 °C является оптимальным методом получения оксида цинка с контролируемой морфологией.
Керамические материалы на основе полученного порошка применимы, в первую очередь, для катализа и производства сорбентов. Для синтеза плотной керамики электротехнического назначения необходимо введение добавок, таких как висмут, сурьма, кобальт, марганец, ванадий.
Для дальнейших исследований целесообразно оптимизировать условия синтеза для минимизации содержания хлора и углерода в конечном продукте, а также возможный поиск другой эвтектической системы.


