Получение стигмаст-4-ен-3-она из -ситостерола с использованием актинобактерий рода Rhodococcus
Автор: Ноговицина Е.М., Тарасова Е.В., Гришко В.В., Ившина И.Б.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Биотехнология
Статья в выпуске: 1, 2010 года.
Бесплатный доступ
Подобраны оптимальные условия биоконверсии -ситостерола в стигмаст-4-ен-3-он в присутствии повышенных концентраций исходного субстрата. Установлено, что максимальная (49.5 %) степень образования целевого продукта достигается в процессе биотрансформации 2 г/л -ситостерола представителями Rhodococcus erythropolis при использовании Твина-80 в качестве эмульгатора стерола. При этом эффективными индукторами холестеролоксидазной активности родококков являются пальмитиновая кислота и н-гексадекан.
Актинобактерии, селективная биотрансформация, b-ситостерол, стигмаст-4-ен-3-он, индукция, холестеролоксидаза
Короткий адрес: https://sciup.org/147204882
IDR: 147204882 | УДК: 57.088.6+577.175.62
Текст научной статьи Получение стигмаст-4-ен-3-она из -ситостерола с использованием актинобактерий рода Rhodococcus
Окислительная биодеградация стеролов животного и растительного происхождения в природе осуществляется преимущественно бактериями, принадлежащими к родам Arthrobacter, Brevibacte-rium, Corynebacterium, Mycobacterium, Nocardia, Streptomyces, Rhodococcus (Doukyu, 2009; Kreit, Sampson, 2009; Pollegioni et al., 2009). Бактериальные культуры, обладающие стеролтрансформирующей способностью, используются в разработке эффективных методов получения физиологически активных производных на основе наиболее доступных стеролов – холестерола и фитостеролов (β-ситостерола, кампестерола, стигмастерола). Как правило, на первом этапе окислительной биотрансформации стеролов (рис. 1) образуются 4-ен-3-оновые соединения, получение которых катализируется бифункциональным ферментом холесте-ролоксидазой (Doukyu, 2009; Kreit, Sampson, 2009). На основе использования холестеролокси-дазы, катализирующей реакции окисления не только стеролов, но и стероидов андростанового и прегнанового ряда, а также соединений нестероидной структуры (аллиловых, моно- и полициклических спиртов), разрабатываются эффективные методы получения биологически активных соединений и их оптически активных интермедиатов (Pollegioni et al., 2009). Например, трансформация растительного стерола β-ситостерола под действием холестеролоксидазы приводит к образованию стигмаст-4-ен-3-она, перспективного в качестве лекарственного средства при лечении анрогенза-висимых заболеваний (Streber, 1993).
Ранее нами (Гришко и др., 2009; Ноговицина и др., 2009) было показано, что направленная биоконверсия β-ситостерола в стигмаст-4-ен-3-он достигается при использовании н- гексадекана в качестве ростового субстрата и представителей R. ruber , катализирующих в данных условиях образование до 98% целевого продукта. Необходимо отметить, что эффективное получение 4-ен-3-онового продукта при использовании штаммов R. ruber возможно только в условиях добавления β-ситостерола в концентрации 0.5 г/л через 2 сут роста бактериальных клеток. Применение пальмитиновой кислоты в качестве индуктора холестеро-локсидазной активности родококков позволяет сократить продолжительность процесса биотрансформации стерола в стигмаст-4-ен-3-он с 7 до 5 сут, при этом максимальная (56.3%) степень образования целевого продукта достигается при использовании родококков другого вида ( R. erythropolis ) в условиях добавления β-ситостерола одновременно с инокулятом.
Цель настоящей работы – поиск условий селективной биотрансформации β-ситостерола в стиг-маст-4-ен-3-он при использовании повышенных концентраций исходного стерола.
Материалы и методы
В работе использовали культуры родококков (табл. 1) из Региональной профилированной кол- лекции алканотрофных микроорганизмов ИЭГМ (акроним ИЭГМ, Каталог штаммов…, 1994; , принадлежащих к видам R. erythropolis (6) и R. ruber (6).
HO
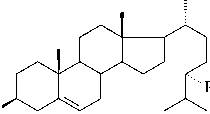
Холестерол (R = H) Кампестерол (R = CH3) β -Ситостерол (R = C2H5)
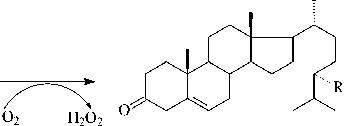
Холест-5-ен-3-он (R = H)
Кампест-5-ен-3-он (R = CH 3 )
Стигмаст-5-ен-3-он (R = C 2 H 5 )
O
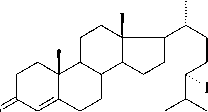
Холест-4-ен-3-он (R = H)
Кампест-4-ен-3-он (R = CH 3 )
Стигмаст-4-ен-3-он (R = C2H5)
Рис. 1 . Первый этап бактериальной трансформации природных стеролов
Таблица 1
Коллекционные штаммы Rhodococcus spp., используемые в работе
|
Вид |
Количество штаммов |
Номер штамма в коллекции ИЭГМ |
|
R. erythropolis |
6 |
ИЭГМ 10, ИЭГМ 179, ИЭГМ 183, ИЭГМ 267, ИЭГМ 487, ИЭГМ 766 |
|
R. ruber |
6 |
ИЭГМ 72, ИЭГМ 85, ИЭГМ 94, ИЭГМ 172, ИЭГМ 232, ИЭГМ 233 |
Родококки выращивали в условиях периодического культивирования на орбитальном шейкере (150 об/мин) при температуре 28°С. Базовый состав минеральной среды включал следующие компоненты (г/л): KNO 3 – 1.0; KH 2 PO 4 – 1.0; K 2 HPO 4 – 1.0; NaCl – 1.0; MgSO 4 – 0.2; СaCl 2 – 0.02. В среду добавляли 1.0 г/л дрожжевого экстракта и 0.1 об.% микроэлементов по Постгейту (Романенко, Кузнецов, 1974). В качестве посевного материала использовали родококки (5.0×105 кл/мл), выращенные на скошенном мясопептонном агаре и отобранные в экспоненциальной фазе роста. Эксперименты по биотрансформации β-ситостерола в соокислительных условиях проводили в присутствии 0.1 об.% н -гексадекана или 1.0% глюкозы. В ростовую среду дополнительно вносили 0.2 г/л пальмитиновой кислоты.
Эксперименты по исследованию влияния концентрации индукторов холестеролоксидазной активности родококков на уровень конверсии β-ситостерола в стигмаст-4-ен-3-он проводили в присутствии пальмитиновой кислоты (0.05-0.5 г/л) или н-гексадекана (0.5-20.0 г/л). β-Cитостерол (0.5; 1.0; 2.0 г/л) добавляли в среду культивирования родококков в виде раствора в изопропаноле одновременно с инокулятом. В отдельных эксперимен- тах в качестве эмульгатора β-cитостерола использовали синтетический сурфактант Твин-80.
Продукты бактериального окисления β-сито-стерола экстрагировали этиловым эфиром уксусной кислоты. Объединенные этилацетатные вытяжки промывали насыщенным водным раствором NaCl и сушили с помощью обезвоженного Na 2 SO 4 . Растворитель удаляли в вакууме роторного испарителя. Образование стигмаст-4-ен-3-она контролировали методом тонкослойной хроматографии на силикагеле сравнением с эталонным соединением, при этом использовали пластины с флуоресцентной добавкой (Merck, Германия) и УФ облучатель LG/58 (Россия). Экспрессное определение содержания β-ситостерола в культуральной жидкости проводили ферментативным методом C.C. Allain (Allain et al., 1974) с детекцией при 500 нм на спектрофотометре Lambda EZ201 (Perkin-Elmer, США) с помощью коммерческой тест-системы контроля уровня холестерола (ООО «Ольвекс Диагностикум», Санкт-Петербург). Количественный анализ продуктов биотрансформации β-ситостерола осуществляли методом УФ спектроскопии (Гришко и др., 2009). Соотношение продуктов реакции подтверждали данными хрома-то-масс-спектрометрии с использованием системы Agilent 6890/ 5973N (кварцевая колонка HP-5MS
SN US 15189741-1) (Agilent technology, США). Статистическую обработку полученных результатов осуществляли с использованием компьютерной программы Excel 2003, рассчитывая среднее арифметическое и стандартную ошибку. Эксперименты проводили в 3-4-х кратной повторности.
Результаты и их обсуждение
По нашим данным, максимальный индуктив- ный эффект пальмитиновой кислоты на стеролтрансформирующую активность R. erythropolis проявляется только при росте бактериальных клеток в присутствии н-гексадекана, при этом уровень конверсии β-ситостерола в стигмаст-4-ен-3-он в 1.5 раза выше, чем при использовании глюкозы в качестве дополнительного ростового субстрата (рис. 2).
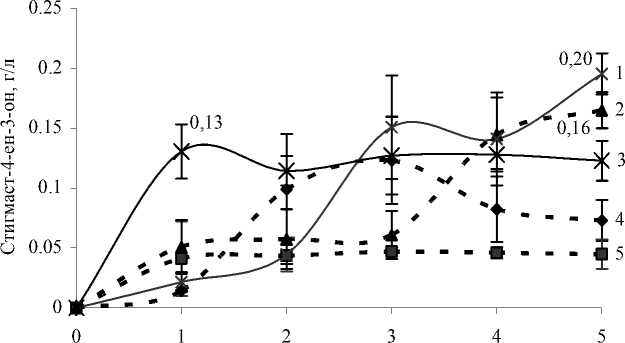
Время, сут
Рис. 2. Биотрансформация β-ситостерола с использованием клеток R. erythropolis ИЭГМ 487:
1 – в присутствии пальмитиновой кислоты и н- гексадекана; 2 – без добавления косубстратов в присутствии пальмитиновой кислоты; 3 – в присутствии пальмитиновой кислоты и глюкозы; 4 – в присутствии н- гексадекана без добавления пальмитиновой кислоты; 5 – в присутствии глюкозы без добавления пальмитиновой кислоты
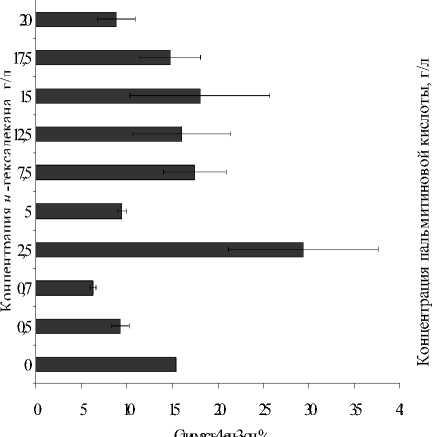
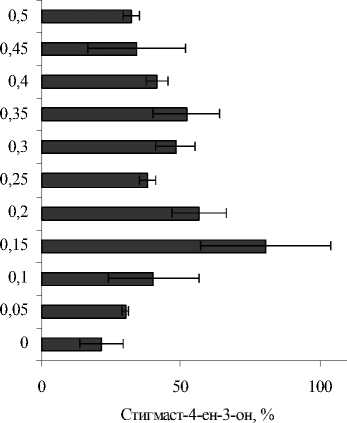
Рис. 3. Влияние концентраций н -гексадекана и пальмитиновой кислоты на процесс биоконверсии β-ситостерола в стигмаст-4-ен-3-он с использованием клеток R. erythropolis ИЭГМ 487
Установлено, что эффективность процесса биоконверсии β-ситостерола в стигмаст-4-ен-3-он зависит от концентрации индукторов холестеро-локсидазы в ростовой среде. При этом максимальная (до 80.6%) степень образования целевого про- дукта достигается в условиях добавления 0.5 г/л β-ситостерола в присутствии 0.15 г/л пальмитиновой кислоты и 2.5 г/л н-гексадекана (рис. 3).
По нашим данным, использование более высоких концентраций β-ситостерола приводит к зна3цуйчительному снижению стеролтрансформирующей активности родококков. Так, при добавлении 1.0 или 2.0 г/л β-ситостерола в виде раствора в изопропаноле содержание стигмаст-4-ен-3-она в сумме продуктов реакции составляет лишь 26.4 и 39.2% соответственно. Установлено, что добавление синтетического детергента Твина-80 при 2-х
Таблица 2
Влияние синтетического сурфактанта Твина-80 на уровень биоконверсии β-ситостерола в стигмаст-4-ен-3-он
или 4-х кратном повышении исходной концентрации β-ситостерола способствует более эффективному образованию стигмаст-4-ен-3-она по сравнению с результатами, полученными в условиях введения стерола в виде раствора в изопропаноле (табл. 2).
|
Концентрация β-ситостерола |
Растворитель β-ситостерола |
Сумма продуктов реакции, % |
Содержание в сумме продуктов реакции, % |
|
|
β-Ситостерола |
Стигмаст-4-ен-3-она |
|||
|
1.0 |
Изопропанол |
0.53 ± 0.034 |
0.38 ± 0.004 |
0.14 ± 0.059 (26.4) |
|
Твин-80 |
0.85 ± 0.151 |
0.51 ± 0.055 |
0.32 ± 0.108 (37.6) |
|
|
2.0 |
Изопропанол |
1.94 ± 0.543 |
1.16 ± 0.325 |
0.76 ± 0.044 (39.2) |
|
Твин-80 |
1.85 ± 0.458 |
0.96 ± 0.122 |
0.87 ± 0.168 (47.0) |
|
В скобках приведено процентное содержание стигмаст-4-ен-3-она в сумме продуктов реакции.
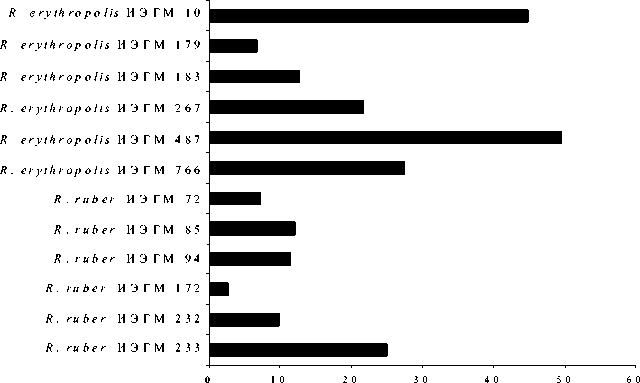
С ти гм а с т-4 -е н -3 -о н , %
Рис. 4. Стеролтрансформирующая активность исследуемых штаммов родококков в присутствии Твина-80
В результате скрининга стерол-трансформи-рующей активности коллекционных культур родо-кокков в условиях добавления β-ситостерола в концентрации 2 г/л в присутствии Твина-80, н- гексадекана и пальмитиновой кислоты установлено, что более эффективными биокатализаторами процесса биотрансформации β-ситостерола являются представители вида R. erythropolis , катализирующие образование до 49.5% целевого продукта (рис. 4). В то время как степень образования стиг-маст-4-ен-3-она из β-ситостерола штаммами R. ruber в данных условиях не превышает 25%.
Таким образом, в результате проведенных исследований подобраны условия направленной биоконверсии β-ситостерола в стигмаст-4-ен-3-он актинобактериями рода Rhodococcus в условиях добавления повышенных (до 2 г/л) концентраций исходного субстрата.
Работа поддержана грантами Президента РФ «Ведущие научные школы» НШ-64403.2010.4; Российского фонда фундаментальных исследова- ний и Министерства промышленности, инноваций и науки Пермского края № 10-04-96032-р-урал и грантом междисциплинарного проекта фундаментальных исследований, выполняемых в учреждениях УрО РАН.
Гришко , В.В. Биокаталитическое получение физиологически активных соединений на основе растительного β-ситостерола / В.В. Гришко, Е.М. Ноговицина, И.Б. Ившина // Катализ в промышленности. 2009. № 1. С. 67–74.
Каталог штаммов Региональной профилированной коллекции алканотрофных микроорганизмов / под ред. И.Б. Ившиной М.: Наука, 1994. 163 с.
Ноговицина , Е.М. Влияние индукторов холестеро-локсидазной активности клеток родококков на процесс биоконверсии β-ситостерола / Е.М. Но-говицина, В.В. Гришко, И.Б. Ившина // Вестн.
Перм. ун-та. Сер. Биология. 2009. Вып. 10. С. 119–123.
Романенко , В.И. Экология микроорганизмов пресных водоемов / В.И. Романенко, С.И. Кузнецов; отв. ред. С.В. Обручев. Л.: Наука, 1974. 194 с.
Allain , C. Enzymatic determination of total serum cholesterol / C. Allain, L.S. Poon, C.S.G. Chan, [et al.] // Clin. Chem. 1974. Vol. 20. P. 470–475.
Doukyu , N. Characteristics and biotechnological applications of microbial cholesterol oxidases // Appl. Microbiol. Biotechnol. 2009. Vol. 83. P. 825–837.
Kreit , J. Cholesterol oxidase: physiological functions / J. Kreit, N.S. Sampson // FEBS J. 2009. Vol. 276, № 23. P. 6844–6856.
Patent 5264428 USA. Use stigmasta-4-en-3-on in the treatment of androgen dependent disease / S. Streber, 23.11.1993.
Pollegioni , L. Cholesterol oxidase: biotechnological applications / L. Pollegioni, L. Piubelli, G. Mollas // FEBS J. 2009. Vol. 276. P. 6857–6870.
Поступила в редакцию 15.03.2010
Stigmast-4-ene-3-one formation from p-sitosterol using actinobacteria
Stigmast-4-ene-3-one formation from β-sitosterol using actinobacteria of the genus Rhodococcus
Ye.M. Nogovitsina Ye.V. Tarasova V.V. Grishko I.B. Ivshina
Institute of Ecology and Genetics of Microorganisms, Ural Branch, Russian Academy of Sciences. 13, Golev str., Optimal β-sitosterol bioconversion occurred in the presence of increased substrate concentrations. It was own that maximal (49.5%) levels of stigmast-4-ene-3-one formation were achieved during transformation of go/lLestsetrooslteorxoidabsye R ac h t o iv d i o t c o in cc r u h s od e o ry c t o h c r c o i p a olis eaurstnogbea satelmroitiecmacuids anedr n T-wheexenad-8e0ca.nTe us, e ect ve nductors o y pp p .
ГУ РАН «Институт экологии и генетики микроорганизмов УрО РАН»
ГОУВПО «Пермский государственный университет»
ГУ РАН «Институт технической химии УрО РАН»
ГОУВПО «Пермский государственный университет»
Список литературы Получение стигмаст-4-ен-3-она из -ситостерола с использованием актинобактерий рода Rhodococcus
- Гришко, В.В. Биокаталитическое получение фи зиологически активных соединений на основе растительного -ситостерола/В.В. Гришко, Е.М. Ноговицина, И.Б. Ившина//Катализ в промышленности. 2009. № 1. С. 67-74.
- Каталог штаммов Региональной профилированной коллекции алканотрофных микроорганизмов/под ред. И.Б. Ившиной М.: Наука, 1994. 163 с.
- Ноговицина, Е.М. Влияние индукторов холестеролоксидазной активности клеток родококков на процесс биоконверсии -ситостерола/Е.М. Ноговицина, В.В. Гришко, И.Б. Ившина//Вестн. Перм. ун-та. Сер. Биология. 2009. Вып. 10. С. 119-123.
- Романенко, В.И. Экология микроорганизмов пресных водоемов/В.И. Романенко, С.И. Кузнецов; отв. ред. С.В. Обручев. Л.: Наука, 1974. 194 с.
- Allain, C. Enzymatic determination of total serum cholesterol/C. Allain, L.S. Poon, C.S.G. Chan, [et al.]//Clin. Chem. 1974. Vol. 20. P. 470-475.
- Doukyu, N. Characteristics and biotechnological applications of microbial cholesterol oxidases//Appl. Microbiol. Biotechnol. 2009. Vol. 83. P. 825-837.
- Kreit, J. Cholesterol oxidase: physiological functions/J. Kreit, N.S. Sampson//FEBS J. 2009. Vol. 276, № 23. P. 6844-6856.
- Patent 5264428 USA. Use stigmasta-4-en-3-on in the treatment of androgen dependent disease/S. Streber, 23.11.1993.
- Pollegioni, L. Cholesterol oxidase: biotechnological applications/L. Pollegioni, L. Piubelli, G. Mollas//FEBS J. 2009. Vol. 276. P. 6857-6870.


