Получение, структура и фотокаталитические свойства органо-неорганического нанокомпозита, содержащего полититаноксид и наночастицы серебра
Автор: Саломатина Евгения Владимировна, Шарова Анастасия Юрьевна, Смирнова Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.8, 2016 года.
Бесплатный доступ
Проведено комплексное исследование поликонденсационно-полимеризационного процесса получения органо-неорганических сополимеров из Ti(OPri)4 и гидроксиэтилметакрилата и в присутствии AgNO3, методами диэлектрической спектроскопии и калориметрии. Скорости процессов зависят от состава исходной реакционной смеси. При УФ-облучении образцов получены полимерные нанокомпозиты, содержащие наночастицы серебра размером от 4 до 12 нм. Условия синтеза оказывают существенное влияние на структуру неорганических цепей в полимерной органической матрице. Нанокомпозиты проявляют фотокаталитическую активность в реакции разложения метиленового оранжевого при УФ-облучении.
Органо-неорганические сополимеры, изопропоксид титана, гидроксиэтилметакрилат, гидролитическая поликонденсация, диэлектрическая спектроскопия, полимеризация, калориметрия, структура, наночастицы серебра, фотокаталитическая активность
Короткий адрес: https://sciup.org/147160368
IDR: 147160368 | УДК: 541.64:542.8 | DOI: 10.14529/chem160403
Synthesis, structure and photocatalytic properties of organic-inorganic nanocomposites containing poly(titanium oxide) and silver nanoparticles
The comprehensive investigation of polycondensation and polymerization syntheses of organic-inorganic copolymers based on Ti(OPri)4 and hydroxyethylmethacrylate in the presence of AgNO3 has been carried out by dielectric spectroscopy and calorimetry. The rates of the processes depend on the composition. The higher content of hydroxyethyl methacrylate leads to the slower polycondensation of titanium alkoxide and faster polymerization. Introduction of AgNO3 into the reaction system leads to the polycondensation acceleration, as well as the inhibition of organic monomer polymerization. After UV-irradiation of samples the polymer nanocomposites containing Ag nanoparticles with size 4-12 nm have been obtained. The synthesis conditions have a significant impact on the structure of inorganic polymer chains in the organic matrix. The nanocomposites exhibit photocatalytic activity in the decomposition of methylene orange under UV irradiation.
Текст научной статьи Получение, структура и фотокаталитические свойства органо-неорганического нанокомпозита, содержащего полититаноксид и наночастицы серебра
В настоящее время ведется активная разработка тонких пленок, покрытий и порошков диоксида титана анатазной модификации в различных полимерных средах [1], а также гелей и полимерных материалов, обладающих высокой фотоактивностью за счет протекания на поверхности TiO 2 при УФ-облучении (λ ≤ 355 нм) обратимого одноэлектронного перехода Ti4++ e ^ Ti3+. Этот процесс обратим во времени и лежит в основе создания на базе указанных материалов самоочищающихся антибактериальных поверхностей [2], солнечных батарей [3], оптических устройств различного назначения [4] и катализаторов нового поколения [5]. Уникальные свойства диоксида титана могут быть усилены путем его совмещения с наночастицами различных металлов [6].
Важным аспектом при получении материалов, содержащих диоксид титана и наночастицы металлов, является их прочность и долговечность, а также структура и восприимчивость к световому воздействию TiO2, размер наночастиц металлов. Оптимального сочетания всех этих качеств можно добиться, на наш взгляд, в процессе поликонденсационно-полимеризационного синтеза органо-неорганических сополимеров на основе алкоксида титана и совместимого с ним винилового органического мономера.
Следует отметить, что кинетика поликонденсации алкоксидов титана как в спиртовых средах, так и в присутствии виниловых мономеров, когда конечным продуктом является гель поли-тианоксида, практически не исследована. Остается неисследованной и радикальная полимеризация системы по двойным связям винилового мономера в присутствии сформированного в ней неорганического полимера.
Целью работы явилось изучение процесса получения органо-неорганических сополимеров – гидролитической поликонденсации изопропоксида титана в среде гидроксиэтилметакрилата (ГЭМА) и полимеризации последнего, методами диэлектрической спектроскопии и калориметрии соответственно, в том числе в присутствии AgNO3 как прекурсора наночастиц серебра. Исследование влияния условий синтеза на структуру сополимеров, получение на их основе композиций, содержащих наночастицы серебра.
Экспериментальная часть
Исходными мономерами для получения органо-неорганических сополимеров являлись тет-раизопропоксид титана Ti(OPri) 4 фирмы «ACROS Organics» с содержанием основного вещества
98 % без дополнительной очистки, и гидроксиэтилметакрилат (ГЭМА) (содержание основного вещества 99,8 %, «НИИ Полимеров», г. Дзержинск):
OPr'
Ti
Pr'O OPr'
OPr'
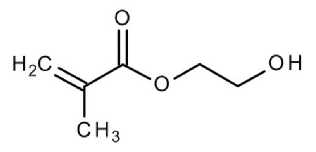
В качестве прекурсора наночастиц (НЧ) серебра использовали AgNO 3 марки ч.д.а. («Реахим», Уральский завод химреактивов, Россия) с содержанием основного вещества 99,95 %. Органо-неорганические сополимеры получали из смесей с различным исходным мольным соотношением компонентов [ГЭМА]/[Ti(OPri)4]. Гидролитическую поликонденсацию алкоксида титана проводили в присутствии небольших количеств H 2 O (~ 0,52·10–3 моль/л) и HCl (0,12·10–3 моль/л). Радикальную полимеризацию инициировали азоизобутиронитрилом (АИБН), очищенным перекристаллизацией из этанола, в количестве 0,5 масс. % по отношению к общей массе смеси. В некоторые смеси мономеров предварительно вводили AgNO 3 (1–3 масс. % по отношению к массе Ti(OPri) 4 ). Реакционные смеси заливали в формы, состоящие из двух стекол с тефлоновой прокладкой между ними. Гидролитическую поликонденсацию по превращению алкоксида титана в полититаноксид проводили при комнатной температуре в боксе с сухим воздухом. Вторую стадию процесса – радикальную полимеризацию по двойным связям метакрилового мономера – проводили при 70 °С в воздушном термостате в течение нескольких часов.
Гидролитическую поликонденсацию алкоксида титана при 25 °С изучали методом диэлектрической спектроскопии при помощи низкочастотного комплекса импедансных измерений проводящих сред, разработанного авторами работ [7–9]. Реакционные смеси заливали в измерительные ячейки и погружали в них две платиновые пластины площадью 0,35 см2 каждая, расположенные на расстоянии l = 1 мм параллельно друг другу и подключенные к источнику переменного тока. Измеряли частотные зависимости активной (ReZ, Ом) и реактивной (ImZ, Ом) состав- ляющих комплексного сопротивления системы и их изменение во времени в ходе поликонденсации в диапазоне частот 10 Гц до 20000 Гц. Амплитуда сигнала, подаваемого на исследуемую систему, не превышала 5–10 мВ. В этом случае исключается разрушающее влияние электрического поля на компоненты реакционной смеси [8, 10]. Полученные зависимости ImZ = f(ReZ), а также этих величин от частоты внешнего электрического поля, позволяют определить характеристики релаксационных процессов, а изменение этих зависимостей во времени – судить о структурных превращениях и исследовать их кинетику [11–12].
После завершения поликонденсации методом ИК-спектроскопии на приборе Infralum FT 801 определяли содержание двойных связей в реакционной системе. Для этого контролировали отношение интенсивностей полос поглощения ( h 1 / h 2 ), соответствующих валентным колебаниям связей С=С (ν 1 =1637 см–1) и С=О (ν2 =1720 см–1) мономера во времени от момента смешения компонентов до завершения стадии формирования полититаноксида (рис. 1, табл. 1). Установлено, что количество двойных С=С связей винилового мономера не изменяется вплоть до завершения поликонденсации ( Т = 25 °С, длительное время поликонденсации).
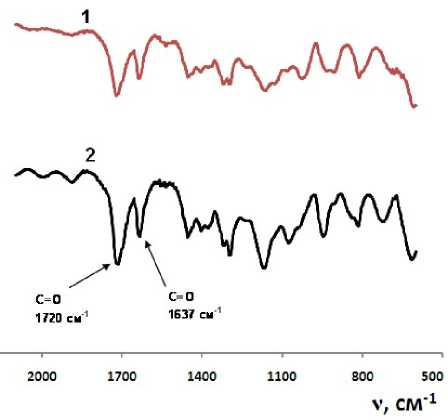
Рис. 1. ИК-спектры реакционной системы непосредственно после смешения компонентов (кривая 1 – h 1 (С=C)/h 2 (C=O) = 0,594) и через 24 ч (кривая 2 – h 1 (С=C)/h 2 (C=O) = 0,590) для исходного мольного соотношения [ГЭМА]/[Ti(OPri) 4 ] = 6:1 (h – интенсивность валентных колебаний)
Таблица 1 Отношение интенсивностей валентных колебаний С=С и С=О связей во времени при различных мольных соотношениях мономеров
|
[ГЭМА]/[Ti(OPri) 4 ] = 4 |
[ГЭМА]/[Ti(OPri) 4 ] = 6 |
[ГЭМА]/[Ti(OPri) 4 ] = 10 |
[ГЭМА]/[Ti(OPri) 4 ] = 4 + 3 масс. % AgNO 3 |
||||
|
Время, ч |
h 1 (С=C)/ h 2 (C=O) |
Время, ч |
h 1 (С=C)/ h 2 (C=O) |
Время, ч |
h 1 (С=C)/ h 2 (C=O) |
Время, ч |
h 1 (С=C)/ h 2 (C=O) |
|
0,3 |
0,669 |
0 |
0,594 |
0 |
0,608 |
0 |
0,545 |
|
1 |
0,660 |
0,6 |
0,583 |
1 |
0,609 |
0,7 |
0,553 |
|
24 |
0,682 |
23 |
0,590 |
25,8 |
0,603 |
24,7 |
0,559 |
|
72 |
0,684 |
47 |
0,597 |
52 |
0,613 |
53 |
0,547 |
|
100 |
0,667 |
100 |
0,597 |
100 |
0,634 |
103 |
0,554 |
Полимеризацию системы после завершения ее поликонденсации исследовали калориметрическим методом на термографической установке [13], когда часть приготовленных реакционных смесей отбирали в стеклянные ампулы и выдерживали при 25 °С в боксе сухим воздухом в течение времени, необходимого для завершения поликонденсации алкоксида титана. Затем ампулы запаивали и помещали в измерит е льные ячейки термостатируемого блока термографической установки. Полимеризацию проводили при температуре 70 ° С, время установления изотермического режима после помещения в блок ампул не превышало 5 минут. Масса реакционной смеси в ампуле составляла 0,18 –0,20 г. В образовавшемся полимере бромид-броматным методом определяли количество остаточного мономера [14], которое составляло ~ 0,5 масс. %. По результатам тепловыделения рассчитывали глубину конверсии мономера в каждый момент времени, строили интегральную и дифференциальную кривые скорости полимеризации. Площадь под кривой «напряжение-время» соответствовала максимальному значению конверсии. В качестве эталона при расчетах было использовано тепловыделение при полимеризации метилметакрилата, для которого ΔН° = –13,3 ккал/моль [15].
Структуру сополимеров и порошков, полученных после сжигания сополимеров, изучали методами рентгенофазового анализа (РФА) и рассеивания рентгеновских лучей на малых углах (РМУ). РФА-эксперимент выполняли на рентгеновском дифрактометре “Bruker D8 Discover”, с использованием CuKa излучения. Образцы сополимеров и порошков, оставшихся после их сжигания, измельчали и помещали в кювету из плавленого кварца. Съемку дифрактограмм проводили для углового диапазона 10–60° по углу дифракции 2θ в симметричной геометрии со щелью 0,6 мм на первичном пучке и линейным позиционно чувствительным детектором LynxEye. Малоугловые рентгенограммы регистрировали с помощью малоугловой камеры КРМ-1 с коллимацией первичного пучка по схеме Кратки, излучение CuKα, монохроматизированное Ni-фильтром; интенсивность рассеянного излучения регистрировали в угловом интервале от 5' до 160'. Точность регистрации не менее 3 %.
Оптические свойства сополимеров исследовали на спектрофотометре УФ- и видимого диапазонов UV-1650 (Shimadzu, Япония). Формирование НЧ Ag+ контролировали методом оптической спектроскопии (ОС) по изменению интенсивности полосы поглощения при X = 390-420 нм, соответствующей плазмонному резонансу НЧ Ag [16].
Фотокаталитические свойства полититаноксида, в том числе легированного НЧ Ag, в составе органо-неорганического композиционного материала исследовали на примере разложения метиленового оранжевого (МО) при действии УФ-света. Эти реакции часто используются в качестве модельных для оценки каталитической активности TiO2 [17]. Готовили растворы МО с концентрацией 0,1 масс. % в воде, погружали в них тонкие пленки органо-неорганических сополимеров (толщина пленок 0,2 мм) как катализаторов. Далее растворы МО подвергали УФ-облучению (источник – ртутная лампа ДРТ-400), толщина поглощающего слоя составляла 2 см. Методом ОС на длине волны λ = 480 нм контролировали разложение МО во времени при УФ-воздействии по изменению спектров их растворов, содержащих катализатор. Полученные спектры были использованы для построения кинетических кривых разложения МО.
Результаты и обсуждение
Наличие функциональных групп в ГЭМА и Ti(OR)4 и полимерах, образующихся в ходе гидролитической поликонденсации алкоксида титана и обладающих собственным дипольным моментом, позволяет исследовать релаксационные процессы, связанные с ориентацией фрагментов молекул, содержащих эти функциональные группы по изменению комплексного сопротивления системы (|Z|) при наложении на нее внешнего переменного электрического поля. Анализ зависимостей мнимой части сопротивления (ImZ) от реальной (ReZ) – годографов – дает полное представление об изменениях, происходящих в системе со временем [10, 18].
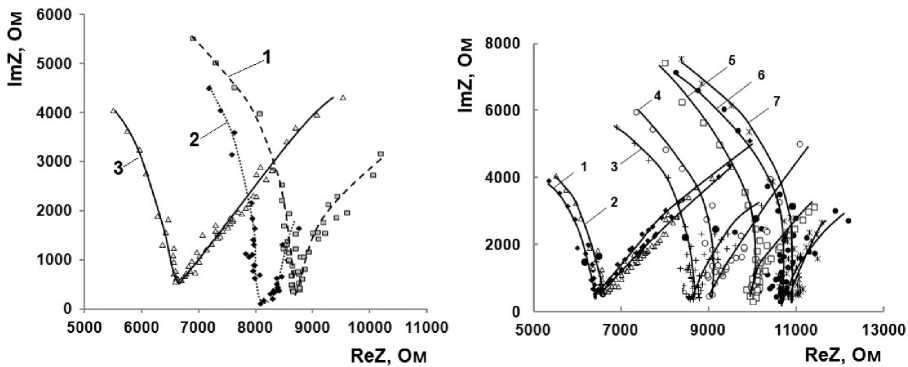
Была исследована поликонденсация алкоксида титана в системах с различным исходным мольным соотношением компонентов [ГЭМА]/[Ti(OPri)4], в том числе содержащих AgNO3. Качественная картина зависимости ImZ = f(ReZ) в процессе поликонденсации алкоксида титана во всех случаях носит однотипный характер (рис. 2, а). Годографы представляют собой незаконченные полуокружности, сходящиеся в одной точке («галка»). Такой вид зависимостей ImZ = f(ReZ) – часть полуокружности – согласно работе [18] свидетельствует о релаксационных процессах, протекающих без фазового разделения. Наличие двух полуокружностей указывает на конформационные переходы, связанные с пространственной ориентацией фрагментов молекул, в двух различных соединениях, содержащих функциональные группы (в системе протекают параллельно два процесса). Из рис. 2, б видно, что со временем происходит нарастание левой и укорачивание правой полуокружностей. Мы полагаем, что правая «ветвь» кривой отражает расход алкоксида титана в процессе поликонденсации, левая «ветвь» – формирование полититаноксида.
б)
а)
Рис. 2. Экспериментальные диаграммы, полученные при исследовании гидролитической поликонденсации алкоксида титана: а – годографы ImZ = f (ReZ) для систем с разным исходным мольным соотношением [ГЭМА]/[Ti(OPri) 4 ] (время поликонденсации 24 часа): 1 – 10:1, 2 – 6:1, 3 – 4:1; б – годографы ImZ = f (ReZ) для смеси исходного состава [ГЭМА]/[Ti(OPri) 4 ] = 10:1 во времени: 1 – 0,25 ч, 2 – 1 ч, 3 – 24 ч, 4 – 41 ч, 5 – 49 ч, 6 – 71 ч, 7 – 167 ч
Годографы, полученные при поликонденсации алкоксида титана в присутствии AgNO3, представлены на рис. 3 и также включают в себя две незаконченные полуокружности. Причем, как и в первом случае, по мере протекания гидролитической поликонденсации алкоксида титана происходит сокращение правой «ветви» и нарастание левой до некоторого предельного значения. Все это также указывает на снижение содержания одного из компонентов системы – расходование Ti(OR) 4 и нарастание содержания другого – образование полититаноксида. При этом наблюдается увеличение скорости поликонденсации. Из рис. 3 видно, что кривые ImZ = f(ReZ) через 2 и 7 суток в системах с AgNO 3 практически совпадают.
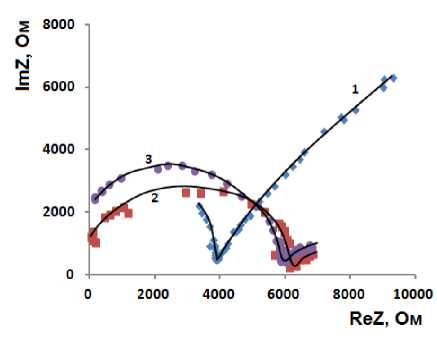
Рис. 3. Годографы системы исходного состава [ГЭМА]/[Ti(OPri) 4 ] = 4:1 + 3 масс.% AgNO 3 (по отношению к массе Ti(OPri) 4 ): кривая 1 – через 15 минут, 2 – через 2 дня, 3 – через 7 дней после смешения компонентов
Для построения зависимости степени превращения алкоксида титана от времени в процессе поликонденсации была выбрана частота F = 8 кГц, при которой фиксируются релаксационные процессы, обусловленные увеличением содержания полимера (полититаноксида) в системах с различным исходным мольным соотношением [ГЭМА]/[Ti(OPri) 4 ] и в присутствии AgNO 3 . В табл. 2 представлены значения реальной части сопротивления на частоте F = 8 кГц для различных составов реакционной смеси во времени. По данным табл. 2 рассчитывали степень завершенности (q) поликонденсации алкоксида титана, как отношение значения изменения реального сопротивления в момент времени t (ReZt) к максимальному значению реального сопротивления ReZcotst в конце процесса (рис. 4).
Из рис. 4, а видно, что скорость поликонденсации зависит от состава исходной реакционной системе. Наблюдается существенное увеличение времени поликонденсации при разбавлении алкоксида титана виниловым мономером. Так, при соотношении [ГЭМА]/[Ti(OPri)4] = 4:1 процесс близок к завершению через 60 часов, в то время как при соотношении [ГЭМА]/[Ti(OPri) 4 ] = 10:1 процесс длится в два раза медленнее (115 часов). Введение в систему AgNO 3 (1 масс. % по отношению к Ti(OPri) 4 ) как показано на примере реакционной смеси исходного состава [ГЭМА]/[Ti(OPri)4] = 4:1 ускоряет поликонденсацию, которая близка к завершению уже спустя 50 часов после смешения компонентов. Это явление может быть связано с тем, что AgNO3, диссоциируя в реакционной смеси, может также выступать в качестве катализатора процесса, как и HCl. Следует отметить, что время завершения поликонденсации многократно превышает время структурирования системы (6–12 часов).
Таблица 2
Изменение реальной части комплексного сопротивления системы на частоте 8 кГц и соответствующее значение степени завершенности поликонденсации алкоксида титана
|
[ГЭМА]/[Ti(OPri) 4 ] |
|||||||||||
|
4 |
6 |
10 |
4 + 1 масс. % AgNO 3 |
||||||||
|
Время, ч |
ReZ t , Ом |
q |
Время, ч |
ReZ t , Ом |
q |
Время, ч |
ReZ t , Ом |
q |
Время, ч |
ReZ t , Ом |
q |
|
1,50 |
3855 |
0,53 |
0,10 |
6209 |
0,48 |
0,25 |
200 |
0,04 |
10 |
915 |
0,13 |
|
3,33 |
4002 |
0,55 |
0,25 |
7055 |
0,54 |
1,00 |
522 |
0,10 |
22 |
1414 |
0,20 |
|
3,40 |
4437 |
0,61 |
0,80 |
7129 |
0,55 |
2,00 |
462 |
0,09 |
25 |
1933 |
0,28 |
|
3,70 |
4510 |
0,62 |
24 |
7141 |
0,55 |
24,00 |
2492 |
0,50 |
30 |
4109 |
0,60 |
|
25,20 |
6330 |
0,87 |
48,00 |
7196 |
0,56 |
41,75 |
3189 |
0,64 |
38 |
6051 |
0,88 |
|
63,00 |
6838 |
0,94 |
49,25 |
7979 |
0,62 |
49,17 |
3274 |
0,66 |
45 |
6213 |
0,91 |
|
93,10 |
7129 |
0,98 |
50,00 |
9317 |
0,72 |
50,58 |
4091 |
0,83 |
48 |
6584 |
0,96 |
|
143,5 |
7275 |
1,00 |
72,00 |
9317 |
0,72 |
115,0 |
4618 |
0,93 |
64 |
6803 |
0,99 |
|
141,8 |
12890 |
1,00 |
167,4 |
4937 |
1,00 |
132 |
6815 |
1,00 |
|||
б)
а)
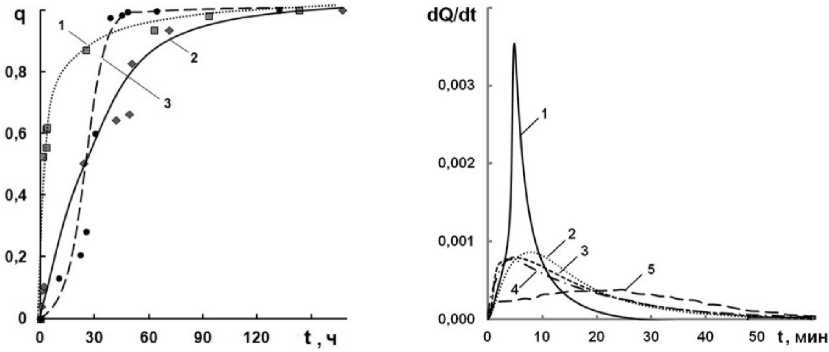
Рис. 4. а – степень завершенности гидролитической поликонденсации (q) алкоксида титана в смеси исходного состава [ГЭМА]/[Ti(OPri) 4 ]: кривая 1 – 4:1, кривая 2 – 10:1, кривая 3 – [ГЭМА]/[Ti(OPri) 4 ]= 4:1 + 1 масс. % AgNO 3 (относительно массы Ti(OPri) 4 ); б – зависимость скорости полимеризации (dQ/dt)от времени для смесей с различным мольным соотношением звеньев [ГЭМА]/[(≡TiO n ) m ]: 1 – ГЭМА, 2 – 10:1, 3 – 6:1, 4 – 4:1, 5 – 4:1 + 1 масс. % AgNO 3 (относительно от массы Ti(OPri) 4 ). Q – глубина превращения винилового мономера, t – время
Радикальная полимеризация винилового мономера ГЭМА при 70 ºС осуществлялась после завершения гидролитической поликонденсации алкоксида титана в системе и была изучена термографическим методом (рис. 4, б). Из рис. 4, б видно, что гомополимеризация ГЭМА характеризуется высокой скоростью и протекает с ярко выраженным гель-эффектом – процесс завершается за 25 минут. Это может быть обусловлено ассоциацией мономера за счет водородных связей. По-лититаноксид, присутствующий в системе, приводит к замедлению скорости полимеризации и снижению гель-эффекта (рис. 4, б, кривые 2–4). Мы предполагаем, что это явление обусловлено несколькими причинами: отсутствием подвижности части этилметакрилатных групп, химически связанных с полититаноксидом; затруднением диффузии свободного ГЭМА в структурированной вязкой среде образовавшегося геля полититаноксида. Кроме того, возможно уменьшение концентрации радикалов (как первичных, так и радикалов роста) в системе в результате их «гибели» при взаимодействии с поли(титаноксид-этилметакрилатом) по связи Ti–O. Присутствие в полимеризующейся системе AgNO3 приводит к практически полному вырождению гель-эффекта. Полимеризация, как и в случае отсутствия прекурсора завершается примерно за 1 час (рис. 4, б, кривая 5).
Конечный продукт двухстадийного синтеза представляет собой оптически прозрачный сополимер с различным соотношением звеньев [ГЭМА]/[(≡TiO)n] ((≡TiO)n – полититаноксид) с трехмерной структурой, так как не растворяется в органических растворителях (диметилформамиде, диметилсульфоксиде, ацетоне и бензоле). Образование трехмерной структуры сополимера является результатом взаимодействия ГЭМА и Ti(OPri)4 после смешения за счет протекания реакции переэтерефикации из-за большей нуклеофильности ГЭМА [19–20].
Существенно, что выбранный режим получения сополимеров позволяет избежать восстановления допанта во время синтеза. Подтверждением этого являлось отсутствие в УФ-спектрах образцов после полимеризации максимума плазмонного резонанса НЧ Ag (λ = 390–430 нм).
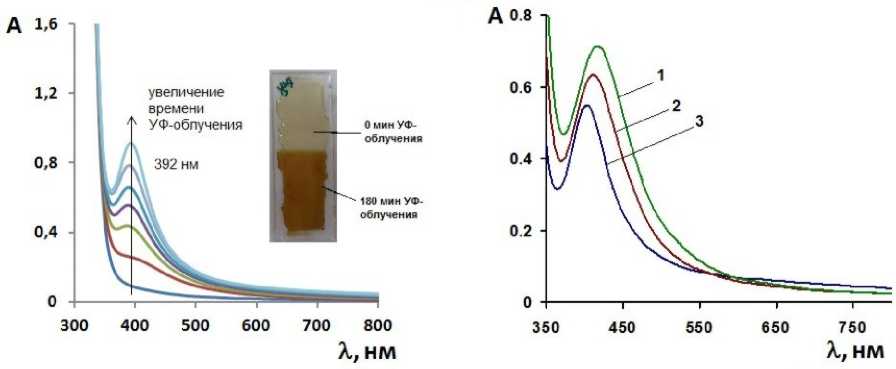
НЧ серебра в гибридных сополимерах получали УФ-восстановлением AgNO 3 . Формирование НЧ Ag контролировали по изменению УФ-спектров сополимеров, в которых наблюдается появление и нарастание полосы плазмонного резонанса НЧ серебра в области 390–430 нм (рис. 5, а). Изменение интенсивности полосы поглощения ионов Ag+ на λ = 360 нм в ходе УФ-воздействия, а следовательно и расходование AgNO 3 , зафиксировать не удалось в силу наложения друг на друга полос поглощения, характерных для ионов Ti4+, ГЭМА и Ag +. Визуально образование НЧ Ag сопровождается изменением цвета образца от прозрачного бесцветного до темно-коричневого (рис. 5, а), вставка – фотография образца, часть которого подвергнута УФ-воздействию).
а)
б)
Рис. 5. Спектры поглощения сополимеров, содержащих AgNO 3 : а – формирование НЧ Ag в сополимерах состава [ГЭМА]/[(≡TiO) n ] = 4:1 + 3 масс. % AgNO 3 (от массы Ti(OPri) 4 ); б – влияние концентрации допанта на положение максимума плазмонного резонанса НЧ Ag, сформированных в сополимерах состава [ГЭМА]/[(≡TiO) n ] = 4:1 после УФ-облучения в течение 120 мин: кривая 1 – 1 масс. % (λ max (Ag) = 392 нм); кривая 2 – 2 масс. % (λ(Ag) = 411 нм); кривая 3 – 3 масс. % (λ max (Ag) = 416 нм)
Многие свойства нанокомпозиционных материалов зависят от размеров частиц в их составе [21]. Качественно о размере НЧ можно судить по положению максимума их плазмонного поглощения в материалах [21]. Поэтому было исследовано влияние концентрации допанта и соотношения органического и неорганического компонентов на положение максимума плазмонного резонанса НЧ Ag, а следовательно, и размер НЧ. Оказалось, что увеличение концентрации AgNO 3 в сополимере приводит к смещению максимума полосы поглощения НЧ серебра с 392 до 416 нм. Это свидетельствует о формировании более крупных частиц (рис. 6, б).
а)
б)
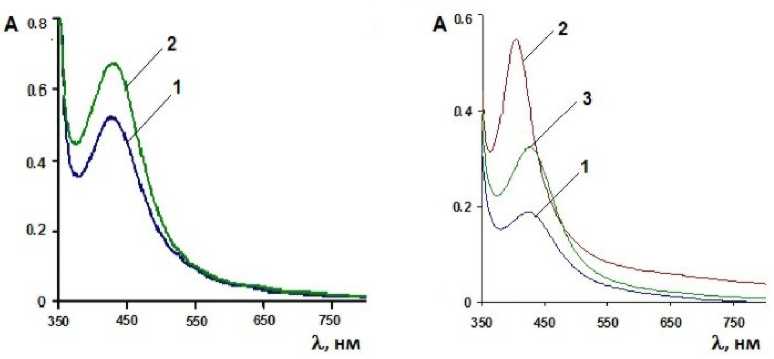
Рис. 6. Спектры поглощения сополимеров с НЧ Ag: а – влияние соотношения компонентов [ГЭМА]/[(≡TiO) n ] на положение максимума плазмонного поглощения НЧ Ag при фиксированной исходной концентрации AgNO 3 – 3 масс.% (от массы Ti(OPri) 4 ): кривая 1 – 4:1, λ max (Ag) = 416 нм, кривая 2 – 10:1, λ max (Ag) = 429 нм; б – спектры поглощения композитов состава [ГЭМА]/[(≡TiO) n ] = 4:1+ 1 масс. % AgNO 3 : кривая 1 – 30 мин УФ (λ max = 423 нм; А max =0,188), кривая 2 – 120 мин УФ (λ max = 403 нм; А max =0,549), 3 – через 14 часов после прекращения УФ-облучения (λ max = 426 нм; А max =0,323)
Варьирование соотношения органического и неорганического компонентов при фиксированной концентрации AgNO 3 приводит к смещению λ max с 416 до 429 нм (рис. 6, а). Подобное изменение размеров НЧ может быть связано с тем, что структура сополимера с пониженным содержанием полититаноксида является менее сшитой, что облегчает диффузию атомов и ионов серебра в процессе сборки НЧ. Обращает на себя внимание, спустя 12 часов после прекращения УФ-облучения образцов наблюдается трансформация НЧ Ag – с одной стороны, существенно снижается интенсивность максимума поглощения НЧ, и в то же время происходит его батохром-ный сдвиг, что свидетельствует об укрупнении НЧ (рис. 6, б).
Присутствие в составе сополимеров НЧ Ag, обладающих свойством поверхностного плазмонного резонанса, может являться причиной сенсибилизации полититаноксида в видимом диапазоне длин волн, и как следствие – повышать эффективность разделения зарядов по реакции Ti4++ e → Ti3+ [22].
Исследование структуры сополимеров
С позиции использования пленок, содержащих полититаноксид и НЧ серебра как новых каталитических систем принципиально важной является их структура. В литературе отмечается, что наибольшую эффективность в фотокатализе проявляет анатазная форма диоксида титана [21]. В зависимости от условий синтеза можно ожидать формирование различных структур как полититаноксида, так и органо-неорганических сополимеров. Структура полученных материалов была исследована с применением методов РМУ и РФА.
Согласно данным РФА экспериментов образцы гибридных сополимеров, независимо от состава, имеют аморфную структуру. Об этом свидетельствует наличие в их дифрактограммах аморфного гало в области малых углов (рис. 7). Отсутствие кристаллических областей в дифрак-тограммах образцов, по-видимому, может быть объяснено неполной завершенностью гидролитической поликонденсации алкоксида титана, когда часть цепей полититаноксида остаются связанными с ГЭМА. Эти органические фрагменты будут препятствовать образованию строго упорядо- ченной структуры части атомов Ti и O. В то же время в дифрактограмме образца, содержащего НЧ Ag, заметен очень слабый узкий пик около 38°, который соответствует фазе серебра (рис. 7, кривая 5). Однако размер НЧ не может быть оценен по этому пику.
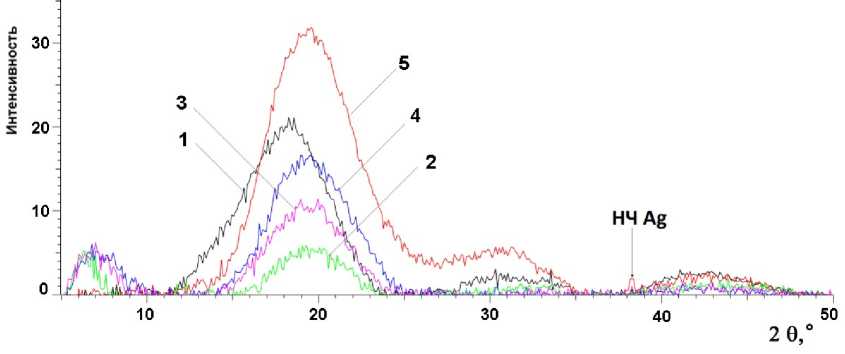
Рис. 7. Дифрактограммы образцов сополимеров, синтезированных при различном мольном соотношении компонентов [ГЭМА]/[(≡TiO) n ] (кривая 1 – 2:1, кривая 2 – 4:1 , кривая 3 – 6:1, кривая 4 – 10:1) и содержащих НЧ Ag (кривая 5 – [ГЭМА]/[(≡TiO) n ] = 6:1 + 0,5 масс.% НЧ Ag
Внутренняя структура сополимеров была исследована методом РМУ, который успешно применяется для изучения надмолекулярной структуры вещества в конденсированном состоянии (рис. 8, а). Из рисунка видно, что сополимеры содержат НЧ полититаноксида со средним размером от 4 до 6 нм, что также указывает на частичную упорядоченность структуры материалов. НЧ Ag, сформированные в сополимерах при УФ-восстановлении AgNO 3 , имеют средний размер 9 нм и узкие распределение по размерам от 2 до 20 нм (рис. 8, а, кривая 2).
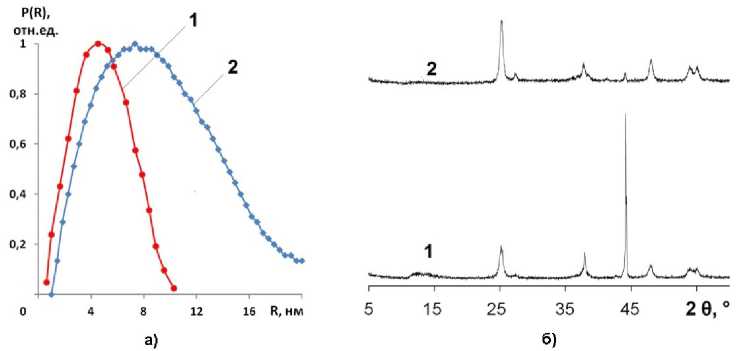
Рис. 8. Структура сополимеров [ГЭМА]/[(≡TiO) n ] = 6:1: (а) распределение неоднородностей, содержащихся в сополимере, по размерам (кривая 1 – НЧ полититаноксида, кривая 2 – 0,5 масс. % НЧ Ag); (б) дифрактограммы продуктов деструкции исходного сополимера (кривая 1) и сополимера с 0,5 масс.% НЧ Ag (кривая 2)
Дополнительный анализ структуры цепей полититаноксида в сополимерах был проведен на основании РФА-исследования порошков, оставшихся после деструкции органической части материалов при T = 500 °С. Оказалось, что во всех случаях зола представляет собой диоксид титана (содержание TiO2 в золе соответствует его количеству, рассчитанному на основании состава начальной реакционной смеси), однако его кристаллическая модификация зависит от условий синтеза сополимера (рис. 8, б). Так, зола, оставшаяся после сжигания образца без НЧ Ag, представляет собой диоксид титана с кристаллической решеткой анатаза (пространственная группа I4 1 /amd, код 94566) (рис. 8, б, кривая 1). В то же время на дифрактограмме золы образца с НЧ Ag видны пики двух аллотропных модификаций диоксида титана – анатаза (95 масс. % от массы диоксида титана в золе) и рутила (5 масс. % от массы диоксида титана в золе) и металлического золота (рис. 8, б, кривая 2).
Таким образом, сополимер без НЧ серебра имеет структуру неорганических цепей близкую к анатазной, в то время как присутствие в мономерной смеси AgNO 3 при синтезе приводит к формированию сополимере цепей полититаноксида смешанной структуры – анатаза и рутила, причем в соотношении, близком к оптимальному для проявления фотокаталитических свойств [23–24].
Совокупность полученных результатов позволяет заключить, что гибридные сополимеры, полученные из ГЭМА и изопропоксида титана, имеют трехмерную структуру, в которой цепи полититаноксида формируют агломераты размером ~ 6 нм с кристаллической решеткой близкой к анатазной или к анатазной, смешанной с рутильной, соединяются химическими связями с органической полимерной матрицей и равномерно распределены в ней. Наночастицы Ag находятся в материале в высокодисперсном состоянии.
Все это дает основание предполагать, что нанокомпозиты, содержащие НЧ полититаноксида в сочетании с НЧ серебра, будут проявлять фотокаталитическую активность.
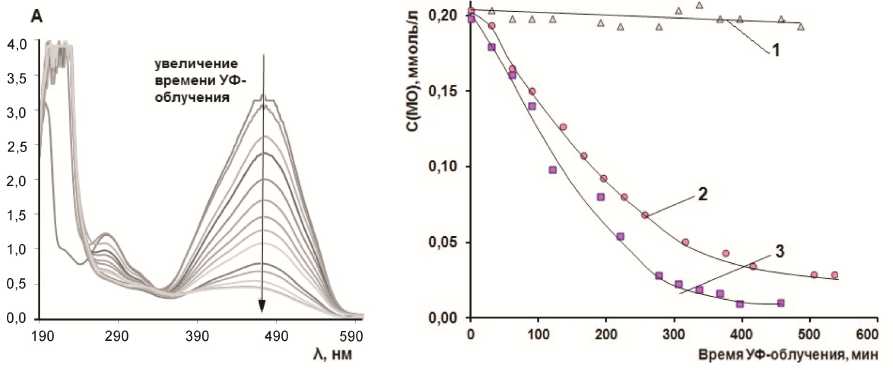
Фотокаталитические свойства органо-неорганических сополимеров были исследованы на модельной реакции фоторазложения МО в водном растворе. В литературе предложено несколько схем разложения МО на TiO 2 при УФ-облучении, одна из которых предполагает глубокое окисление красителя до CO 2 и воды [22]. При этом в спектре МО происходит изменение интенсивности характерной полосы поглощения в области 470–480 нм [22]. В качестве фотокатализаторов были испытаны тонкие пленки сополимеров толщиной 0,2 мм, содержащие большое количество полититаноксида (размер кластеров от 3 до 6 нм) и НЧ Ag (размер частиц от 2 до 20 нм). Процесс разложения МО в присутствии сополимеров контролировали спектрофотометрически по уменьшению интенсивности полосы поглощения на длине волны 480 нм (рис. 9, а). Оказалось, что все исследованные образцы проявляют фотокатализатическую активность и вызывают обесцвечивание раствора МО под действием УФ-света. Сравнение глубины обесцвечивания растворов МО при использовании различных фотокатализаторов показано на рис. 9, б.
а)
б)
Рис. 9. Фотокаталитические свойства сополимеров: а – изменение спектра поглощения раствора МО в воде по мере увеличения времени его УФ-облучения при использовании в качестве катализатора сополимера исходного состава [ГЭМА]/[(≡TiO) n ] = 4:1 + 0,2 масс.% НЧ Ag; б – изменение концентрации МО в растворе во времени при его УФ-облучении без катализатора (кривая 1), с использованием катализаторов состава [ГЭМА]/[(≡TiO) n ] = 4:1 (кривая 2) и [ГЭМА]/[(≡TiO) n ] = 4:1 + 0,5 масс. % НЧ Ag (кривая 3)
Видно, что при УФ-облучении раствора МО его концентрация практически не изменяется в течение 10 часов («глухой» опыт). При использовании сополимеров в качестве фотокатализаторов обесцвечивание МО происходит уже с первых минут УФ-воздействия. Существенное снижение концентрации МО и вместе с тем более глубокое его превращение, наблюдается для катализатора, содержащего НЧ Ag. Для сравнения – за одинаковое время (400 мин) УФ-облучения раствора МО с катализатором без НЧ Ag разложение МО происходит на 65 %, в то время как введение НЧ Ag в состав сополимера увеличивает глубину превращения МО до 90 %.
Заключение
Исследована кинетика конденсационно-полимеризационных процессов получения органонеорганических сополимеров из изопропоксида титана и ГЭМА в присутствии AgNO3. Установлено, что AgNO3 существенно ускоряет гидролитическую поликонденсацию алкоксида титана, приводит к подавлению гель-эффекта радикальной полимеризации ГЭМА и изменяет структуру полититаноксида в органической полимерной матрице. Предложенный подход к получению нанокомпозитов, включающих полититаноксид, позволяет избежать преждевременного восстановления AgNO 3 и формировать из него наночастицы Ag со средним размером 9 нм «in one pot reac-tion» для создания катализаторов с высокой активностью. Органо-неорганические сополимеры, содержащие полититаноксид, проявляют фотокаталитические свойства в реакциях разложения МО. Лигирование полититаноксида НЧ Ag в сополимере приводит к возрастанию скорости разложения МО и увеличению глубины протекания процесса – до 90 %.
Работа выполнена при поддержке РФФИ (№ 14-03-31981), программы У.М.Н.И.К. (договор 1511 ГУ/2014) и Министерства образования и науки РФ (гос. контракт № 4.1537.2014К).
Список литературы Получение, структура и фотокаталитические свойства органо-неорганического нанокомпозита, содержащего полититаноксид и наночастицы серебра
- Rozes, L. Titanium oxo-Clusters: Precursors for a Lego-Like Construction of Nanostructured Hybrid Materials/L. Rozes, C. Sanchez//Chem. Soc. Rev. -2011. -V. 40, № 2. -P. 1006-1030 DOI: 10.1039/C0CS00137F
- Synthesis, Characterization and Demonstration of Self-Cleaning TiO2 Coatings on Glass and Glazed Ceramic Tiles/K. Murugan, R. Subasri, T.N. Rao and et al.//Progress in Organic Coatings. -2013. -V. 76, № 12. -P. 1756-1760. DOI 10.1016/j.porgcoat.2013.05.012.
- Solution Processable Titanium Dioxide Precursor and Nanoparticulated Ink: Application in Dye Sensitized Solar Cells/P. Bosch-Jimenez, Y.Yu, M. Lira-Cantu and et al.//J. Colloid and Interface Sci. -2014. -V. 416. -P. 112-118 DOI: 10.1016/j.jcis.2013.11.013
- Optical 3D-Storage in Sol-Gel Materials with a Reading by Optical Coherence Tomography-Technique/J.-A. Reyes-Esqueda, L. Vebreb, R. Lecaque et al.//Opt. Comm. -2003. -V. 220, № 1-3. -P. 59-66 DOI: 10.1016/S0030-4018(03)01354-3
- A Novel TiO2 Composite for Photocatalytic Wastewater Treatment/M.S. Hamdy, W.H. Saputera, E.J. Groenen and et. al.//J. Catalysis. -2014. -V. 310. -P. 75-83 DOI: 10.1016/j.jcat.2013.07.017
- A Review on Catalytic Applications of Au/TiO2 Nanoparticles in the Removal of Water Pollutant/A. Ayati, A. Ahmadpour, F.F. Bamoharram and et. al.//Chemosphere. -2014. -V. 107. -P. 163-174 DOI: 10.1016/j.chemosphere.2014.01.040
- Москвичев, А.Н. Исследование свойств и кинетики полимеризации анаэробных герметиков методом импедансных измерений/А.Н. Москвичев, А.А. Москвичев//Изв. высш. уч. завед. Сер.: Хим. и хим. технол. -2007. -Т. 50, № 3. -С. 69-71.
- Низкочастотный комплекс импедансных измерений характеристик проводящих сред/А.В. Афанасьев, А.Н. Москвичев, А.А. Москвичев и др.//Вестник ННГУ им. Н.И. Лобачевского. Радиофизика. -2008. -№ 3. -С. 60-64.
- Москвичев, А.Н. Метод импедансных измерений для исследования свойств и кинетики полимеризации олигомерных композиций/А.Н. Москвичев, А.А. Москвичев//Труды НГТУ им. Р.Е. Алексеева. Хим., химич. и биотех. -2007. -Т. 80, № 1. -С. 223-229.
- Impedance Spectroscopy: Theory, Experiment, and Applications/ed. by Ye. Barsucov, R. Macdonald. -2nd Edition. -Copyright. John Wiley & Sons, 2012. -616 p.
- Метод диэлектрической спектроскопии как метод исследования процессов отверждения композиций на основе эпоксидных олигомеров/Д.Л. Родин, А.В. Солопченко, А.В. Кепман и др.//Бутлеровские cообщения. -2013. -Т. 35, № 8. -С. 31-41.
- Механизм анионной полимеризации 2-гидроксиэтил(мет)акрилатов под действием щелочных металлов и их алкоксидов/Б.А. Розенберг, Г.Н. Бойко, Л.М. Богданова и др.//Высокомолек. соед. Сер. А. -2003. -Т. 45, № 9. -С. 1429-1439.
- Арулин, В.И. Термографический метод исследования кинетики полимеризации в условиях, близких к изотермическим/В.И. Арулин, Л.И. Ефимов//Труды по Химии и Химической Технологии. -1970. -Вып. 2. -С. 74-77.
- Морозов, Л.А. Методы анализа акрилатов и метакрилатов. Практическое руководство/Л.А. Морозов, Ю.А. Кашеварова, О.М. Слепцова. -М.: Химия, 1972. -527 с.
- Липатов, Ю.С. Справочник по химии полимеров/Ю.С. Липатов. -Киев: Наукова думка, 1971. -342 с.
- Hirakawa, T. Charge Separation and Catalytic Activity of Ag@TiO2 Core-Shell Composite Clusters under UV-irradiation/T. Hirakawa, P.V. Kamat//J. Am. Chem. Soc. -2005. -V. 127. -P. 3928-3934 DOI: 10.1021/ja042925a
- Niu, P. Photocatalytic Degradation of Methyl Orange by Titanium Dioxide-Decatungstate Nanocomposite Films Supported on Glass Slides/P. Niu, J. Hao//Colloids and Surfaces A: Physicochem. Eng. Aspects. -2013. -V. 431. -P. 127-132 DOI: 10.1016/j.colsurfa.2013.04.033
- Соловьева, Л.М. Аналитическое построение годографов комплексного сопротивления и проводимости электрических эквивалентных схем/Л.М. Соловьева//Электродные процессы в галогенидных и окисных электролитах. -УБЦ. АН СССР, 1981. -С. 68.
- Mehrotra, R.C. Alkoxides and Alkylalkoxides of Metals and Metalloids/R.C. Mehrotra//lnorganica Chimica Acta. Reviews. -1967. -V. 1. -P. 99-112 DOI: 10.1016/0073-8085(67)80023-8
- Mehrotra, R.C. Chemistry of Alkoxide Precursors/R.C. Mehrotra//J. Non-Crystalline Solids. -1990. -V. 121, no. 1-3. -P. 1-6 DOI: 10.1016/0022-3093(90)90094-3
- Помогайло, А.Д. Наночастицы металлов в полимерах/А.Д. Помогайло, А.С. Розенберг, И.Е. Уфлянд. -М.: Химия, 2000. -672 с.
- Brookite Versus Anatase TiO2 Photocatalysts: Phase Transformations and Photocatalytic Activities/T.A. Kandiel, L. Robben, A. Alkaimad and et. al.//Photochem. and Photobiol. Sci. -2013. -no. 12. -P. 602-609 DOI: 10.1039/C2PP25217A
- Direct Z-Scheme Anatase/Rutile Bi-Phase Nanocomposite TiO2 Nanofiber Photocatalyst with Enhanced Photocatalytic H2-Production Activity/F. Xu, W. Xiao, B. Chenga, J. Yua//International Journal of Hydrogen Energy. -2014. -V. 39, no. 28. -P. 15394-15402 DOI: 10.1016/j.ijhydene.2014.07.166
- Rutile TiO2 Nanowires on Anatase TiO2 Nanofibers: A Branched Heterostructured Photocatalysts via Interface-Assisted Fabrication Approach/C. Wang, X. Zhang, C. Shao and et. al.//Journal of Colloid and Interface Science. -2011. -V. 362, no. 1. -P. 157-164.


