Получение водорастворимых (1-гидроксиэтилиден)дифосфонатов марганца(II)
Автор: Семенов В.В., Петров Б.И., Лазарев Н.М.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.17, 2025 года.
Бесплатный доступ
Предложены два способа получения водорастворимых координационных соединений марганца(II) из MnSO4, (1-гидроксиэтилиден)дифосфоновой кислоты H4L и моноэтаноламина. Первый заключается в осаждении из водного раствора MnSO4 карбоната марганца и превращении его в трудно растворимый (1-гидроксиэтилиден)дифосфонат H2MnL·3Н2О добавлением H4L. Последующая реакция с моноэтаноламином приводит к получению хорошо растворимого бис(моноэтаноламиний) (1-гидроксиэтилиден)дифосфоната марганца(II) дигидрата (H3NCH2CH2OH)2MnL·2Н2О. Во втором способе к раствору сульфата марганца и ОЭДФ прибавляется моноэтаноламин. Образующаяся при этом смесь (1-гидроксиэтилиден)дифосфоната марганца(II) (H3NCH2CH2OH)2MnL с бис(моноэтаноламиний)сульфатом (H3NCH2CH2OH)2SO4 образует устойчивый при хранении крепкий раствор. Углекислый газ, выделяющийся в реакции карбоната марганца с ОЭДФ, понижает реакционную способность моноэтаноламина в результате образования комплекса с углекислотой HOCH2CH2NHCOO-+NH3CH2CH2OH, что приводит к ингибированию взаимодействия (1-гидроксиэтилиден)дифосфоната H2MnL·3Н2О с моноэтаноламином. Нагревание и перемешивание реакционной смеси, полученной при взаимодействии карбоната марганца с ОЭДФ, в течение 1 ч вызывает удаление углекислого газа, вследствие чего последующее прибавление водного раствора моноэтаноламина приводит к образованию прозрачного раствора бис(моноэтаноламиний) (1-гидроксиэтилиден)дифосфоната марганца(II) дигидрата (H3NCH2CH2OH)2MnL·2Н2О. Ингибирование реакции моноэтаноламином таким образом исключается. Сделанная попытка использовать вместо моноэтаноламина водный раствор аммиака не привела к успеху. В реакции сульфата марганца(II) с тетрааммониевой солью ОЭДФ был получен труднорастворимый продукт состава 2(NH4)HMnL·H2MnL. Исследовано термическое поведение полученных соединений в температурном диапазоне 25-640 °С.
Марганец(ii), (1-гидроксиэтилиден)дифосфоновая кислота, моноэтаноламин, комплексонаты, растворимость
Короткий адрес: https://sciup.org/147248062
IDR: 147248062 | УДК: 546.185, | DOI: 10.14529/chem250103
Synthesis of water-soluble manganese(II) (1-hydroxyethylidene)diphosphonates
Two methods for obtaining water-soluble coordination compounds of manganese(II) from MnSO4, (1-hydroxyethylidene)diphosphonic acid (HEDP) H4L, and monoethanolamine have been proposed. The first method involves precipitation of manganese carbonate from an aqueous solution of MnSO4 and its conversion to sparingly soluble (1-hydroxyethylidene)diphosphonate H2MnL.3H2O by adding H4L. The subsequent reaction with monoethanolamine results in the formation of highly soluble bis(monoethanolamine) (1-hydroxyethylidene)diphosphonate manganese(II) dihydrate (H3NCH2CH2OH)2MnL.2H2O. In the second method, monoethanolamine is added to a solution of manganese sulfate and HEDP. The resulting mixture of manganese(II) (1-hydroxyethylidene) diphosphonate (H3NCH2CH2OH)2MnL with bis(monoethanolamine) sulfate (H3NCH2CH2OH)2SO4 forms a strong solution that is stable during storage. Carbon dioxide released in the reaction of manganese carbonate with HEDP reduces the reactivity of monoethanolamine as a result of the formation of a complex with carbon dioxide HOCH2CH2NHCOO-+NH3CH2CH2OH, which leads to inhibition of the interaction of (1-hydroxyethylidene) diphosphonate H2MnL.3H2O with monoethanolamine. Heating and stirring the reaction mixture obtained by the interaction of manganese carbonate with HEDP for 1 h causes the removal of carbon dioxide, as a result, the subsequent addition of an aqueous solution of monoethanolamine leads to the formation of a transparent solution of manganese(II) bis(monoethanolaminium) (1-hydroxyethylidene) diphosphonate dihydrate (H3NCH2CH2OH)2MnL.2H2O. Inhibition of the reaction by monoethanolamine is thus excluded. An attempt to use an aqueous solution of ammonia instead of monoethanolamine has been unsuccessful. A poorly soluble product of the composition 2(NH4)HMnL·H2MnL is obtained in the reaction of manganese(II) sulfate with the tetraammonium salt of HEDP. The thermal behavior of the obtained compounds has been studied in the temperature range of 25-640°C.
Текст научной статьи Получение водорастворимых (1-гидроксиэтилиден)дифосфонатов марганца(II)
Ацетаты и формиаты 3d-металлов образуют с моноэтаноламином [1] нерастворимые комплексы сложного состава. Так, при добавлении амина к раствору формиата марганца быстро выпадает осадок коричневого цвета сложного состава Mn4(OH)6(HCOO)2·H2NCH2CH2OH·2H2O. В то же время известно, что амины [H2NCH2CH2OH и H2NC(CH2OH)3] способны переводить в водную среду труднорастворимые соединения марганца(II) с (1-гидроксиэтилиден)дифосфоновой (ОЭДФ) [2, 3] и нитрилотриуксусной кислотами (НТА) [4], полученные из основного карбоната марганца(II) и сернокислого марганца(II). Координационные соединения марганца(II) с промышленными комплексонами (НТА, ЭДТА, ОЭДФ) обладают малой растворимостью [5] в водной среде, что затрудняет их использование в качестве фармацевтических препаратов, ингибиторов солеотложения в нефтяной промышленности, стабилизаторов пищевых продуктов, препаратов для химической очистки теплоэнергетического оборудования и микрокомпонентных добавок в минеральные удобрения. Цель настоящего исследования заключалась в разработке способов получения водорастворимого комплексоната, в котором в качестве источника использовалась одна из самых дешевых и доступных солей марганца(II) – пятиводный сульфат MnSO4·5H2O, в качестве промышленного комплексона – (1-гидроксиэтилиден)дифосфоновая кислота и в качестве промотора растворимости – моноэтаноламин. Ранее последний использовался [6] в процессе получения метилата марганца(II) из его карбоната. Продукты реакции ацетата марганца с алифатическими кислотами С7–С20 и моноэтаноламином, растворимые в органических средах, предложено [7] использовать в качестве сиккативов для масляных красок. Получены кристаллы соединений маганца(II) [8] и кобальта(II) [9–12] с ОЭДФ, в том числе в условиях гидротермального синтеза. Аморфные комплексы обладают большей растворимостью в водной среде и имеют преимущество для приложений в фармации и сельском хозяйстве.
Четырехосновная 1-гидроксиэтилидендифосфоновая кислота обладает хорошими хелатирующими свойствами, переводит в водную фазу оксиды и гидроксиды железа [13] и других металлов, в связи с чем может использоваться в процессах очистки трубопроводов теплосетей:
но сн3
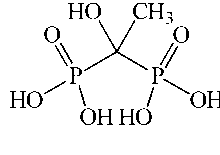
(1-Гидроксиэтилиден)дифосфоновая кислота H 4 L (ОЭДФ)
Предложены [14, 15] ингибиторы солеотложения для котловых систем, в состав которых входят также аммиак, триэтаноламин и морфолин. Реакции комплексобразования H4L в водных растворах изучены [16–19] для многих металлов. 1-Гидроксиэтилидендифосфоновая кислота использовалась [20] в синтезах комплексов изотопов технеция-99 и рения-188, предназначенных для визуализации отложений соединений кальция в кровеносных сосудах.
Экспериментальная часть
В работе использовали (1-гидроксиэтилиден)дифосфоновую кислоту H 4 L·H 2 O квалификации «ч» производства ПАО «Химпром», г. Новочебоксарск, ТУ 2439-363-05783441-2002, моно-этаноламин квалификации «ч» производства ООО «Синтез ОКА», г. Дзержинск, ТУ 2423-00278722668-2010, сульфат марганца(II) MnSO 4 ·5H 2 O, «ч», АО «Химреактив», Н. Новгород, ГОСТ 435-77. Карбонат марганца MnCO 3 ·2H 2 O (по данным РФА родохрозит), получали из сульфата марганца(II) и кислого углекислого калия.
(1-Гидроксиэтилиден)дифосфонат марганца(II) тригидрат H 2 MnL·3Н 2 О. К раствору 20 г MnSO 4 ·5H 2 O (8,30·10–2 моль) в 100 мл Н 2 О прибавляли при перемешивании 16,61 г КНСО 3 (1,66·10–1 моль) в 30 мл Н 2 О. Через 2 ч к полученной суспензии карбоната марганца прибавляли 18,60 г ОЭДФ (8,30·10–2 моль) в 30 мл Н 2 О. Прозрачный светло-розовый раствор нагревали 0,5 ч при перемешивании. Через 12 ч к полученной вязкой творожистой массе добавляли 100 мл Н2О, размешивали, фильтровали, осадок промывали водой, сушили на воздухе при 110 °С. Получили 22,30 г (7,56·10–2 моль, 91 %) (1-гидроксиэтилиден)дифосфоната марганца(II) тригидрата H2MnL·3Н2О в виде хрупкой светло-розовой массы, легко дробящейся до порошка. Растворимость 0,94 г в 100 мл Н 2 О. ИК-спектр, ν, см–1: 3620–2700 ш., 2406, 1638, 1590 пл, 1295 пл, 1194 пл, 1164, 1140, 1093, 1072, 1045, 991, 929, 917, 815, 661, 646, 586, 550, 488, 450. Найдено (%): C 7,95; H 3,83. С 2 H 12 O 10 P 2 Mn. Вычислено (%): C 7,68; H 3,86.
Бис (моноэтаноламиний) (1-гидроксиэтилиден)дифосфонат марганца(II) дигидрат (H 3 NCH 2 CH 2 OH) 2 MnL · 2Н 2 О. К суспензии 5,00 г H 2 MnL·3Н 2 О (1,60·10–2 моль) в 20 мл Н 2 О прибавляли при перемешивании 1,95 г (3,20·10–2 моль) H 2 NCH 2 CH 2 OH в 10 мл Н 2 О. Через 10 мин суспензия растворилась. Смесь фильтровали, фильтрат упаривали, остаток сушили при 110 °С.
Получили 6,42 г (1,53·10–2 моль, 96 %) (H 3 NCH 2 CH 2 OH) 2 MnL·2Н 2 О в виде прочной массы кремового цвета, размалывающейся до желтого порошка. ИК-спектр, ν, см–1: 3620–2250 ш, 2129, 2073, 1629, 1605, 1566, 1542, 1343, 1271, 1137, 1093, 1057, 1000, 958, 881, 812, 661, 589, 553, 476. Найдено (%): C 17,93; H 5,73; N 6,77. С 6 H 24 N 2 O 11 P 2 Mn. Вычислено (%): C 17,28; H 5,80; N 6,72.
Растворимость 20 г в 100 мл Н 2 О.
Реакция сернокислого марганца(II) с тетракис (моноэтаноламиниевой) солью ОЭДФ. К раствору 5,00 г MnSO 4 ·5H 2 O (2,07·10–2 моль) в 20 мл Н 2 О прибавляли по каплям раствор (H 3 NCH 2 CH 2 OH) 4 L, полученный из 4,65 г (2,07·10–2 моль) ОЭДФ и 5.07 г (8,30·10–2 моль) моно-этаноламина. Выпадающий осадок по мере прибавления раствора (H 3 NCH 2 CH 2 OH) 4 L постепенно растворился. Смесь перемешивали 2 ч, фильтровали, упаривали, остаток сушили при 110 °С. Получили 10,8 г желто-розовой гигроскопичной твердой массы, которую нагревали в вакууме до 250 °С. Получили 9,35 г (H 3 NCH 2 CH 2 OH) 2 H 2 MnLSO 4 (1,95·10–2 моль, 94 %) в виде твердого слабо гигроскопичного аморфного продукта, подвергающегося размолу до желтого порошка. ИК-спектр, ν, см–1: 3600–2200 ш., 1620, 1516, 1501, 1462, 1379, 1349, 1260, 1140 пл., 1066, 1006 пл., 932 пл., 821, 762, 723, 661, 610, 553. РФА: аморфное гало в интервале углов отражения 2Ɵ 15–34о. Найдено (%): C 15,71, H 4,99, N 6,01, S 7,06. С 6 H 22 N 2 O 13 P 2 SMn. Вычислено (%): C 15,04; H 4,63; N 5,85; S 6,69.
Реакция сернокислого марганца(II) с ОЭДФ и моноэтаноламином. К раствору 5,00 г MnSO 4 ·5H 2 O (2,07·10–2 моль) в 20 мл Н 2 О прибавляли раствор 4,65 г (2,07·10–2 моль) ОЭДФ в 20 мл Н2О. Через 1 ч к прозрачному раствору прибавляли по каплям при перемешивании 5,07 г (8,30·10–2 моль) моноэтаноламина в 10 мл Н2О. После приливания 10 мл раствора наблюдали выпадение осадка, который быстро растворился в результате добавления всего объема (14,5 мл) раствора моноэтаноламина. Прозрачный раствор упарили, остаток нагревали в вакууме до 150 °С. Получили 9,20 г (1,92·10–2 моль, 93 %) (H 3 NCH 2 CH 2 OH) 2 H 2 MnLSO 4 в виде белых крупных трудно измельчающихся кусков. Найдено (%): C 15,04, H 5,09, N 6,06, S 7,04. С 6 H 22 N 2 O 13 P 2 SMn. Вычислено (%): C 15,04; H 4,63; N 5,85; S 6,69. Через 12 ч масса порошкообразного соединения увеличилась на 10 % за счет поглощения влаги воздуха. Смешивание с водой привело к образованию белого нефильтрующегося золя и осадка, что свидетельствовало о потере растворимости полученного продукта.
Бис (моноэтаноламиний)сульфат (H 3 NCH 2 CH 2 OH) 2 SO 4 . К раствору 5,11 г (8.36·10–2 моль) моноэтаноламина в 30 мл Н2О прибавляли по каплям 5,10 мл раствора 8,20 моль·л–1 H2SO4 (4,18·10–2 моль). Реакционная смесь самопроизвольно нагревалась, оставалась прозрачной. После упаривания при 110 °С получили 9,35 г прозрачной вязкой жидкости, которую нагревали в вакууме до 120 °С. Получили 7,50 г (3,40·10–2 моль, 82 %) бис (моноэтаноламиний)сульфата (H 3 NCH 2 CH 2 OH) 2 SO 4 в виде прочной стекловидной массы, внутри которой через 2 ч появились пучки белых нитей. Раздробленное до порошка соединение покрывалось жидкой пленкой, промывание ацетоном и удаление растворителя в вакууме приводило к получению «сухого» пересыпающегося порошка. ИК-спектр, ν, см–1: 3600 – 2200 ш, 2076, 1629, 1525, 1459, 1376, 1337, 1271, 1218, 1143, 1110, 1069, 1015, 976, 866, 836, 792, 711, 619, 580, 518, 473. Найдено (%): C 21,41; H 7,83; N 12,41; S 13,95. С 4 H 16 N 2 O 6 S. Вычислено (%): C 21,81, H 7,32, N 12,72, S 14,56.
Реакция сернокислого марганца(II) с тетрааммониевой солью ОЭДФ. К раствору 5,00 г MnSO 4 ·5H 2 O (2,07·10–2 моль) в 20 мл Н 2 О прибавляли по каплям раствор (NH 4 ) 4 L, полученный из 4,65 г (2,07·10–2 моль) ОЭДФ и 8,00 мл раствора аммиака 10,37 моль·л–1 (8,30·10–2 моль). Через 48 ч выпавший мелкодисперсный осадок не отстоялся. Мутную смесь фильтровали, осадок промывали водой, сушили при 110 °С. Получили 5,35 г (6,56∙10–3 моль, 95 %) продукта состава 2(NH 4 )НMnL· H 2 MnL в виде белого порошка. ИК-спектр, ν, см–1: 3229, 2046, 1644, 1459, 1429, 1376, 1104, 1069, 1000 пл., 956, 926 пл., 818, 723, 661, 562, 482. Найдено (%): C 8,20; H 3,46; N 3,73. С 6 H 28 N 2 O 21 P 6 Mn 3 . Вычислено (%): C 8,84, H 3,46; N 3,44.
ИК-спектры соединений в виде суспензии в вазелиновом (область 1400–400 см–1) и фторированном (4000–1400 см–1) маслах между пластинами KBr регистрировали на ИК Фурье-спектрометре ФСМ 1201.
Рентгенографические исследования выполнены на рентгеновском дифрактометре Shimadzu XRD-7000. Анализ проводился с использованием программы DIFFRACplus Evaluation package Release 2009, Bruker (Германия).
Элементный анализ выполнен на автоматическом элементном анализаторе Vario EL cube (Elementar Analysensysteme GmbH) в конфигурации CHNS, газ-носитель – гелий марки 6.0.
Термический анализ выполнен на приборе синхронного термического анализа TGA/DSC 3+ METTLER TOLEDO, скорость нагрева составляла 5 град/мин, скорость подачи аргона – 20 мл/мин.
Обсуждение результатов
Из выпускаемых в промышленных масштабах неорганических солей марганца для целей сельского хозяйства [21] наилучшим образом подходят сульфат и нитрат. Товарная форма микроудобрений, поставляемых на рынок, представляет собой близкие к насыщенным растворы солей биометаллов. Альтернативная форма – быстрорастворимые порошки или гранулы. В связи с этим испытания на растворимость сухих продуктов синтеза комплексонатов представляется актуальной проблемой. Обезвоживание может приводить к получению координационных полимеров и потери растворимости. Самым доступным и дешевым промотором растворимости является моно-этаноламин (МЭА), выпускаемый химической промышленностью РФ в больших количествах.
Испытание карбоната марганца, полученного осаждением кислым углекислым калием из раствора MnSO 4 , в целом подтвердило его высокую реакционную способность. Взаимодействие с ОЭДФ протекало без нагревания, приводило к быстрому растворению суспензии карбоната марганца и последующему выпадению (через 30–40 мин) обильного осадка (1-гидроксиэтилиден)дифосфоната марганца H2MnL. Приливание вслед затем к вязкой суспензии водного раствора моноэтаноламина вызывало ее растворение, однако оно было не полным.
MnCO 3 + H 4 L = H 2 MnL + CO 2 + H 2 O (1)
H 2 MnL + 2 H 2 NCH 2 CH 2 OH = (H 3 NCH 2 CH 2 OH) 2 MnL (2)
Реакционная смесь оставалась мутной, хотя количество осадка было минимальным. Причина наблюдаемого несоответствия ожидаемым результатам заключалась в понижении реакционной способности моноэтаноламина вследствие поглощения им углекислого газа, выделившегося в реакции карбоната марганца с ОЭДФ. Проверка методом кислотно-основного титрования водного раствора, полученного в результате фильтрования осадка H 2 MnL, показала, что в фильтрате остается растворенной более 4 % угольной кислоты относительно количества взятого в реакцию КНСО3. Известно [22], что моноэтаноламин является наилучшим реагентом для абсорбции углекислоты из топочных газов.
HOCH 2 CH 2 NH 2 + CO 2 = HOCH 2 CH 2 NHCOOH (3)
HOCH 2 CH 2 NHCOOH + H 2 NCH 2 CH 2 OH = HOCH 2 CH 2 NHCOO‒+NH 3 CH 2 CH 2 OH (4)
Понижение его реакционной способности в результате образования комплекса с углекислотой подтвердилось проведением реакции чистого (не свежевыделенного) H 2 MnL с МЭА и с его комплексом с СО 2 . Суспензия H 2 MnL растворялась под действием водного раствора чистого МЭА через 10 мин, а под действием раствора МЭА, насыщенного углекислым газом, только через 60 мин. Нагревание и перемешивание реакционной смеси, полученной при взаимодействии карбоната марганца с ОЭДФ, в течение 1 ч вызывало удаление углекислого газа, вследствие чего последующее прибавление водного раствора МЭА приводило к образованию прозрачного раствора бис (моноэтаноламиний) (1-гидроксиэтилиден)дифосфоната марганца(II) (H 3 NCH 2 CH 2 OH) 2 MnL. Ингибирование реакции моноэтаноламином таким образом было исключено. Упаривание раствора и сушка остатка привели к получению целевого соединения с выходом 96 %. Оно содержало 2 молекулы воды и представляло собой массу кремового цвета, размалывающуюся до желтого порошка с растворимостью 20 г в 100 мл Н 2 О, что допускает возможность использования хелатированного соединения в качестве микроудобрения в порошкообразном виде. Устойчивые при длительном хранении водные растворы высоких концентраций обычно образуют аморфные производные биометаллов. На рис. 1 показаны рентгенограммы исходного карбоната марганца (родохрозита, кривая 1 ), продукта его реакции с ОЭДФ (H 2 MnL·3Н 2 О, кривая 2 ) и (H 3 NCH 2 CH 2 OH) 2 MnL·2Н 2 О (кривая 3 ). Конечный продукт представляет собой глубоко аморфизованное соединение, чем и объясняется его хорошая растворимость в водной среде.
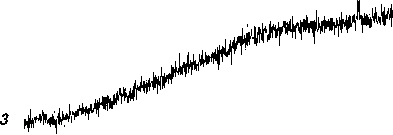
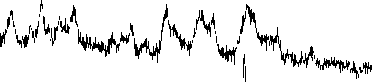
o
15 20 25 30 35 40 2 ® ,
Рис. 1. Рентгенограммы MnCO 3 ( 1 ), H 2 MnL · 3Н 2 О ( 2 ) и (H 3 NCH 2 CH 2 OH) 2 MnL · 2Н 2 О ( 3 )
Реакция сульфата марганца(II) с тетракис(моноэтаноламиниевой) солью ОЭДФ (реакция (5)) привела к образованию бис (моноэтаноламиний) (1-гидроксиэтилиден)дифосфоната марганца(II) и бис (моноэтаноламиний) сульфата. Прибавление раствора моноэтаноламиниевой соли ОЭДФ к раствору сульфата марганца вызывало выпадение белого хлопьевидного осадка, который постепенно растворялся.
MnSO 4 + (H 3 NCH 2 CH 2 OH) 4 L = (H 3 NCH 2 CH 2 OH) 2 MnL + (H 3 NCH 2 CH 2 OH) 2 SO 4 (5)
Разделение этой смеси не являлось необходимым в случае использования ее в сельскохозяйственных мероприятиях. Получающийся прозрачный розовый раствор при хранении осадка не выделял. Упаривание приводило к застудневанию смеси. После сушки при 110 °С получалась светлая желто-розовая твердая масса, по консистенции подобная гудрону и не подвергающаяся размолу до порошка. Нагревание ее в вакууме до 250 °С привело к окончательному отверждению, убыли 7 % массы и потере растворимости. Согласно элементному анализу формула получившегося продукта может быть представлена как (H 3 NCH 2 CH 2 OH) 2 H 2 MnLSO 4 . Она отличалась от ожидаемой (H3NCH2CH2OH)4MnLSO4 на два фрагмента моноэтаноламина предположительно потерянного в результате термообработки. Однако в другом аналогичном эксперименте сухой остаток не подвергался столь интенсивной обработке, но имел такую же брутто формулу. Из этого следовало, что во время упаривания в концентрированном растворе происходило накопление кислых моноэтаноламиниевых солей (H 3 NCH 2 CH 2 OH)HMnL и (H 3 NCH 2 CH 2 OH)HSO 4 . «Лишний» моноэтаноламин удалялся во время упаривания и сушки. Такой состав явился причиной потери растворимости сухого остатка в водной среде.
Изменение порядка смешивания реагентов, т. е. прибавление раствора сульфата марганца к раствору тетрааминиевой соли ОЭДФ, привело к аналогичному результату. Выпадение белого осадка замедляло процесс синтеза. Быстрое приливание второго компонента вызывало образование вязкой суспензии, затрудняющей эффективное перемешивание. Осадок представлял собой труднорастворимый (1-гидроксиэтилиден)дифосфонат марганца(II) H 2 MnL. Растворимость сухого H 2 MnL·2Н 2 О составляла только 0,94 г в 100 мл Н 2 О.
Наилучшие условия получения смеси (H 3 NCH 2 CH 2 OH) 2 MnL/(H 3 NCH 2 CH 2 OH) 2 SO 4 создавались, когда к сульфату марганца и ОЭДФ прибавляли МЭА. Раствор, содержащий эквимолярные количества MnSO 4 и H 4 L, не генерировал выпадения осадка H 2 MnL в кислой среде. Моноэтано-ламин вызывал появление осадка только после прибавления двух третей от исходного количества. Смесь легко перемешивалась на всем протяжении реакции, осадок быстро растворялся.
Бис (моноэтаноламиний) (1-гидроксиэтилиден)дифосфонат марганца(II) (H 3 NCH 2 CH 2 OH) 2 MnL·2Н 2 О представляет собой негигроскопичное соединение, легко размалывающееся до светло-розового порошка. Визуально наблюдаемое его отличие от полученного в реакции (5) продукта обусловлено присутствием бис (моноэтаноламиний)сульфата
(H 3 NCH 2 CH 2 OH) 2 SO 4 . Синтезированный из моноэтаноламина и серной кислоты, он представлял собой бесцветную стекловидную чрезвычайно гигроскопичную массу, покрывающуюся влажной пленкой вследствие поглощения атмосферной влаги.
2 H 2 NCH 2 CH 2 OH + H 2 SO 4 = (H 3 NCH 2 CH 2 OH) 2 SO 4 (6)
Соединение подвергали размолу до крупнозернистого порошка, влажную пленку смывали ацетоном, полученный сухой порошок хранили в запаянной трубке или под плотной пробкой.
Существенную разницу в протекании вышеописанных реакций можно объяснить следующим образом. В водном растворе имеет место равновесие тетракис(моноэтаноламиниевой) соли
ОЭДФ согласно уравнениям (7)–(10).
(H3NCH2CH2OH)H3L = (H3NCH2CH2OH)+ + H3L–(7)
(H3NCH2CH2OH)2H2L = 2 (H3NCH2CH2OH)+ + H2L2–(8)
(H3NCH2CH2OH)3HL = 3 (H3NCH2CH2OH)+ + HL3–(9)
(H3NCH2CH2OH)4L = 4 (H3NCH2CH2OH)+ + L4–(10)
Прибавление к этому раствору сульфата марганца вызывало быстрое выпадение труднорастворимого H2MnL из-за высокой концентрации H2L2–. Иная ситуация складывалась, когда к раствору MnSO 4 + H 4 L прибавляли моноэтаноламин. Равновесие реакции
MnSO 4 + H 4 L = H 2 MnL + H 2 SO 4
сдвинуто влево, вследствие чего осадок H2MnL не выпадал. В растворе присутствовали Mn2+, SO 4 2‒, H+, H 3 L‒, H 2 L2‒. Добавленный H 2 NCH 2 CH 2 OH быстро взаимодействовал с катионами H+, давая моноэтаноламиниевую соль (H 3 NCH 2 CH 2 OH)+. Последняя реагировала прежде всего с анионами SO 4 2‒, H 3 L‒, H 2 L2‒.
2 (H 3 NCH 2 CH 2 OH)+ + SO 4 2‒ = (H 3 NCH 2 CH 2 OH) 2 SO 4
(H 3 NCH 2 CH 2 OH)+ + H 3 L‒ = (H 3 NCH 2 CH 2 OH)H 3 L
2 (H 3 NCH 2 CH 2 OH)+ + H 2 L2‒ = (H 3 NCH 2 CH 2 OH) 2 H 2 L
Осадок труднорастворимого H 2 MnL получался в результате конкурирующей реакции
Mn2+ + H2L2‒ = H2MnL в условиях небольшой концентрации дианиона H2L2‒ и превращался в растворимый (H3NCH2CH2OH)2MnL по реакции 2.
Сделанная попытка использовать вместо моноэтаноламина водный раствор аммиака не привела к успеху. В реакции сульфата марганца(II) с тетрааммониевой солью ОЭДФ был получен труднорастворимый продукт состава 2(NH 4 )HMnL·H 2 MnL.
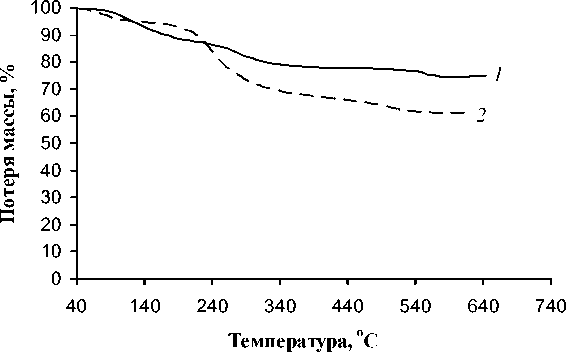
Устойчивость на воздухе порошкообразных препаратов, предназначенных для использования в качестве микрокомпонентных добавок в минеральные удобрения, представляется необходимым качеством, обеспечивающим долговременное хранение без потери растворимости. Дигидрат бис (моноэтаноламиний)(1-гидроксиэтилиден)дифосфоната марганца (H 3 NCH 2 CH 2 OH) 2 MnL·2Н 2 О при хранении в течение 1 года сохранил способность растворяться в воде. Данные термогравиметрического анализа (рис. 2) свидетельствуют о несколько меньшей его термической устойчивости по сравнению с исходным тригидратом (1-гидроксиэтилиден)дифосфоната марганца(II) H2MnL·3Н2О, что обусловлено существенно большей органической составляющей в структуре молекулы. При нагревании до 640 °С соединения теряют соответственно 25 и 37 % от первоначальной массы. У первого из них наиболее интенсивные потери протекают при 118, 178, 276 и 553 °С, у второго при 82, 241 и 499 °С. Низкотемпературные пики на кривых дифференциальной термогравиметрии (ДТГ) (118 и 82 °С) следует отнести на потери молекул воды. В кристаллическом соединении H 2 MnL·3Н 2 О кристаллогидратная вода удерживается более прочно, чем в аморфном (H 3 NCH 2 CH 2 OH) 2 MnL·2Н 2 О.
а)
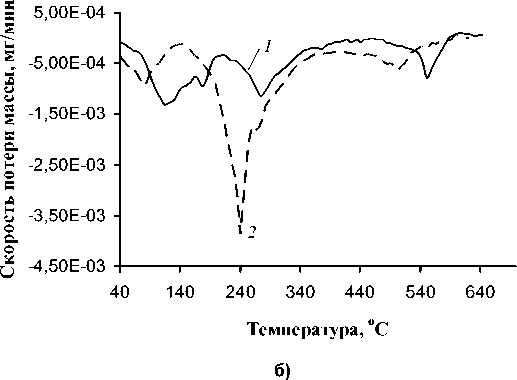
Рис. 2. Термический анализ (1-гидроксиэтилиден)дифосфоната марганца(II) тригидрата H 2 MnL · 3Н 2 О ( 1 ) и бис (моноэтаноламиний) (1-гидроксиэтилиден)дифосфоната марганца(II) дигидрата (H 3 NCH 2 CH 2 OH) 2 MnL · 2Н 2 О ( 2 ): а – ТГА, б – ДТГ
Выводы
Бис (моноэтаноламиний) (1-гидроксиэтилиден)дифосфонат марганца(II)
(H 3 NCH 2 CH 2 OH) 2 MnL·2Н 2 О, полученный в сухом виде из карбоната марганца, (1-гидроксиэтилиден)дифосфоновой кислоты и моноэтаноламина, показал высокую растворимость в водной среде (20 г в 100 мл Н 2 О), что позволяет использовать его в качестве микроком-понентной добавки в удобрения.
Смесь (1-гидроксиэтилиден)дифосфоната марганца(II) (H3NCH2CH2OH)2MnL с бис(моноэтаноламиний)сульфатом (H3NCH2CH2OH)2SO4, синтезированная из тет- ра(моноэтаноламиниевой) соли (1-гидроксиэтилиден)дифосфоновой кислоты (H3NCH2CH2OH)4L и сернокислого марганца(II), образует устойчивый водный раствор, однако после выделения в сухом виде теряет растворимость.


