Полуэмпирические исследования механизмов краевого модифицирования углеродных нанотруб функциональными группами
Автор: Шляхова А.А., Прокофьева Е.В.
Рубрика: Физико-математические науки
Статья в выпуске: 6, 2007 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/14967638
IDR: 14967638
Текст обзорной статьи Полуэмпирические исследования механизмов краевого модифицирования углеродных нанотруб функциональными группами
-
1. ИССЛЕДОВАНИЯ ЭЛЕКТРОННО-ЭНЕРГЕТИЧЕСКОГО СТРОЕНИЯ УГЛЕРОДНЫХ НАНОТРУБ С КРАЕВЫМИ ГРУППАМИ
-
2. МЕХАНИЗМЫ ФУНКЦИОНАЛИЗАЦИИ УГЛЕРОДНЫХ НАНОТРУБ
Краевые электронные состояния играют большую роль в понимании явлений, происходящих на поверхности твердого тела. Они определяют особенности структуры и некоторые физико-химические свойства. Поэтому представляет интерес рассмотреть полубеско-нечные углеродные тубулены, в которых все атомы системы расположены на одной и той же цилиндрической поверхности, а свободные валентности замыкаются различными функциональными группами. Возможность замыкания открытого конца тубулена гетероатомами и функциональными группами открывает перспективы получения новых соединений на основе углеродных нанотрубок.
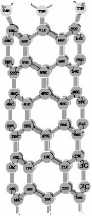
Расчеты углеродных тубуленов с краевыми функциональными группами 1 выполнены для нанотрубок ( n , 0) и ( n , n ) типов в рамках модели молекулярного кластера (МК) с использованием полуэмпирической расчетной схемы MNDO. В качестве псевдоатомов, замыкающих одну границу тубулена, использовались атомы водорода, а другой конец: 1) замыкался атомами кислорода, которые либо замещали углерод в вершинах граничных гексагонов (рис. 1 а), либо образовывали мостиковые структуры между соседними вершинами (рис. 1 б); 2) замыкался гидроксильными группами ОН (рис. 1 в); 3) замыкался аминогруппами NH2 (рис. 1 г). Расстояния между ближайшими атомами углерода принимались равными 1,4 Å, а геометрия атомов функциональных групп оптимизировалась.
Основные энергетические характеристики нанотрубки с шестью краевыми атомами кислорода приведены в таблице 1. Анализ электрон- но-энергетического строения данной структуры установил, что атомы О дают вклад в валентную зону [2р-атомные орбитали (АО) кислорода] и не дают вклад в граничные уровни зон (валентной и проводимости). Зона проводимости (ЗП), дно зоны проводимости и потолок валентной зоны (ВЗ) выполнены 2s- и 2р-АО углерода. В случае замыкания открытого конца нанотрубки атомами кислорода заряды на атомах О, расположенных на расстояниях 1,41 Å и 1,39 Å от атомов углерода тубулена (С–О-связь), равны -0,18, а граничащих с ними атомах С – +0,14. То есть имеет место перенос электронной плотности с атомов углерода трубки на атомы кислорода. Углы наклона атомов О к оси трубки незначительны (~ 4– 5°). Анализ зарядового перераспределения показал, что возмущение поверхности нанотрубки, вызванное краевыми атомами О, затухает до нулевых зарядов уже через один слой углеродных гексагонов.
В случае замыкания открытой границы трубки (6, 0) тремя атомами кислорода длины связи С–О оказываются равными 1,82 Å. Краевые группы наклонены к центру трубки на угол порядка 13°. Заряды на атомах О равны -0,2, а на соседних атомах С – +0,16. То есть также имеет место перенос электронной плотности с поверхности тубулена на атомы О. Возмущение поверхности нанотрубки полностью затухает через один слой углеродных гексагонов. Основные энергетические характеристики системы приведены в таблице 1. Выяснено, что дно ЗП и потолок ВЗ выполнены 2р-АО атомов С тубулена, а краевые атомы О дают вклад в валентную зону (2р-АО кислорода).
Выявлены особенности геометрической структуры тубулена (6, 0), открытая граница которого замыкается шестью гидроксильными группами (рис. 1 в). Длины связей С–О оказались равными 1,34 Å, О–Н – 0,95 Å. Атомы во- дорода гидроксильной группы отклоняются от оси трубки на углы 111°, 112° и 113°. На атомах О концентрируется заряд -0,22, а на соседних атомах водорода – заряд 0,21. Основные энергетические характеристики системы также приведены в таблице 1. Обнаружен вклад 2р-АО атомов водорода гидроксильной группы в потолок валентной зоны 2. Дно зоны проводимости выполнено из 2р- и 2s-АО атомов углерода трубки, s-АО атомов водорода гидроксильных групп дают вклад в валентную зону.
Для нанотрубки, модифицированной тремя аминогруппами (NH2) (рис. 1 г), установлены следующие параметры и закономерности: длины связей rC-N = 1,36 Å, rN-H = 1Å; краевые группы наклонены к оси трубки на угол 23°.
Были исследованы механизмы присоединения функциональных групп О, ОН и NH2 к открытой границе полубесконечной нанотрубки (6, 0) (рис. 2 а, б, в, г). Рассмотрены два варианта образования мостиковой структуры атомом кислорода на границе нанотрубки: в первом варианте между соседними атомами С, во втором – на оборванных связях атомов углерода (рис. 2 а, б).
Пошаговое приближение функциональных групп к открытым границам тубуленов позволило построить профили поверхности потенциальной энергии систем «нанотрубка – кислород», «нанотрубка – гидроксильная группа» и «нанотрубка – аминогруппа» (зависимость энергии от расстояния RC-O, RC-OH, RC-NH2 функциональных групп до атома углерода поверхности). На рис. 3 и 4, нормированных на энергию системы на бесконечном расстоянии, хорошо прослеживается наличие энергетического минимума (см. табл. 2). Эти точки минимума являются результатом образования химической связи между функциональной группой и атомом углерода поверхности трубки с обменом электронной плотностью между ними 3. Величина энергии имеет смысл энергии химической связи. Кроме того, анализ кривой присоединения функциональных групп к открытой границе тубулена (6, 0) обнаружил безба-рьерный характер присоединения.

а)
-
• • •
v^^v
II II II
^>-^А
-
I II II I
V”^v
ID II ID
.^A^A
^-V5^
• M .6
-
б)

в)
г)
Рис. 1. Тубулен (6, 0) с краевыми группами:
-
а) атомы О замещают атомы С; б) атомы О образуют мостиковые структуры;
-
в) замыкание гидроксильными группами; г) замыкание аминогруппами
Таблица 1
Основные энергетические характеристики углеродных нанотрубок, модифицированных функциональными группами *
|
Тип тубулена |
Функциональная группа |
E v , эВ |
Е с , эВ |
∆ E g , эВ |
|
(6, 0) |
6 ⋅ О |
-7,02 |
-3,72 |
3,3 |
|
(6, 0) |
3 ⋅ О |
-6,75 |
-3,91 |
2,84 |
|
(6, 0) |
6 ⋅ (ОН) |
-5,21 |
-3,25 |
1,96 |
|
(6, 0) |
3 ⋅ (NH 2 ) |
-5,43 |
-3,4 |
1,75 |
* Ev – верхняя граница валентной зоны (потолок ВЗ); Ec – нижняя граница зоны проводимости (дно ЗП); ∆ Eg – ширина запрещенной зоны, определяемая как разность Ec – Ev и отвечающая за тип проводимости твердой структуры.
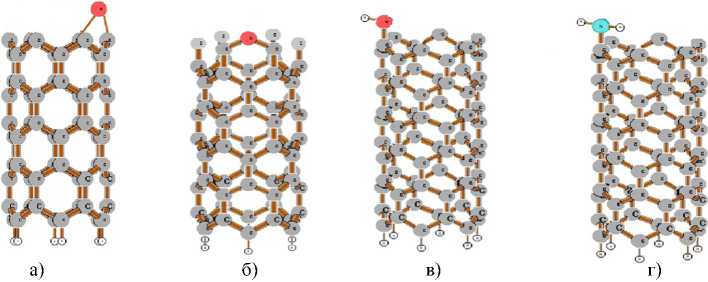
Рис. 2. Присоединение функциональных групп:
а) атом кислорода образовывает мостиковую структуру между соседними атомами углерода; б) атом кислорода образовывает мостиковую структуру на оборванных связях углерода; в) присоединение гидроксильной группы к граничному атому С; г) присоединение аминогруппы к граничному атому углерода
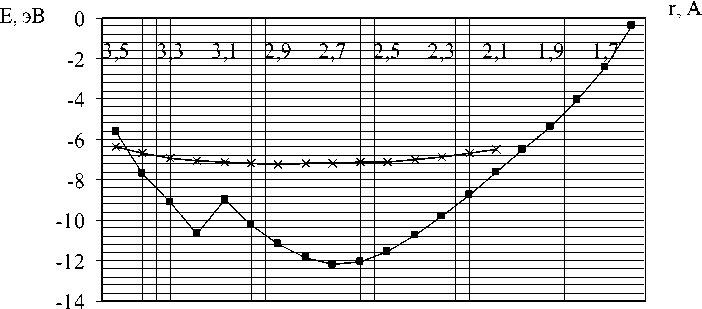
—■— О образ. мостик. стр-ру между сосед С
О образ. мостик. стр-ру на оборван. связях
Рис. 3. Профили поверхностей потенциальных энергий взаимодействия нанотрубки (6, 0) с функциональным атомом кислорода, образующим мостиковую структуру между соседними атомами углерода и на оборванных связях углерода
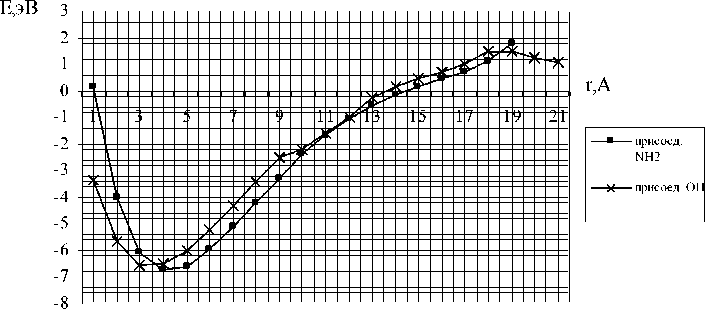
Рис. 4. Профили поверхностей потенциальных энергий взаимодействия нанотрубки (6, 0) с функциональной гидроксильной группой и функциональной аминогруппой
Таблица 2
Основные энергетические характеристики присоединения функциональных групп к открытому концу тубулена (6, 0)
|
Функциональная группа |
R св , Å |
Е св , эВ |
|
O (вариант I) |
1,8 |
-7,23 |
|
O (вариант II) |
2,7 |
-12,2 |
|
OH |
1,3 |
-6,75 |
|
NH 2 |
1,3 |
-6,57 |
ЗАКЛЮЧЕНИЕ
-
1. Анализ электронного строения полу-бесконечных тубуленов, замкнутых выбранными функциональными группами O, OH, и NH2, установил основные вклады атомных орбиталей модифицирующих атомов в зону проводимости и валентную зону получающихся систем.
-
2. Выявлены особенности геометрической структуры нанотрубок, модифицированных функциональными группами, проанализирован характер симметрии групп относительно оси тубулена.
-
3. Анализ зарядовых распределений установил наличие переноса электронной плотности с поверхности трубки на ближайшие атомы краевых функциональных групп во всех рассмотренных случаях.
-
4. Выполненные исследования механизмов присоединения функциональных групп к границе тубулена позволили определить энер-
- гии связи и доказали стабильность данных процессов и образующихся систем (отрицательные значения Есв) для всех выбранных типов краевых групп.
-
5. Анализ профилей поверхности потенциальных энергий краевых процессов установил безбарьерный характер присоединения всех выбранных функциональных групп к открытой границе полубесконечного тубулена.
Список литературы Полуэмпирические исследования механизмов краевого модифицирования углеродных нанотруб функциональными группами
- Zaporotskova I.V., Lebedev N.G., Zaporotskov P.A. Effects of boundary functional groups in single wall nanotubes: semi-empirical researches//Abs. «Fullerenes and Atomic clusters». 2005. June 27 -July 1. St.-Peterburg, 2005. P. 314.
- Ивановский А.Л. Квантовая химия в материаловедении. Нанотубулярные формы вещества. Екатеринбург: УрОРАН, 1999. 176 с.
- Харрис П. Углеродные нанотрубы и родственные структуры. Новые материалы XXI века. М.: Техносфера, 2003. 336 с.


