Постлучевой эпидуральный фиброз со стенозом позвоночного канала: особенности клиники, диагностики и лечения (клинический случай)
Автор: Скляренко О.В., Ларионов С.Н., Животенко А.П., Сороковиков В.А., Горбунов А.В., Потапов В.Э.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клинический случай
Статья в выпуске: 1 т.15, 2025 года.
Бесплатный доступ
Цель исследования: продемонстрировать особенности диагностики и лечения постлучевого эпидурального фиброза на примере клинического случая пациентки с прогрессирующим болевым синдромом после лучевой терапии.
Постлучевой фиброз d005355, d014157], эпидуральный фиброз [d005355, d013116], стеноз позвоночного канала [d013130], лучевая терапия [d011878], декомпрессивно-стабилизирующее вмешательство [d003627, ], спондилодез [d013123], осложнения лучевой терапии [d011832], патологический перелом [d050723], радикулопатия [d011843], нейровизуализация [d059906], транспедикулярная фиксация [d062326]
Короткий адрес: https://sciup.org/143184370
IDR: 143184370 | УДК: 616.832-007.271:615.849.1-06 | DOI: 10.20340/vmi-rvz.2025.1.CASE.5
Postradiative stenosis of the spinal canal: features of the clinic, diagnosis and treatment (clinical case)
Postradiation epidural fibrosis is one of the rare complications of cancer treatment in patients receiving radiation therapy, leads to a mosaic clinical picture, including manifestations of polyneuropathy, caudogenic intermittent lameness syndrome and can significantly affect the quality of life of patients. Depending on the type of cancer, the volume of the affected tissues and the level of damage to the spine, radiation fibrosis syndrome is characterized by a diverse clinical picture. The main clinical manifestations of post-radiation fibrosis of the spinal canal at the level of the lumbar spine are pain, numbness, paresthesia in the lower extremities. A thorough history and physical examination, combined with the use of neuroimaging data, help establish an accurate diagnosis and select an effective treatment. When studying the problem of post-radiation fibrosis, it is extremely difficult to predict the time, risk group and specificity of characteristic symptoms, given the development of pathology in elderly and senile patients, against the background of existing degenerative changes in the spine. However, there is a close relationship with dosage, anatomical impact, nature of damage and clinical symptoms. Conservative methods of treating post-radiation fibrosis with spinal canal stenosis include the use of analgesic, antiinflammatory therapy. With a prolonged course of pain syndrome, insufficient effectiveness of conservative treatment, local blockades or epidural injections are carried out. In the absence of the effect of conservative treatment, indications for surgical intervention arise.
Текст научной статьи Постлучевой эпидуральный фиброз со стенозом позвоночного канала: особенности клиники, диагностики и лечения (клинический случай)
По данным Международного агентства по изучению рака в период с 2012 по 2022 гг. число новых случаев онкозаболеваний во всём мире увеличилось на 50%, а смертность от рака возросла на 18%. По прогнозам, в течение следующих 30 лет заболеваемость продолжит расти, и к 2050 году число новых случаев увеличится на 77% [1, 2]. Одним из эффективных методов лечения рака является лучевая терапия, которая может проводиться как с лечебной, так и с паллиативной целью [3–5]. При лучевой терапии высокоэнергетические фотоны и протоны индуцируют повреждение ДНК раковых клеток. Несмотря на снижение токсичности излучения при применении современных установок для проведения радиотерапии, пациенты, получившие лучевую терапию, подвержены риску развития осложнений [6–8]. Так, например, постлучевой фиброз возникает вследствие некроза тканей с повреждением микрососудов и пролиферацией фибробластов. К основным фазам изменений в тканях, вызванных радиационным фиброзом, относится хроническое воспаление с индукцией секреции макрофагов и нейтрофилов, аномальной пролиферацией фибробластов и ремоделированием внеклеточного матрикса. Этот процесс усиливается различными секретируемыми цитокинами, такими как TNF-α, IL-1, фактор роста фибробластов и of the Medical Institute “REAVIZ”: Rehabilitation, Doctor and Health. эпидермальный фактор роста, так и их взаимодействиями. Важным звеном патогенеза является стимулирующее влияние TGF-β1, способствующее трансформации фибробластов [9–11].
К ранним проявлениям последствий лучевой терапии относятся изменения кожи, потеря волосяного покрова, различные алгические синдромы. К поздним эффектам – скованность, нарушение чувствительности и слабость мышц, контрактуры, сопровождающиеся выраженным болевым синдромом, [12, 13]. Клиническая картина постлучевого фиброза варьируется в зависимости от локализации и дозы облучения, а также тяжести поражения анатомических структур. Болевой синдром при постлучевом фиброзе полиморфен и возникает вследствие повреждения периферических рецепторов и нервов, нервных корешков, сплетений, головного и спинного мозга. В случае повреждения сенсорной нервной системы или повреждения нисходящих модулирующих путей преобладает нейропатический компонент боли, особенностью которого является несоответствие локализации патологического очага зонам иннервации [14]. Постлучевой фиброз с вовлечением в патологический процесс корешков спинного мозга и периферических нервов характеризуется алгиче-скими формами поли- и невропатии, перифериче- скими парезами с нарушением чувствительности, дистальными амиотрофиями. Вовлечение в патологический процесс вегетативной нервной системы приводит к нарушению функции тазовых органов [15].
Тщательный сбор анамнеза, дозы и типа излучения, клинический осмотр, оценка характера боли, времени появления и прогрессирования симптомов, использование данных интроскопических исследований, таких как МРТ и МСКТ, позволяет установить правильный диагноз и подобрать наиболее эффективную тактику лечения.
Клинический случай
Пациенка Л., 1959 г.р., направлена в нейрохирургическое отделение Иркутского научного центра хирургии и травматологии (ИНЦХТ) 15.08.2024 г. для проведения декомпрессивно-стабилизирующего вмешательства.
При первичном осмотре и сборе анамнеза пациентка предъявляла следующие жалобы: болевой синдром, локализующийся в нижних конечностях, сопровождающийся преходящей мышечной слабостью, возникающей при физической активности, а именно при ходьбе на расстояние 30 метров, что заставляло её присаживаться и наклоняться вперед, после чего пациентка отмечала облегчение; отмечала случаи падения при быстрой ходьбе через пешеходные переходы в связи со слабостью мышц нижних конечностей; парестезии (чувство онемения и покалывания) в области передней поверхности голеней, а также тыльной поверхности обеих стоп чаще усиливающиеся в ночное время, больше выраженные проявления отмечает в левой ноге.
Как следует из собранного анамнеза, первые признаки заболевания проявились примерно за год до госпитализации, когда пациентку стали беспокоить боли в нижних конечностях, что привело к изменениям в походке. Отмечается неуклонное прогрессирование симптоматики. В течение трёх месяцев, предшествовавших обращению в ИНЦХТ, пациентка получала консервативную терапию под наблюдением невролога и ревматолога по месту жительства, однако без существенного улучшения состояния. В январе 2024 года был проведён курс из шести эпидуральных инъекций по методике Катлена с использованием препарата Кеналог, однако, несмотря на предпринятые меры, положительной динамики в состоянии больной отмечено не было. После этого она продолжила получать симптоматическое лечение под наблюдением участкового невролога. В связи с отсутствием положительной динамики на проводимую терапию в январе 2024 года пациентка приняла решение обратиться за консультацией к врачу-нейрохирургу в консультативно-диагностическую поликлинику ИНЦХТ, где для определения дальнейшей тактики лечения ей было рекомендовано пройти комплекс нейровизуализационных исследований, направленных на изучение состояния поясничного отдела позвоночника.
Анамнез жизни: росла и развивалась соответственно возрасту.
Перенесённые заболевания: гепатит В (2022 г); артериальная гипертензия, принимает престариум 10 мг/сут; бисопролол 2,5 мг, по 1 табл. утром.
Перенесенные операции: 2006 г. – экстирпация матки с придатками по поводу рака с последующей дистанционной лучевой терапией, проводившейся ежедневно с понедельника по пятницу в течение пяти недель, начиная с первого дня недели. Разовая доза составляла 2,0 Гр, суммарная доза за курс 60 Гр.
Объективный осмотр. Общее состояние оценивается как удовлетворительное. Пациентка способна самостоятельно передвигаться без использования дополнительных средств опоры, однако бережёт правую нижнюю конечность, отмечается хромота. При аускультации и пальпации внутренних органов значимых отклонений от нормы не обнаружено.
Локальный статус. При визуальном осмотре поясничного отдела позвоночника наблюдается уменьшение выраженности поясничного лордоза. Активные движения в поясничном отделе значительно затруднены. При пальпации отмечается болезненность остистых отростков и прилегающих к позвоночнику областей в проекции сегментов L IV -L V и L V -S I . Болевые ощущения иррадиируют по задней поверхности правого бедра. Болевой синдром усиливается при смене положения тела и вертикальной нагрузке на позвоночник. При пальпации выявляется повышенный тонус паравертебральных мышц.
Неврологический статус. Признаков дисфункции черепно-мозговых нервов не выявлено. Сухожильные рефлексы с рук D = S, живые, коленные D = S, живые, ахилловые S снижен, D живой. Слабость мышц-разгибателей левой стопы 3 балла. Дистальная гипотрофия мышц обеих нижних конечностей. Мышечная гипотония, более выраженная слева. Выявлен положительный симптом натяжения Ласега с углом 40° слева. Мозаичный тип нарушений чувствительности по передней и наружной поверхности обеих бедер и голеней, преимущественно слева. Интенсивность боли, измеренная с помощью визуально-аналоговой шкалы (ВАШ), соответствовала 7 баллам.
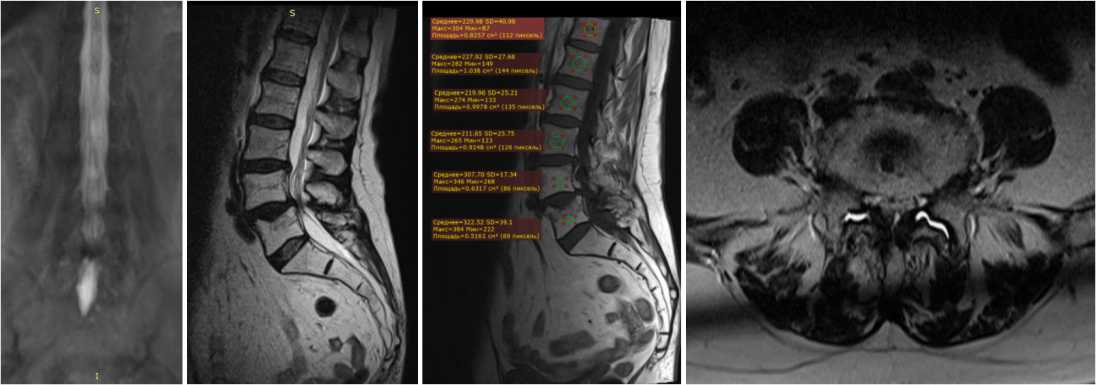
МРТ поясничного отдела позвоночника (15.06.2024): выявлена совокупность дегенеративных и дистрофических изменений в поясничном отделе позвоночника, включающая деформирующий спондилез и спондилоартроз на уровне L IV -L V IV степени по A. Fujiwara, приводящий к критическому сужение позвоночного канала класса D по Schizas C. [16]. Антесподилолистез L IV I ст. Протрузии дисков L III -L IV , L IV -L V . Застарелый консолидированный компрессионный перелом L V (рис. 1).
А Б В Г
Рисунок 1. Магнитно-резонансная томография поясничного отдела позвоночника: А. МРТ миелографии фронтальная проекция с дефектом наполнения дурального мешка на уровне L IV -L V . Б. Т 2 -взвешенное изображение с гетерогенной структурой тел позвонков в сагиттальной проекции с признаками консолидированного перелома тела L V (деформация тела L V позвонка). В. Т 1 -взвешенное изображение в сагиттальной проекции с указание ROI на уровне тел позвонков аномальный сигнал костного мозга с повышенной интенсивностью в телах L IV и L V тел позвонков. Г. Т 2 -взвешенном изображении в аксиальной плоскости определяется гиперинтенсивный сигнал в области суставной щели гипертрофированных дугоотростчатых суставов на уровне L IV -L V , что указывает на реактивный отек фасеточных пространств Figure 1. Magnetic resonance imaging of the lumbar spine: A. MRI myelography frontal projection with a filling defect of the dural sac at the L IV -L V level. Б. T 2 -weighted image with a heterogeneous structure of the vertebral bodies in the sagittal projection with signs of a consolidated fracture of the L V body (deformation of the L V vertebral body). В. Sagittal T 1 -weighted image with region of interest (ROI) at the vertebral body level revealed abnormal bone marrow signal with increased intensity in the L IV and L V vertebral bodies. Г. T 2 -weighted axial imaging reveals a hyperintense signal in the area of the joint space of the hypertrophied facet joints at the L IV -L V level, indicating reactive edema of the facet spaces
Диагноз клинический
Комбинированный абсолютный стеноз позвоночного канала на уровне L IV -L V класса D по Schizas C., обусловленный постлучевым эпидуральным фиброзом и деформирующим спондилоартроз IV степени по A. Fujiwara. Спондилез. Антеспондилолистез L IV I степени. Протрузии дисков L III -L IV , L IV -L V . Синдром ка-удогенной перемежающейся хромоты. Радикулопатия L 5 , S 1 слева с парезом стопы. Затянувшийся умеренно выраженный болевой и мышечно-тонический синдромы (МКБ 10–М48.0).
Лабораторная диагностика
Общий анализ крови: эр. 4,7×1012 г/л; гем. 142 г/л; лейк. 7,1×109/л; п. 2, с. 52, э. 2, б. 1, м. 6, л. 35, СОЭ 14 мм/ч.
Биохимический анализ крови: глюкоза 4,9 ммоль/л; общий белок 69,7 г/л; бил. общий 7,4 мкмоль/л; прямой билирубин 2,3 мкмоль/л; непрямой билирубин 7 мкмоль/л; ХС 5,7 ммоль/л; АЛТ 31,1; АСТ 20,9; мочевина 6,2 ммоль/л; креатинин 68 мкмоль/л; СРБ 4,1 мг/л .
ОАМ: цвет с/ж; уд. вес 1023; б – нет , сахар – отр., эпит. 0–1 в п/зр, лейк. 2–3 в п/зр.
После клинического разбора и обсуждения с учётом данных дополнительных исследований пациентке рекомендовано оперативное лечение.
Хирургическое вмешательство
После антисептической обработки операционной зоны, под эндотрахеальным наркозом, в положении пациента лёжа на животе (нижние конечности обернуты эластичными бинтами для предотвращения тромбоэмболии лёгочной артерии) выполнен линейный разрез кожи и подкожно-жировой клетчатки по центру спины в области остистых отростков LIII-SI (протяженностью 10 см). Края операционной раны расширены с помощью ранорасширителей. Проведена ламинэктомия четвёртого поясничного позвонка (LIV). Получен доступ в позвоночный канал. С помощью микрохирургической техники, 5,5-кратного увеличения и специализированных микроинструментов выполнена декомпрессия дурального мешка и спинномозговых корешков в зоне стеноза. Дугоотростчатые суставы LIV и LV позвонков с обеих сторон имели признаки гипертрофии, деформации и сдавливали дуральный мешок и спинномозговые корешки, вдаваясь медиальной поверхностью в просвет позвоночного канала. Выполнена широкая резекция медиальных и латеральных отделов дуго-отростчатых суставов LIV и LV позвонков с обеих сторон, а также удалена гипертрофированная жёлтая связка на уровне LIV/LV позвоночно-двигательного сегмента. Проведена фораминотомия для освобождения корешков L5 с обеих сторон. Выполнен радикулолиз спинномозговых корешков L4 и L5 с обеих сторон. Отмечается отсутствие жировой ткани в эпидуральном пространстве и выраженный фиброз [2, 5]. Проведён менингорадикулолиз с реконструкцией позвоночного канала в восходящем и нисходящем направлениях. Твёрдая мозговая оболочка выглядела истонченной и имела ослабленную пульсацию Паравертебральные мышцы отделены от остистых отростков с обеих сторон до основания поперечных отростков LIII, LIV и LV позвонков. С помощью костного шила сформированы каналы для введения транспедикулярных винтов в тела LIII, LIV и LV позвонков в стандартных точках. Под рентгенологическим контролем установлены полиаксиальные транспедикулярные винты (два винта размером 5,5×45 и четыре винта размером 6,5×50). Головки транспедикулярных винтов расположены в соответствии с физиологическим изгибом позвоночника. Продольные стержни, подо- бранные по длине, адаптированы к лордозу оперируемого сегмента. Стержни установлены в головки винтов и зафиксированы заглушками. В область операции установлен активный дренаж. Рана ушита послойно. Наложена асептическая повязка. Кровопотеря во время операции составила 100,0 мл. Проведён МСКТ контроль послеоперационный зоны хирургического вмешательства.
Контрольная МСКТ ПОП от 16.08.2024 г.: наличие металлоконструкции на уровне L III -L IV -L V , фиксирующей ПДС. Дефект дуг, отсутствие остистых отростков L IV -L V . Остеохондроз поясничного отдела позвоночника III период. Спондилез II степени (рис. 2).
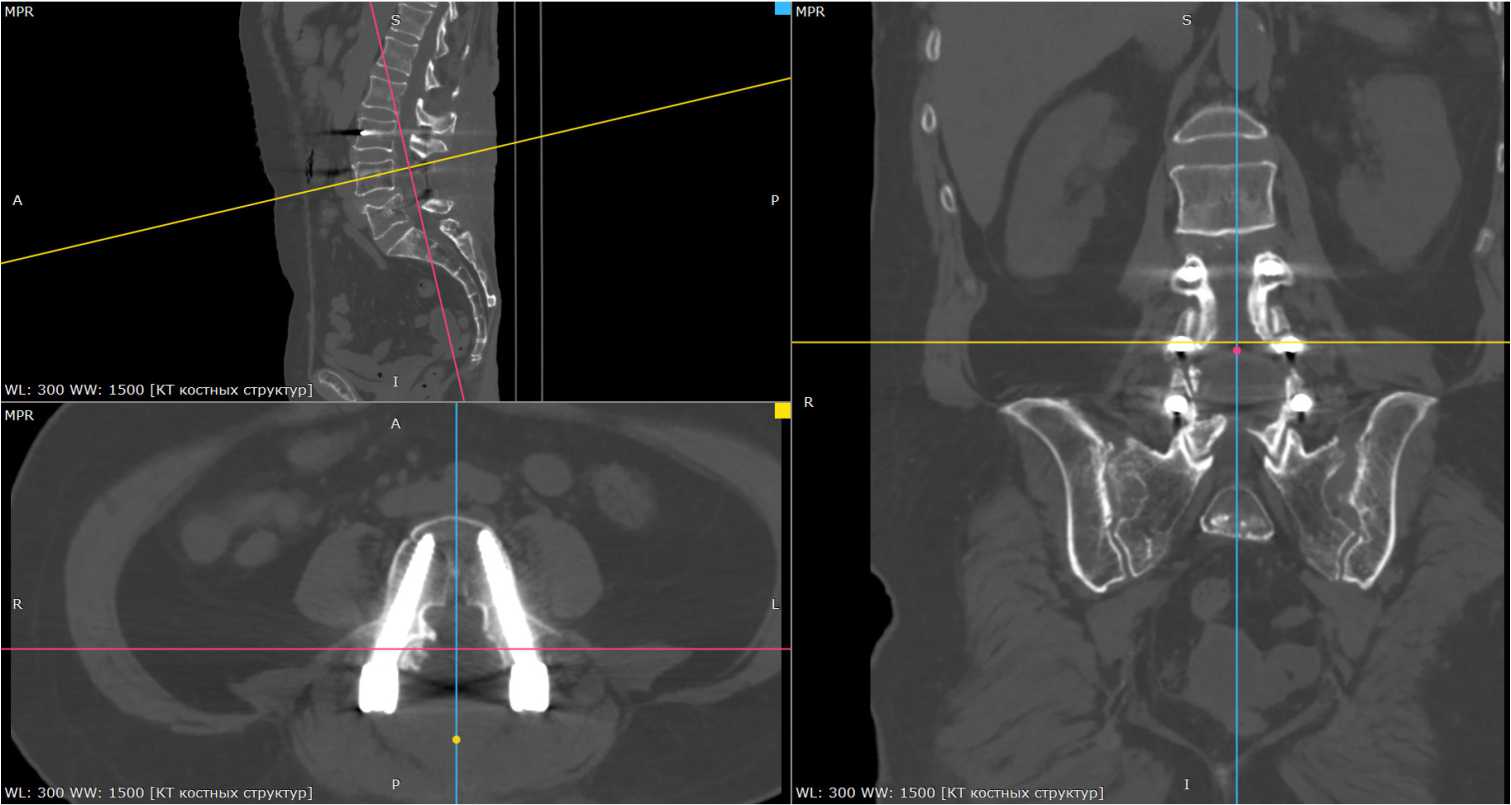
Рисунок 2. Мультиспиральная компьютерная томография зоны хирургического вмешательства поясничного отдела позвоночника: а — аксиальная плоскость; б — фронтальная плоскость; в — сегетальная плоскасть. Стрелками указан уровень декомпрессии позвоночного канала в объёме ламинэктомии на уровне L IV -L V позвонков
Figure 2. Multispiral computed tomography of the surgical intervention area of the lumbar spine: a — axial plane; b — frontal plane; c — segetal plane. Arrows indicate the level of decompression of the spinal canal in the volume of laminectomy at the level of the L IV -L V vertebrae
Послеоперационный период
После операции пациентке проводилась консервативная терапия, включавшая: внутримышечное введение цефтриаксона в дозе 1,0 г два раза в день; внутримышечные инъекции кетопрофена (кетонал) по 2,0 мл два раза в день; пероральный прием тиза-нидина (2 мг) вечером; прием капсул омепразола (20 мг) утром; внутривенные инфузии пентоксифиллина (5,0 мл, разведенных в 200 мл физиологического раствора) один раз в день в течение 10 дней.
В послеоперационном периоде состояние пациентки оставалось удовлетворительным, и в течение 48 часов после хирургического вмешательства наблюдалось снижение интенсивности вертеброген-ного болевого синдрома. Перед выпиской оценка боли по ВАШ составила 2 балла. Ранняя активизация пациентки была проведена на вторые сутки после операции. Для стабилизации поясничного отдела позвоночника использовался ортопедический корсет.
Обсуждение
Сложности клинической диагностики коморбид-ной патологии у лиц пожилого возраста, особенно после комбинированного лечения по поводу онкологической патологии, общеизвестны. Как правило, пациенты обращаются к врачу при возникновении болевого синдрома и не связывают клинические проявления с ранее проведённой лучевой терапией, а акцентируют внимание на дегенеративную патологию позвоночника, как то спондилоартроз или радикулит, и длительное время получают симптоматическое лечение. К сожалению, клинические проявления не специфичны и обусловлены проявлениями радикулопатии или плексопатии, вызванных радиационным повреждением нервных корешков и нервных сплетений, сопровождаются слабостью, изменениям чувствительности, двигательными нарушениями. Миелопатия, вызванная повреждением спинного мозга, проявляется нарушением походки, усталостью, спастичностью, слабостью и потерей проприоцепции. При поражении мышечной ткани возникают фиброзно-склеротические изменения, что приводит к потере объёма движений, спазмам, миофасциальным болям и фиксированным контрактурам. Осложнения лучевой терапии могут быть ранними, развиваться остро (возникают во время или сразу после лечения), отсроченными (до 3 месяцев после завершения лечения), либо поздними (через несколько месяцев или лет после завершения лечения). Лучевой фиброз может поражать любой тип ткани, включая кожу, мышцы, связки, сухожилия, нервы, сердце, лёгкие, желудочно-кишечный тракт, органы мочеполовой системы и кости [17]. Также сложности диагностики обусловлены и тем фактом, что лучевой фиброз чаще является поздним осложнением рентгенотерапии, которое может не проявляться клинически в течение нескольких месяцев или даже лет. Однако после появления первых симптомов заболевание либо быстро прогрессирует, или принимает медленный и, зачастую, не обратимый характер.
На современном этапе развития медицины диагностика осложнений лучевой терапии не всегда проста. Ранние побочные эффекты лучевой терапии, локализованные в зоне облучения, предсказуемы, тогда как поздние проявления имеют скрытый характер и требуют анализа не только клинических проявлений, но и современной инструментальной диагностики. Так, к наиболее значимым проявлениям поражения позвоночника относятся жировая дистрофия костной ткани, остеонекрозы и патологические переломы вследствие нарушения остеогенеза. Основные костные осложнения лучевой терапии связаны с асептическим некрозом и патологическими переломами. Неврологические нарушения (миелопатия и радикулопатия) вызываются компрессионным фиброзом, ишемией или их сочетанием [18, 19].
Переломы позвоночника, возникающие в отдалённом периоде лучевой терапии, могут имитировать метастазы, требуя внимательного отношения и углубленной диагностики. МРТ выявляет такие переломы в 20–80% случаев раньше, чем КТ, обнаруживая отёк и линейную гипоинтенсивность на T2-взвеше-ном изображении или после контрастирования на T1-взвешеном изображении — признак уплотнения кости, что отличает лучевые переломы от злокачественных [20].
В представленном клиническом случае на МРТ-изображениях выявлены признаки перенесённого остеонекроза L IV -L V позвонков и патологического перелома L V позвонка. На T 1 -взвешеном изображении визуализируется аномальный сигнал костного мозга с повышенной интенсивностью, на T 2 -взвешеном изображении – с гетерогенной структурой, деформация тела L V позвонка, вовлечение суставных поверхностей и реактивный отёк фасеточных пространств на уровне L IV -L V . Данные анамнеза (лучевая терапия в дозе 60 Гр), диффузное замещение красного костного мозга, выявленные интраоперационные изменения позволили нам диагностировать у пациентки эпидуральный постлучевой фиброз, как основную причину клинических симптомов. Дегенеративная патология позвоночника (спондилез, спондилоарт-роз) усугубили течение патологического процесса и привели к формированию комбинированного центрального стеноза позвоночного канала, что послужило основанием к хирургическому лечению, а интраоперационные проявления уточнили основные морфологические особенности патологии.
Заключение
Проблема постлучевого эпидурального фиброза представляет собой сложное и многогранное осложнение лечения онкологических заболеваний. Эта патология встречается не так часто, и ещё реже диагностируется, но значительно ухудшает качество жизни пациентов, лишая их привычной активности и вызывая физический и психологический дискомфорт. Важной особенностью постлучевого фиброза является разнообразие и полиморфность клинических проявлений, что затрудняет своевременную диагностику. Сложность диагностики усугубляется тем, что многие из этих пациентов относятся к группе риска, имея сопутствующие заболевания, характерные для пожилого возраста, что может затруднять интерпретацию клинических проявлений.
Важно отметить, что в каждым случаем необходим индивидуальный подход, учёт локализации первичного онкологического процесса, уникальные обстоятельства проведённой ранее терапии. Объединяя усилия медицинских специалистов разных профилей, можно достичь более эффективных результатов в лечении пациентов с постлучевым эпидуральным фиброзом. Также необходима и исследовательская работа для выявления предрасполагающих факторов и разработки новых стратегий управления этим сложным состоянием.
Информированное согласие 25.01.2024 г.). Авторы подтверждают соответствие
От пациентки получено письменное доброволь- своего авторства международным критериям ICMJE.
ное информированное согласие на публикацию описания клинического случая (дата подписания


