Построение радиомической классификационной модели RadMenGr для различения менингиом головного мозга Grade 1 и Grade 2
Автор: Васильев Ю.А., Карпенко А.К., Романенко М.О., Омелянская О.В., Владзимирский А.В., Блохин И.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Цифровые технологии в медицине и здравоохранении
Статья в выпуске: 1 т.41, 2026 года.
Бесплатный доступ
Предоперационная дифференциальная диагностика степени злокачественности менингиом остается затруднительной при рутинной магнитно-резонансной томографии (МРТ) головного мозга. Отсутствие надежных неинвазивных инструментов ограничивает возможности ранней стратификации риска и выбора тактики лечения. Цель: построение радиомической классификационной модели RadMenGr, ориентированной на предсказание степени злокачественности менингиом (Grade 1 или Grade 2) на основе T1-взвешенных изображений с контрастным усилением. Материал и методы. Ретроспективное одноцентровое исследование выполнено с использованием открытого анонимизированного набора данных Meningioma-SEG-CLASS. В анализ включены 95 пациентов, в том числе 53 пациента с менингиомами Grade 1, 42 – с менингиомами Grade 2. Из изображений, размеченных вручную, с помощью библиотеки PyRadiomics были извлечены 105 радиомических признаков. Классификация выполнена с применением алгоритма Naive Bayes после дискретизации признаков методом Entropy-MDL. Оценка диагностической эффективности проводилась с использованием метрик AUC, чувствительности, специфичности и точности. Для оценки стабильности AUC использовался бутстрап-анализ с 10 000 итераций и расчетом 95% доверительного интервала. Результаты. На валидационной выборке (n = 46) ROC-AUC составила 0,805 (95% ДИ: 0,671–0,915). Нижняя граница 95% ДИ AUC превышает значение по нулевой гипотезе (AUC = 0,63), что подтверждает статистическую значимость полученных результатов (p < 0,05). Заключение. В ходе исследования была разработана радиомическая классификационная модель, направленная на дифференциальную диагностику менингиом Grade 1 и Grade 2. Применение алгоритма Naive Bayes на признаках, извлеченных из T1-взвешенных изображений с контрастным усилением и преобразованных методом дискретизации, позволило достичь значимого уровня диагностической точности. Однако ширина доверительного интервала указывает на невысокую стабильность модели, что требует ее валидации на большой репрезентативной выборке.
Радиомика, текстурный анализ, менингиома, классификация, дифференциальный диагноз, магнитно-резонансная томография
Короткий адрес: https://sciup.org/149150653
IDR: 149150653 | УДК: 616.831-006.328-073.7-047.58 | DOI: 10.29001/2073-8552-2026-41-1-213-220
Siberian Journal of Clinical and Experimental Medicine Development of a radiomic classification model RadMenGR for discriminating Grade 1 and Grade 2 intracranial meningioma
Background. Preoperative differentional diagnosis of meningioma grade remains challenging with routine brain magnetic resonance imaging (MRI). The lack of reliable non-invasive tools limits the potential for early risk stratification and treatment planning. Aim: To develop an interpretable classification radiomic model RadMenGR for predicting meningioma grade (Grade I or Grade II) based on contrast-enhanced T1-weighted images. Material and Methods. This retrospective single-center study was conducted using the open-source anonymized dataset MeningiomaSEG-CLASS. 95 patients were included in the analysis (53 with Grade 1 and 42 with Grade 2 tumors). 105 radiomic features were extracted from manually segmented MR images using PyRadiomics. Classification was performed with a Naive Bayes algorithm following feature discretization using the Entropy / MDL method. Diagnostic performance was assessed using the area under the curve (AUC), sensitivity, specificity, and accuracy. Bootstrap analysis with 10,000 iterations and a 95% confidence interval was used for validation. Results. On the validation cohort (n = 46), the ROC-AUC was 0.805 (95% CI: 0.671–0.915). The lower bound of the 95% CI for the AUC exceeded the value under the null hypothesis (AUC = 0.63), confirming the statistical significance of the results (p < 0.05). Conclusion. This study developed an interpretable radiomic classification model for the differential diagnosis of Grade 1 and Grade 2 meningiomas. The application of a Naive Bayes algorithm to features extracted from contrast-enhanced T1-weighted images and transformed using a discretization method enabled the achievement of a significant level of diagnostic accuracy. However, the width of the confidence interval points to a lack of model robustness, necessitating validation on an independent cohort.
Текст научной статьи Построение радиомической классификационной модели RadMenGr для различения менингиом головного мозга Grade 1 и Grade 2
Менингиомы – гетерогенная группа новообразований с различным биологическим поведением и клиническими исходами [1]. Согласно данным Central Brain Tumor Registry (США) за 2016–2020 гг., менингиомы составляли более трети (40,8%) всех впервые диагностированных опухолей центральной нервной системы [2]. Заболеваемость менингиомами в США составляет 9,73 случая на
100 тыс. человек в год [2]. В структуре случаев болезни опухоли степени Grade 1 (опухоли низкой степени злокачественности, характеризующиеся медленным ростом и доброкачественным течением) составляют 80%, Grade 2 (атипичные опухоли с высоким риском рецидива и более агрессивным течением) – 18%, а Grade 3 (анапластические опухоли с выраженной инвазивностью и неблагоприятным прогнозом) – 2% [1].
Несмотря на высокую распространенность менингиом, в настоящее время остаются нерешенными ключевые вопросы стратификации риска и индивидуализации подходов к лечению. Согласно руководству Европейской ассоциации нейроонкологии EANO, большинство рекомендаций по диагностике и лечению основаны на данных низкого уровня достоверности – преимущественно ретроспективных исследованиях (уровень доказательности III) и экспертных заключениях (уровень надежности рекомендаций C) [3].
Для пациентов с опухолями Grade 1 и Grade 2, которые не всегда удается однозначно дифференцировать с помощью неинвазивных методов рутинной диагностики [4], прогноз и тактика ведения существенно различаются. Так, менингиомы Grade 1 являются наиболее распространенными и обычно характеризуются благоприятным прогнозом. После тотальной резекции (Simpson 1) риск рецидива в течение 10 лет составляет от 20 до 39%. У бессимптомных пациентов с небольшими опухолями Grade 1 возможно динамическое наблюдение без немедленного вмешательства, при этом магнитно-резонансная томография (МРТ) проводится раз в год в течение первых 5 лет, а затем один раз в два года [3]. Менингиомы Grade 2, напротив, демонстрируют более агрессивное клиническое поведение и сопровождаются существенно более высоким риском рецидива. Даже после полной резекции риск рецидива через 5 лет может достигать 30%, а после субтотальной резекции – до 40%. В связи с этим пациенты с Grade 2 требуют активного наблюдения, включающего МРТ каждые 6 мес. в течение первых 5 лет, а затем ежегодно [3]. После неполной резекции Grade 2 менингиом однозначно рекомендуется адъювантная лучевая терапия, а при полной резекции данный вопрос остается открытым и должен решаться индивидуально. Поэтому задача прогнозирования гистологического типа менингиом до операции приобретает клиническую значимость, позволяя потенциально изменить стратегию лечения и наблюдения.
МРТ является методом выбора для визуализации менингиом, обеспечивая высокую контрастность мягких тканей и точное определение границ образования [3]. Исследование позволяет оценить размеры опухоли, степень инвазии, вовлечение сосудов и окружающих структур, а также наличие перитуморального отека. Благодаря высокой пространственной разрешающей способности МРТ применяется для диагностики, планирования хирургического вмешательства, лучевой терапии и последующего наблюдения.
В исследовании F. Brugada-Bellsolà и соавт. [5] была оценена применимость шкалы AIMSS (Asian Intracranial Meningioma Scoring System), предназначенной для стратификации риска быстрого роста случайно обнаруженных при МРТ бессимптомных менингиом. Решение по тактике лечения данных новообразований зависит от прогноза роста. В исследовании ретроспективно проанализировано 69 опухолей у 46 пациентов. Авторы показали, что при помощи четырех простых радиологических признаков (размер, наличие кальцинатов, перитуморальный отек, интенсивность сигнала на T2-МРТ) можно достоверно различать низкий и средний риск роста опухоли. Несмотря на ограниченность AIMSS в предсказании быстрого роста в группе высокого риска, что связано с небольшим размером выборки, работа подчеркивает практическую ценность раннего прогноза: своевременное выявление склонности к росту позволяет избежать запоздалого вмешательства и минимизировать хирургические риски.
Радиомика является перспективным направлением для неинвазивного анализа медицинских изображений, однако ее широкое внедрение ограничено доступностью моделей и их интерпретируемостью [6]. Согласно метаанализу T. Lee и соавт., из 268 анализируемых исследований только 39,9% ( n = 107) были доступными для повторного использования, а среди методов глубокого обучения этот показатель составил всего 11,5% [7]. В контексте данного исследования доступность модели означала, что статья содержала полную техническую информацию, позволяющую независимо воспроизвести модель на новом наборе данных.
Цель исследования: построение радиомической классификационной модели RadMenGr, которая ориентирована на предсказание степени злокачественности менингиомы Grade 1 или Grade 2 на основе T1-взвешенных МРТ с контрастным усилением.
Материал и методы
Критерии соответствия
Данное исследование представляет собой одноцентровой ретроспективный анализ. В исследовании RadMenGr вторично использовался открытый набор данных Meningioma-SEG-CLASS [8], содержащий сегментированные и классифицированные изображения менингиом Grade 1 и Grade 2. Пациентам проводилось хирургическое лечение с 2010 по 2019 гг. Для каждого пациента были доступны предоперационные в режимах T1, T1 с контрастным усилением (T1-CE) и T2-FLAIR. Сканирование проводилось на аппаратах различных производителей, включая 1.5 Т и 3Т модели от GE (Optima, Discovery, Signa), Philips (Achieva, Intera), Toshiba (Titan, MRT 200, Galan), Hitachi (Oasis, Echelon) и Siemens (Symphony, Skyra). Параметры сканирования для последовательностей T1-CE и T2-FLAIR приведены в таблице 1. Набор данных также содержит данные о возрасте и поле пациентов, степени злокачественности и гистологическом варианте менингиом, наличии инвазии в мозг, митотическом индексе и локализации опухоли. Из исследования исключались пациенты с наличием множественных менингиом.
Таблица 1 . Параметры сканирования
Table 1 . Scanning parameters
|
Параметр |
T1-CE |
T2-FLAIR |
|
Время повторения (TR), мс |
7–8 |
8000–11000 |
|
Время эхо (TE), мс |
2–3 |
120–159 |
|
Размер вокселя |
256 × 256 |
256–512 × 256–512 |
|
Изотропное пространственное разрешение в плоскости, мм |
1,016 |
0,4–0,9 |
|
Толщина среза, мм |
1–2 |
2–7 |
|
Поле обзора (FOV), мм² |
100 |
80–100 |
|
Угол наклона, градусы |
15° |
90°–180° |
Основной исход исследования
Основным исходом исследования являлась диагностическая точность разработанной модели для предоперационного различения менингиом Grade 1 и Grade 2 на основании радиомических признаков.
Методы регистрации исходов
Радиомический анализ
Перед извлечением признаков все МР-изображения прошли процедуру нормализации интенсивности, что обусловлено высокой вариабельностью сигналов внутри и между МР-исследованиями. Все изображения и соответствующие сегментации были ресемплированы до изотропного воксельного разрешения 2 мм × 2 мм × 2 мм. Для интерполяции применялся B-spline интерполятор, обеспечивающий гладкие преобразования и сохранение непрерывности тканей при изменении масштаба.
Радиомические признаки извлекались с использованием оригинальных фильтров. Параметры извлечения включали ширину бина 25, сдвиг воксельного массива 1000 и радиус ядра 2. Из масок области интереса Т1-взвешенных изображений с контрастным усилением с помощью PyRadiomics были извлечены следующие 105 текстурных признаков.
Работа с данными
Для разработки модели данные были разделены на обучающую и валидационную подгруппы с использованием стратифицированной выборки для сохранения баланса классов. Дискретизация признаков для уменьшения их числа проведена с помощью виджета «Preprocess», опция Entropy-MDL. Построение радиомической модели выполнено методом наивного Баейса (Naïve Bayes). Для интерпретации и визуализации модели использовались виджеты «Explain Model» (SHapley Additive exPlanations) и «Feature Importance». График Feature Importance показывает оценку важности признаков по уменьшению AUC при пермутации значений каждого признака (выбранное число пермутаций – 500).
Анализ данных выполнен в RStudio версии 4.1.2 [9], Jamovi версии 2.6.24 и Orange версии 3.37. В качестве порогового уровня статистической значимости было принято значение 0,05 (одностороннее). Вся последовательность построения модели представлена на рисунке 1 в виде схемы взаимодействия виджетов в интерфейсе Orange.
Статистический анализ
Расчет и обоснование размера выборки
Для оценки необходимого размера выборки был использован веб-калькулятор MedCalc (https://www. с функцией сравнения двух ROC AUC как ключевых показателей диагностической точности модели . В качестве нулевой гипотезы принималось предположение, что модель обладает низкой дискриминирующей способностью: AUC ≤ 0,63. Согласно T. Upreti и соавт. [4], такое значение отражает диагностическую точность признака перитуморального отека, который является одним из наиболее часто встречающихся и легко визуализируемых рентгенологических признаков на МРТ. В качестве значения альтернативной гипотезы выбрана ожидаемая производительность на основе результатов ранее опубликованных работ. В исследовании J.H. Park и соавт. [10], комбинирующем текстурные и клинические признаки, модели машинного обучения достигали AUC от 0,80 до 0,87 для дифференциальной диагностики Grade 1 и Grade 2 менингиом. Это значение отражает реалистич- ную цель для предоперационной классификационной модели. Таким образом, значение альтернативной гипотезы соответствовало ожидаемому уровню AUC > 0,83.
Для достижения мощности теста 80% (1 - β = 0,8) при уровне значимости α = 0,05 (односторонняя) и равном размере групп расчет показал, что для оценки метрик диагностической модели на внутренней валидационной выборке потребуется минимум по 23 наблюдения в каждой группе, то есть 46 пациентов.
Методы статистического анализа данных
Для проверки нормальности распределения параметров выборки использовался тест Шапиро – Уилка. Номинальные переменные были приведены в виде процентного соотношения каждого из классов к общей выборке. Оценка качества классификационной модели проводилась с использованием следующих метрик: чувствительность, специфичность, точность, ROC-AUC, прогностическая ценность положительного и отрицательного результата (PPV и NPV). Для проверки значимости результатов нижняя граница 95% доверительного интервала AUC сравнивалась с пороговым значением AUC при нулевой гипотезе. Для оценки стабильности AUC был проведен бутстрап-анализ с 10 000 итераций.
Результаты
Объекты исследования
После исключения из набора данных одного пациента по причине наличия множественных менингиом в исследование были включены 95 пациентов: 53 пациента с менингиомой Grade 1 и 42 пациента с менингиомой Grade 2. Распределение возраста пациентов соответствовало нормальному распределению (p > 0,05). Средний возраст составил 56 ± 14 лет. Среди пациентов преобладали женщины (67 человек, 70,5%), мужчины (28 человек) составили 29,5%.
Основные результаты исследования
Для валидационной выборки ( n = 46) ROC-AUC составила 0,805 (95% ДИ: 0,671–0,915). Чувствительность модели достигла 0,85 (95% ДИ: 0,64–0,948), а специфичность – 0,577 (95% ДИ: 0,389–0,745), точность равнялась 0,696 (95% ДИ: 0,552–0,809), прогностическая ценность положительного результата (PPV) – 0,607 (95% ДИ: 0,424–0,764), а прогностическая ценность отрицательного результата (NPV) – 0,833 (95% ДИ: 0,608–0,942). Матрица сопряжения приведена в таблице 2, метрики диагностической точности с 95% ДИ – в таблице 3.
Таблица 2 . Матрица сопряжения для валидационной выборки
Table 2 . Confusion matrix for the validation set
|
Степени злокачественности менингиом |
Прогноз модели (Grade 1) |
Прогноз модели (Grade 2) |
Итого |
|
Grade 1 |
15 |
11 |
26 |
|
Grade 2 |
3 |
17 |
20 |
|
Итого |
18 |
28 |
46 |
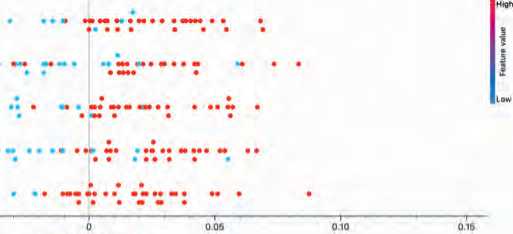
На рисунке 2 представлен SHAP-график пяти наиболее значимых признаков, используемых моделью для предсказания Grade 2 менингиом. К этим радиомиче-ским признаками относятся: original_shape_SurfaceArea (Признаки формы_Площадь поверхности), original_
Таблица 3 . Диагностические метрики RadMenGr
Table 3 . Diagnostic metrics of RadMenGr
|
Метрика |
Значение |
95% ДИ |
|
AUC |
0,805 |
0,671–0,915 |
|
Чувствительность |
0,850 |
0,640–0,948 |
|
Специфичность |
0,577 |
0,389–0,745 |
|
Точность |
0,696 |
0,552–0,809 |
|
PPV |
0,607 |
0,424–0,764 |
|
NPV |
0,833 |
0,608–0,942 |
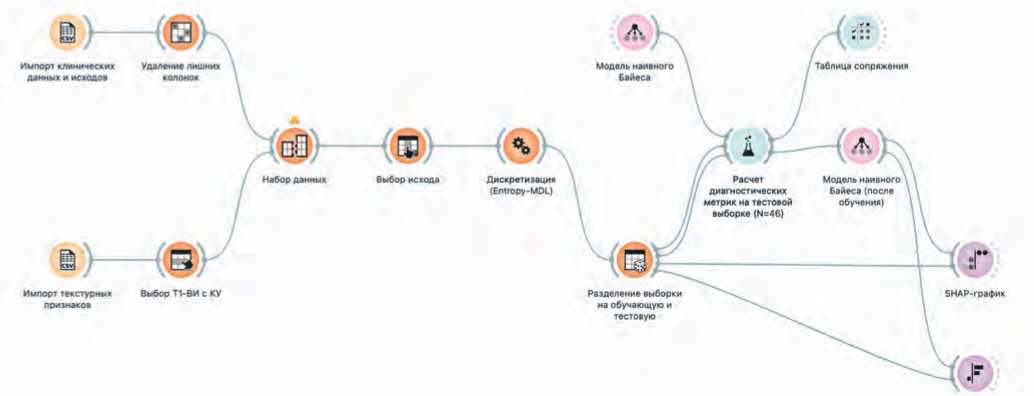
Рис. 1. Схема модели в интерфейсе Orange Fig. 1. Orange workflow diagram
Вклад признаков в АиС (пармутации}
shape_VoxelVolume (Признаки формы_Воксельный объем), original_glrlm_RunLengthNonUniformity (Матрица длин серий уровней серого_Неравномерность длины ряда), original_shape_LeastAxisLength (Признаки формы_Наименьшая длина оси) и original_shape_ Maximum2DDiameterColumn (Признаки формы_Мак-симальный 2D диаметр, колонка). Для большинства перечисленных признаков высокие значения (красные точки) смещают предсказание модели вправо, увеличивая вероятность целевого класса, тогда как низкие значения (синие точки) – влево, уменьшая ее. Именно характеристики формы образования (4 из 5 признаков) и показатели его неоднородности являются ключевыми детерминантами решения модели, причем большие размеры и выраженная неоднородность чаще ассоциированы с повышенной вероятностью целевого класса.
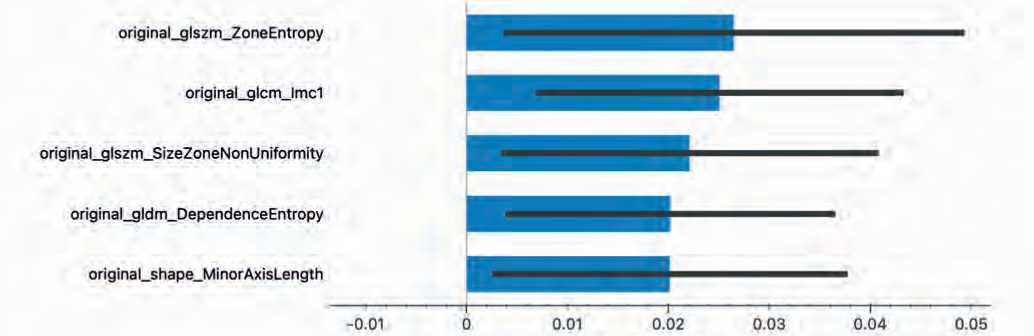
Также был получен график Feature Importance, на котором представлены Топ-5 радиомических признаков по степени влияния на AUC классификационной модели:
original_glszm_ZoneEntropy – Характеристики матрицы размера зон уровня серого_Энтропия зон; original_glcm_ Imc1 - Характеристики матрицы совпадения уровней серого_Информационная мера корреляции 1; original_ glszm_SizeZoneNonUniformity – Характеристики матрицы размера зон уровня серого_Размер зон неоднородности; original_gldm_DependenceEntropy – Матрица зависимости уровней серого_Энтропия зависимости; original_ shape_MinorAxisLength – Признаки формы_Длина малой оси (рис. 3). Из графика видно, что наибольший вклад в AUC внесли радиомические признаки энтропии и корреляции (glszm_ZoneEntropy, glcm_Imc1).
Для оценки стабильности AUC был проведен бутстрап-анализ с 10 000 итераций. Полученный доверительный 95% интервал составил от 0,671 до 0,915. Результат отражает хорошую дискриминационную способность модели и ее низкую стабильность.
При сопоставлении нижней границы 95% доверительного интервала с пороговым значением AUC не выявлено их пересечения (0,67 vs 0,63). Это свидетельствует о наличии статистически значимой разницы между AUC модели и AUC H0 ( p < 0,05).
Обсуждение
Менингиомы головного мозга не имеют специфических клинических симптомов и часто являются случайной находкой при МРТ. Степень злокачественности менингиомы влияет на агрессивность роста опухоли и вероятность рецидива после лечения [1].
ongtnal_shape_Surf*ceA/ea
onginal_shape_VoxelVolu
onginal_shapa_k*astAxisLength onginal_ihape_Maximum2DDta •o'lS *040 -005 impact on model output Рис. 2. SHAP-график вклада радиомических признаков в предсказание класса Grade 2 (см. расшифровку признаков в тексте) Fig. 2. SHAP plot of radiomic feature contributions to Grade 2 class prediction (see feature descriptions in the text) Decrease in AUC Рис. 3. Топ-5 радиомических признаков по степени влияния на AUC классификационной модели Fig. 3. Top 5 radiomic features ranked by their influence on the classification model's AUC На данный момент золотым стандартом верификации опухоли и определения степени ее злокачественности остается хирургическая резекция и гистологическое исследование. Однако по данным нейровизуализации может быть выбрана стратегия лечения, которая варьируется от динамического наблюдения за пациентом до радикальной резекции новообразования с последующим курсом адъювантной терапии [11]. Возможность определить степень злокачественности предоперационно по одной временной точке позволит усовершенствовать планирование лечения для каждого конкретного случая. Радиомический анализ менингиом активно развивается. Согласно систематическому обзору 2023 г., наиболее распространенной темой оригинальных работ является классификация менингиом с другими новообразованиями центральной нервной системы (102 публикации 54%), в то время как оценке степени злокачественности менингиом посвящено 27 публикаций (14%) [12]. Среди моделей, различающих степень злокачественности менингиом, 74% определяли менингиомы низкой и высокой степени злокачественности (Grade 1 и Grade 2 + 3) и только 11% моделей различали исключительно Grade 1 и Grade 2. Следует отметить, что Всемирная организация здравоохранения также объединяет Grade 2 и 3 как менингиомы высокой степени злокачественности. Средний показатель площади под кривой ROC-AUC для всех моделей составил 0,85 с диапазоном от 0,69 до 0,97. Чувствительность моделей достигла 79,7 (в диапазоне от 54 до 100%), а специфичность составила 84,0 (в диапазоне от 62,5 до 100%). Нами была разработана диагностическая модель RadMenGr, которая определяет степень злокачественности менингиом (Grade 1 или Grade 2) на основе ра-диомических признаков МР-изображений. Площадь под ROC-кривой (AUC) составила 0,805, что превышает метрики врачей-рентгенологов, доступные в литературе [4]. Так, наибольшую точность в различении рентгенологами менингиом высокой и низкой степени злокачественности демонстрируют признаки «нечеткость контуров образования» и «гетерогенное контрастирование образования» (AUC 0,788 и 0,703 соответственно) [4]. Границы 95% доверительного интервала демонстрируют невысокую стабильность разработанной модели, для повышения ее стабильности необходимо проведение дальнейших исследований на большей выборке с внешней валидацией. Наибольший вклад в SHAP-график прогноза нашей мо- дели вносят радиомические признаки формы. Высокая чувствительность модели при умеренной специфичности указывает на хорошую способность прогнозирования более агрессивных менингиом Grade 2. В нашей работе мы осознанно сосредоточились на анализе открытого набора данных и извлеченных радио-мических признаков и оценке того, насколько эффективно может работать алгоритм Naive Bayes на небольшой, но репрезентативной выборке. Отдельно необходимо отметить использование Entropy-MDL. В радиомическом анализе извлекаются сотни признаков, а выбранный нами способ дискретизации автоматически группирует непрерывные значения в компактные, информативные интервалы, резко сокращая размерность данных и устраняя избыточные признаки, которые напрямую ведут к переобучению. Это принципиально повышает обобщающую способность моделей машинного обучения и снижает их чувствительность к шуму в исходных признаках [13]. При поиске исследований иностранных авторов со схожей методологией обращает на себя внимание работа A.T. Hale и соавт. [14], где была использована модель на основе Naive Bayes, которая классифицировала менингиомы Grade 1 и 2. Выборка составила 124 пациента, AUC – 0,71, авторы использовали набор клинических и рентгенологических характеристик. Однако данная модель не является радиомической. В анализ были включены такие рентгенологические признаки, как объем опухоли, ее локализация, перитуморальный отек и др. В работе A.T. Hale и соавт. было показано сравнение различных алгоритмов машинного обучения, включая ANN, SVM, k-NN и Naive Bayes с фокусом на достижении максимальной прогностической точности. В нашей работе был продемонстрирован потенциал Naive Bayes классификатора как простого и интерпретируемого метода, способного давать клинически значимую предсказательную силу в условиях ограниченной выборки [15]. Таким образом, наше исследование является дополнительным вкладом в понимание того, какие методы могут быть применимы в условиях ограниченных ресурсов. В другой работе авторы P.F. Yan и соавт. [16] использовали алгоритм Naive Bayes для анализа текстурных признаков, извлеченных из Т1-ВИ с контрастным усилением, и морфологических признаков, выявленных врачом-рентгенологом (форма, контур, степень контрастирования). Для обработки данных применялось программное обеспечение MaZda, а отбор признаков осуществлялся с помощью алгоритма CfsSubsetEval в среде WEKA. В финальную модель были включены три текстурных признака (Horzl_RLNonUni, S(2,2)SumOfSqs, WavEnHL_s-3) и три признака формы (GeoFv, GeoW4, GeoW5b). Несмотря на высокий показатель AUC (0,88) при обучении на текстурных признаках, модель демонстрировала низкую чувствительность (0,57) при высокой специфичности (0,92), что может быть связано с выраженным дисбалансом классов в выборке: лишь 21 случай с высокой степенью злокачественности при 110 случаях с низкой степенью злокачественности. При таких соотношениях алгоритмы склонны к смещению в сторону преобладающего класса, что критично в клинических задачах, где особенно важна надежность в обнаружении более агрессивных форм опухолей. Также стоит отметить, что в работе P.F. Yan и соавт. для извлечения признаков использовалось программное обеспечение MaZda, которое, как показано в сравнительном исследовании J.C. Korte и соавт. [17], уступает более современным открытым программным обеспечениям, таким как PyRadiomics, по воспроизводимости извлекаемых радиомических признаков. Кроме того, MaZda не соответствует IBSI-стандартам, в отличие от PyRadiomics, что ограничивает использование MaZda в современных исследованиях, ориентированных на воспроизводимость и переносимость моделей. В исследовании J.H. Park и соавт. [10] была реализована комбинированная модель для предсказания степени злокачественности менингиом, включающая ради-омические и визуальные признаки. Примечательно, что визуальные признаки, обработанные с помощью Naive Bayes, показали высокую эффективность (AUC = 0,82), в то время как модель, работающая с радиомическими данными, на основе LightGBM продемонстрировала более низкий результат (AUC = 0,72). В отличие от этой работы, в нашем исследовании был использован Naive Bayes непосредственно на предварительно дискретизированных радиомических признаках. Это позволило достичь AUC = 0,805 при использовании только одного типа изображений (T1-CE) и без привлечения клинической оценки. Таким образом, модель RadMenGr демонстрирует конкурентные результаты по сравнению с более сложными алгоритмами машинного обучения. Ограничения исследования Настоящее исследование носит ретроспективный характер с вторичным использованием открытого набора данных, собранного на базе одного центра. При сборе данных не проводилась оценка постоянства параметров получаемых изображений и соответствия их качества, что могло оказать влияние на извлеченные текстурные признаки, поэтому необходим контроль технического состояния магнитно-резонансного томографа по клиническим изображениям головного мозга [18, 19]. Помимо этого, малый размер выборки ограничивает применимость полученных результатов. Также из исследования был исключен один пациент с множественными менингиомами для минимизации систематической ошибки, поскольку такие случаи не представляют собой типичную картину для большинства пациентов с менингиомами. Распределение между типами менингиом, cогласно данным Всемирной организации здравоохранения, составляет: 80% Grade 1, 18% Grade 2 и 2% Grade 3 соответственно [1]. Однако распределение в когорте, использованной для создания модели RadMenGr, отличается и составляет 55% на 45% для Grade 1 и Grade 2. Менингиомы же Grade 3 в исследование не включались, что представляет собой дополнительное ограничение модели. Заключение Настоящее исследование направлено на создание радиомической классификационной модели для предоперационного прогнозирования степени злокачественности менингиом. Применение алгоритма Naive Bayes на признаках, извлеченных из T1-взвешенных изображений с контрастным усилением и преобразованных методом дискретизации, демонстрирует принципиальную возможность для стратификации менингиом Grade 1 и Grade 2. Однако для внедрения разработанной радиомической модели в клиническую практику требуется ее валидация в многоцентровых исследованиях на большой репрезентативной выборке.