Предоперационная оценка риска кровотечения у кардиохирургических пациентов
Автор: Зюзин В.С.
Журнал: Хирургическая практика @spractice
Рубрика: Обзоры литературы
Статья в выпуске: 2 т.9, 2024 года.
Бесплатный доступ
Цель. Изучить роль шкал оценки риска кровотечения, индивидуального и наследственного анамнеза, анализа предыдущих кровотечений и их влияния на риск всех возможных осложнений, в том числе и летального исхода, у взрослых пациентов после кардиохирургического вмешательства по сравнению с рутинной тактикой.Материалы и методы. Поиск публикаций проводился с использованием базы данных PubMed, Transfusion Evidence Library, eLibrary.ru за период с 2019 по 2023 г. Поисковые термины включали слова: шкалы оценки риска кровотечения в кардиохирургии взрослых, предоперационная анемия в кардиохирургии взрослых, переливание эритроцитсодержащих компонентов в кардиохирургии взрослых. Исключение дублирующих статей осуществлялось вручную. Дополнительный поиск проводился среди списков литературы отобранных публикаций.Материалы и методы. Поиск публикаций проводился с использованием базы данных PubMed, Transfusion Evidence Library, eLibrary.ru за период с 2019 по 2023 г. Поисковые термины включали слова: шкалы оценки риска кровотечения в кардиохирургии взрослых, предоперационная анемия в кардиохирургии взрослых, переливание эритроцитсодержащих компонентов в кардиохирургии взрослых. Исключение дублирующих статей осуществлялось вручную. Дополнительный поиск проводился среди списков литературы отобранных публикаций.Результаты. Всего было найдено 2011 публикаций. На первом этапе отбора учитывали клинические исследования, метаанализы, рандомизированные контролируемые исследования, обзоры и регулярные обзоры без языковых ограничений на основе содержания аннотации. На втором этапе для исследований, прошедших предыдущий этап, решение принималось на основании оценки полнотекстового варианта, в котором были представлены последствия предоперационной анемии, послеоперационных кровотечений, трансфузионной терапии у взрослых кардиохирургических пациентов. В итоге в данный описательный обзор были включены 40 публикаций.Заключение. Предоперационная оценка риска кровотечения является мультимодальной междисциплинарной проблемой, требующей пациентоориентированного подхода. Она должна начинаться еще на подготовительном этапе и требует участия врачей первичного звена, кардиологов, хирургов, анестезилогов-реаниматологов, врачей лабораторной диагностики и трансфузиологов. Краеугольным камнем является сбор индивидуального и семейного анамнеза. Получение информации, основанной на вовлечении пациента путем задавания наводящих на размышления вопросов, использовании шкал оценки риска кровотечения, анализе данных о предыдущих кровотечениях, подкрепленное данными лабораторных тестов, представляет собой наиболее научный подход к разработке индивидуального плана ведения пациента с риском кровотечения.
Предоперационная подготовка, предоперационная оценка риска кровотечения, гемостаз, трансфузия, компоненты крови
Короткий адрес: https://sciup.org/142242577
IDR: 142242577 | УДК: 616-005.1 | DOI: 10.5922/2223-2427-2024-9-2-6
Preoperative bleeding risk assessment in cardiac surgery patients
Aim: To investigate the role of bleeding risk scores, personal and family medical history, and previous bleeding incidents in assessing the impact on the risk of all possible complications, including mortality, in adult patients following cardiac surgery.Methods. The search for publications was conducted using the PubMed, Transfusion Evidence Library, and eLibrary.ru databases, covering the period from 2019 to 2023. Search terms included: ‘bleeding risk assessment scales in adult cardiac surgery’, ‘preoperative anemia in adult cardiac surgery’, and ‘transfusion of red blood cell-containing components in cardiac surgery adults’. Duplicate articles were manually excluded. An additional search was performed among the reference lists of selected publications.Results. A total of 2,011 publications were found. In the first stage of selection, clinical studies, meta-analyses, randomized controlled trials, reviews, and regular reviews without language restrictions were considered based on the content of the abstract. In the second stage, for studies that passed the initial screening, decisions were made based on an assessment of the full-text versions, which presented the consequences of preoperative anemia, postoperative bleeding, and transfusion therapy in adult cardiac surgery patients. Ultimately, 40 publications were included in the review.Conclusion. Preoperative bleeding risk assessment is a multimodal, interdisciplinary challenge that necessitates a patient-centered approach. It should commence at the preparatory stage and involve primary care physicians, cardiologists, surgeons, anesthesiologists, laboratory diagnostic specialists, and transfusiologists. The cornerstone of this process is the thorough collection of individual and family medical histories. Obtaining detailed information through patient involvement, utilizing bleeding risk rating scales, reviewing previous bleeding incidents, and supporting these findings with laboratory test data represent the most scientific approach to developing an individualized management plan for patients at risk of bleeding.
Текст обзорной статьи Предоперационная оценка риска кровотечения у кардиохирургических пациентов
To cite this article: Zyuzin VS. Preoperative bleeding risk assessment in cardiac surgery patients. Surgical practice (Russia). 2024;9(2):80—96.
Одним из основных принципов предоперационной подготовки пациента является оптимизация гемостаза и минимизация кровопотери. Выявление риска кровопотери до проведения оперативного вмешательства — неотъемлемая часть стратегии обеспечения оптимальных результатов лечения. Традиционно большинству пациентов назначают обширный список предоперационных анализов для прогнозирования кровотечения.
Однако у большего числа пациентов данные тесты имеют ограниченную клиническую значимость и редко влияют на тактику лечения или на результаты [1—3]. Это справедливо и в отношении таких показателей, как активированное частичное тромбопластиновое время (АЧТВ), международное нормализованное отношение (МНО) и количество тромбоцитов [4]. Указанное также относится к пожилым людям возрастом старше 70 лет, у которых частота отклонений от нормы лабораторных показателей может быть увеличена, но не связана с какими-либо неблагоприятными клиническими исходами в периоперационном периоде [5].
Существует множество факторов, обусловленных как индивидуальными особенностями пациента, так и видом и объемом планируемого хирургического вмешательства, определяющими размер кровопотери в периоперационном периоде (рис. 1). При планировании операции важно учитывать все факторы, которые будут вызывать кровотечение, и разработать план ведения пациента для минимизации периоперационной кровопотери [6; 7].
Частота кровотечений в кардиохирургии зависит от сложности и объема операции и варьируется от 2 до 16 % [8; 9]. Ее вероятность, а также объем обусловлены исходным состоянием пациента, выраженностью нарушений гемостаза до операции, объемом вмешательства, условиями проведения искусственного кровообращения (ИК) [10; 11]. В свою очередь, кровопотеря была связана с операционной летальностью. Кровотечение после операций с ИК приводит к четырехкратному увеличению 30-дневной летальности, широкому спектру послеоперационных осложнений и увеличению длительности госпитализации [12; 13].
Кровопотеря, являясь независимым фактором риска летальности, также способствует развитию или обострению уже существующей анемии, а также вторичному риску трансфузии эритроцитов. Значительная кровопотеря, как экстренная, так и прогнозируемая, может привести к неблагоприятным последствиям в виде увеличения сроков госпитализации, присоединения внутрибольничной инфекции, повышенного риска инсульта, инфаркта миокарда, легочной эмболии и смерти [14; 15].
Хотя гемотрансфузия может спасти жизнь при остром неконтролируемом кровотечении, данные показывают, что пациенты, которым не назначали компоненты крови, часто имели лучшие результаты по сравнению с теми, кто их получал [16; 17].
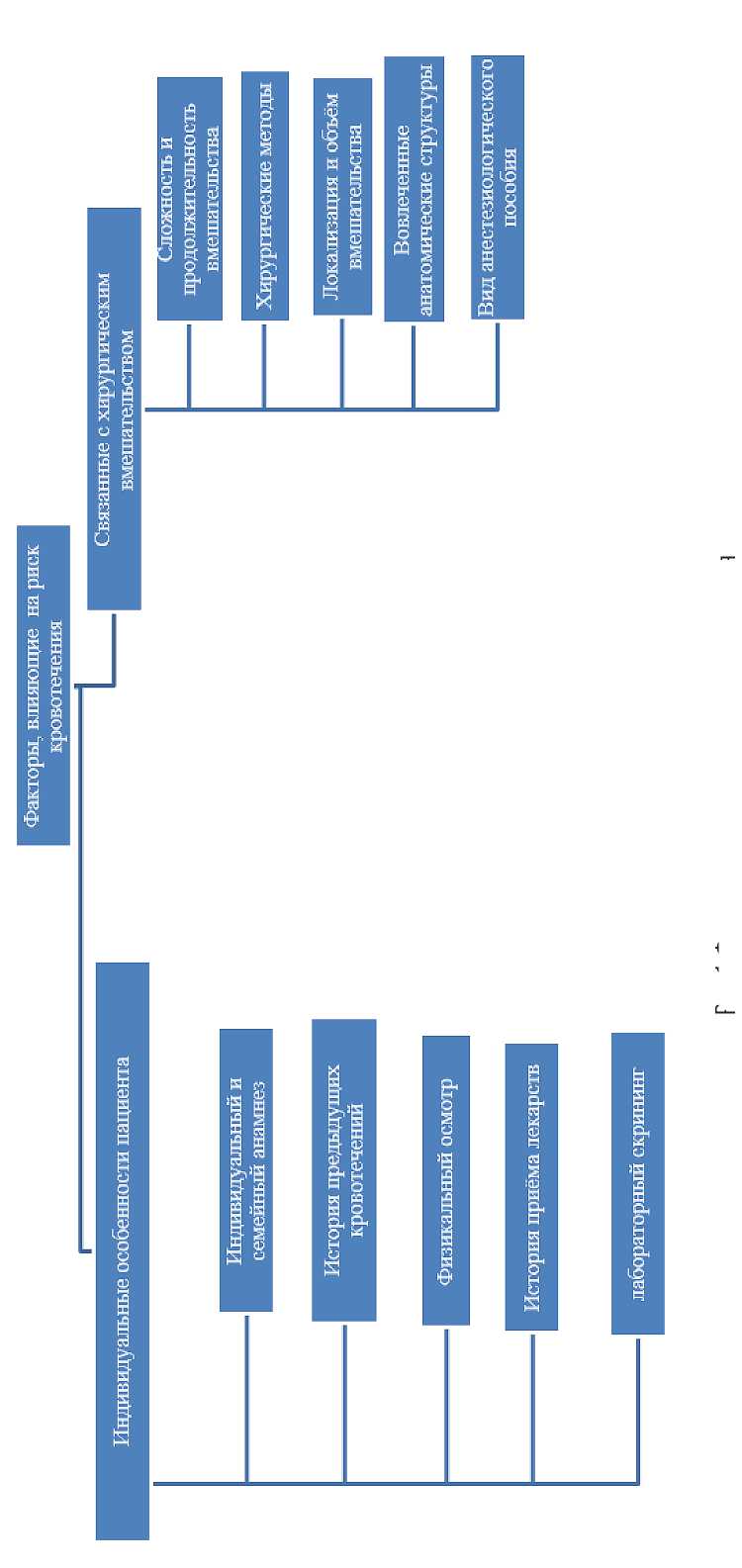
Рис. 1. Факторы, влияющие на риск кровотечения Fig. 1. Factors affecting the risk of bleeding
В ряде исследований сравнили влияние ограничительной и либеральной стратегий гемотрансфузии на смертность в течение 30 дней после кардиохирургических операций. Авторы пришли к выводу, что ни одна из стратегий не имеет заведомого преимущества. Следовательно, у пациентов с сопутствующей сердечно-сосудистой патологией при наличии железодефицитной анемии (ЖДА) тяжелой степени гемотрансфузионная терапия должна проводится по индивидуальным показаниям. При определении показаний к гемотрансфузии следует принимать во внимание наличие у пациента сопутствующей патологии, например ишемической болезни сердца, что может потребовать гемотрансфузии даже при умеренном снижении гемоглобина [18—20].
Трансфузионная терапия может быть связана с развитием таких осложнений, как острые и/или отсроченные гемолитические реакции, острое повреждение легких (TRALI), перегрузка объемом (TACO), трансмиссивные инфекции, септический шок, вторичный гемохроматоз, увеличение сроков госпитализации [21].
Таким образом, каждое применение компонентов крови должно быть научно обоснованным.
Хотя анемия, кровопотеря и трансфузионная терапия являются независимыми факторами риска, важно помнить, что они обладают кумулятивным эффектом. Первые два фактора, взаимно дополняя друг друга, повышают риск периоперационного применения аллогенной крови. Когда все эти факторы объединяются, риск неблагоприятных исходов увеличивается (рис. 2) [22].
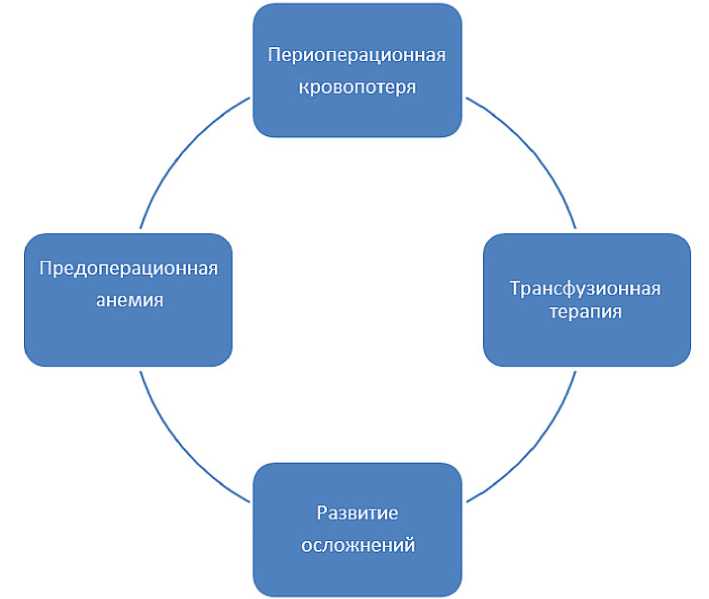
Рис. 2. Взаимосвязь факторов риска развития кровотечения
Fig. 2. Interrelation of risk factors for bleeding
Цель исследования — изучение роли шкал оценки риска кровотечения, индивидуального и наследственного анамнеза, анализа предыдущих кровотечений в оценке влияния на риск всех возможных осложнений, в том числе летального исхода, у взрослых пациентов после кардиoхирургического вмешательства по сравнению с рутинной тактикой.
Материалы и методы
Поиск публикаций проводился с использованием базы данных PubMed, Transfusion Evidence Library, eLibrary.ru за период с 2019 по 2023 г. Поисковые термины включали слова: шкалы оценки риска кровотечения в кардиохирургии взрослых, предоперационная анемия в кардиохирургии взрослых, переливание эритроцитсодержащих компонентов в кардиохирургии взрослых . Исключение дублирующих статей осуществлялось вручную. Дополнительный поиск проводился среди списков литературы отобранных публикаций. Количество цитирований включенных в обзор источников определялось с помощью Google Scholar в феврале 2024 г.
Всего было найдено 2011 публикаций. На первом этапе отбора учитывали клинические исследования, метаанализы, рандомизированные контролируемые исследования, обзоры и регулярные обзоры без языковых ограничений на основе содержания аннотации. На втором этапе для исследований, прошедших предыдущий этап, решение принималось на основании оценки полнотекстового варианта, в котором были представлены последствия предоперационной анемии, послеоперационных кровотечений, трансфузионной терапии у взрослых кардиохирургических пациентов. В итоге в данный описательный обзор были включены 40 публикаций.
Оценка рисков, связанных с хирургическим вмешательством
Хирургическое вмешательство почти всегда приводит к некоторой кровопотере. На основе прогнозируемого риска кровотечения в течение 30 дней после проведения хирургические вмешательства Международным обществом по тромбозу и гемостазу (ISTH) предложено разделять процедуры с минимальным, низким/умеренным и высоким риском (табл. 1) [23].
Таблица 1. Классификация кардиохирургических процедур по уровню риска развития потенциального кровотечения в кардиохирургии
Table 1. Classification of cardiac surgery procedures according to the risk of potential bleeding
|
Риск кровотечения в течение 30 дней после манипуляции |
||
|
Высокий (более 2 %) |
Средний (0—2 %) |
Низкий (близок к 0 %) |
|
Операции на аорте |
Торакоскопическая радиочастотная абляция |
Имплантация кардиовертера-дефибриллятора |
|
Протезирование или пластика клапанов сердца |
Стентирование коронарных сосудов |
Каротидная эндероартериоэк-томия |
|
Коронарное шунтирование |
Эндопротезирование крупных суставов |
Коронарография |
Нарушение гемостаза может привести к чрезмерному кровотечению или тромбообра-зованию. Кроме хирургического фактора на гемостаз могут влиять и другие интраоперационные факторы (табл. 2) [1; 2].
Таблица 2. Факторы, влияющие на нарушение гемостаза
Table 2. Factors influencing hemostasis disorders
|
Фактор |
Основные причины |
|
Потеря крови |
Расслоение сосудов приводит к кровопотере, что, в свою очередь, может привести к нарушению гемостаза |
|
Гемодилюция |
Замещение большого объема жидкости может привести к гемодилюции и дилюционной коагулопатии |
|
Приобретенная дисфункция тромбоцитов |
Функция тромбоцитов может быть изменена экстра корпоральными схемами, например схемами искусственного кровообращения и т. д. |
|
Потребление тромбоцитов и факторов свертывания крови |
Потребление факторов свертывания крови и тромбоцитов может происходить внутри экстракорпоральных контуров из-за сильного кровотечения и/или активации каскада свертывания крови |
|
Активация фибринолитических и воспалительных путей |
Травма тканей приводит к воспалительным и гемостатическим изменениям |
|
Гипотермия |
Низкая температура окружающей среды в операционной, активное охлаждение пациента |
|
Эмболические события |
Тромбо-, воздушная или жировая эмболия могут возникнуть во время операции и привести к ишемическому и геморрагическому поражению |
Управление вышеуказанными факторами и использование стратегии интраоперационного кровосбережения позволяет нивелировать негативное действие этих факторов.
Оценка рисков, связанных с индивидуальным состоянием пациента Предоперационная анемия как независимый фактор риска
По данным исследования, проведенного с 1990 по 2019 г. более чем в 200 странах, глобальная распространенность анемии среди всех возрастов составила 24,3%. Наиболее распространенными причинами в 2021 г. были алиментарный дефицит железа, гемоглобинопатии и гемолитические анемии. В этом же исследовании анемия в Российской Федерации оценена в 13—16 % [24]. Согласно данным Росстата, по состоянию на 2023 г., распространенность анемии в Российской Федерации составляет 961 на 100 000 человек [25].
В исследовании «Эвкалипт» оценивали распространенность анемии на территории России у лиц в возрасте ≥ 65 лет. Обследовав более 4 тыс. человек в возрасте от 65 до 107 лет, проживающих в 11 регионах Российской Федерации, пришли к выводу, что распространенность анемии у пожилых людей составила 23,9 % [26].
По данным Болотовой и соавт. железодефицитная анемия составляет 70—80 % от всех анемий. Дефицит железа с анемией или без нее выявляется в 43—100 % случаев у пациентов с хронической сердечной недостаточностью [27].
Распространенность послеоперационной анемии может достигать 90 % у пациентов, перенесших обширное хирургическое вмешательство, и более чем в двух третях случаев будет диагносцироваться ЖДА. Она является негативным прогностическим фактором при хронической сердечной недостаточности, связанной с прогрессированием заболевания, снижением качества жизни и увеличением смертности от сердечно-сосудистых заболеваний. Если нет противопоказаний, можно начать пероральную терапию препа- ратами железа и оценить состояние пациента по показателям гемоглобина и железа; частота мониторинга и продолжительность терапии должны зависеть от основного состояния и конкретных целей лечения. В случае анемии тяжелой степени, непереносимости пероральной терапии, дефицита времени для подготовки к операции можно рассмотреть возможность внутривенного введения препаратов железа в соответствующих дозах [28].
Особую клиническую задачу составляют обследование и маршрутизация пациентов с анемией перед плановым хирургическим вмешательством (рис. 3) [29].
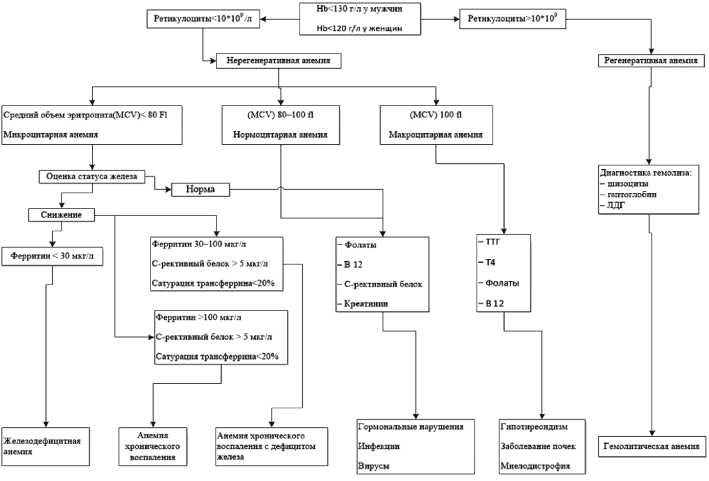
Рис. 3. Диагностика предоперационной анемии
Fig. 3. Diagnosis of preoperative anemia
Как уже отмечалось, предоперационная анемия значительно влияет на развитие осложнений и увеличение летальности в кардиохирургии. Так, в ряде работ авторы пришли к выводу о том, что предоперационная анемия ассоциирована с увеличением сроков госпитализации, времени пребывания и частоты повторных поступлений в отделения интенсивной терапии, повышенным риском смертности. Пациенты с предоперационной анемией, перенесшие плановое хирургическое вмешательство, с большей вероятностью получат компоненты аллогенной крови даже при незначительной периоперационной кровопотере [30—32].
Увеличение продолжительности жизни привело к росту количества хирургических вмешательств у пожилых людей. Пожилые пациенты часто принимают комбинированную лекарственную терапию, изменяющую реологические свойства крови. Множественные сопутствующие заболевания, снижение физиологического резерва подвергают пожилых пациентов повышенному риску во время операции [33; 34].
Один из лучших способов прогнозирования хирургического кровотечения — тщательный сбор анамнеза пациента и его семьи, а также физикальное обследование, направленное на выявление нарушений гемостаза. Обследование должно быть проведено в сроки, чтобы его результаты были актуальны к моменту начала проведения операции, а оставшегося времени хватило для коррекции выявленных отклонений [35]. Исследование индивидуального и семейного анамнеза включает расспрос о хронических заболеваниях, наследственных или приобретенных нарушениях гемостаза, сосудистых или анатомических аномалиях, заболеваниях, вызывающих нарушения гемостаза.
При опросе по поводу предыдущих кровотечений следует избегать вопросов, на которые можно ответить односложно. Стандартизация вопросов пациентам может помочь врачам получить более точную оценку риска и предотвратить вариативность на практике (табл. 3). Важно расспросить женщин о гинекологическом и акушерском анамнезе, включая любые послеродовые кровотечения. Обильное менструальное кровотечение может восприниматься женщиной как нормальное, если у нее было обильное менструальное кровотечение во время менархе или обильное менструальное кровотечение наблюдается у других женщин в семье [36].
Таблица 3. Примеры вопросов, которые могут указывать на склонность к кровотечениям
Table 3. Examples of questions that may indicate a risk of bleeding
|
Тема |
Вопросы |
|
Анамнез пациента |
Пожалуйста, расскажите обо всех ваших медицинских проблемах. Говорили ли вам когда-нибудь, что у вас заболевание печени, почек или крови? Были ли у кого-либо из ваших ближайших или дальних родственников когда-либо проблемы с обильным кровотечением? Есть ли у вас патологии суставов? |
|
Спонтанное кровотечение |
Мучают ли вас частые носовые кровотечения? Была ли у вас когда-нибудь кровь в стуле или моче? Появляются ли у вас большие синяки в необычных местах даже при отсутствии очевидной травмы? Были ли у вас раньше кровотечения в мышцах или суставах? |
|
Кровотечение, связанное с проведением медицинского вмешательства |
Какие операции у вас были? Были ли после них длительные кровотечения? Было ли у вас длительное кровотечение после небольшой раны или пореза? Вам когда-нибудь удаляли зубы? Были ли у вас какие-либо незначительные процедуры, такие как биопсия кожи или колоноскопия/бронхоскопия с биопсией? Было ли кровотечение после стоматологических или незначительных процедур, если да, то было ли оно немедленным или отсроченным? Вам 叩 иходилось обращаться за медицинской помощью из-за кровотечения? Вам делали переливание крови? Было ли у кого-либо из родственников обильное кровотечение после операции или удаления зубов? |
|
Анемия или дефицит железа |
Требовались ли вам когда-нибудь переливание крови или терапия железом? Вам когда-нибудь говорили, что у вас анемия или дефицит железа? |
|
Лекарственные препараты |
Какие лекарства вы принимаете? Принимали ли вы аспирин или другие обезболивающие в течение последних 10 дней? Принимаете ли вы безрецептурные лекарства, БАДы или растительные 叩 е-параты? |
Структурированные, подробные вопросы могут помочь врачам получить более точную оценку риска и предотвратить вариативность на практике (табл. 4).
Таблица 4. Ограничения по сбору анамнеза предыдущих кровотечений
Table 4. Limitations on gathering the anamneses of previous bleedings
|
Ограничивающий фактор |
Описание |
Стратегии оптимизации выявления рисков |
|
Неэффективные вопросы медицинских работников |
Не 叩 авильные вопросы могут привести к тому, что необходимая информация будет упущена, что приведет к неадекватному анамнезу кровотечений |
Задавая структурированные, подробные вопросы, вы получите более релевантные и точные ответы |
|
Субъективность ответов пациента |
Типичным примером является ситуация, когда пациент заявляет, что у него не было хирургического анамнеза, но он пропустил экстракцию зубов или тонзиллэктомию. Пациенты могут помнить об этих процедурах, но не считают перенесенное ими кровотечение чрезмерным, поскольку у них нет других оснований для сравнения |
В таких ситуациях могут помочь хорошо структурированные вопросы, а также тщательный сбор анамнеза. Использование шкал оценки кровотечения также может быть полезным, если есть какие-либо опасения по поводу наследственных нарушений свертываемости крови |
|
Неспровоцирован-ноcть пациента |
Пациент с легким наследственным нарушением свертываемости крови может ранее не сталкиваться с чрезмерным кровотечением. Однако в этих случаях информативным будет положительный семейный анамнез кровотечений |
Расс 叩 осы о семейном анамнезе 叩 о-блем с кровотечением могут помочь выявить любые потенциально невы-явленные наследственные нарушения свертываемости крови |
|
Приобретенное расстройство |
Проведенные хирургические процедуры в прошлом без сопутствующего кровотечения не исключают приобретенного позднее нарушения гемостаза |
Расспросы о текущих симптомах кровотечения и 叩 оведение тщательного медицинского осмотра с акцентом на признаки кровотечения будут полезны при выявлении пациентов с приобретенными расстройствами |
Шкалы оценки риска кровотечения
Прогнозирование вероятности кровотечения на основе анамнестических данных — сложная задача, поскольку ответы пациентов и их интерпретация клиницистами являются субъективными. Вспомогательным инструментом в данном случае выступают шкалы оценки риска кровотечения. Изначально они были разработаны для выявления пациентов с наследственными нарушениями свертываемости крови, например болезнью Виллебранда. Цель шкал — сокращение ненужных лабораторных исследований, прогнозирование будущего риска кровотечений и информирование о лечении. Они представляют собой стандартизированный опросник, после заполнения которого определяется вероятность нарушения свертываемости крови: чем выше балл, тем она выше. Пациентам с подозрением на наследственное нарушение свертываемости крови потребуется дальнейшее обсле- дование для постановки официального диагноза. Однако общее применение этих инструментов в условиях предоперационной оценки риска кровотечений ограничено, поскольку они не могут идентифицировать пациентов с повышенным риском будущих кровотечений при отсутствии последующего диагноза нарушения свертываемости крови [37].
Существует множество шкал для взрослых и детей, а также для конкретных состояний. Одна из них — шкала Международного общества по тромбозам и гемостазу (ISTH) [38]. Это проверенный инструмент, который позволяет выявить наследственные нарушения, но он не всегда работает в отношении пациентов с приобретенными нарушениями свертываемости крови. Следующие показатели шкалы ISTH указывают на необходимость дальнейшего исследования: мужчины ≥ 4, женщины ≥ 6, дети ≥ 3. Данный опросник также оказался эффективным инструментом для выявления дефектов функции тромбоцитов [38].
Оценка фармакологической терапии
Примерно половина всех пациентов, перенесших вмешательство, регулярно принимают хотя бы один лекарственный препарат, а большинство, особенно пожилые, получают комбинированную терапию препаратами, способными влиять на гемостаз. Поэтому важно собрать полноценный анамнез приема лекарственных препаратов, в том числе отпускаемых без рецепта, биологически активных добавок и тех лекарств, которые пациент принимает нерегулярно или без назначения врача. Полученная информация может изменить план профилактики или лечения кровотечения или запланированного вмешательства [39—41].
Основным риском, связанным с антиагрегантной терапией, является кровотечение. Для пациентов с повышенным риском тромботических осложнений необходимо взвесить соотношение пользы и риска, связанных с отменой этих препаратов, и оценить угрозу кровотечения во время операции. Пациентам может быть назначена как монотерапия, так и комбинированная терапия. Хотя все эти препараты влияют на функцию тромбоцитов, механизм действия и связанный с этим риск кровотечения различаются [42].
Варфарин применяется при широком спектре тромбоэмболических заболеваний для первичной и вторичной профилактики. Хирургическое вмешательство обычно можно провести с минимальным риском кровотечения при уровне МНО 1,5 или менее. Важно соотносить риск тромбоза при прекращении/прерывания антикоагулянтной терапии по сравнению с риском возможного кровотечения [43].
Пероральные антикоагулянты прямого действия (ПАПД) все чаще используются вместо варфарина из-за меньшего количества побочных эффектов и отсутствия необходимости лабораторного мониторинга. Для определения тактики ведения пациентов, получающих ПАПД в периоперационном периоде, важно сопоставить риск развития тромбоза при временном прекращении приема препарата с риском кровотечения [44].
Как и в случае с варфарином, возможно, нет необходимости прекращать прием при выполнении процедур с низким риском кровотечения (см. табл. 1), хотя убедительных доказательств в поддержку этой практики не было установлено. ПАПД за счет быстрого начала действия и короткого периода полувыведения могут быть отменены незадолго до процедуры [45].
ISTH при проведении процедуры с минимальным риском кровотечения рекомендует продолжить прием антикоагулянтов, так чтобы избежать пиковых концентраций препарата в крови в день вмешательства. Если риск кровотечения высок и необходимо временно прекратить прием, решающее значение имеет предоперационная подготовка.
Одной из проблем, вызывающих озабоченность по поводу ПАПД, является обратимость действия. На настоящий момент одобренный реверсивный агент имеется только у дабигатрана [46].
Нестероидные противовоспалительные средства (НПВП), относящиеся к классу неселективных ингибиторов циклооксигеназы 2 (ЦОГ-2), влияют на агрегацию тромбоцитов и повышают риск кровотечений. Многие неселективные ингибиторы ЦОГ-2 можно приобрести без рецепта, поэтому крайне важно, чтобы клиницисты доводили до пациентов, что им необходимо знать про все принимаемые лекарства, а не только отпускаемые по рецепту. У пациентов, перенесших операцию на сердце, прием ацетилсалициловой кислоты можно продолжать до момента операции [47].
Некоторые антидепрессанты, в том числе селективные ингибиторы обратного захвата серотонина (СИОЗС), могут увеличивать риск кровотечения из-за нарушения агрегации тромбоцитов. Риск кровотечения возрастает при одновременном приеме антиагрегантов или НПВП. Следует избегать резкой отмены СИОЗС короткого действия, поскольку это может вызвать синдром отмены [39].
Широкий спектр биологически активных добавок продемонстрировал влияние in vitro на гемостаз. Сообщалось о повышенном риске кровотечения при приеме большого количества дополнительных лекарств, в том числе гинкго, женьшеня, имбиря, витамина Е, зеленого чая, зверобоя, куркумы и рыбьего жира. Прием растительных лекарственных средств рекомендуется прекратить за две недели до операции. Пациентам, недавно перенесшим инсульт или получившим стент с лекарственным покрытием в течение последних 12 месяцев или стент без покрытия в течение последних 6 недель, требуется прекратить терапию за 7—10 дней до операции [48].
Оценка лабораторных показателей
Нарушения функции тромбоцитов не могут быть идентифицированы при помощи общего анализа крови (ОАК) и часто сопровождаются нормальным количеством тромбоцитов. При выявлении тромбоцитопении важно учитывать ее этиологию. Занижение истинного количества может быть результатом агрегации вследствие воздействия или недостаточного количества антикоагулянта (обычно ЭДТА, но иногда цитрата и гепарина). Автоматические анализаторы не дифференцируют скопление тромбоцитов от отдельной клетки. В таких случаях рекомендуется подсчет тромбоцитов по методу Фонио. Скрининг функциональной активности может быть полезен для пациентов, принимающих антиагре-ганты, или с состоявшимися кровотечениями в анамнезе [49; 50].
Рутинное предоперационное использование тестов на коагуляцию не рекомендуется. Эти тесты не предназначены для выявления нарушений коагуляции или прогнозирования кровотечения в периоперационном периоде. Предоперационное тестирование коагуляции является плохим предиктором кровотечения [51; 52].
В работе Raphael и соавт. было показано, что у 97 % пациентов с отклонениями в тестах на коагуляцию кровотечения нет, 70 % пациентов, у которых произошло кровотечение во время операции, имеют нормальные показатели коагуляции. Наличие состоявшегося кровотечения в анамнезе в 12,5 раз более вероятно предсказывает кровотечение во время последующей операции, чем скрининговый тест на коагуляцию [4].
Предоперационная оценка активированного частичного тромбопластинового времени (АЧТВ), протромбинового времени (ПВ), международного нормализованного отношения (МНО) и фибриногена необходима пациентам с нарушениями свертываемости крови, кровотечениями в анамнезе или явными клиническими показаниями. Обычные тесты на коагуляцию, ос面енно МНО, полезны для пациентов, принимающих варфарин или 叩оходя-щих соответствующую терапию, для определения дальнейшей тактики терапии на основе текущих лабораторных результатов [37].
Вязкоэластические тесты, такие как тромбоэластография (TEG ® ) и тромбоэластоме-трия (ROTEM ® ), могут предоставить информацию о кинетике и силе образования сгустка и фибринолизе во время операции, чтобы помочь целенаправленному замещению компонентами крови и мониторингу гемостаза. Их не следует использовать для оценки риска кровотечения перед операцией [50].
Заключение
Предоперационная оценка риска кровотечения — мультимодальная междисциплинарная проблема, требующая пациентоориентированного подхода. Она должна начинаться еще на подготовительном этапе и требует участия врачей первичного звена, кардиологов, хирургов, анестезилогов-реаниматологов, врачей лабораторной диагностики и трансфу-зилогов. Краеугольным камнем является сбор индивидуального и семейного анамнеза. Получение информации, основанной на вовлечении пациента путем задавания наводящих на размышления вопросов, использовании шкал оценки риска кровотечения, анализе данных о предыдущих кровотечениях, подкрепленное данными лабораторных тестов, представляет собой наиболее научный подход к разработке индивидуального плана ведения пациента с риском кровотечения.
Список литературы Предоперационная оценка риска кровотечения у кардиохирургических пациентов
- Antwi-Kusi A, Addison W, Obasuyi BI, Domoyeri P. Preoperative Laboratory Testing by Surgeons: Implication on Anaesthetic Management. International Journal of Clinical Medicine. 2019;10:345-352. https://doi.org/10.4236/ijcm.2019.106027
- Martin SK, Cifu AS. Routine Preoperative Laboratory Tests for Elective Surgery. JAMA. 2017 Aug 8;318(6):567-568. https://doi.org/10.1001/jama.2017.7508
- Guttikonda N, Nileshwar A, Rao M, Sushma TK. Preoperative laboratory testing - Comparison of National Institute of Clinical Excellence guidelines with current practice - An observational study. J Anaesthesiol Clin Pharmacol. 2019 Apr-Jun;35(2):227-230. https://doi.org/10.4103/joacp.JOACP_342_17
- Raphael J, Mazer CD, Subramani S, Schroeder A, Abdalla M, Ferreira R, Roman PE, Patel N, Welsby I, Greilich PE, Harvey R, Ranucci M, Heller LB, Boer C, Wilkey A, Hill SE, Nuttall GA, Palvadi RR, Patel PA, Wilkey B, Gaitan B, Hill SS, Kwak J, Klick J, Bollen BA, Shore-Lesserson L, Abernathy J, Schwann N, Lau WT. Society of Cardiovascular Anesthesiologists Clinical Practice Improvement Advisory for Management of Perioperative Bleeding and Hemostasis in Cardiac Surgery Patients. Anesth Analg. 2019 Nov;129(5):1209-1221. https://doi.org/10.1213/ANE.0000000000004355
- Ebrahim M, Larsen PB, Hannani D, Liest S, Jørgensen LN, Jørgensen HL. Preoperative risk factors including serum levels of potassium, sodium, and creatinine for early mortality after open abdominal surgery: a retrospective cohort study. BMC Surg. 2021 Jan 26;21(1):62. https://doi.org/10.1186/s12893-021-01070-0
- Stierer TL, Collop NA. Preoperative testing and risk assessment: perspectives on patient selection in ambulatory anesthetic procedures. Ambulatory Anesthesia. 2015;2:67-77. https://doi.org/10.2147/AA.S59819
- Rydz N, James PD. The evolution and value of bleeding assessment tools. J Thromb Haemost. 2012 Nov;10(11):2223-9. https://doi.org/10.1111/j.1538-7836.2012.04923.x
- Saour M, Zeroual N, Aubry E, Blin C, Gaudard P, Colson PH. Blood Loss Kinetics During the First 12 Hours After On-Pump Cardiac Surgical Procedures. Ann Thorac Surg. 2021 Apr;111(4):1308-1315. https://doi.org/10.1016/j.athoracsur.2020.06.108
- Shou BL, Aravind P, Ong CS, Alejo D, Canner JK, Etchill EW, DiNatale J, Prokupets R, Esfandiary T, Lawton JS, Schena S. Early Reexploration for Bleeding Is Associated With Improved Outcome in Cardiac Surgery. Ann Thorac Surg. 2023 Jan;115(1):232-239. https://doi.org/10.1016/j.athoracsur.2022.07.037
- Ahmed A, Yehia A, Toema A. A Retrospective Multicenter Experience: Does Packing the Surgical Field Help to Stop Bleeding After Cardiac Surgery. Heart Surg Forum. 2023 Feb 23;26(1):E105-E107. https://doi.org/10.1532/hsf.5323
- Pereira KMFSM, de Assis CS, Cintra HNWL, Ferretti-Rebustini REL, Püschel VAA, Santana-Santos E, Rodrigues ARB, de Oliveira LB. Factors associated with the increased bleeding in the postoperative period of cardiac surgery: A cohort study. J Clin Nurs. 2019 Mar;28(5-6):850-861. https://doi.org/10.1111/jocn.14670
- Newcomb AE, Dignan R, McElduff P, Pearse EJ, Bannon P. Bleeding After Cardiac Surgery Is Associated With an Increase in the Total Cost of the Hospital Stay. Ann Thorac Surg. 2020 Apr;109(4):1069-1078. https://doi.org/10.1016/j.athoracsur.2019.11.019
- Gombocz K, Beledi A, Botos F, Wrana G, Feiler E, Csecs R, Racz Z, Rashed A. Successful combined application of reoperation protocol with target-guided hemostatic therapy for the treatment of severe bleeding in cardiac surgical patients. Orv Hetil. 2020 Aug;161(34):1414-1422. Hungarian (in Hungarian). https://doi.org/10.1556/650.2020.31829
- Elassal AA, Al-Ebrahim KE, Debis RS, Ragab ES, Faden MS, Fatani MA, Allam AR, Abdulla AH, Bukhary AM, Noaman NA, Eldib OS. Re-exploration for bleeding after cardiac surgery: revaluation of urgency and factors promoting low rate. J Cardiothorac Surg. 2021 Jun 7;16(1):166. https://doi.org/10.1186/s13019-021-01545-4
- Купряшов А. А., Самуилова О. В., Самуилова Д. Ш. Бережное отношение к крови больного как приоритетная стратегия в кардиохирургии. Гематология и трансфузиология. 2021;66(3):395-416.
- Klein AA, Chau M, Yeates JA, Collier T, Evans C, Agarwal S, Richards T; UK Cardiac and Vascular Surgery Interventional Anaemia Response (CAVIAR) study team. Preoperative intravenous iron before cardiac surgery: a prospective multicentre feasibility study. Br J Anaesth. 2020 Mar;124(3):243-250. https://doi.org/10.1016/j.bja.2019.11.023
- Ali JM, Wallwork K, Moorjani N. Do patients who require re-exploration for bleeding have inferior outcomes following cardiac surgery? Interact Cardiovasc Thorac Surg. 2019 Apr 1;28(4):613-618. https://doi.org/10.1093/icvts/ivy285
- Shehata N, Whitlock R, Fergusson DA, Thorpe KE, MacAdams C, Grocott HP, Rubens F, Fremes S, Lellouche F, Bagshaw S, Royse A, Rosseel PM, Hare G, Medicis E, Hudson C, Belley-Cote E, Bainbridge D, Kent B, Shaw A, Byrne K, Syed S, Royse CF, McGuiness S, Hall J, Mazer CD. Transfusion Requirements in Cardiac Surgery III (TRICS III): Study Design of a Randomized Controlled Trial. J Cardiothorac Vasc Anesth. 2018 Feb;32(1):121-129. https://doi.org/10.1053/j.jvca.2017.10.036
- Estcourt LJ, Roberts DJ. Six-month outcomes after restrictive or liberal transfusion for cardiac surgery (TRICS III trial). Transfus Med. 2019 Apr;29(2):77-79. https://doi.org/10.1111/tme.12596
- Shehata N, Mistry N, da Costa BR, Pereira TV, Whitlock R, Curley GF, Scott DA, Hare GMT, Jüni P, Mazer CD. Restrictive compared with liberal red cell transfusion strategies in cardiac surgery: a meta-analysis. Eur Heart J. 2019 Apr 1;40(13):1081-1088. https://doi.org/10.1093/eurheartj/ehy435
- Shander A, Hardy JF, Ozawa S, Farmer SL, Hofmann A, Frank SM, Kor DJ, Faraoni D, Freedman J; Collaborators. A Global Definition of Patient Blood Management. Anesth Analg. 2022 Sep 1;135(3):476-488. https://doi.org/10.1213/ANE.0000000000005873
- Levi M, Sivapalaratnam S. Coagulation and anticoagulation in the intraoperative setting. Transfus Apher Sci. 2019 Aug;58(4):386-391. https://doi.org/10.1016/j.transci.2019.06.013
- Spyropoulos AC, Brohi K, Caprini J, Samama CM, Siegal D, Tafur A, Verhamme P, Douketis JD; SSC Subcommittee on Perioperative and Critical Care Thrombosis and Haemostasis of the International Society on Thrombosis and Haemostasis. Scientific and Standardization Committee Communication: Guidance document on the periprocedural management of patients on chronic oral anticoagulant therapy: Recommendations for standardized reporting of procedural/surgical bleed risk and patient-specific thromboembolic risk. J Thromb Haemost. 2019 Nov;17(11):1966-1972. https://doi.org/10.1111/jth.14598
- Safiri S, Kolahi AA, Noori M, Nejadghaderi SA, Karamzad N, Bragazzi NL, Sullman MJM, Abdollahi M, Collins GS, Kaufman JS, Grieger JA. Burden of anemia and its underlying causes in 204 countries and territories, 1990-2019: results from the Global Burden of Disease Study 2019. J Hematol Oncol. 2021 Nov 4;14(1):185. https://doi.org/10.1186/s13045-021-01202-2
- Смелов П. А. Здравоохранение в России. М., Статистический сборник Росстат, 2021.
- Ховасова Н. О., Воробьева Н. М., Ткачева О. Н., Котовская Ю. В., Наумов А. В., Селезнева Е. В., Овчарова Л. Н. Распространенность анемии и ее ассоциации с другими гериатрическими синдромами у лиц старше 65 лет: данные российского эпидемиологического исследования ЭВКАЛИПТ. Терапевтический архив. 2022;94(1):24-31.
- Болотова Е. В., Крутова В. А., Дудникова А. В., Просолупова Н. С., Сороченко А. А. Актуальные вопросы диагностики, лечения и профилактики железодефицитной анемии : учебное пособие. Краснодар, Кубанский гос. мед. ун-т, 2022. 144 с.
- Menon A, Warnakulasuriya SR. Perioperative anaemia and iron deficiency. Br J Hosp Med (Lond). 2022 Aug 2;83(8):1-3. https://doi.org/10.12968/hmed.2022.0040
- Алгоритм ведения пациентов с железодефицитной анемией на этапе оказания ПМСП. Под ред. О. М. Драпкиной. М., Видокс, 2021.
- Quarterman C, Shaw M, Hughes S, Wallace V, Agarwal S. Anaemia in cardiac surgery - a retrospective review of a centre’s experience with a pre-operative intravenous iron clinic. Anaesthesia. 2021 May;76(5):629-638. https://doi.org/10.1111/anae.15271
- Evans CR, Jones R, Phillips G, Greene G, Phillips M, Morris-Clarke R. Observational study of pre-operative intravenous iron given to anaemic patients before elective cardiac surgery. Anaesthesia. 2021 May;76(5):639-646. https://doi.org/10.1111/anae.15396
- Klein AA, Chau M, Yeates JA, Collier T, Evans C, Agarwal S, Richards T; UK Cardiac and Vascular Surgery Interventional Anaemia Response (CAVIAR) study team. Preoperative intravenous iron before cardiac surgery: a prospective multicentre feasibility study. Br J Anaesth. 2020 Mar;124(3):243-250. https://doi.org/10.1016/j.bja.2019.11.023
- Han B, Li Q, Chen X. Effects of the frailty phenotype on post-operative complications in older surgical patients: a systematic review and meta-analysis. BMC Geriatr. 2019 May 24;19(1):141. https://doi.org/10.1186/s12877-019-1153-8
- Bennett J, Fung D, Hodson R, Agarwal A. Implementation of a Surgical Liaison Service for Elderly Patients: A Single Unit Experience. Geriatrics (Basel). 2019 Jul 28;4(3):46. https://doi.org/10.3390/geriatrics4030046
- Fasulo MR, Biguzzi E, Abbattista M, Stufano F, Pagliari MT, Mancini I, Gorski MM, Cannavò A, Corgiolu M, Peyvandi F, Rosendaal FR. The ISTH Bleeding Assessment Tool and the risk of future bleeding. J Thromb Haemost. 2018 Jan;16(1):125-130. https://doi.org/10.1111/jth.13883
- Elbatarny M, Mollah S, Grabell J, Bae S, Deforest M, Tuttle A, Hopman W, Clark DS, Mauer AC, Bowman M, Riddel J, Christopherson PA, Montgomery RR; Zimmerman Program Investigators; Rand ML, Coller B, James PD. Normal range of bleeding scores for the ISTH-BAT: adult and pediatric data from the merging project. Haemophilia. 2014 Nov;20(6):831-5. https://doi.org/10.1111/hae.12503
- Schmidt PC, Kamdar NS, Erekson E, Swenson CW, Uppal S, Morgan DM. Development of a Preoperative Clinical Risk Assessment Tool for Postoperative Complications After Hysterectomy. J Minim Invasive Gynecol. 2022 Mar;29(3):401-408.e1. https://doi.org/10.1016/j.jmig.2021.10.008
- Adler M, Kaufmann J, Alberio L, Nagler M. Diagnostic utility of the ISTH bleeding assessment tool in patients with suspected platelet function disorders. J Thromb Haemost. 2019 Jul;17(7):1104-1112. https://doi.org/10.1111/jth.14454
- Sousa-Uva M, Milojevic M, Head SJ, Jeppsson A. The 2017 EACTS guidelines on perioperative medication in adult cardiac surgery and patient blood management. Eur J Cardiothorac Surg. 2018 Jan 1;53(1):1-2. https://doi.org/10.1093/ejcts/ezx448
- Pérez-Jover V, Mira JJ, Carratala-Munuera C, Gil-Guillen VF, Basora J, López-Pineda A, Orozco-Beltrán D. Inappropriate Use of Medication by Elderly, Polymedicated, or Multipathological Patients with Chronic Diseases. Int J Environ Res Public Health. 2018 Feb 10;15(2):310. https://doi.org/10.3390/ijerph15020310
- Cardiac Society of Australia and New Zealand. Guidelines for the management of antiplatelet therapy in patients with coronary stents undergoing non-cardiac surgery. Heart Lung Circ. 2010 Jan;19(1):2-10. https://doi.org/10.1016/j.hlc.2009.10.008
- Primary Panel:; Bainey KR, Marquis-Gravel G, Belley-Côté E, Turgeon RD, Ackman ML, Babadagli HE, Bewick D, Boivin-Proulx LA, Cantor WJ, Fremes SE, Graham MM, Lordkipanidzé M, Madan M, Mansour S, Mehta SR, Potter BJ, Shavadia J, So DF, Tanguay JF, Welsh RC, Yan AT; Secondary Panel:; Bagai A, Bagur R, Bucci C, Elbarouni B, Geller C, Lavoie A, Lawler P, Liu S, Mancini J, Wong GC. Canadian Cardiovascular Society/Canadian Association of Interventional Cardiology 2023 Focused Update of the Guidelines for the Use of Antiplatelet Therapy. Can J Cardiol. 2024 Feb;40(2):160-181. https://doi.org/10.1016/j.cjca.2023.10.013
- Tran HA, Chunilal SD, Tran H. An update of consensus guidelines for warfarin reversal. Med J Aust. 2014 Feb 3;200(2):82. https://doi.org/10.5694/mja13.10685
- Douketis JD, Spyropoulos AC, Duncan J, Carrier M, Le Gal G, Tafur AJ, Vanassche T, Verhamme P, Shivakumar S, Gross PL, Lee AYY, Yeo E, Solymoss S, Kassis J, Le Templier G, Kowalski S, Blostein M, Shah V, MacKay E, Wu C, Clark NP, Bates SM, Spencer FA, Arnaoutoglou E, Coppens M, Arnold DM, Caprini JA, Li N, Moffat KA, Syed S, Schulman S. Perioperative Management of Patients With Atrial Fibrillation Receiving a Direct Oral Anticoagulant. JAMA Intern Med. 2019 Nov 1;179(11):1469-1478. https://doi.org/10.1001/jamainternmed.2019.2431
- Hoffmann C, Leven C, Le Mao R, De Moreuil C, Lacut K. Direct oral anticoagulants: In which indications? Which one to prescribe? For or against their use in frail patients and in atypical cases? Which monitoring and management haemorrhage complications? Rev Med Interne. 2020 Sep;41(9):598-606 (in French). https://doi.org/10.1016/j.revmed.2020.05.026
- Jarrett JB, Gimbar RP. Idarucizumab (Praxbind) for Dabigatran (Pradaxa) Anticoagulant Reversal. Am Fam Physician. 2017 Jun 15;95(12):798-800
- Mahboubi-Rabbani M, Zarei R, Baradaran M, Bayanati M, Zarghi A. Chalcones as Potential Cyclooxygenase-2 Inhibitors: A Review. Anticancer Agents Med Chem. 2024;24(2):77-95. https://doi.org/10.2174/0118715206267309231103053808
- Stefanini GG, Vicenzi M. Stent thrombosis: prevention is the only effective treatment. EuroIntervention. 2020 Jul 17;16(4):e279-e281. https://doi.org/10.4244/EIJV16I4A48
- Jones S, Achuthan R, Ooi S, Kim B. Audit of routine preoperative blood test requests for patients undergoing elective breast surgery: Less is more. J Perioper Pract. 2021 Oct;31(10):379-385. https://doi.org/10.1177/1750458920952755
- Kietaibl S, Ahmed A, Afshari A, Albaladejo P, Aldecoa C, Barauskas G, De Robertis E, Faraoni D, Filipescu DC, Fries D, Godier A, Haas T, Jacob M, Lancé MD, Llau JV, Meier J, Molnar Z, Mora L, Rahe-Meyer N, Samama CM, Scarlatescu E, Schlimp C, Wikkelsø AJ, Zacharowski K. Management of severe peri-operative bleeding: Guidelines from the European Society of Anaesthesiology and Intensive Care: Second update 2022. Eur J Anaesthesiol. 2023 Apr 1;40(4):226-304. https://doi.org/10.1097/EJA.0000000000001803
- Liontos L, Fralick M, Longmore A, Hicks LK, Sholzberg M. Bleeding Risk Using INR/aPTT Pre-Surgery: Systemtic Review (BRUISR). Blood. 2017;130:4654-4654. https://doi.org/10.1182/BLOOD.V130.SUPPL_1.4654.4654
- Haas T, Fries D, Tanaka KA, Asmis L, Curry NS, Schöchl H. Usefulness of standard plasma coagulation tests in the management of perioperative coagulopathic bleeding: is there any evidence? Br J Anaesth. 2015 Feb;114(2):217-24. https://doi.org/10.1093/bja/aeu303


