Применение дренирования панкреатикоеюноанастомоза после гастропанкреатодуодеональной резекции по поводу злокачественных образованиях поджелудочной железы и большого дуоденального сосочка
Автор: Ивануса С.Я., Лазуткин М.В., Шершень Д.П., Акиев Р.М., Елисеев А.В., Попов А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Онкология
Статья в выпуске: 3 (81), 2022 года.
Бесплатный доступ
Введение. На сегодняшний день успех лечения новообразований панкреатодуоденальной зоны в значительной мере обусловлен хирургическим этапом. Частота несостоятельности панкреатодигестивного анастомоза после выполнения гастропанкреатодуоденальной резекции (ГПДР) составляет от 1 % до 58 % [1]. Цель. Улучшить результаты хирургического лечения больных после ГПДР путём применения дренирования панкреатикоеюнонастомоза (ПЕА). Материалы и методы. Проанализированы результаты 32 гастропанкреатодуоденальных резекций. В 29 случаях операции выполнены по поводу злокачественных опухолей головки поджелудочной железы, что составило 90,6 %. По поводу рака большого дуоденального сосочка выполнено 3 оперативных вмешательства. По классификации TNM (2010 г.) I и II стадия злокачественной опухоли выявлена у 75 %, а III стадия диагностирована в 25 % наблюдениях. Декомпрессию панкреатоеюноанастомоза и гепатикоеюноанастомоза (ГЕА) производили с помощью дренирования главного панкреатического протока и печеночного протока по Фелькеру 27 пациентам (84,4 %). В пяти случаях выполнено наложение инвагинационного ПЕА (15,6 %). Результаты. У шести (23,6 %) пациентов, перенесших ГПДР с дренированием панкреатического протока, несостоятельность ПЕА диагностирована в ранние сроки, с формированием панкреатической фистулы по типу «В». Из пяти пациентов, которым не было выполнено дренирование, неосложненное течение послеоперационного периода было у 3 пациентов. В двух (40 %) наблюдениях развилась фистулы «С» типа. Заключение. Улучшение послеоперационных результатов ГПДР удаётся достичь путём дренирования панкреатического протока.
Гастропанкреатодуоденальная резекция, панкреатикоеюноанастомоз, злокачественные образования поджелудочной железы, большой дуоденальный сосочек, дренирование панкреатического протока
Короткий адрес: https://sciup.org/142236444
IDR: 142236444 | УДК: 61.617-089 | DOI: 10.17238/2072-3180-2022-3-9-14
The application of pancreaticoejunoanastomosis drainage after gastropancreatoduodenal resection for malignant formations of the pancreas and large duodenal papilla
Introduction. Currently, the success of the treatment of neoplasms of the pancreatoduodenal zone is largely due to the surgical stage. The incidence of pancreatodigestive anastomosis failure after performing gastropancreatoduodenal resection (GPDR) ranges from 1% to 58%. The purpose of the study. To improve the results of surgical treatment of patients after GPDR by using long-term skeletal drainage of pancreatoejunonastomosis. Materials and methods. The experience of the general surgery clinic is 32 gastropancreatoduodenal resections. In 29 cases, the operation was performed for malignant tumors of the head of the pancreas, which amounted to 90,6 %. For cancer of the large duodenal papilla, 3 surgical interventions were performed. According to the TNM classification (2010), stage I and II of a malignant tumor were detected in 75 %, and stage III was diagnosed in 25 % of cases. Decompression of pancreatic and biliodigestive anastomoses was performed using long-term skeletal drainage of the main pancreatic duct by Felker in 27 patients (84,4 %). In five cases, an ivagination PA was applied (15,6 %). Treatment results. In 6 (23,6 %) patients who underwent GPDR with long-term skeleton drainage, the failure of PEA was diagnosed early, with the formation of pancreatic fistula type "B". Of the 5 patients who did not undergo skeleton drainage, 3 patients had uncomplicated postoperative period. In two (40 %) observations, "C" type fistulas developed. Conclusion. Improvement of postoperative GPDR results can be achieved through the use of long-term frame drains.
Текст научной статьи Применение дренирования панкреатикоеюноанастомоза после гастропанкреатодуодеональной резекции по поводу злокачественных образованиях поджелудочной железы и большого дуоденального сосочка
На сегодняшний день успех лечения новообразований панкреатодуоденальной зоны в значительной мере обусловлен хирургическим этапом. Вмешательства на поджелудочной железе (ПЖ) традиционно относятся к хирургии крайне высокого операционного риска, что во многом связано со значимой частотой таких осложнений, как несостоятельность панкреатикоею-ноанастомоза, панкреатические фистулы, острый панкреатит, перитонит. Частота несостоятельности панкреатодигестивного анастомоза после выполнения гастропанкреатодуоденальной резекции (ГПДР) составляет от 1% до 58 % [1, 2, 3].
В 2005 году международной группой по изучению панкреатических свищей (ISGPF) было сформулировано определение панкреатической фистулы. Панкреатической фистулой считается отделяемое по дренажам на третьи сутки после операции, с уровнем амилазы в три раза превышающем ее показатель в крови. Выделяют 3 типа фистулы: А, В, С [4]. Панкреатическая фистула класса А – это бессимптомная фистула, характеризующаяся только повышением уровня амилазы дренажной жидкости. Клинических проявлений, каких-либо осложнений нет, дополнительных методов лечения данный тип не требует. Тип В клинически характеризуется повышением температуры тела, появлением локальных болей в животе, тошноты, рвоты, чаще всего отмечается лейкоцитоз. Тип С, наиболее тяжелый, характеризуется развитием перитонита или сепсиса и требует повторной открытой операции с целью санации очагов инфекции [5]. В 2016 году ISGPF была пересмотрена классификация панкреатических фистул. В современной классификации определение панкреатической фистулы тип А заменено на «biochemical leak» (ферментативное просачивание (ФП) [6].
Разработка множества технологических приемов и внедрение в клиническую практику различных медикаментозных способов профилактики послеоперационных осложнений не привели к существенному снижению частоты данного осложнения. Основным патогенетическим механизмом развития несостоятельности является местно-деструктивное действие ферментов поджелудочной железы в зоне линии шва, дальнейшее скопление сока железы с развитием зон воспаления и некрозов как в самой поджелудочной железе, так и в окружающих тканях, нарушение перфузии ткани ПЖ [4]. При наличии панкреатической фистулы формирование инфицированных жидкостных скоплений возникает в 1–17 %, кровотечений – в 3–13 %, летальность достигает 28 % случаев [3].
На протяжении эволюционного периода становления хирургии поджелудочной железы развивалась техника реконструктивного этапа резекционных методик. В 70–80 годы ХХ века было предложено множество способов выключения поджелудочной железы из пищеварительного тракта. Среди них такие как: ушивание наглухо культи ПЖ, формирование наружной вирсунгостомы, пломбировка главного панкреатического протока (ГПП) различными материалами [5]. Однако в связи с неэффективностью этих методик и развитием не менее тяжелых осложнений такие попытки были оставлены. Современная концепция реконструктивного этапа направлена на выбор способа включения культи поджелудочной железы в пищеварение. Из множества вариантов, наиболее перспективными признаны различные варианты анастомозов: инва-гинационный панкреатоеюноанастомоз (ПЕА) с антирефлюкс-ными свойствами, ПЕА на дренаже (наружном, потерянном), продольный ПЕА, концепетлевой (телескопический) ПЕА, панкреатогастроанастомоз (ПГА) и другие [2, 6].
Активное изучение и ретроспективный анализ результатов резекций поджелудочной железы обусловлены тем, что безопасность панкреато-гастроинтерстинальной реконструкции является одной из ведущих проблем хирургии поджелудочной железы [7, 8].
Цель исследования. Оценить результаты хирургического лечения больных после ГПДР с применением дренирования панкреатикоеюнонастомоза.
Материалы и методы
Проанализированы результаты 32 гастропанкреатодуоде-нальных резекций. В 29 случаях операции выполнены по поводу злокачественных опухолей головки поджелудочной железы, что составило 90,6%. По поводу рака большого дуоденального сосочка выполнено 3 оперативных вмешательства.
На восстановительном этапе гастропанкреатодуоденальной резекции все анастомозы формировали последовательно на одной петле тощей кишки, которую проводили через окно в брыжейке поперечной ободочной кишки. Первым формировали панкреатокишечное соустье, которое было проксимальным. Формировался анастомоз по типу «конец в бок», отступя от культи тонкой кишки 10 см, между культей поджелудочной железы и тонкой кишкой. Задняя полуокружность культи ПЖ укрывается одиночными узловыми атравматическими швами 3/0 стенкой тонкой кишки. Напротив панкреатического протока выполняли энтеротомию, диаметром равную диаметру панкреатического протока. Одиночными узловыми атравматическими швами 3/0 формируют заднюю стенку анастомоза. После чего в панкреатический проток на 5–7 см вводился дренаж диаметром, соответствующим диаметру протока, с отверстиями, в просвете протока. На установленном дренаже формировалась передняя стенка панкреатикоеюноанастомоза одиночными узловыми швами. Передняя полуокружность культи ПЖ одиночными узловыми швами укрывалась тонкой кишкой. В область анастомоза устанавливался контрольный ПВХ дренаж для оценки количества и выполнения биохимического исследования отделяемого (рис. 1). Затем последовательно выполняли гепатикоеюноанастомоз по Фелькеру и энтероэнетроанастомоз (рис. 1).
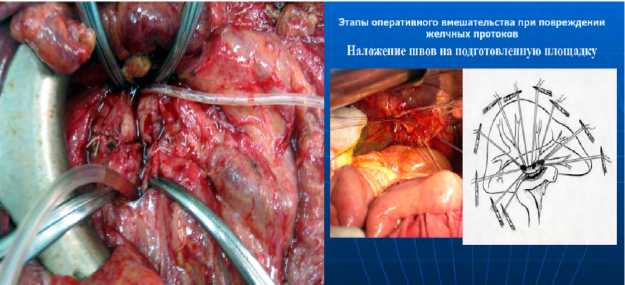
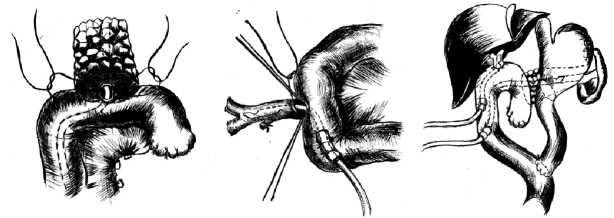
Рис. 1. Наложение панкреатико- и холедохо-энтероанастомозов
Fig. 1. Superposition of pancreatic- and choledocho-enteroanastomoses
Установленные дренажи в панкреатикоеюноанастомоз и гепатикоеюноанастомоз выводили через петлю тонкой кишки в правом подреберье.
Дренирование ПЕА и ГЕА позволяло обеспечить наружный отток панкреатического сока и желчи в условиях послеоперационного отека тканей, контролировать эффективность антисекреторной терапии, осуществлять ранний контроль состоятельности ПЕА и ГЕА, косвенно выполнять оценку функционирования отводящей кишки, ПЕА и ГЕА.
Несостоятельность ПЕА анастомоза диагностировали на основании критериев Международной группы по изучению панкреатических фистул (ISGPF).
Проводился мониторинг количества отделяемого по дренажу через ПЕА и биохимическое исследование отделяемого по дренажу установленного в проекции ПЕА.
На 3-е, 6-е сутки после операции выполнялось исследование уровня амилазы по дренажу из брюшной полости (рис. 2). При отсутствии увеличения уровня амилазы, в три раза превышающий ее показатель в крови и клинической картины, выполнялась этапная фистулография на 7-е сутки. В случае отсутствия несостоятельность ПЕА, отсутствия гипертензии в отводящей кишке, дренаж удалялся на 10-е сутки.
Основными диагностическими признаками несостоятельность ПЕА являлись: увеличение уровня амилазы отделяемого по дренажу из брюшной полости, в три раза превышающий ее показатель в крови, снижение или прекращение поступления желчи и панкреатического секрета по каркасным дренажам, появление лейкоцитоза, появление свободной или отграниченной жидкости в зоне наложенных дигестивных анастомозов по данным компьютерного и ультрасонографического контроля.
При появлении данных признаков выполнялась фистулография через каркасный дренаж.
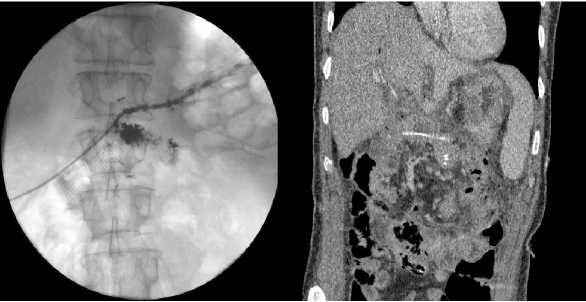
Рис. 2. Каркасное дренирование панкреатического протока
Fig. 2. Carcass drainage of the pancreatic duct
Так, при «ферментативной утечке» (n=2), отсутствовали рентгенологические признаки значимого распространения контрастного препарата за пределы главного панкреатического протока и камеры анастомоза (рис. 3).
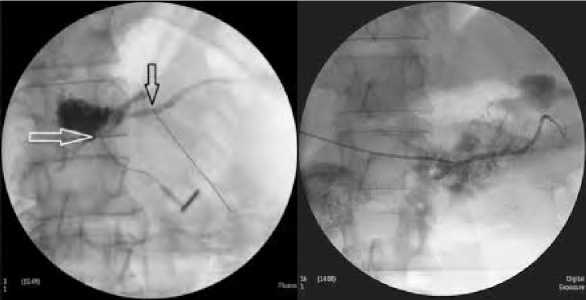
Рис. 3. Панкреатическая фистулография. Стрелками обозначены панкреатический проток и зона несостоятельности анастомоза Fig. 3. Pancreatic fistulography. The arrows indicate the pancreatic duct and the zone of anastomosis failure
Проводилась наблюдательная выжидательная тактика, удаление дренажа осуществлялось после прекращения выделения панкреатического сока по нему в течение 7–10 дней.
Консервативная терапия оказалась эффективна в 6 наблюдениях (94,5 %) и заключалась в применении аналогов соматостатина в дозировке 1000 мг в сутки с переводом на парентеральное питание. Эффективность антисекреторной терапии контролировали по дебету панкреатического секрета, отделяемого по дренажу.
При фистуле типа «В» (n=4) использовались малоинвазивные технологии для пункционного дренирования скоплений жидкости, производилась смена антибактериальных препаратов, пациенты переводились на парентеральное питание (рис. 4). Применение парентерального питания способствовало компен- сации нарушений трофического статуса, снижению количества сока поджелудочной железы, попадающего в пищеварительный тракт в результате снижения гуморальной стимуляции, и приводило к снижению количества секрета поджелудочной железы, выделяющегося через фистулу. Проводились этапные фистулографии каждые 7 дней. В случае закрытия фистулы, выполнялось удаление дренажа на 3-е сутки после фистулографии.
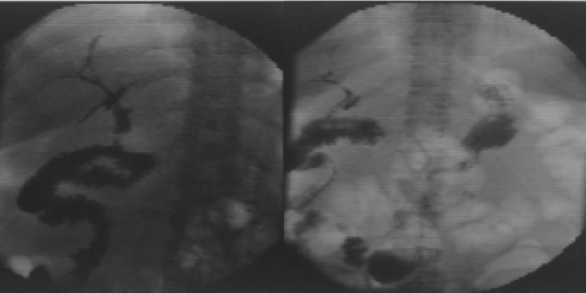
Рис. 4. А) Фистулография через каркасный дренаж состоятельного билиодигестивного анастомоза Б) Панкреатическая фистулография на фоне несостоятельности ПЕА
Fig. 4. A) Fistulography through the frame drainage of a well-established biliodigestive anastomosis B) Pancreatic fistulography against the background of the insolvency of the PEA
Несостоятельность панкреатодигестивного анастомоза, которая ассоциирована с септическим состоянием больного, скоплением жидкости, которое невозможно дренировать с помощью миниинвазивных технологий, продолжающееся аррозивное кровотечение, перфорация полого органа являются показаниями к повторной операции. Именно необходимость релапаротомии является критерием фистулы типа С. Данный тип несостоятельности наблюдался у двух пациентов после ГПДР с применением инвагинационного анастомоза. Отсутствие каркасного дренажа исключило возможность раннего выявления несостоятельности ПЕА. В связи с этим диагноз устанавливался на основании компьютерной томографии и последующих релапаротомий в более поздние сроки (рис. 5).
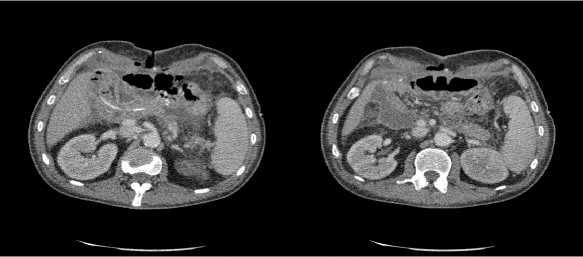
Рисунок 5. Признаки несостоятельности ПЕА по данным компьютерной томографии
Fig. 5. Signs of insolvency of the PEA according to computed tomography.
Повторные операции у данной группы больных обладают высокой летальностью, достигающей 80%. Однако среди наших наблюдений летальных исходов не было.
Результаты
Таким образом, среди 27 пациентов, перенесших ГПДР с длительным каркасным дренированием, несостоятельность ПЕА диагностирована в ранние сроки за счет имеющегося фистульного дренажа в 6 (23,6 %) наблюдениях с формированием панкреатической фистулы по типу «В» и ферментативной утечке. В данной группе больных на фоне применения консервативной терапии в сочетании с парентеральным питанием отмечали закрытие фистулы, с последующим удалением дренажа на до 24–40 суток после оперативного вмешательства. У пяти пациентов, которым не было выполнено каркасное дренирование панкреатико- и билиодигестивного анастомозов по Фёлькеру, неосложненное течение послеоперационного периода было отмечено у 3 пациентов. В двух наблюдениях с развитием фистулы «С» типа потребовались многократные повторные хирургические вмешательства с длительным применением VAC-систем и увеличением сроков лечения до 65 дней.
Обсуждения
В клинической деятельности мы отдаем предпочтение технике анастомоза с временной наружно-внутренней каркасной декомпрессией. Сохраняющийся отток панкреатического секрета по каркасному дренажу позволяет обеспечить свободный отток панкреатического секрета из культи железы, а также снизить нагрузку на линию шва анастомоза. Исследование морфофункционального состояния культи по динамике выделения панкреатического секрета и содержания в нем ферментов, предполагает возможность контроля эффективности анти-секреторной терапии.
Введение контрастного препарата в ранние сроки послеоперационного периода позволяет оценить адекватность санации культи поджелудочной железы, оценить функцию отводящей петли, уровень имеющегося пареза. При развитии несостоятельности панкреатоеюно- или билиодигестивного анастомозов после ГПДР такой подход позволяет раньше диагностировать элементы несостоятельности, а также продолжить отводящую функцию желчи и панкреатического секрета из протоков.
Улучшение послеоперационных результатов ГПДР удаётся достичь, в том числе, за счёт более раннего перехода на парентеральное питание.
Заключение
Несмотря на непрерывное совершенствование методик хирургического лечения заболеваний поджелудочной железы и ранней диагностики осложнений, гастропанкре-атодуоденальная резекция остаётся одним из наиболее ответственных и трудоемких хирургических вмешательств в абдоминальной хирургии, сопряженным с высоким риском тяжелых послеоперационных осложнений и летального исхода. Временное наружно-внутреннее каркасное дренирование общего желчного и панкреатического протоков является высокоэффективным, простым и безопасным способом дренирования культи поджелудочной железы. Данный метод способствует адекватной и контролируемой декомпрессии протоковой системы ПЖ в послеоперационном периоде, что позволяет существенно уменьшить частоту специфических послеоперационных осложнений – острого послеоперационного панкреатита, несостоятельности панкреато- и гепатикоэнтероанастомоза.
Список литературы Применение дренирования панкреатикоеюноанастомоза после гастропанкреатодуодеональной резекции по поводу злокачественных образованиях поджелудочной железы и большого дуоденального сосочка
- Кубышкин В. А. Рак поджелудочной железы / В. А. Кубышкин, В. А. Вишневский. - М.: Медпрактика, 2013. - 385 c.
- Levenick J., Sutton J., Smith K., Gordon S., Suriawinata A., Gardner T. Pancreaticoduodenectomy for the treatment of groove pancreatitis. Dig. Dis. Sci. Jul., 2012, № 57 (7), рр. 1954-1958.
- Daamen L., Smits F., Besselink M., Busch O., Borel Rinkes I., van Santvoort H., Molenaar I. A web-based overview, systematic review and meta-analysis of pancreatic anastomosis techniques following pancreato-duodenectomy. HPB (Oxford), 2018, № 20 (9), рр. 777-785.
- Bassi C., Marchegiani G., Dervenis C. et. al. The 2016 update of the International Study Group (ISGPS) definition and grading of postoperative pancreatic fistula: 11 Years After. Surgery, 2017, № 161(3), рр. 584-591.
- Figueras J., Sabater L., Planellas P., Muñoz-Forner E., Lopez-Ben S., Falgueras L., Sala-Palau C., Albiol M., Ortega-Serrano J., Castro-Gutierrez E. Randomized clinical trial of pancreaticogastrostomy versus pancreatico-jejunostomy on the rate and severity of pancreatic fistula after pancreaticoduodenectomy. Br. J. Surg., 2013, № 100 (12), рр. 1597-1605.
- Kushiya H., Nakamura T., Asano T. et al. Predicting the Outcomes of Postoperative Pancreatic Fistula After Pancreatoduodenectomy Using Prophylactic Drain Contrast Imaging J. Gastrointest Surg., 2020, № 25 (6), рр. 1445-1450.
- Topal B., van de Sande S., Fieuws S. et al. Effect of centralization of pancreaticoduodenectomy on nationwide hospital mortality and length of stay. Br. J. Surg., 2007, № 94 (11), рр. 1377-1381.
- Ивануса С. Я. Современные возможности применения рентгеноэндоваскулярных вмешательств в диагностике и лечении воспалительных заболеваний поджелудочной железы / С. Я. Ивануса, М. В. Лазуткин, С. А. Алентьев // Военно-медицинский журнал. - 2014. - № 335 (9). - С. 36-42. URL: https://journals.eco-vector.com/0026-9050/article/view/74281/ru_RU.


