Применение мембранного сепараторного интерфейса для масс-спектрометрического анализа анестезиологических препаратов в биологических жидкостях
Автор: Елохин В.А., Ершов Т.Д., Елизаров Андрей Юрьевич
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Приборостроение для биологии и медицины
Статья в выпуске: 2 т.24, 2014 года.
Бесплатный доступ
Описан масс-спектрометрический интерфейс для измерения концентрации анестезиологических препаратов в биологических жидкостях (плазме крови и моче). Забор проб биологических жидкостей осуществлялся во время сбалансированной ингаляционной (севофлуран, фентанил) анестезии и тотальной внутривенной (пропофол, фентанил) анестезии. Описанная методика измерения концентрации препаратов в биологических жидкостях не требует пробоподготовки для ввода образца в интерфейс масс-спектрометра. В интерфейсе использовалась гидрофобная селективная мембрана, которая позволяла выделять анестезиологические препараты из биологических жидкостей: ингаляционный анестетик севофлуран, гипнотик пропофол. Продемонстрирована возможность использования мембранного интерфейса для измерения абсолютной концентрации внутривенного гипнотика пропофол в плазме крови.
Масс-спектрометр, мембранный интерфейс, севофлуран, анестезия, лекарственные и биологические вещества
Короткий адрес: https://sciup.org/14264919
IDR: 14264919 | УДК: 543.51:
Application interface membrane separator mass-spectrometric analysis of anesthetic drugs in biological fluid
Described interface mass-spectrometry for measuring the anesthetic concentration in biological fluids (plasma and urine). Sampling was carried out in biological fluids during balanced inhalation (sevoflurane, fentanyl) and total intravenous anesthesia (propofol, fentanyl) anesthesia. The described technique of measuring the concentration of drugs in biological fluids requires no sample preparation for introduction of the sample into the mass spectrometer interface, which used selective hydrophobic membrane, which can allocate anesthetic drugs from biological fluids: inhalation anesthetic sevoflurane, propofol hypnotic. The possibility of using the membrane interface for absolute measurement of the absolute concentration of intravenous hypnotic propofol in blood plasma.
Текст научной статьи Применение мембранного сепараторного интерфейса для масс-спектрометрического анализа анестезиологических препаратов в биологических жидкостях
Хромато-масс-спектрометрические методики анализа биологических жидкостей требуют длительной пробоподготовки, которая, как правило, сопряжена с использованием жидкофазной экстракции препарата или в последнее время твердофазной экстракции. Биологические жидкости на 80–90 % состоят из воды, и их прямой ввод в колонку хроматографа невозможен. Анестезиологический эффект связан с концентрацией медикаментозного агента в крови, поэтому для решения практических задач анестезиологии (в том числе мониторинга глубины анестезии) является актуальным создание простой методики, позволяющей производить измерения концентрации анестетиков в биологических жидкостях в условиях клиники, т. е. не используя многоступенчатой пробоподго-товки. Так как медикаментозные препараты, используемые для анестезии, известны заранее, а концентрации анестетиков относительно высоки и их осколочные пики в масс-спектре, как правило, не накладываются, то разделение компонентов биологической жидкости в хроматографической колонке является необязательной процедурой.
В статье приводятся результаты исследований, направленных на определение возможности применения селективного мембранного интерфейса квадрупольного масс-спектрометра для анализа сево-флурана и пропофола in vivo в плазме крови и мо- че для решения задач анестезиологии и фармакокинетики (определения скорости удаления препарата из организма).
В настоящее время разработаны методики абсолютного измерения концентрации широкого класса органических соединений, растворенных в воде, которые демонстрируют высокие аналитические возможности мембранных интерфейсов. Так, при использовании квадрупольного масс-спектрометра был достигнут предел обнаружения концентрации препарата не хуже 10–8–10–7 % (0.1–5 мкг/л) [1–5]. К недостаткам мембранных интерфейсов следует отнести большее время отклика по сравнению с капиллярным вводом, зависимость характеристик мембраны от температуры и селективность между различными соединениями.
ОБОРУДОВАНИЕ И МЕТОДИКА ИЗМЕРЕНИЙ
Мембранный сепараторный интерфейс состоит из мембраны (polydimethylsiloxane) толщиной 75 мкм (для фиксации мембраны на отверстии во фланце интерфейса диаметром 6 мм использовалась пористая титановая пластина) и системы дифференциальной откачки, обеспечивающей перепад давлений 1000—3·10–2—4·10–6 мбар, где 3·10–2 мбар — давление в дифференциальной камере, 4·10–6 мбар — давление в камере масс-спектрометра соответственно. Конструкция m/z 131
Севофлуран (Abbot)
m / z 181
120 140 160 180
m / z
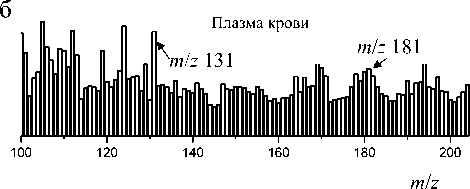
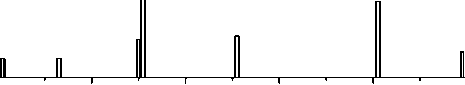
Рис. 1. Масс-спектры: а — севофлурана (Аббот); б — плазмы крови, забор которой осуществлялся во время ингаляционной анестезии севофлураном, полученный при помощи мембранного сепараторного интерфейса интерфейса позволяла осуществлять его нагрев до температуры 45 °С. Камера масс-спектрометра и камера дифференциальной откачки вакуумировались при помощи турбомолекулярного насоса и первой ступени откачки того же насоса. Скорость откачки камеры масс-спектрометра и дифференциальной камеры составляла 60 и 20 л/с соответственно. Эти камеры разделены диафрагмой диаметром 100 мкм. В работе использовался квадрупольный масс-спектрометр (Prizma Plus, Pfeiffer Vacuum).
РЕГИСТРАЦИЯ СЕВОФЛУРАНА
На рис. 1, б, и 2 приведены масс-спектры плазмы крови и мочи, забор которых осуществлялся во время ингаляционной анестезии севофлураном. Концентрация севофлурана в дыхательном контуре аппарата ингаляционной анестезии составляла 3 об %. Анальгетик фентанил вводился в. в. каждые 20 мин в количестве 0.1 мкг. На рис. 1, а, представлен масс-спектр чистого препарата, полученный парофазным методом. На рис. 1, б, представлен масс-спектр плазмы крови, забор которой осуществлялся во время низкопоточной ингаляционной анестезии из периферической вены. На масс-спектре присутствуют материнский и осколочные пики севофлурана и осколочные пики соединения compound A (C 4 H 2 F 6 O). Известно, что ингаляционный анестетик севофлуран в дыхательном контуре взаимодействует с поглотителем СО 2
Моча
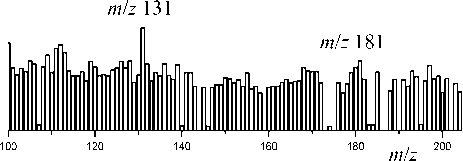
Рис. 2. Масс-спектр мочи, забор которой осуществлялся во время ингаляционной анестезии се-вофлураном, полученный при помощи мембранного сепараторного интерфейса и образует высокотоксичное соединение Compound A, которое может вызывать некроз почечных канальцев (нефропатия) [5–9]. Клинические исследования влияния указанных соединений на прогноз нефропатии широко представлены в литературе и на сегодняшний момент исследования демонстрируют разнонаправленный характер на прогноз нефропатии, что обусловливает потребность в дальнейших исследованиях [10–13]. Оперативное определение концентрации Compound A и севофлурана в плазме крови при помощи масс-спектрометра с мембранным интерфейсом позволит вносить изменения во введение анестезии в случае прогноза печеночных осложнений у пациента.
На рис. 2 представлен масс-спектр мочи, полученный при помощи мембранного сепараторного интерфейса. Забор мочи осуществлялся во время ингаляционной анестезии севофлураном. В масс-спектре присутствуют пики 131 m/z, 181 m/z , которые соответствуют наиболее интенсивным осколочным пикам севофлурана. Начата работа по определению скорости выделения севофлурана из организма в случае печеночной недостаточности.
РЕГИСТРАЦИЯ ПРОПОФОЛА
Во время тотальной внутривенной анестезии использовался режим инфузии, управляемой по целевой концентрации (ИУЦК) пропофола в крови. Его концентрация выбиралась в диапазоне 2–3.5 мкг/мл и обеспечивалась при помощи шприцевого насоса (B|Braun) под управлением программы ИУЦК — STANPUMP [14]. Эта программа обеспечивает с высокой точностью поддержание заданной концентрации пропофола в крови во время анестезии. Каждые 15 мин производился забор крови из периферических вен. Мониторинг концентрации пропофола в крови осуществлялся
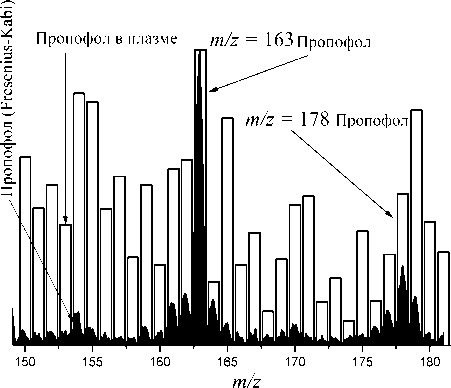
Рис. 3. Масс-спектр препарата пропофола (Fresenius-Kabi) и плазмы крови, забор которой осуществлялся во время тотальной внутривенной анестезии пропофолом
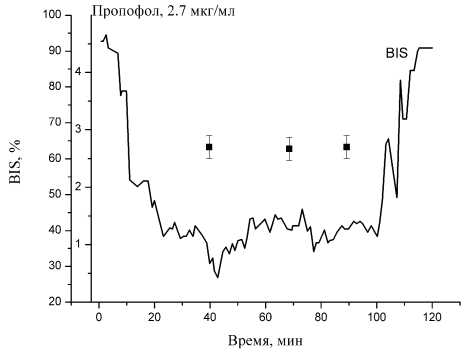
Рис. 4. Мониторинг BIS-индекса во время аде-номэктомии гипофиза. Представлены результаты измерения абсолютной концентрации пропофола в трех временн ы х точках
при помощи энцефалографии (BIS-индекс, Vista, Aspect Medical).
Внутривенный гипнотик пропофол практически нерастворим в воде, но хорошо растворяется в жирах, поэтому этот медикаментозный препарат вводится внутривенно в составе эмульсии следующего состава: 10 % — соевое масло; 1.2 — очищенные яичные фосфолипиды (эмульгатор); 2.25 % — глицерин; вода и гидроксид натрия, регулирующий pH.
Эмульсифицированная форма пропофола поступила на фармрынок в 1986 г. и в настоящее время является гипнотиком "выбора" при проведении ингаляционной или внутривенной анестезии. Масс-спектр препарата пропофол (Fresenius-Kabi), полученный при помощи мембранного интерфейса, представлен на рис. 3. Эмульсия пропофола наносилась непосредственно на мембрану интерфейса масс-спектрометра. Массовые пики и их отношение совпадают с данными NIST (. В качестве внутреннего стандарта был приготовлен раствор пропофола в препарате для парентерального (внутривенного) питания (Ин-тралипид, Fresenius-Kabi), состав которого соответствует растворителю препарата пропофол (Fresenius-Kabi). Анестезия проводилась при концентрации пропофола в крови 2.7 мкг/мл. Вид временнóй зависимости BIS-индекса представлен на рис. 4, из которого следует, что во время анестезии (время 5–25 мин) глубина гипнотического эффекта была постоянна, что было обусловлено стабильной концентрацией пропофола в крови. При помощи мембранного интерфейса были выполнены измерения концентрации пропофола. После каждого измерения осуществлялся прогрев интерфейса до 45 °С, затем он охлаждался до комнатной температуры. Концентрация пропофола в трех временных точка совпадала с концентрацией, установленной по ИУЦК.
В результате серии из четырех измерений было получено совпадение концентрации пропофола в плазме крови и целевой концентрации пропофола по программе STANPUMP с точностью, не хуже 5 %. Таким образом, была продемонстрирована возможность использования мембранного сепараторного интерфейса для абсолютных измерений концентрации пропофола в плазме крови без использования пробоподготовки.
Высокая растворимость пропофола в липидах позволяет ему легко проходить через гематоэнцефалический барьер (ГЭБ), чем объясняется его быстрая терапевтическая активность. В работе производился забор крови из периферической вены и из хиазмально-селлярной области головного мозга во время аденомоктомии гипофиза. Измерения концентрации пропофола в плазме крови этих двух образцов выполнялись при помощи мембранного сепараторного интерфейса. Было получено, что концентрация пропофола в хиазмально-селлярной области была на 45 ± 3 % ниже, чем в периферической вене, что объясняется свойством ГЭБ [15].
ВЫВОДЫ
В результате измерений (до 30 циклов) деградация свойств мембраны обнаружена не была. Время выхода на рабочий режим масс-спектро-метера с мембранным интерфейсом не превышало 10 мин. Время одного измерения — 1 мин. На примере пропофола продемонстрирована возможность измерения абсолютной концентрации внутривенных анестезиологических препаратов. Использование мембранного интерфейса в виду просты в эксплуатации и сервисном обслуживании имеет перспективы использования в практической анестезиологии для экспресс-анализа концентрации анестезиологических препаратов в плазме крови и моче.
Авторы благодарят сотрудников кафедры анестезиологии и реаниматологии Военно-медицинской академии им. С.М. Кирова за содействие в проведении исследований.
Работа выполнена при поддержке РФФИ, проект №12-08-00402-а


