Применение метода флюоресцентного анализа для экспресс-диагностики антибиотикочувствительности микрофлоры у больных с абдоминальной инфекцией
Автор: Гостищев В.К., Хоменко В.А., Кузьмина А.Г., Кузьмин Г.П., Ивахов Г.Б.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 2 (36), 2014 года.
Бесплатный доступ
Выбор адекватного антибиотика осуществлен посредством флуоресцентного анализа плазмы крови с применением лабораторно-диагностической установки «Spectrolux MB», разработанной в Научно-производственном центре медицинских и промышленных биотехнологий «Spectrolux», Москва. Для определения чувствительности к антибиотикам используется способность микроорганизмов и продуктов их жизнедеятельности флюоресцировать под действием лазерного излучения в зависимости от их особенностей и активности физиологических процессов. Пациенты имеют различную чувствительность к одинаковым антибиотикам и типу микробов. Одно из преимуществ флуоресцентного анализа - определение реакции организма на адекватную антибактериальную терапию и ее влияние на микрофлору. Это позволяет лечении пациента оценки обработка, которая начинается с ранней антибиотик определения чувствительности специально для него.
Флюоресценция, антибиотик, экспресс-диагностика, сепсис
Короткий адрес: https://sciup.org/142211142
IDR: 142211142 | УДК: 616-089;
Текст научной статьи Применение метода флюоресцентного анализа для экспресс-диагностики антибиотикочувствительности микрофлоры у больных с абдоминальной инфекцией
Одной из наиболее сложных проблем в хирургии остаётся лечение абдоминальных гнойно-воспалительных заболеваний и их осложнений. В структуре хирургической заболеваемости перитонит и вызывающие его деструктивные поражения органов брюшной полости занимают одно из первых мест. Летальность при распространенных формах перитонита составляет 15–20%, за последние 20–30 лет заметного снижения летальности не отмечено [3]. Высокая летальность при перитоните зависит от позднего обращения больных за медицинской помощью, увеличения числа больных пожилого и старческого возраста со сниженной иммунобиологической реактивностью, страдающих тяжелыми сопутствующими заболеваниями; увеличения числа онкологических заболеваний, осложняющихся перитонитом [1]. Более того, в последние годы приходится сталкиваться с запущенными формами этих заболеваний.
Абдоминальную хирургическую инфекцию можно рассматривать как совокупность утвердившихся в клинической медицине нозологических форм, отражающих осложненное течение острых хирургических заболеваний и повреждений, но допустимо и иначе – с позиций единой клинической проблемы сепсиса. Как известно, брюшина непременно отвечает воспалением на любой патологический процесс, индуцированный инфекционно-воспалительной или травматической деструкцией органов живота и таза. При этом обширная площадь брюшинного покрова, достигающая двух квадратных метров, его сложное строение, реактивность, а также важность физиологических функций – экссудативной, резорбтивной и барьерной – не оставляют сомнений в опасности распространенного воспаления брюшины для жизнедеятельности организма. [2].
Современные положения комплексного лечения абдоминального сепсиса основываются на принципах этиотропной, патогенетической направленности терапии и хирургии, цель которых ликвидация инфекции брюшной полости, устранение эндотоксикоза и полиорганной недостаточности.
В этом аспекте роль ранней полноценной антибактериальной терапии после операции в комплексном лечении трудно переоценить: адекватная антибиотикотерапия способна предотвратить генерализацию инфекции, развитие различных послеоперационных осложнений и фатальную полиорганную недостаточность [1]. Современная хирур- гическая концепция ведения больных с абдоминальным сепсисом требует не только адекватного хирургического пособия, но и проведения ранней рациональной антибиоти-котерапии, ее мониторинга, определения степени эндотоксикоза, микробиологического мониторинга абдоминальной хирургической инфекции. Микробиологическая диагностика сепсиса является определяющей в выборе адекватных режимов антибактериальной терапии.
Результаты этиотропной терапии сепсиса значительно лучше, чем эмпирической [3]. Одним из основополагающих моментов лечения больных с абдоминальным сепсисом является адекватная антибактериальная терапия в раннем послеоперационном периоде. В послеоперационном периоде приходится прибегать к эмпирической антибактериальной терапии без микробиологического подтверждения микробной флоры и ее свойств. Проводимая терапия часто не является адекватной и в свою очередь может способствовать развитию послеоперационных осложнений как системных, так и местных, экономически большим затратам, увеличению сроков лечения, повышению уровня летальности.
Соблюдение условий выбора эффективных препаратов при использовании методов экспресс-диагностики может способствовать рациональному использованию антимикробных препаратов, тем самым снизить частоту развития гнойно-воспалительных заболеваний и таким образом приведет к сокращению сроков госпитализации (самая большая статья расходов на оказание медицинской помощи), а также позволит снизить показатели заболеваемости и летальности [7]. Наиболее значимо определение чувствительности микроорганизмов к антибиотикам в отношении группы микробов, среди которых выделяется большое число антибиотикоустойчивых штаммов [5, 6].
В этой связи важным является разработка новых клинико-микробиологических методов выбора антимикробных препаратов [4]. Выявленные закономерности флюоресценции микроорганизмов в чистых и смешанных культурах явились экспериментальным обоснованием применения экспресс-метода лазерной флюоресценции для выявления микробов и процессов, вызванных микробами, для экспресс-диагностики гнойно-воспалительных заболеваний различной этиологии и локализации [8]. Особенно перспективен метод при лечении данных заболеваний в ур-гентной хирургии.
Цель и задачи
-
1. Определить возможности экспресс-диагностики этиологии абдоминальной хирургической инфекции при использовании метода флюоресцентного анализа. Провести сравнительный анализ лазерно-флуоресцентной диагностики плазмы крови с классическими микробиологическими исследованиями перитонеального экссудата.
-
2. Разработать методику выбора ранней рациональной антибактериальной терапии у больных с абдоминаль-
- ным сепсисом на основе спектрального анализа лазерно-индуцированной флюоресценции плазмы крови;
-
3. На основе метода флюоресцентного анализа определить эффективность проводимой антибактериальной терапии при лечении больных с абдоминальной хирургической инфекцией;
Материалы и методы
На кафедре общей хирургии ПМГМУ им И.М. Сеченова на базе ГКБ №23 была усовершенствована и применена методика подбора больным адекватной антибиотикотерапии методом флюоресцентного анализа плазмы крови с использованием лабораторно-диагностической установки «Спектролюкс МБ», разработанной в НПЦ медицинских и промышленных биотехнологий «Спектролюкс», г. Москва. Для оценки антибиотикочувствительности используется способность микроорганизмов и продуктов их жизнедеятельности флюоресцировать при воздействии гелий-неонового лазерного излучения с длиной волны 633 нм, в зависимости от особенностей и активности физиологических процессов в них. У различных больных чувствительность к одному и тому же антибиотику для одного и того же вида микробов различна. В этом один из плюсов метода флюоресцентного анализа – определяется реакция организма на введение адекватного антибактериального препарата и его воздействие на микрофлору, что позволяет лечить не болезнь, а больного, учитывая, что лечение начнется с раннего определения антибиотикочувствительности именно для этого пациента.
Показатели флюоресценции: 800
F = IF = ∫ I (λ) d λ – интегральная интенсивность флюо- 643
ресценции (S2)*.
800 642,8
Kf m = F / R = (∫ I (λ) d λ)/(∫ I (λ) d λ) – показатель норми- 643 622,8
рованной флюоресценции (S2/S1)*.
k а = [( I 1 – I 2 )/( I 1 + I 2 )]/2 – отношение интенсивностей флюоресценции I 1 и I 2 (Аэробность)*, где
-
I 1 = = ∫ I (λ) d λ/Δλ – интегральная интенсивность (S3)*; 670
-
I 2 = ∫ I (λ) d λ/Δλ – интегральная интенсивность (S4)*; 700
* в скобках представлены обозначения, использованные в ранних публикациях.
Метод включает в себя забор крови из вены у больного до операции и назначения антибактериальной терапии, в том числе и проведения антибиотикопрофилактики, в объеме 20 мл (5 пробирок). После чего больному оказывается необходимое оперативное пособие, санация гнойного очага. Кровь в пробирках центрифугируется в течение 5 минут, при скорости 1000 оборотов в одну минуту. После чего полученная плазма распределяется в необходимое ко-
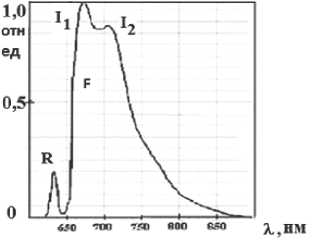
Рис. 1. Спектр флюоресценции (пример)
личество кювет (возможно использование до 10 кювет одновременно). Кювета емкостью – 1,5 мл.
Проводится предварительное исследование плазмы крови, по результатам которого выявляется превалирующий микробный агент (аэроб или анаэроб) (рис. 2, 3).
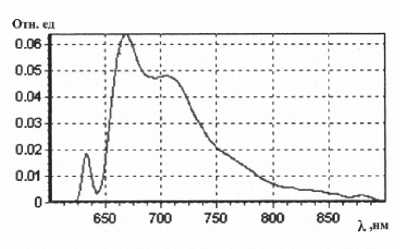
Рис. 2. Спектрограмма, характерная для инфекции с преобладанием аэробной флоры. Ка<0,2
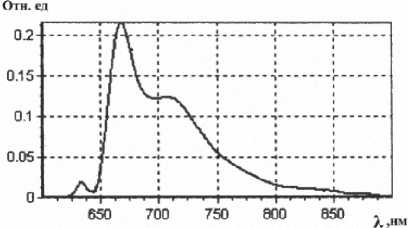
Рис. 3. Спектрограмма, характерная для инфекции с преобладанием анаэробной флоры. Ка>0,2
Исследуется разница в показателях спектра, параметрах графика. Изменения одного из основных показателей – К а , позволяют определить превалирующий микробный агент. При К а <0,2, спектрограмма характерна для инфекции с преобладанием аэробной флоры; при К а >0,2 – для инфекции с преобладанием анаэробной флоры.
По показателю K f определяется степень интоксикации, чем выше показатель флюоресценции, тем более выражена интоксикация. По степени снижения показателя К f можно судить об эффективности проводимой терапии, снижении степени интоксикации.
Растворы антибиотиков, чаще всего применяемые в процессе лечения, в рассчитанной концентрации и добавляются к исследуемым образцам. Одна кювета – контроль.
После чего проводится измерение показателей в течение 2– 4 часов, с интервалом в 30 минут в автоматическом режиме (в конструкции аппарата есть встроенный термостат, который поддерживает температуру 370С).
После чего анализируется график, полученный для конкретного пациента, и назначается соответствующий препарат (рис. 4).
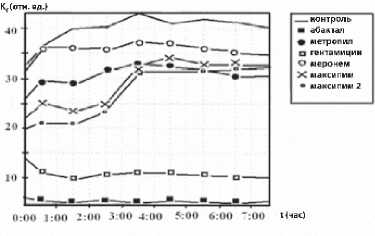
Рис.4 Зависимость показателя нормированной флюоресценции Kf = F/R от времени. На вставке показаны символы, соответствующие различным антибиотикам
Больной А.: при добавлении растворов антибактериальных препаратов отмечается снижение интенсивности флюоресценции (K f ), особенно препаратов абактал и гентамицин, таким образом, можно сделать вывод о чувствительности микробной ассоциации к этим антибактериальным препаратам. При добавлении других препаратов наблюдаются идентичные тенденции, но с менее значительным снижением интенсивности флюоресценции. Данный процесс характеризуется как умеренная чувствительность.
На основе интегральных расчетов формируется спектрометрическая кривая, позволяющая судить о степени интоксикации, чувствительности аэробно-анаэробной ассоциации к определенному антибактериальному препарату, эффективности проводимой терапии (возможность проведения мониторинга, через сутки, через 3 суток после операции для оценки эффективности проводимой терапии).
Снижение уровня флюоресценции ( Kf ) говорит об адекватности выбранного антибактериального препарата, тогда как отсутствие изменений или повышение флюоресценции указывает на неэффективность антибактериального препарата, наличие антибиотикорезистентности микробной флоры.
Результаты и обсуждение
На базе кафедры общей хирургии проведен проспективный мультифакторный анализ применения флюоресцентного метода для экспресс-диагностики антибиотикорези-стентности у больных с абдоминальным сепсисом. В группу исследования были включены 123 оперированных пациента.
Все больные были разделены по полу, возрасту, наличию сопутствующих заболеваний, хирургической патологии, объему перенесенного оперативного вмешательства. Тяжесть состояния (оценка органно-системных нарушений)
на момент поступления оценивалась по шкале SOFA. Учитывая, что популяция больных с сепсисом является гетерогенной не только по характеру и выраженности нарушений гомеостаза, но также по возрасту и сопутствующей патологии, что отражается на течении патологического процесса, необходима оценка общей тяжести состояния (проводилась по шкале APACHE III).
Исследована плазма 123 пациентов с различной острой хирургической патологией (35 (28,5%) – острый гангренозный аппендицит с ограниченным перитонитом; 8 (6,5%) – панкреонекроз; 16(13%) – перфорация язвы желудка с фибринозно-гнойным перитонитом перитонитом; 27 (22%) – острый гангренозный калькулезный холецистит с ограниченным перитонитом; 6 (4,8%) – сегментарный мезентериальный тромбоз; 15 (12,2%) – кишечная непроходимость с распространенным перитонитом; 16 (13%) – перфорация дивертикула толстой кишки). Женщин – 72 (58,5%); мужчин – 51 (41,5%).
Согласно возрастной классификации (ВОЗ) больные с абдоминальным сепсисом были разделены на пять возрастных категорий: 1) молодой (до 45 лет) – 41 пациентов (33,3%); 2) зрелый (от 45 до 59 лет) – 25 (20,4); 3) 61–74 лет, пожилой возраст, – 37 пациентов (30%); 4) 75 лет и старше – старческий – 15 (12,2%) пациентов; 5) долгожители – 90 лет и старше – 5 (4,1%) пациентов. У всех пациентов 3, 4, 5 возрастных групп имелось несколько сопутствующих заболеваний, причём наиболее распространенной (90%) сопутствующей патологией явились заболевания сердечнососудистой системы, в частности атеросклеротическое поражение.
При оценке тяжести состояния пациентов на 1 сутки послеоперационного периода установлено, что у пациентов с острым гангренозным аппендицитом, осложненным ограниченным перитонитом средняя величина АРАСНЕ III составила 59,4 баллов; у пациентов с панкреонекрозом – 86,7 балла, при перфорации язвы желудка с фибринозно-гнойным перитонитом – 58,5 баллов; у пациентов с острым деструктивным холециститом – 69,8; сегментарным мезентериальным тромбозом – 78,4; у больных с кишечной непроходимостью средняя величина АРАСНЕ III составила – 80,4; при перфорации дивертикула с абсцессом – 52,4.
Критерием включения в исследование являлись пациенты различного возраста и пола с признаками абдоминальной инфекции, требующие оперативного лечения, назначения адекватной антибактериальной терапии. Критерии исключения (по ходу исследования): отказ больного от исследования; возникновение новых заболеваний или осложнений, по тем или иным причинам препятствующие выполнению исследования.
При поступлении в хирургическое отделение больной с клинико-инструментальной картиной острого гнойновоспалительного заболевания и при его согласии включа- ется в исследование. Производится забор крови в объеме 20 мл. После центрифугирования, полученная плазма распределяется в спектрометрические кюветы, 1 – всегда контроль. Готовятся растворы антибактериальных препаратов, рассчитанных по формуле с использованием данных по фармакокинетике и фармакодинамике, характерных для каждого антибактериального препарата. Концентрация антибактериального препарата в растворе не превышает Сmax – максимальная в плазме крови (in vivo). После чего проводится исследование и анализ графического изображения. В обязательном порядке проводится суточный мониторинг – измерение показателей флюоресценции в течение суток через каждый час, после чего делается окончательное заключение по эффективности антибактериального препарата для конкретного больного. Выбор антибиотика методом флюоресцентного анализа основывается на мониторинге изменений флюоресценции плазмы крови под действием антибактериального препарата в сравнении с контролем (плазма без добавления антибиотика). При ургентной хирургической патологии, учитывая рекомендации применения антибиотиков при гнойно-воспалительных заболеваниях, выбор препарата для исследования сделан по одному из следующих групп: бета-лактамы, аминогликозиды, нитроимидазолы, фторхинолоны. Выбор антибиотика для исследования методом флюоресцентного анализа происходит с учетом особенностей фармакокинетики: длительности периода полувыведения (T½ более 1-го часа), с наименьшим связыванием препарата с белками крови, с максимальным накоплением в плазме крови в течение 2–24 часов, с парентеральным путем введения. Для исключения погрешности отдельно проводится измерение растворов антибиотиков в заданной концентрации (дополнительный контроль) при той же экспозиции. Эффективность выбора определяется следующим образом: по принятой методике производится измерение флюоресценции плазмы крови человека после введения антибактериального препарата через 2, 4, 12 и 24 часа. Микрофлора чувствительна к антибактериальному препарату, если под его действием происходит снижение нормированной мощности флюоресценции (Kf) более чем на 20%. Проводится лечение выбранным препаратом. На 2 и 5 сутки проводится дополнительный забор крови, для оценки эффективности проводимого лечения. При адекватно проведенном лечении показатели флюоресценции плазмы совпадают или близки по значению к показателям донора. Устойчивой к действию антибактериального препарата считается микрофлора, чья флюоресценция плазмы не изменяется или растет относительно контроля. Необходима коррекция концентрации вводимого препарата или замена его на другой.
При незначительном изменении флюоресценции результат трактуется как бактериостатический, который соответственно методике пограничных разведений трактуется как умеренный. В данном случае проводится контрольное исследование через сутки.
У всех больных проводится интраоперационный забор перитонеальной жидкости на микробиологический посев для определения этиологического фактора и определения антибиотикограммы по результатам посева. Далее идет сравнение результатов, оценка клинической эффективности проводимой терапии.
При бактериологическом исследовании выявлено, что информативные результаты посева были только в 54%, в остальных посевах рост микрофлоры не определен. Соответственно, антибиотикограмма определялась только в 54% случаях. В то же время по анализу спектральных характеристик было выявлено 86% случаев микс-инфекции. Результаты микробиологического исследования перитонеального экссудата: при перфорации язвы желудка с ограниченным фибринозно-гнойным перитонитом – энтеробактерии, псевдомонады, аэробные кокки; при остром гангренозном аппендиците и перфорации толстой кишки – стафилококки, стрептококки, энтерококки, кишечная палочка, энтеробактерии; при панкреонекрозе – псевдомонады, кишечная колика, энтерококки. Микробные ассоциации выявлены у 20% больных.
Клиническая эффективность антибактериальных препаратов с учетом субъективных и объективных параметров при применении метода флюоресцентного анализа и назначения антибактериального препаратов согласно результатам исследования достигнута в 74% случаев. Клиническая эффективность трактовалась следующим образом – на фоне выбранной антибактериальной терапии отмечена положительная динамика в течении послеоперационного периода – нормализация температуры тела, объективная положительная оценка состояния больного, снижение показателей SIRS.
В 26% был необходим повторный анализ, коррекции антибактериальной терапии. Полученные различия в мощности флюоресценции позволяют рекомендовать назначение того препарата, в пробе с которым наблюдается снижение флюоресценции по сравнению с контролем до 20%.
Выводы
-
1. Проводимое исследование с использованием флюоресцентных методов диагностики позволило в 86% случаев подтвердить наличие микс-инфекции с участием анаэробной флоры, тогда как у этих же пациентов микробиологические данные посева экссудата были неинформативны у 46%.
-
2. Клиническая эффективность проводимой антибактериальной терапии с учетом данных флюоресценции плазмы достигнута в 74% случаев (исключая больных с развившимися нехирургическими осложнениями), что позволяет
-
3. Применяемый метод флюоресцентного анализа на аппарате «Спектролюкс МБ» показал свою высокую эффективность и достоверность у больных с абдоминальной инфекцией в хирургии (подтверждено микробиологически и клинически).
-
4. Данный метод флюоресцентного анализа позволяет в режиме реального времени подобрать адекватную и эффективную химиотерапию в течение 2–4 часов от момента поступления больного в стационар, что позволяет улучшить результаты лечения данной патологии, сократить время пребывания пациента в стационаре.
-
5. Метод флюоресцентного анализа позволяет проанализировать по количественным спектральнофлюоресцентным показателям собственную флюоресценцию бактерий. Метод флюоресцентного анализа имеет ряд преимуществ перед существующими методами диагностики микробного агента, такие как объективность, достоверность и оперативность исследования.
рассматривать данный метод как перспективное направление в ранней диагностике анаэробной неклостридиальной инфекции и в разработке оптимальной антибактериальной терапии у больных с абдоминальной инфекцией и требует продолжения исследований для дальнейшего развития.
Список литературы Применение метода флюоресцентного анализа для экспресс-диагностики антибиотикочувствительности микрофлоры у больных с абдоминальной инфекцией
- Гостищев В.К. Инфекции в хирургии. 2007. C. 20-25, 462470.
- Гостищев В.К., Сажин В.П., Авдовенко А.Л. Перитонит. 1992. С. 8-30.
- Савельев В.С. Сепсис в начале 21 века. 2006. С. 5-10.
- Александров М.Т., Афанасьева Р.А., Гапоненко О.Г., Козьма С.Ю., Кузьмин Г.П., Лизунова И.А., Пашков Е.П., Смирнова В.В., Шабашева И.Ф. Лазерная флюоресцентная диагностика в медицине и биологии. Теория и возможности применения. «НПЦ Спектролюкс», 2007.
- Колесников Д.Л., Кукош М.В., Трухалев В.А., Коптева Л.Н. Сравнение эффективности антибиотиков, используемых для анти-биотикопрофилактики при остром аппендиците//Хирургическая практика. 2013. № 2. С. 37-41.
- Под ред. в.С. Савельева. Абдоминальная хирургическая инфекция. Российские национальные рекомендации. М., 2011.
- Руководство по инфекционному контролю в стационаре. Перевод с англ./Под ред. Р. Венцеля, Т. Бревера, Ж.-П. Бутулера. Смоленск: МАК-МАХ, 2003.
- Montravers P. еt al. Emergence of antibiotic-resistant bacteria in cases of peritonitis after intraabdominal surgery affects the efficacy of empirical antimicrobial therapy//Clin. Infect. Dis. 1996. Vol. 23. P. 486-494.


