Применение обогатительно-селективной среды для культивирования сальмонелл
Автор: Чугунова Елена Олеговна
Журнал: Вестник Омского государственного аграрного университета @vestnik-omgau
Рубрика: Ветеринарные науки
Статья в выпуске: 2 (22), 2016 года.
Бесплатный доступ
Рассмотрены преимущества разработанного состава питательной среды для обогащения сальмо- нелл по сравнению с аналогом. Основой для создания питательной среды послужила забуференная пеп- тонная вода, в которую перед бактериальным посевом добавляли пропиленгликоль. Работа выполнена на базе Пермского ветеринарного диагностического центра в период с 2014 по 2015 г. В процессе исследо- ваний использовали референтные культуры Salmonella spp., Sh. flexneri, E. coli, Pr. vulgaris, S. aureus иL. monocytogenes. В результате выявлена существенная разница в скорости размножения бактерий рода Salmonella при культивировании. Предложенная среда способствовала увеличению чистой культуры сальмонелл в среднем на 38,57 %. При культивировании Salmonella spp. в ассоциации с сопутствующей микрофлорой был также получен прирост бактериальной массы сальмонелл в опыте на 15,04-61,54 %. Исключение составило культивирование со штаммами S. choleraesuis. Чистые культуры данных штаммов показали прирост бактериальных клеток в опытных образцах на 8,97 % больше, чем в контрольных.В ассоциации с другими микроорганизмами как контрольные, так и опытные пробы были примерно оди- наковой мутности. Однако количество бактериальных клеток было большим и составило 1,3 х 108. Таким образом, предложенный состав обогатительной питательной среды может быть с успехом применим в ветеринарных лабораториях, так как позволяет выделять в короткие сроки Salmonella spp.
Сальмонеллы, сопутствующие микроорганизмы, питательные среды, обогащение, бактериальная биомасса
Короткий адрес: https://sciup.org/142199178
IDR: 142199178 | УДК: 579.672
Application of selective nutritional medium for enrichment of salmonella
The article shows the advantage of nutritional medium for Salmonella enrichment compared to a similar one. Buffering peptone water was the prototype of the nutritional medium. It had been supplemented with pro- pylene glycol before tests. We used Salmonella spp., Sh. flexneri, E. coli, Pr. vulgaris, S. aureus and L. mono- cytogenes for investigation. Research took place in Perm Veterinary laboratory in 2014-2015. The essential dif- ference between the speed of Salmonella reproduction at cultivation in experimental and control samples of a nutritional medium was revealed as a result. The developed nutritional medium promoted increase in pure cul- ture of Salmonella spp. on average by 38.57 %. Salmonella spp. in association with the accompanying microflo- ra was increased by 15.04-61.54 % in the workable nutritional medium. The strains of S. choleraesuis made an exception. Pure cultures of these strains showed a gain of bacteria in experimental nutritional medium 8.97 % more than in the control ones. S. choleraesuis in association with other microorganisms were approximately identical concentrating after cultivation in both nutritional mediums. However the quantity of bacteria cells was1.3 х 108. Thus, our nutritional medium can be used in laboratories. Thus the nutritional medium obtained can be used in veterinarian laboratories as it allows to promptly generate Salmonella spp.
Текст научной статьи Применение обогатительно-селективной среды для культивирования сальмонелл
Пищевые сальмонеллезы – широко распространенные болезни людей, их регистрируют во всех странах, на всех континентах. Возбудители поражают человека и длительное время сохраняются в окружающей среде [1]. Вместе с тем, растущий темп жизни общества отражается на его питании. Быстрые способы приготовления еды, полуфабрикаты из супермаркетов требуют все большего внимания к мерам профилактики и гигиены [2].
Бактерии рода Salmonella могут присутствовать в пищевых продуктах в незначительном количестве вместе с большим числом других бактерий [3]. Для изоляции сальмонелл из продуктов питания используют несколько групп сред: обогатительные, селективные и идентифи-
кационные. Обогатительные среды содержат минимальное количество селективных агентов и отличаются высокой питательностью [4], что способствует развитию как Salmonella spp., так и сопутствующей микрофлоры. Известно, что выделение чистых культур микроорганизмов значительно осложняется, если в микробной ассоциации присутствует протей, способный к роению (Покровский В.И., 1985). Для подавления роения протеев обычно используют различные химические вещества (Cowan S.T., Steel K.J., 1974). Они в ряде случаев ингибируют и рост искомых микроорганизмов [5]. В связи с этим актуальна разработка обогатительноселективной среды, способствующей увеличению биомассы сальмонелл при подавлении сопутствующей микрофлоры.
Объекты и методы
Объектом исследования служили референтные штаммы S. typhimutium, S. enteritidis, S. gallinarum-pullorum, S. dublin, S. choleraesuis, S. infantis, S. hamburg, S. virchow, Sh. flexneri , E. coli , Pr. vulgaris , S. aureus , L. Monocytogenes , полученные из ФГБУ «Научный центр экспертизы средств медицинского применения» Минздрава России и выделенные из мясной и яичной продукции. Исследования проводили, используя суточные агаровые культуры изучаемых микроорганизмов. Исходную бактериальную суспензию, содержащую 1 х 108 МТ/см3 или 0,5 ед. мутности по МакФарланду (McF), готовили с помощью оптического прибора Densi-La-Meter (Erba Lachema, Чехия). Далее делали ряд последовательных разведений до получения рабочей суспензии, содержащей 1 х 101 МТ/см3, которую использовали для культивирования в забуфе-ренной пептонной воде (ЗПВ), приготовленной по ГОСТ 31659‒2012 (контроль) и в питательной среде, предложенной автором (опыт).
При разработке обогатительно-селективной среды в стандартную ЗПВ добавляли пропи-ленгликоль (1,2 пропиленгликоль, пропандиол-1,2) «чистый» [6]. В испытуемую и контрольную питательную среду инокулировали взятые в опыт микроорганизмы и инкубировали при 37 °С в течение 24 ч. На следующий день устанавливали прирост бактериальной массы по степени мутности на приборе Densi-La-Meter. Мутность бактериальной суспензии выражали в единицах МакФарланда (McF).
Опыты проводили в 10-кратной повторности. Статистический анализ результатов исследования проведен в программе Statistica 6.0 с использованием методов вариационной статистики [7]. Вычисляли средние величины (М), их стандартную ошибку (m) и среднеквадратическое отклонение ( σ ). Достоверность различий между показателями оценивали с использованием непарного t-критерия Стъюдента. Различия считали статистически значимыми при p < 0,05. Результаты статистической обработки в таблицах представлены в виде средней арифметической и ее стандартной ошибки (M ± m).
Результаты исследований
Установлена способность разработанной питательной среды влиять на скорость размножения сальмонелл. Визуально испытуемая среда после инкубации с бактериями рода Salmonella была более мутной, чем ЗПВ контрольных образцов. Измерив степень мутности контрольных и опытных образцов ЗПВ на оптическом анализаторе DensiLaMeter, подтвердили свойство разработанной среды катализировать процесс увеличения биомассы сальмонелл (табл. 1).
Таблица 1
Прирост бактериальной массы Salmonella spp. при культивировании в питательных средах
|
Серотип сальмонелл |
Степень мутности, ед. McF |
Прирост бактериальной массы |
||
|
Опыт |
Контроль |
Абсолютное значение, ед. McF |
% |
|
|
S. typhimurium |
1,838 ± 0,091 |
1,013 ± 0,035 |
0,825 |
44,89 |
|
S. Dublin |
1,1 ± 0,0531 |
0,913 ± 0,099 |
0,187 |
17,00 |
|
S. choleraesuis |
0,725 ± 0,0893 |
0,66 ± 0,05 |
0,065 |
8,97 |
|
S. enteritidis |
1,11 ± 0,0641 |
0,675 ± 0,046 |
0,435 |
39,19 |
|
S. gallinarum-pullorum |
1,538 ± 0,0521 |
1,05 ± 0,053 |
0,488 |
31,73 |
|
S. infantis |
2,163 ± 0,0521 |
0,963 ± 0,052 |
1,2 |
55,48 |
|
S. hamburg |
2,388 ± 0,0351 |
0,8 ± 0,0 |
1,588 |
66,50 |
|
S. virchow |
1,738 ± 0,091 |
0,96 ± 0,052 |
0,778 |
44,76 |
|
Среднее значение |
1,568 ± 0,562 |
0,879 ± 0,15 |
0,70 |
38,57 |
1Р < 0,001; 2Р < 0,01; 3Р < 0,05.
При анализе полученных результатов установлено, что разработанный состав питательной среды для этапа предобогащения сальмонелл сопровождается приростом бактериальной массы. Прирост бактериальной массы в опытных образцах среды для серотипов S. typhimurium, S. infantis, S. virchow составил более 40 % по сравнению с контролем. Наибольшая степень размножения отмечена при культивировании штаммов серотипа S. hamburg – 66,50 %. Однако штаммы S. choleraesuis показали слабую способность ферментировать пропиленгликоль, что отразилось на результате: прирост бактериальной массы бактерий в опытной среде оказался выше всего на 8,97 %, чем в контрольной.
Определенный интерес вызывает способность исследуемой питательной среды влиять на размножение кишечной палочки, протея, шигелл, золотистого стафилококка и листерий. После 24-часовой инкубации контрольных и опытных образцов ЗПВ со штаммами вышеперечисленных микроорганизмов оказалось, что разработанная среда в разной степени ингибирует размножение данных бактерий (табл. 2).
Таблица 2
Прирост бактериальной массы при культивировании ассоциации микроорганизмов в питательных средах
|
Вид микроорганизмов |
Степень мутности, ед. McF |
Прирост бактериальной массы |
||
|
Опыт |
Контроль |
Абсолютное значение, ед. McF |
% |
|
|
Р. vulgaris |
0,488 ± 0,0641 |
0,613 ± 0,064 |
–0,125 |
–20,39 |
|
E. coli |
0,775 ± 0,0461 |
0,975 ± 0,046 |
–0,2 |
–20,51 |
|
S. aureus |
0,588 ± 0,0351 |
0,713 ± 0,035 |
–0,125 |
–17,53 |
|
L. monocytogenes |
0,025 ± 0,046 |
0,038 ± 0,052 |
–0,013 |
–34,21 |
|
Sh. flexneri |
0,3 ± 0,01 |
0,663 ± 0,052 |
–0,363 |
–54,75 |
1Р < 0,001.
Опытная ЗПВ тормозит размножение золотистого стафилококка на 17,53 %, литерий на 34,21 %, шигелл – более чем на 50 %. По результатам исследований выявлено свойство испытуемой среды сдерживать прирост бактериальной массы протея и кишечной палочки на 20 %. Данный факт имеет огромное значение в повседневной лабораторной практике, так как часто именно БГКП и рода Proteus подавляют развитие сальмонелл, что приводит к ложноотрицательным результатам исследований.
Для объективности оценки полученных данных провели посев ассоциации микроорганизмов на разработанную неселективную среду. Для этого сальмонеллы и взятые в опыт штаммы прочих микроорганизмов в равных количествах (по 1 х 101 МТ/см3) инокулировали в опытные и контрольные флаконы с ЗПВ (табл. 3) .
Очевидна позитивная роль испытуемой среды для неселективного размножения сальмонелл. Прирост бактериальной массы сальмонелл в опытных образцах был на 13,64–64,89 % больше, чем в контроле. Наглядно результаты данного опыта отражены на рисунке.
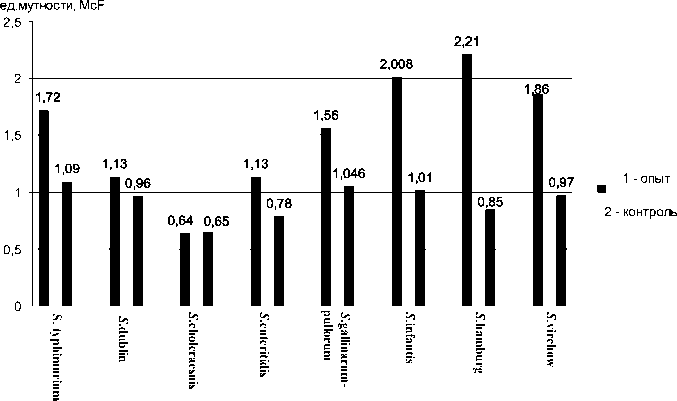
Влияние испытуемой питательной среды на размножение сальмонелл в ассоциации с другими видами микроорганизмов, ед. мутности McF
Таблица 3
Прирост бактериальной массы сальмонелл в ассоциации с сопутствующими микроорганизмами
|
Вид микроорганизмов |
Степень мутности, ед. McF |
Прирост бактериальной массы |
||
|
Опыт |
Контроль |
Абсолютное значение, ед. McF |
% |
|
|
S. typhimurium |
+ |
|||
|
Р. vulgaris |
1,73 ± 0,0951 |
1,08 ± 0,079 |
0,65 |
37,80 |
|
E. coli |
1,70 ± 0,0821 |
1,07 ± 0,082 |
0,63 |
37,06 |
|
S. aureus |
1,73 ± 0,0821 |
1,12 ± 0,079 |
0,61 |
35,26 |
|
L. monocytogenes |
1,74 ± 0,0521 |
1,10 ± 0,082 |
0,64 |
36,78 |
|
Sh. flexneri |
1,72 ± 0,0791 |
1,08 ± 0,079 |
0,64 |
37,21 |
|
Среднее значение |
1,72 ± 0,0181 |
1,09 ± 0,02 |
0,63 |
36,63 |
|
S. Dublin + |
||||
|
Р. vulgaris |
1,11 ± 0,0881 |
0,93 ± 0,048 |
0,18 |
16,22 |
|
E. coli |
1,16 ± 0,0521 |
0,96 ± 0,052 |
0,20 |
17,24 |
|
S. aureus |
1,16 ± 0,0521 |
0,99 ± 0,032 |
0,17 |
14,66 |
|
L. monocytogenes |
1,10 ± 0,01 |
0,95 ± 0,053 |
0,15 |
13,64 |
|
Sh. flexneri |
1,14 ± 0,071 |
0,96 ± 0,07 |
0,18 |
15,79 |
|
Среднее значение |
1,13 ± 0,031 |
0,96 ± 0,02 |
0,17 |
15,04 |
|
S. choleraesuis + |
||||
|
Р. vulgaris |
0,63 ± 0,048 |
0,63 ± 0,048 |
0,0 |
0,0 |
|
E. coli |
0,66 ± 0,052 |
0,69 ± 0,088 |
–0,03 |
–4,55 |
|
S. aureus |
0,63 ± 0,048 |
0,65 ± 0,053 |
–0,02 |
–3,17 |
|
L. monocytogenes |
0,64 ± 0,052 |
0,62 ± 0,042 |
0,02 |
3,13 |
|
Sh. flexneri |
0,62 ± 0,042 |
0,64 ± 0,048 |
–0,02 |
–3,23 |
|
Среднее значение |
0,64 ± 0,015 |
0,65 ± 0,03 |
–0,01 |
–1,54 |
|
S. enteritidis + |
||||
|
Р. vulgaris |
1,13 ± 0,0821 |
0,80 ± 0,082 |
0,33 |
29,20 |
|
E. coli |
1,15 ± 0,071 |
0,86 ± 0,084 |
0,29 |
25,22 |
|
S. aureus |
1,16 ± 0,0521 |
0,72 ± 0,079 |
0,44 |
37,93 |
|
L. monocytogenes |
1,09 ± 0,0571 |
0,83 ± 0,067 |
0,26 |
23,85 |
|
Sh. flexneri |
1,12 ± 0,0791 |
0,69 ± 0,074 |
0,43 |
38,39 |
|
Среднее значение |
1,13 ± 0,031 |
0,78 ± 0,07 |
0,35 |
30,97 |
|
S. gallinarum-pullorum + |
||||
|
Р. vulgaris |
1,70 ± 0,071 |
1,03 ± 0,048 |
0,67 |
39,41 |
|
E. coli |
1,51 ± 0,0741 |
1,05 ± 0,071 |
0,46 |
30,46 |
|
S. aureus |
1,49 ± 0,0741 |
1,07 ± 0,067 |
0,42 |
28,19 |
|
L. monocytogenes |
1,55 ± 0,0531 |
1,04 ± 0,052 |
0,51 |
32,90 |
|
Sh. flexneri |
1,57 ± 0,0671 |
1,04 ± 0,07 |
0,53 |
33,76 |
|
Среднее значение |
1,56 ± 0,081 |
1,046 ± 0,015 |
0,514 |
32,95 |
|
S. infantis + |
||||
|
Р. vulgaris |
1,99 ± 0,0741 |
0,97 ± 0,067 |
1,02 |
51,26 |
|
E. coli |
1,92 ± 0,0421 |
0,94 ± 0,052 |
0,98 |
51,04 |
|
S. aureus |
1,91 ± 0,642 |
1,06 ± 0,052 |
0,85 |
44,50 |
|
L. monocytogenes |
2,11 ± 0,0331 |
1,06 ± 0,053 |
1,05 |
49,76 |
|
Sh. flexneri |
2,11 ± 0,0741 |
1,02 ± 0,079 |
1,09 |
51,66 |
|
Среднее значение |
2,008 ± 0,11 |
1,01 ± 0,05 |
0,998 |
49,70 |
|
S. hamburg + |
||||
|
Р. vulgaris |
2,20 ± 0,1151 |
0,84 ± 0,052 |
1,36 |
61,82 |
|
E. coli |
2,13 ± 0,1421 |
0,89 ± 0,088 |
1,24 |
58,22 |
|
S. aureus |
2,30 ± 0,0821 |
0,89 ± 0,074 |
1,41 |
61,30 |
|
L. monocytogenes |
2,18 ± 0,1321 |
0,82 ± 0,079 |
1,36 |
62,39 |
|
Sh. flexneri |
2,25 ± 0,071 |
0,79 ± 0,057 |
1,46 |
64,89 |
|
Среднее значение |
2,21 ± 0,071 |
0,85 ± 0,04 |
1,36 |
61,54 |
|
S. virchow + |
||||
|
Р. vulgaris |
1,73 ± 0,5762 |
0,96 ± 0,052 |
0,77 |
44,51 |
|
E. coli |
1,83 ± 0,0821 |
0,99 ± 0,057 |
0,84 |
45,90 |
|
S. aureus |
2,02 ± 0,1031 |
0,97 ± 0,048 |
1,05 |
51,98 |
|
L. monocytogenes |
1,87 ± 0,0821 |
0,98 ± 0,079 |
0,89 |
47,59 |
|
Sh. flexneri |
1,86 ± 0,0521 |
0,97 ± 0,082 |
0,89 |
47,85 |
|
Среднее значение |
1,86 ± 0,11 |
0,97 ± 0,01 |
0,89 |
47,85 |
Заключение
Таким образом, выявлена существенная разница между скоростью размножения бактерий рода Salmonella при культивировании в опытных и контрольных образцах питательной среды. Разработанная среда способствовала увеличению чистой культуры сальмонелл в среднем на 38,57 %. При работе с Salmonella spp. в ассоциации с сопутствующей микрофлорой также получили прирост бактериальной массы сальмонелл в опытных образцах. Причем разница биомассы сальмонелл составила от 15,04 до 61,54 % в пользу испытуемой питательной среды. Исключение составили образцы со штаммами S. choleraesuis. Чистые культуры данных штаммов показали прирост бактериальных клеток в опытных образцах на 8,97 % больше, чем в контрольных. При работе с S. choleraesuis в ассоциации с другими микроорганизмами как контрольные, так и опытные пробы были примерно одинаковой мутности, однако количество бактериальных клеток составило 1,3 х 108. Принимая во внимание тот факт, что разрешающая способность бактериологического метода составляет 1 х 105 МТ/см3 [8], а экспесс-методов около 1 х 105–106 МТ/см3 [9], разработка может быть с успехом применима в испытательных лабораториях.
Список литературы Применение обогатительно-селективной среды для культивирования сальмонелл
- Сагабиева, Н.Н. Эпизоотологический мониторинг сальмонеллеза крупного рогатого скота в Курской области: дис. … канд. вет. наук/Н.Н. Сагабиева. -2004. -135 с.
- Слаусгальвис, В. Сальмонеллез: меры борьбы и контроль/В. Слаусгальвис//Животноводство России. -2010. -№ 2. -С. 60-61.
- Микробиологический контроль мяса животных, птицы, яиц и продуктов их переработки: cправочник/С.А. Артемьева, Т.Н. Артемьева, А.И. Дмитриев, В.В. Дорутина. -М.: Колос, 2002. -288 с.
- Шуляк, Б.Ф. Руководство по бактериальным инфекциям собак: в 2 ч./Б.Ф. Шуляк. -М.: ОЛИТА, 2003. -608 с.
- Султанов, З.З. Разработка и усовершенствование технологий получения микробиологических питательных основ и сред: дис. … д-ра биол. наук/З.З. Султанов. -Махачкала, 2008. -271 с.
- Приемопередающее устройство: пат. 2570386 Рос. Федерация. № 2014136524/15; заявл. 08.09.2014; опубл. 10.12.2015. Бюл. № 34. -5 с.
- Мастицкий, С.Э. Методическое пособие по использованию программы Statistica при обработке биологических исследований. -Минск/С.Э. Мастицкий. -Минск: РУП «Институт рыбного хозяйства», 1987. -79 с.
- № 63Fricker, C.R. The isolation of salmonellas andcampylobacters/C.R. Fricker//AppI Bact. -1987. -№ 63 (2). -С. 99-116.
- Пашкова, А.П. Совершенствование элективных питательных сред и биологические свойства свежевыделенных эшерихий и сальмонелл: дис. … канд. биол. наук. -Курск, 2006. -С. 50-54.


