Применение паравертебральной блокады при операциях на аортальном клапане и корне аорты у подростков: серия клинических случаев
Автор: Тарасов Е.М., Хиновкер В.В., Свалов А.И., Бодров Д.А., Фёдоров Д.А.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Случаи из клинической практики
Статья в выпуске: 2 т.29, 2025 года.
Бесплатный доступ
Актуальность. Адекватный контроль болевого синдрома в интра- и послеоперационном периоде является важным аспектом в детской кардиохирургии. Применение паравертебральной блокады как метода регионарной анестезии представляет интерес в связи с ограниченным количеством разрешенных обезболивающих пре- паратов для детей и необходимостью снижения рисков, связанных с использованием опиоидов. Цель. Оценить эффективность и анальгетический потенциал при- менения паравертебральной блокады у подростков при операциях на аортальном клапане и корне аорты. Методы. Проведен ретроспективный анализ данных пяти пациен- тов в возрасте 14–17 лет, перенесших операции на аортальном клапане и корне аорты. Всем пациентам в дополнение к внутривенному обезболиванию опиоидными анальгетиками выполнена паравер- тебральная блокада под ультразвуковой навигацией с введением раствора ропивакаина. Оценивались интра- и послеоперационная потребность в опиоидах, интенсивность болевого синдрома и длительность искусственной вентиляции легких в послеоперационном периоде, осложнения, ассоциированные с применением блокады. Результаты. У всех пациентов достигнут адекватный контроль бо- левого синдрома с минимальной потребностью в опиоидах. Интраоперационная потребность в фентаниле составляла 1,67 [1,5; 2,1] мкг/кг/ч. Четверо пациентов (80 %) были экстубированы на операционном столе, один – через 10 минут после транспортиров- ки в отделение реанимации. Медиана послеоперационной боли по 10-балльной шкале составила 2 балла. Послеоперационная доза фентанила составляла 0,83 [0,83; 0,99] мкг/кг/ч. Осложнений, свя- занных с паравертебральной блокадой, не зафиксировано. Заключение. Применение паравертебральной блокады в дет- ской кардиохирургии позволяет эффективно купировать болевой синдром, использовать низкие дозы опиоидных анальгетиков и способствовать ранней экстубации трахеи, что ускоряет восстановление пациентов и снижает риск послеоперационных осложнений. Для подтверждения результатов необходимы дальнейшие исследования.
Паравертебральная блокада, детская кардиохирургия, послеоперационное обезболивание, ранняя экстубация, клинический случай
Короткий адрес: https://sciup.org/142245856
IDR: 142245856 | DOI: 10.21688/1681-3472-2025-2-47-54
The use of paravertebral block in aortic valve and aortic root surgery in adolescents: a case series
Introduction: Adequate pain control during the intra- and postoperative periods is a crucial aspect of pediatric cardiac surgery. The use of paravertebral block as a regional anesthesia method is of interest due to the limited number of approved analgesics for children and the need to reduce risks associated with the opioid use. Objective: To evaluate the effectiveness and safety of paravertebral block in adolescents undergoing aortic valve and aortic root surgery. Methods: A retrospective analysis of data from five patients aged 14–17 years who underwent aortic valve and aortic root surgery was conducted. All patients received paravertebral block under ultrasound guidance with the administration of ropivacaine. Intra- and postoperative parameters were assessed, including pain intensity, opioid requirements, extubation time, and complications. Results: Adequate pain control was achieved in all patients with minimal opioid requirements. Four patients were extubated on the operating table, and one patient was extubated 10 minutes after transfer to the ICU. Postoperative pain was rated as moderate or low. No complications related to PVB were reported. Conclusion: Adequate pain control was achieved in all patients with minimal opioid requirements. The intraoperative fentanyl requirement was 1.67 [1.5;2.1] mcg/kg/hr. Four patients (80%) were extubated on the operating table, and one was extubated 10 minutes after being transferred to the intensive care unit. Postoperative pain was assessed as moderate or mild. The postoperative fentanyl dose was 0.83 [0.83;0.99] mcg/kg/hr. No complications related to the paravertebral block were observed.
Текст научной статьи Применение паравертебральной блокады при операциях на аортальном клапане и корне аорты у подростков: серия клинических случаев
Цитировать: Тарасов Е.М., Хиновкер В.В., Свалов А.И., Бодров Д.А., Фёдоров Д.А. Применение паравертебральной блокады при операциях на аортальном клапане и корне аорты у подростков: серия клинических случаев. Патология кровообращения и кардиохирургия. 2025;29(2):47-54.
Е.М. Тарасов, В.В. Хиновкер, А.И. Свалов, Д.А. Бодров, Д.А. Фёдоров,
How to cite: Tarasov E.M., Khinovker V.V., Svalov A.I., Bodrov D.A., Fedorov D.A. The use of paravertebral block in aortic valve and aortic root surgery in adolescents: a case series. Patologiya krovoobrashcheniya i kardiokhirurgiya = Circulation Pathology and Cardiac Surgery. 2025;29(2):47-54. (In Russ.)
E.M. Tarasov,
V.V. Khinovker,
A.I. Svalov,
D.A. Bodrov,
D.A. Fedorov,
Introduction: Adequate pain control during the intra-and postoperative periods is a crucial aspect of pediatric cardiac surgery. Interest towards paravertebral block as a regional anesthesia method is due to the limited number of approved analgesics for children and the need to reduce risks associated with the opioid using.
Objective: The study was aimed to assess the efficacy and safety of paravertebral block in adolescents undergoing aortic valve and aortic root surgery.
Methods: A retrospective analysis was based on data from five patients aged 14–17 years who underwent aortic valve and aortic root surgery. All patients underwent paravertebral block with the ropivacaine under ultrasound navigation in addition to intravenous analgesia with opioids. Assessed intra- and postoperative parameters included the need for opioids, pain intensity, extubation time, and complications associated with the block using.
Results: Adequate pain control was achieved in all patients with minimal need for opioid. The intraoperative need for fentanyl was 1.67 [1.5; 2.1] µg/kg/h. Four patients (80%) were extubated on the operating table, and one patient was extubated 10 minutes after transfer to the intensive care unit. The median postoperative pain score was 2 points on a 10-point scale. The postoperative fentanyl dose was 0.83 [0.83; 0.99] µg/kg/h. No complications related to the paravertebral block were recorded.
Conclusion: The using of paravertebral block in pediatric cardiac surgery enables effective pain relief, decreasing in doses of opioid analgesics, and early tracheal extubation that accelerates patient recovery and reduces the risk of postoperative complications. Further studies are needed to confirm these findings.
Введение
Адекватное обезболивание во время и после операции играет важную роль в быстром восстановлении пациентов после операций на сердце и магистральных сосудах [1]. Количество медицинских препаратов, разрешенных к применению в педиатрической практике в Российской Федерации, ограничено, что повышает актуальность мультимодального подхода к аналгезии в интра- и послеоперационном периодах [2].
Паравертебральная блокада (ПВБ) становится всё более популярным методом обезболивания в детской хирургии, являясь альтернативой эпидуральной анестезии [1]. Есть данные, что ПВБ обеспечивает лучший контроль болевого синдрома в сравнении с парентеральными опиоидами и нестероидными противовоспалительными средствами (НПВС) и сравнима по эффекту с эпидуральной анальгезией при торакотомных вмешательствах [3]. Применение данного метода в кардиохирургии с использованием гепарина кажется более безопасным с точки зрения формирования нейроаксиаль-ных гематом, в отличие от эпидуральной анестезии (рис. 1) [4].
В настоящий момент безопасность и эффективность применения ПВБ в детской кардиохирургии изучены недостаточно. Для накопления данных требуются когортные и рандомизированные исследования, которые будут опираться на успешный клинический опыт применения данного вида анестезии. В этой статье мы хотим представить наш опыт применения ПВБ у подростков 14–17 лет при операциях на аортальном клапане и корне аорты, оценив потенциал данной методики с точки зрения опиодсберегающих подходов и ранней активизации пациентов.
Методы
В связи с тем, что данные собирались ретроспективно, одобрения локального этического комитета не требовалось. Критериями включения были: оперативные вмешательства на аортальном клапане и корне аорты в условиях общей анестезии с применением ПВБ, возраст пациентов 10–18 лет. Выборка была сплошной среди пациентов, прооперированных с декабря 2023 по июль 2024 г. Всего в исследование попало 5 пациентов.
Пациенты поступали в операционную с установленным периферическим катетером (Vasofix, BBraun, Германия). После поступления проводилась индукция анестезии (пропофол 1–2,5 мг/кг в/в, фентанил 1–2 мкг/кг в/в, рокурония бромид 0,6–1,0 мг/кг в/в), интубация трахеи. Искусственная вентиляция легких (GE Aespire CS 2, GE Healthcare Technologies, США) проводилась в режиме Pressure control ventilation – Volume Guaranteed (англ., вентиляция, контролируемая по давлению с гарантированным дыхательным объемом) с дыхательным объемом 6–7 мл/кг и минутным объемом, необходимым для поддержания SpO2 в пределах целевых значений и нормокапнии. В условиях анестезии пациентам выполняли катетеризацию внутренней яремной вены.
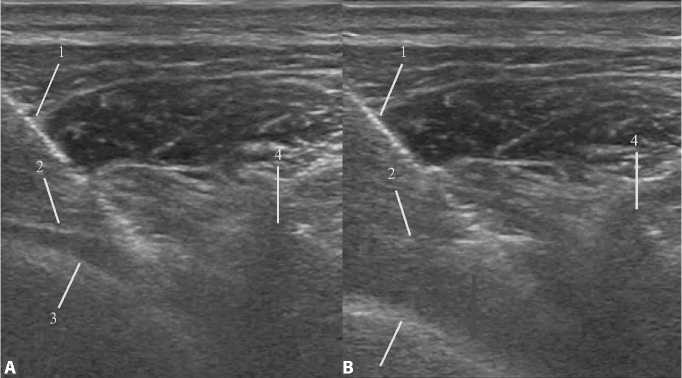
После введения в анестезию пациента помещали в положение на животе. Пункция паравертебрального пространства выполнялась с двух сторон на уровне Th4 – Th5 (иглы Sonoplex 21G 100 мм, Pajunk, Германия) с ультразвуковой (УЗ) навигацией (Philips CX-50, США). Иглу визуализировали методикой «in-plane» (рис. 1, А). Линейный датчик устанавливали в поперечном направлении по отношению к оси позвоночника на уровне Th5 для обнаружения поперечного отростка Th5. Иглу вводили на 0,5–1 см латеральнее датчика и под визуальным контролем проводили до реберно-поперечной связки. Прокол данной связки означал попадание в паравертебральное пространство. После отрицательной аспирационной пробы способом single-shot вводился 0,25 % раствор ропивакаина по 0,5 мл/кг, но не более 30 мл с каждой стороны. Индикатором желаемого распространения местного анестетика было смещение париетальной плевры в переднем направлении по УЗИ (рис. 1, В).
Затем пациента помещали в положение на спине, проводили катетеризацию лучевой артерии (Arteriofix, BBraun, Германия). Поддержание анестезии осуществлялось микроструйным внутривенным введением пропофола в количестве 6–10 мг/кг/ч. В дополнение к регионарной анестезии использовался опиоидный анальгетик фентанил; начальная дозировка – 2 мкг/кг/ч внутривенно. Интраоперационное управление анальгезией проводилось анестезиологом на основе вегетативных реакций организма пациента (артериальное давление, частота сердечных сокращений). Всем пациентам проводились мониторинг нейромышечной проводимости методом «train-of-four» (TOF) и мониторинг глубины анестезии посредством оценки би-спектрального индекса (BIS-мониторинг).
В послеоперационном периоде обезболивание осуществлялось фентанилом (начальная дозировка – 1 мкг/кг/ч в/в) и ацетаминофеном (не более 4 г/сут в/в). При недостаточном контроле острого болевого синдрома (5 баллов и выше по 10-балльной шкале оценки боли) применялись нестероид-
Рис. 1. УЗИ-визуализация паравертебрального пространства (А). Распространение местоного анестетика в паравертебральном пространстве (В).
Примечание. 1 — игла, 2 — рёберно-поперечная связка, 3 — париетальная плевра, 4 — поперечный отросток грудного позвонка; красная стрелка — направление смещения париетальной плевры при введении местного анестетика в паравертебральное пространство
ные противовоспалительные средства (НПВС). Оптимизация анальгезии осуществлялась лечащим доктором на основе выраженности болевого синдрома.
Оцениваемые параметры
Из медицинской документации были получены данные о диагнозе, типе операции, длительности вмешательства и пережатия аорты, расходе опиоидных анальгетиков в интра- и послеоперационном периодах, времени до экстубации трахеи и внепланового введения обезболивающих препаратов. Также в послеоперационном периоде у всех пациентов оценивались интенсивность болевого синдрома до перевода в профильное отделение, наличие послеоперационной тошноты и рвоты (ПОТР), наличие осложнений, связанных с ПВБ (гематома, абсцесс), общая длительность нахождения в ОРИТ, потребность в реинтубации трахеи и наличие послеоперационных осложнений. У всех пациентов боль в послеоперационном периоде оценивалась с помощью 10-балльной шкалы оценки боли через 1, 3, 6, 9, 12, 15 и 18 часов после операции (рис. 2).
Статистический анализ
Статистический анализ выполнялся с помощью компьютерного программного обеспечения jamovi v. 2.5 (Австралия). Ввиду статистически малого количества пробандов, данные представлены медианой и межквартильным интервалом, Медиана [Кв1; Кв3].
Результаты
Данные пациентов
Были проанализированы данные пяти пациентов (см. таблицу). У четверых пациентов (80 %) был врожденный порок сердца (ВПС). Пятый пациент пе- ренес инфекционный эндокардит, осложнившийся формированием абсцесса выходного отдела левого желудочка и фиброзного кольца аортального клапана с перфорацией некоронарной и левой коронарной створок аортального клапана. На момент операции курс антибактериальной терапии был завершен, клинические и лабораторные данные активного инфекционного процесса отсутствовали. Двум пациентам (40 %) было выполнено протезирование аортального клапана, одному (20 %) – протезирование аортального клапана с пластикой корня аорты, еще двум (40 %) – операция Бенталла.
Медианный возраст составил 17 [14; 17] лет, масса тела – 63,2 [60,4; 76,0] кг.
Интра- и послеоперационные данные
Длительность операции – 230 [190; 240] минут, время искусственного кровообращения – 98 [92; 120] минут, а время пережатия аорты – 78 [73; 93] минут. Интраоперационная потребность в фентаниле составила 1,67 [1,5; 2,1] мкг/кг/ч.
Четверо пациентов (80 %) были экстубированы на операционном столе, медиана длительности искусственной вентиляции лёгких (ИВЛ) в послеоперационном периоде составила 0 минут. У пятого пациента длительность ИВЛ в ОРИТ была 10 минут. Послеоперационная доза фентанила составляла 10,75 [10; 11,8] мкг/кг. Двум пациентам (40 %) через 2 часа после вмешательства понадобилось внеплановое введение НПВС. У пациента № 1 НПВС был назначен через час после операции при оценке боли на 5 баллов, а у пациента № 2 – через 9 часов после операции, также при достижении 5 баллов по шкале боли. У обоих пациентов применение НПВС было эффективным и позволило снизить выраженность болевого синдрома.
Общая характеристика пациентов
|
Показатель |
Пациент |
Медиана |
||||
|
1 |
2 |
3 |
4 |
5 |
||
|
Диагноз |
Двустворчатый аортальный клапан. Комбинирова-ный аортальный порок. Аневризматическое расширение восходящего отдела аорты |
Двустворчатый аортальный клапан. Недостаточность аортального клапана |
Инфекционный эндокардит. Абсцесс выходного отдела левого желудочка, фиброзного кольца аортального клапана. Перфорация некоронарной и левой коронарной створок аортального клапана. Пульсирующая гематома выходного отдела левого желудочка |
Двустворчатый аортальный клапан. Комбинированный порок с преобладанием недостаточности. Митрализация, митральная недостаточность |
Двустворчатый аортальный клапан. Комбинированный умеренный аортальный порок без преобладания. Аневризма синусного отдела аорты. |
|
|
Возраст, лет |
17 |
17 |
14 |
17 |
14 |
17 |
|
Пол |
М |
М |
М |
М |
Ж |
|
|
Операция |
Операция Бенталла. Резекция аневризмы восходящего отдела аорты с его протезированием клапансодержа-щим кондуитом |
Протезирование аортального клапана механическим протезом |
Протезирование аортального клапана и пластика ложной аневризмы корня аорты |
Протезирование аортального клапана механическим протезом |
Операция Бенталла. Резекция аневризмы восходящего отдела аорты с его протезированием клапансодержа-щим кондуитом |
|
|
Масса тела, кг |
63,2 |
50,0 |
60,4 |
76,0 |
91,0 |
63,2 |
|
Длительность операции, мин |
190 |
230 |
240 |
180 |
240 |
230 |
|
Время ИК, мин |
98 |
88 |
120 |
92 |
138 |
98 |
|
Длительность пережатия аорты, мин |
78 |
73 |
93 |
65 |
107 |
78 |
Длительность нахождения в ОРИТ составляла 20 [20; 21] часов. Ни у кого из пациентов не было потребности в реинтубации трахеи, не развилась ПОТР, и не было выявлено осложнений, связанных с проведением ПВБ.
Медиана выписки из стационара после операции составила 15 [15; 19] суток.
Обсуждение
Раннее восстановление и ПВБ
Концепция раннего восстановления после операции (англ. Enhanced recovery after surgery, ERAS) приобретает всё большую популярность во всех разделах хирургии [5]. Это обусловлено тем фактом, что данная концепция позволяет уменьшить длительность нахождения пациента в ОРИТ, длитель- ность госпитализации, снизить частоту развития осложнений и оптимизировать использование ресурсов [6; 7]. Послеоперационная боль может быть важнейшим фактором, ведущим к неэффективной вентиляции и нарушению клиренса мокроты [1].
Проведенный Monahan и соавт. метаанализ, который сравнивал применение регионарной анестезии в сочетании с общей анестезией и системной анальгезии в сочетании с общей анестезией в детской кардиохирургии, показал, что применение регионарных методов обезболивания позволило добиться более надежного контроля болевого синдрома в послеоперационном периоде [8]. Однако ни одно из 14 исследований, включенных в этот анализ, не оценивало применение ПВБ. Тем не менее, данные анализа коррелируют с нашими результатами: выраженность болевого синдрома
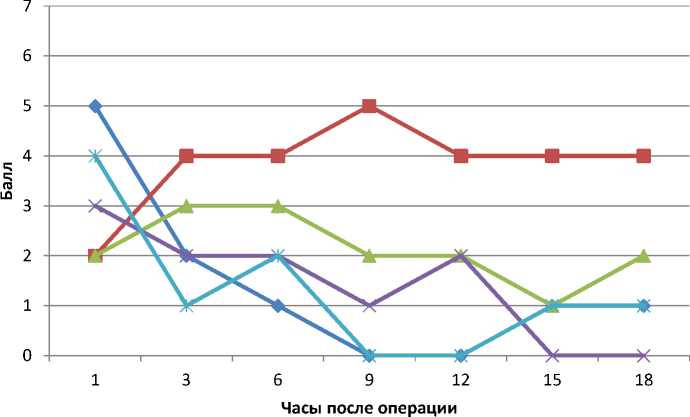
Пациент 1
- ■ -Пациент 2
-A- Пациент 3
Пациент 4
-^Пациент 5
Рис. 2. Оценка послеоперационной боли по 10-балльной шкале оценки боли
у пациентов, у которых использовалась ПВБ, была умеренной или низкой.
Сравнение ПВБ с другими методами регионарной анестезии
Операции на грудной клетке ассоциированы с одним из самых выраженных болевых синдромов в послеоперационном периоде [9]. Это характерно как для стернотомного, так и для торакотомного доступа [10]. Поэтому для улучшения контроля болевого синдрома нейроаксиальные методы обезболивания в хирургии грудной клетки применяются уже не одно десятилетие [11].
В связи с тем, что большинство кардиохирургических вмешательств выполняется в условиях полной гепаринизации, существует риск образования спинальных гематом при проведении эпидуральной или каудальной блокады [12–14].
ПВБ выполняется за пределами центральной нервной системы. Паравертебральное пространство является пространством клиновидной формы, которое сзади ограничено поперечными отростками грудных позвонков и верхними поперечно-реберными связками, париетальной плеврой спереди, а медиально – латеральными поверхностями грудных позвонков и межпозвонковыми дисками (рис. 3) [15]. Данное пространство продолжается в каудальном и краниальном направлениях, что позволяет распространяться местному анестетику в этих направлениях, обеспечивая блокаду на различных уровнях при пункции на одном уровне [16]. В исследовании Davies и соавт., сравнивавших пара- вертебральную и эпидуральную блокады при тора-котомических вмешательствах, было выявлено, что в группе ПВБ легочные осложнения после операций встречались на 64 % реже [17]. В нашей группе ни у кого из пациентов не наблюдалось послеоперационной дыхательной недостаточности, что свидетельствует о благоприятном влиянии ПВБ на респираторную функцию в послеоперационном периоде.
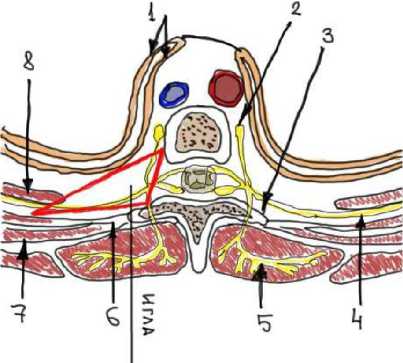
Рис. 3. Анатомия паравертебрального пространства на уровне Th5.
Примечание. 1 – висцеральная и париетальная плевра, 2 – симпатический ганглий, 3 – поперечный отросток, 4 – вентральная ветвь спинномозгового нерва, 5 – дорзальная ветвь, 6 – рёберно-поперечная связка, 7 – ребро, 8 – межрёберная мембрана, красным треугольником
Ранняя экстубация трахеи и опиоидные аналгетики
Вопрос ранней экстубации трахеи в хирургии врожденных пороков сердца стоит достаточно остро. Это связано с тем, что искусственная вентиляция лёгких (ИВЛ) с положительным давлением приводит к уменьшению венозного возврата к сердцу, недостаточному наполнению правого желудочка (ПЖ) и, соответственно, снижению преднагрузки ПЖ [18]. Увеличение внутригрудного давления также увеличивает лёгочное сосудистое сопротивление и, как следствие, постнагрузку на ПЖ [18]. Всё это приводит к снижению ударного объема ПЖ. Увеличение градиента внутригрудного и внегрудного давления приводит к снижению постнагрузки левого желудочка и снижению работы сердца [19]. Следовательно, продленная ИВЛ может оказывать существенное влияние на гемодинамику, особенно у пациентов с гиповолемией или дисфункцией ПЖ, ухудшая послеоперационные исходы [20].
Напротив, спонтанное дыхание улучшает венозный возврат к сердцу во время вдоха, что обусловлено отрицательным внутригрудным давлением. Это, в свою очередь, увеличивает сердечный выброс [19]. Преимущества данного эффекта наиболее выражены у пациентов с одножелудочковой физиологией, перенесших операции Гленна и Фонтена [21]. Однако преимущества самостоятельного дыхания наблюдались и у пациентов, перенесших другие хирургические вмешательства на сердце [22; 23].
Основным модифицируемым фактором риска продленной интубации является интраоперационное применение опиоидных анальгетиков (фентанил) в высоких дозировках (25–50 мкг/кг) [18; 24]. Данные дозировки обусловлены потребностью в снижении стрессового ответа организма, связанного непосредственно с операцией и проведением искусственного кровообращения [25]. El Bendary и соавт. показали, что применение ПВБ в детской кардиохирургии позволило снизить интраоперационную дозу фентанила с 13,6 (± 1,03) до 7,2 (± 1,18) мкг/кг ( p < 0,001) [26]. Данные результаты сопоставимы с нашими: среднее значение интраоперационной дозы фентанила составило 5,76 (95 % ДИ 3,93–7,58) мкг/кг. Такое существенное снижение дозы фентанила позволило экстубировать трахею пациентов прямо на операционном столе или вскоре после транспортировки из операционной [26].
В нашей работе из 5 пациентов четверо (80 %) были экстубированы на операционном столе, и еще один пациент был экстубирован через 10 минут после транспортировки в ОРИТ. Ни одному из них не потребовалась реинтубация трахеи, что подтверждает гипотезу, что применение ПВБ и снижение дозы фентанила позволяет создать условия для ранней активизации пациентов в послеоперационном периоде.
Снижение дозы фентанила в интраоперационном периоде также снижает риск других побочных эффектов, таких как тошнота и рвота, отсутствие которых отмечается у наших пациентов.
Заключение
Наши результаты демонстрируют, что использование паравертебральной блокады в детской кардиохирургии позволяет сохранить адекватный контроль болевого синдрома во время и после операции, ограничивая расход опиоидных анальгетиков. Как следствие опиоидсберегающего подхода, ранняя экстубация и профилактика развития ПОТР могут способствовать ускоренному восстановлению пациентов в послеоперационном периоде. Однако для окончательной оценки эффективности и безопасности ПВБ в данной области необходимо проведение более крупных проспективных рандомизированных контролируемых исследований. Помимо этого, отдельного внимания заслуживает продленная паравертебральная блокада, о применении которой в кардиохирургии имеются лишь единичные публикации.


