Применение сандостатина в профилактике острого воспалительного ответа при операциях реваскуляризации миокарда в условиях искусственного кровообращения
Автор: Зыков Илья Сергеевич, Ломиворотов Владимир Владимирович, Князькова Любовь Георгиевна
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Aнестезиология, реаниматология и перфузиология
Статья в выпуске: 4 т.16, 2012 года.
Бесплатный доступ
Изучено влияние сандостатина на протеазно-ингибиторную систему организма при операциях реваскуляризации миокарда в условиях искусственного кровообращения. Сдвиг протеазно-ингибиторного баланса с преобладанием протеолиза может стать причиной послеоперационных осложнений. Установлено отсутствие влияния препарата на динамику изменений нейтрофильной эластазы, альфа-1-антитрипсина, альфа-2-макроглобулина, С-реактивного белка, церулоплазмина.
Протеазно-ингибиторный баланс, сандостатин, антипротеолиз, искусственное кровообращение
Короткий адрес: https://sciup.org/142140505
IDR: 142140505 | УДК: 616.127-005.4-089.166-78
The application of sandostatin in the prevention of acute inflammatory response at myocardial revascularization under conditions of extracorporeal circulation
The effect of Sandostatin on the protease inhibitor system of the organism at myocardial revascularization under conditions of extracorporeal circulation was investigated. The protease inhibitor balance shift with the predominance of proteolysis can be a cause of postoperative complications. The drug was found to have no effect on the dynamics of changes in neutrophil elastase, alpha-1 -antitrypsin, alpha-2-macroglobulin, C-reactive protein and ceruloplasmin.
Текст научной статьи Применение сандостатина в профилактике острого воспалительного ответа при операциях реваскуляризации миокарда в условиях искусственного кровообращения
Поступила в редакцию 24 октября 2012 г.
В.В. Ломиворо тов, Л.Г. Князькова , 2012
Изучено влияние сандостатина на протеазно-ингибиторную систему организма при операциях реваскуляризации миокарда в условиях искусственного кровообращения. Сдвиг протеазно-ингибиторного баланса с преобладанием протеолиза может стать причиной послеоперационных осложнений. Установлено отсутствие влияния препарата на динамику изменений нейтрофильной эластазы, альфа-1-антитрипсина, альфа-2-макроглобулина, С-реактивного белка, церулоплазмина. Ключевые слова: протеазно-ингибиторный баланс; сандостатин; антипротеолиз; искусственное кровообращение.
Показано, что операции на сердце с искусственным кровообращением (ИК) могут сопровождаться значительным повышением активности некоторых протеиназ и истощением активности их ингибиторов в операционном периоде [1], что может приводить к сдвигу протеазно-ингибиторного баланса плазмы крови в сторону протеолиза. Поскольку выраженное повышение активности протеолиза может стать причиной развития полиорганной и дыхательной недостаточности, а также тромбогеморрагического синдрома, предпринимаются различные меры по профилактике этих осложнений [2]. Поиск фармакологических средств, позволяющих ингибировать гиперпротеолиз и профилактировать развитие послеоперационных осложнений, остается актуальной проблемой анестезиологического обеспечения кардиохирургических вмешательств в условиях ИК.
Наше внимание привлекли экспериментальные работы и результаты клинической практики применения сандостатина в общей хирургии в качестве ингибитора протеолиза при лечении панкреатита. Влияние соматостатина и его аналога сандостатина на организм было показано на нескольких экспериментальных моделях панкреатита с противоречивыми [3], иногда отрицательными [4], а также положительными результатами [5]. Одновременно в клинической практике использование сандостатина приводит к положительным результатам при лечении больных панкреатитом [3]. Так, опыт применения различных дозировок сандостатина (100, 200 или 500 мг три раза ежедневно) показал его эффективность при лечении этого заболевания, а особенно при использовании дозировки препарата 200 мг [6].
Есть данные об антипротеазной активности синтетического аналога соматостатина и его ингибирующем влиянии на нейтрофильную эластазу in vitrо [7]. Установлено, что сандостатин подавляет синтез цитокинов в моноцитах периферической крови при воспалительных реакциях, что делает перспективным его применение при заболеваниях, сопровождающихся развитием системного воспалительного ответа [8]. Показана роль препарата в иммунных реакциях организма. Работ, связанных с применением сандостатина с целью профилактики системного воспалительного ответа в кардиохирургии, нами не обнаружено.
Исходя из анализа данных литературы, можно заключить, что изучение влияния сандостатина на системный воспалительный ответ организма по-прежнему остается актуальной проблемой, в том числе и в случаях кардиохирургических вмешательств с применением ИК. Цель исследования – оценить антипротеолитическую активность сандостатина при операциях реваскуляризации миокарда в условиях ИК.
МАТЕРИАЛ И МЕТОДЫ
За период с 2007 по 2011 г. были обследованы больные ишемической болезнью сердца (ИБС), в числе которых было 46 мужчин и 2 женщины. Средний возраст пациентов 57 лет. Все приглашенные для участия в исследовании лица были разделены на 2 группы: первая – пациенты, проходящие лечение с использованием препарата сан-достатина, и контрольная группа. Всем пациентам была выполнена операция шунтирования пораженных коронарных артерий в условиях нормотермического ИК и кристаллоидной фармакохолодовой кардиоплегии.
Для вводной анестезии использовали фентанил (4 мкг/кг) и дормикум (0,06 мкг/кг). После введения ардуана в дозе 0,1 мг/кг выполняли интубацию трахеи и переводили больного на искусственную вентиляцию легких (ИВЛ) в режиме умеренной гипервентиляции. Анестезия до и после перфузии поддерживалась подачей галогенсодержащего анестетика в дыхательный контур (севоран 1,5–2,0 об%). Во время перфузии вводили дор-микум (0,05–1,0 мг/(кг·ч). По классификации американской ассоциации анестезиологов (ASA), все пациенты имели третью степень анестезиологического риска.
Больным 1-й группы за 10 ч до операции вводили подкожно сандостатин в дозе 0,2 мг, затем после индукции 0,2 мг внутривенно в 50 мл физиологического раствора в течение 3–5 мин. В контрольной группе использовали плацебо-физиологический раствор, который вводили накануне операции подкожно в объеме 2,0 мл.
Обследованные пациенты имели хорошую сократительную функцию миокарда (фракция выброса не менее 50%, по данным УЗИ сердца), не имели эндокринной патологии и почечной дисфункции.
Группы были сопоставимы по клинической характеристике ИБС, объему и характеру хирургического вмешательства, длительности ИК, времени окклюзии аорты (табл. 1). В периферической крови на различных этапах исследования (перед операцией, через 30 и 120 мин после окончания ИК, в 1-е и 3-и сутки после кардиохирургического вмешательства) определяли уровень нейтрофильной эластазы, ее основного ингибитора – альфа-1-антитрипсина, а также альфа-2-макроглобулина, С-реактивного белка (СРБ), церулоплазмина. Оценивали состав периферической крови на этапах исследования: число лейкоцитов в крови, абсолютное и относительное содержание палочкоядерных нейтрофилов, незрелых форм нейтрофилов. Проводили оценку клинического течения послеоперационного периода.
Статистический анализ полученных результатов проведен с помощью программы Statistica 6,0. Для оценки характера распределения в совокупности по выборочным данным использовали тест Колмогорова – Смирнова. Сравнение групп из совокупностей с нормаль- ным распределением проводили с помощью t-критерия Стьюдента для двух зависимых или независимых выборок. Результаты представлены как средние и стандартные ошибки средних (М±m). Статистически значимыми считали различия данных при р<0,05.
РЕЗУЛЬТАТЫ
У больных ИБС перед операцией уровень нейтрофильной эластазы был несколько выше значений, зарегистрированных в группе здоровых лиц (норма <35 нг/мл). Межгрупповых статистически достоверных различий на всех этапах исследования не установлено (табл. 2). Содержание ингибиторов эластазы альфа-1-антитрипсина и альфа-2-мак-роглобулина на всех этапах исследования не имело статистически достоверных различий между группами (табл. 2).
Определение отношения уровня альфа-1-антитрип-сина в плазме к уровню эластазы было использовано для оценки протеазно-ингибиторного баланса. Его показатель не имел достоверных различий между группами на всех этапах исследования (рисунок).
Исходно уровень СРБ в контрольной группе и у пациентов первой группы достоверно не отличался и был в пределах нормальных значений (норма 0,1–0,6 мг/дл). На всех этапах исследования не было обнаружено статистически достоверных различий между уровнем СРБ у пациентов обследованных групп (табл. 2).
Исходное содержание церулоплазмина в обеих группах соответствовало физиологической норме здорового человека (норма 0,19–0,41 г/л), и не отмечалось статистически достоверных различий между группами как исходно, так и на других этапах исследования (табл. 2).
Исходный уровень лейкоцитов у больных всех обследованных групп был в пределах возрастной нормы (норма 4,5–8,0 × 109). Достоверных отличий исходно между группами по общему содержанию лейкоцитов не отмечено. Количество нейтрофилов также было в пределах нормальных значений (норма 1,8–6,5 × 109; 45–70%), и статистически достоверных различий между группами не установлено. Динамика содержания нейтрофилов на всех этапах операции и в ранние сроки после операции имела однонаправленный характер, и достоверных различий между группами не выявлено.
Исходный уровень билирубина в группах не имел статистически достоверных различий и был в пределах нормальных физиологических значений. Содержание креатинина и мочевины исходно во всех группах было в пределах нормы и на всех этапах исследования также не имело достоверных отличий (табл. 3).
При анализе течения послеоперационного периода не было обнаружено межгрупповых различий в объеме отделяемого по дренажам в первые и вторые сутки после
ОБСУЖДЕНИЕ
В ходе проведенного исследования получены данные, которые свидетельствуют о том, что у обследованных пациентов наблюдались признаки гиперпротеолиза, что выражалось в дисбалансе системы протеолиз-анти-
Влияние сандостатина на динамику протеазноингибиторного коэффициента.
Этапы исследования:
-
1 – перед операцией;
-
2 – перед ИК; 3 – 30 мин после ИК; 4 – 2 ч после ИК;
-
5 – 24 ч после ИК;
-
6 – 3-и сутки после ИК.
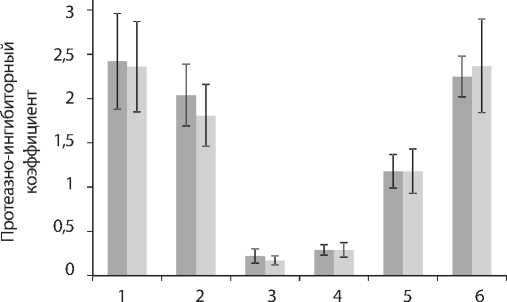
Этапы исследования ■ Сандостатин ■ Контроль
Таблица 3
Содержание в крови билирубина, креатинина, мочевины у обследованных пациентов
|
Группа |
Билирубин, мкмоль/л (норма 3,4–20,5) |
Креатинин, мкмоль/л (норма 44,0–87,0) |
Мочевина, мкмоль/л (норма 2,5–8,3) |
|
|
До операции 1-е сутки п/о |
До операции 1-е сутки п/о |
До операции |
1-е сутки п/о |
|
|
Сандостатин |
15,25±0,96 17,56±2,07 |
95,22±1,92 115,33±3,14 |
5,82±0,27 |
6,91±0,25 |
|
Контроль |
14,79±1,28 13,12±1,58 |
93,05±2,84 105,70±4,82 |
6,75±0,31 |
6,79±0,32 |
Таблица 4
Характеристика послеоперационного периода обследованных пациентов
Полученные результаты указывают на отсутствие влияния сандостатина в терапевтической дозе на уровень нейтрофильной эластазы, альфа-1-антитрипсина, альфа-2-макроглобулина, СРБ, церулоплазмина. Поэтому нецелесообразно применение сандостатина в дозе 0,4 мг с целью антипротеолиза при операциях с ИК.
Единого мнения об эффективности сандостатина и его аналогов при лечении панкреатита также не сформировано. Существует представление о сандостатине как о непосредственном ингибиторе протеолиза и как о пре- парате, который оказывает воздействие на другие звенья патогенеза системного воспаления. В частности, отмечается его влияние на уровень цитокинов, чем объясняются положительные эффекты сандостатина при остром панкреатите [11]. Именно это свойство препарата может предотвратить развитие отдаленных органных повреждений.
Экспериментальные работы показали, что после введения сандостатина наблюдается значимое снижение повышенного уровня воспалительно-ассоциированных цитокинов ИЛ-10 и TGF-beta-1 без изменений вследствие воспаления секреции ферментов поджелудочной железы [12]. Положительное действие сандостатина может быть обусловлено и влиянием его на ИЛ-6 [13], при этом анти-цитокиновые свойства сандостатина изучены недостаточно [14]. Некоторые авторы придерживаются мнения, что антисекреторный эффект сандостатина обусловлен снижением захвата ацинарными клетками поджелудочной железы аминокислот из плазмы [15]. Этот механизм обусловливает уменьшение синтеза панкре- атических ферментов, подавление активности ацинарных клеток и снижение в них аккумуляции ферментов.
Следует предположить, что перспективы дальнейшего изучения клинической роли сандостатина в кардиохирургии – это исследование влияния других доз препарата на развитие воспалительного ответа организма больных, а также дальнейшее выяснение механизмов формирования воспалительной реакции. Авторы не исключают также и ингибирующего влияния использованных в данном исследовании доз сандостатина на весь спектр протеаз и влияния препарата на другие звенья воспалительного ответа, включая цитокины при операциях с ИК.
ВЫВОДЫ
-
1. Применение сандостатина в терапевтических дозах во время операций реваскуляризации миокарда в условиях ИК не оказывает влияния на концентрацию нейтрофильной эластазы, на уровень естественных антипротеолитических ферментов альфа-1-антитрипсина, альфа-2-макроглобулина и на баланс в системе протеолиз-антипротеолиз.
-
2. Применение сандостатина в терапевтических дозах во время операций реваскуляризации миокарда в условиях ИК не оказывает влияния на концентрацию белков острой фазы воспаления.
Список литературы Применение сандостатина в профилактике острого воспалительного ответа при операциях реваскуляризации миокарда в условиях искусственного кровообращения
- Партигулов С.А., Баженова Г.Е., Оглоблина О.Г.//Анестезиология и реаниматология. 1989. № 5. С. 6-9.
- Яворовский А.Г., Трекова Н.А., Зюляева Т.П. и др.//Грудная и серд.-сосудистая хирургия. 2003. № 3. С. 53-57.
- Paran H. et al.//J. Am. Coll. Surg. 1995. V. 181. P. 121-124.
- Degertekin H., Ertan A. et al.//Peptides. 1985. V. 6. P. 1245-1247.
- Paran H. et al.//J. Surg. Res. 1996. V. 62, № 2. P. 201-206.
- Binder M., Uhl W., Friess H. et al.//Digestion. 1994. V. 55. P. 20-23.
- Adeyemi E.O., Savage A.P. et al.//Peptides. 1990. № 11. P. 69-71.
- Гурьянов В.А., Аляутдин Р.Н., Петров В.Е. и др.//Анестезиология и реаниматология. 2002. № 5. С. 68-70.
- Князькова Л.Г., Могутнова Т.А., Зыков И.С. и др.//Патология кровообращения и кардиохирургия. 2009. № 1. С. 43-47.
- Караськов А.М., Ломиворотов В.В.//Биохимическая адаптация организма после кардиохирургических вмешательств. Новосибирск, 2004.
- Uhl W., Buchler M.W. et al.//Gut. 1999. V. 45, №1. P. 97-104.
- Wu H., Chen X., Deng Y. et al.//Sichuan Da Xue Xue Bao Yi Xue Ban. 2003. V. 34, № 2. P. 315-316.
- Jambrik Z., Gyongyosi M., Hegyi P. et al.//Intensive Care Med. 2002. V. 28, № 12. P. 1810-1818.
- Брискин Б.С., Титова Г.П., Рыбаков Г.С. и др.//Анналы хирургической гепатологии. 2001. Т. 6, № 2. С.123-130.
- Гельфанд Б.Р., Бурневич С.З., Гройзик К.Л.//Вестник интенсивной терапии. 1998. № 3. С. 19-24.


