Применение вычислительной гидродинамики для моделирования биореакторов с мешалкой в Ansys Fluent
Автор: Бондаренко Н.А., Гусева Е.В., Сафаров Р.Р.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 2 (96) т.85, 2023 года.
Бесплатный доступ
Биореакторы с мешалкой широко используются в фармацевтической промышленности в производстве различных лекарственны веществ для лечения онкологических заболеваний, болезней сердца и сосудов, вирусных и бактериальных инфекций. Несмотря на широкое использование биореакторов с мешалкой, оптимизация условий перемешивания остается актуальной задачей. В биореакторах такого типа должно осуществляться непрерывное перемешивание клеток в среде с высокой скоростью вращения. В работе рассматривается пример использования вычислительной гидродинамики для исследования и моделирования процесса культивирования бактериальных клеток Escherichia coli в биореакторе периодического действия (NLF, 30 л). Вычислительная гидродинамика использовалась для анализа гидродинамической обстановки в биореакторе с двойной турбинной мешалкой Раштона. Для описания движения потоков и оценки турбулентности в биореакторе периодического действия были использованы многофазная модель Эйлера и модель турбулентности k-𝜀 соответственно, встроенные в программный пакет Ansys Fluent. Была построена геометрическая модель с оригинальными размерами биореактора с мешалкой NLF 30. На основе геометрической модели была создана расчетная сетка по рабочему объему биореактора и проведен подбор оптимальных параметров построения расчетной сетки. В результате моделирования гидродинамического режима были получены профили распределения кинетической энергии турбулентности по объему биореактора и найдены скорости движения клеток при разных скоростях вращения мешалки. Полученные результаты показывают возможность и применимость программного пакета Ansys Fluent для расчета гидродинамической обстановки в биореакторе с мешалкой при разных скоростях перемешивания и при разных объемных долях клеток.
Математическое моделирование, вычислительная гидродинамика, биореактор с мешалкой, модель эйлера, модель турбулентности
Короткий адрес: https://sciup.org/140303197
IDR: 140303197 | УДК: 004.942 | DOI: 10.20914/2310-1202-2023-2-123-129
Application of computational fluid dynamics for simulation of stirred bioreactors in Ansys Fluent
Stirred bioreactors are widely used in the pharmaceutical industry to produce various active substances for the treatment of cancer, heart and vascular diseases, viral and bacterial infections. Despite the widespread use of bioreactors with a stirrer, the optimization of mixing conditions remains an urgent task. In bioreactors of this type, continuous mixing of cells in a medium with a high rotation speed should be carried out. The manuscript considers an example of the use of computational fluid dynamics to study and model the process of cultivation Escherichia coli bacterial cells in a batch bioreactor (NLF, 30 l.). Computational fluid dynamics was used to analyze the hydrodynamic conditions in a bioreactor with a double Rushton turbine stirrer. To describe the movement of flows and evaluate turbulence in a batch bioreactor, the multiphase Euler model and the k-𝜀 turbulence model, respectively, were used, the built-in Ansys Fluent software package. A geometric model was built with the original dimensions of the bioreactor with an NLF 30 stirrer. Based on the geometric model, a computational grid was created for the working volume of the bioreactor and the optimal parameters for constructing the computational grid were selected. As a result of modeling the hydrodynamic regime, the distribution profiles of the turbulence kinetic energy over the volume of the bioreactor were obtained and the velocities of cell movement were found at different speeds of rotation of the stirrer. The obtained results show the possibility and applicability of the Ansys Fluent software package for calculating the hydrodynamic situation in a bioreactor with a stirrer at different stirring rates and at different cell volume fractions.
Текст научной статьи Применение вычислительной гидродинамики для моделирования биореакторов с мешалкой в Ansys Fluent
Каждый биопроцесс представляет собой сложную систему. Биореакторы с мешалкой являются неотъемлемой частью биотехнологического процесса и предоставляют широкий спектр применения для ряда различных отраслей. Биофармацевтические препараты, вакцины, биологические клеточные материалы, пищевые добавки получают путем культивирования
бактерий, грибков или животных клеток в биореакторах. Биореакторы (ферментеры) являются основой биотехнологического процесса культивирования клеток, основной задачей является обеспечение оптимальных условий, способствующих эффективному росту и производству целевых продуктов [1–3].
В биореакторах должны быть соблюдены необходимые массообменные и гидродинами-
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License ческие условия культивирования, регулируются параметры: температура, рН, рО2, скорость перемешивания, пенообразование. Культивируемые клетки находятся в постоянном взаимодействии друг с другом и компонентами среды. Каждое изменение параметров культивирования активирует ответные реакции клеток [4 – 6]. Равномерное перемешивание гарантирует однородность распределения клеточной суспензии, концентрацию питательных веществ и кислорода (если процесс аэробный) в культуральной среде, что увеличивает производительность биореактора [7]. Оптимальным вариантом является подбор скорости перемешивания в соответствии с конкретными условиями процесса, при слишком низких скоростях вращения мешалки происходит снижение роста культуры [8].
Гидродинамические характеристики биореакторов периодического действия в значительной степени зависят от геометрических параметров (тип, размер и положение мешалки, их количество), условий эксплуатации (скорость вращения мешалки, состав среды) и типа клеток. В биореакторах периодического действия можно использовать различные типы мешалок для повышения однородности среды, сокращения времени перемешивания и потребления энергии, а также для контроля условий, вызывающих сдвиговые напряжения, которые при определенных значениях могут негативно влиять на рост и жизнедеятельность клеток [9–11]. Тип мешалки подбирается исходя из условий проведения процесса и вязкости перемешиваемой среды. Традиционно мешалка Раштона широко используется в аэрируемых биореакторах смешения из-за ее способности обеспечивать хорошее перемешивание в объеме питательной среды, диспергировать газ, а также высокой массопередачи газ-жидкость [9]. При невозможности обеспечить требуемый режим перемешивания одной мешалкой на одном валу применяют две и более мешалки одного или различных типов [12, 13]. При размещении на валу нескольких мешалок их конструкция и размеры должны быть одинаковыми, а расстояние между соседними мешалками не должно быть меньше их диаметра.
Применение математического моделирования позволяет исследовать объект и предоставить информацию, которую невозможно получить при помощи экспериментов. Одним из численных подходов, который был успешно использован при моделировании биореакторов, является вычислительная гидродинамика (CFD). Подход продемонстрировал свою хорошую способность прогнозировать движение жидкости в биореакторах с механическим перемешиванием [14, 15].
Вычислительная гидродинамика позволяет рассчитать потоки в биореакторах с простой и сложной геометрией, а также оптимизировать условия процесса без необходимости проведения многочисленных и дорогостоящих экспериментов, сэкономив значительное количество времени и ресурсов [16]. Вычислительная гидродинамика используется в биофармацевтической промышленности в течение многих лет и зарекомендовала себя как важный инструмент для определения технологических характеристик [17].
На рынке программного обеспечения, с точки зрения точности, надежности и скорости проведения расчетов, лидирующую позицию занимает программный пакет Ansys Fluent, представляющий собой интегрированную платформу с широким выбором физических моделей для описания течения жидкостей и газов, процессов тепло- и массообмена, химических реакций в различных процессах и пр. [18].
Программный пакет Ansys Fluent обладает обширными возможностями визуализации результатов математического описания системы как в виде графиков и профилей, так и в виде числовых данных и таблиц.
Методы и этапы
Этапы исследования и моделирования биореактора периодического действия приведены на рисунке 1.
В первую очередь анализируются физикохимические свойства исследуемой культуры клеток, после чего проводится моделирование кинетических зависимостей роста клеток. На основе полученных данных составляется математическая модель, которая должна учитывать процессы гидродинамики биореактора [19].

Рисунок 1. Этапы исследования и моделирования биореактора периодического действия
Figure 1. Stages of research and modeling of a batch bioreactor
Целью данного исследования является демонстрация применения методов вычислительной гидродинамики для анализа гидродинамической обстановки биореакторе периодического действия с двойной турбинной мешалкой Раштона.
Основные этапы моделирования в рамках вычислительной гидродинамики: построение геометрии модели (Geometry), создание на её основе расчётной сетки (Mesh), наложение на сетку свойств рабочего тела, граничных и начальных условий, параметров моделей (Setup), решение полученной модели (Solution) и анализ результатов (Results).
Каждому этапу соответствует свой раздел, в котором возможен ввод и редактирование свойств.
Геометрия биореактора и расчетная сетка
Экспериментальная установка представляет собой цилиндрический биореактор периодического действия рабочим объемом 20 литров фирмы Bioengineering AG (Швейцария), модель NLF 30. Биореактор использовался для культивирования бактериальных клеток Escherichia coli.
Геометрия биореактора с мешалкой, построенная в программном пакете Ansys Fluent 17.0, приведена на рисунке 2. Электронной геометрической моделью биореактора является его непосредственная виртуальная модель, которая описывает геометрические особенности и размеры реального биореактора.
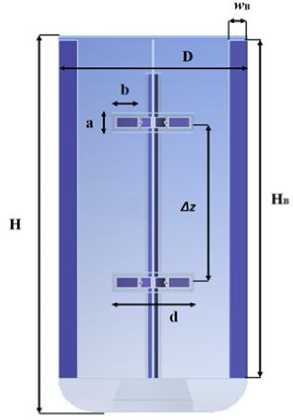
Рисунок 2. Геометрия биореактора с обозначением необходимых параметров
Figure 2. The geometry of the bioreactor with the designation of the required parameters
На основе разработанной геометрической модели была создана расчетная сетка для рассматриваемого моделируемого пространства. Вычислительная сетка создавалась по всей модели биореактора. Была выбрана тетраэдрическая сетка, одна из наиболее популярных расчетных сеток в объемах. Поскольку биореактор периодического действия представляет собой аппарат со сложной структурой потоков, плотность расчетной сетки на поверхности мешалки и отбойников была увеличена путем задания большего количества ячеек в объеме. В свою очередь плотность сетки на поверхности аппарата была снижена, чтобы обеспечить приемлемое время сходимости расчёта.
Расчётная сетка биореактора приведена на рисунке 3.

Рисунок 3. Расчётная сетка по рабочему объёму биореактора
Figure 3. Calculation grid for the working volume of the bioreactor
Размеры сосуда и мешалки приведены в таблице 1.
Таблица 1.
Размеры биореактора и мешалки
Table 1.
Bioreactor and stirrer dimensions
|
Параметр | Parameter |
Значение | Meaning |
|
Рабочий объем (V), л Working volume (V), l |
20 |
|
Диаметр аппарата (D), м Apparatus diameter (D), m |
0,240 |
|
Высота аппарата (H), м Apparatus height (H), m |
0,712 |
|
Диаметр мешалки (d), м Impeller diameter (d), m |
0,090 |
|
Расстояние между двумя мешалками (Δz), м Distance between two impeller (Δz), m |
0,250 |
|
Длина и ширина лопасти мешалки (a • b), м Length and width of the agitator impeller (a • b), m |
0,027 • 0,015 |
|
Высота отбойника (Н в • w В ), м Fender baffle (Н В • w В ), m |
0,450 • 0,025 |
В результате поиска оптимальных параметров построения расчетной сетки было выбрано общее число ячеек: 141905 элементов. При увеличении количества элементов расчетной сетки время моделирования начинает значительно увеличиваться.
Перемешивание осуществлялось мешалкой с двумя крыльчатками (турбина Раштона) с четырьмя лопастями каждая.
Турбина Раштона используется для эффективного перемешивания в биореакторе ипред-ставляет собой дисковую турбину, которая используется во многих процессах культивирования.
На следующем шаге определяются основные параметры и характеристики модели, начальные и граничные условия процесса (входные, выходные параметры), выбираются основные уравнения для решения поставленной задачи.
Результаты
Моделирование гидродинамической обстановки в реакторе периодического действия проводилось в программном комплексе Ansys Fluent 17.0 в структурной схеме модуля Fluid Flow (Fluent) для вычислительной гидродинамики.
Для моделирования гидродинамического режима биореактора задавались следующие допущения:
-
1. Все столкновения клеток со стенками аппарата, отбойниками и мешалкой являются абсолютно упругими, потери энергии отсутствуют;
-
2. Перемешивание внутри биореактора происходит интенсивно, распределение клеток по всему объему биореактора равномерное;
-
3. Плотности и вязкости культуральной среды и клеток отличаются друг от друга, но незначительно, и на протяжении процесса культивирования постоянны.
В исследуемой системе при моделировании биореактора применялась многофазная модель
Эйлера. Это одна из моделей, которая поддерживает моделирование среды «дисперсная фаза-жидкость», в которой одновременно осуществляется решение уравнений сохранения массы и импульса для жидкой (культуральной среды) и дисперсной фазы (клетки бактерий).
Для моделирования турбулентных течений в пакете Ansys Fluent реализован большой набор моделей турбулентности. Для описания процесса турбулентности используется модель k-ɛ, она подходит для описания турбулентности в биореакторе с мешалкой. В Ansys Fluent для моделей заложен стандартный рекомендуемый набор эмпирических констант.
Таким образом, были выбраны необходимые уравнения для моделирования структуры потоков в биореакторе периодического действия, а именно уравнения многофазной модели Эйлера и модель турбулентности k-ε.
Обсуждение
Одним из параметров, который используется для измерения интенсивности турбулентности и оценки эффективности работы мешалки в биореакторах, является кинетическая энергия турбулентности.
Она представляет собой один из важнейших параметров, характеризующий уровень турбулентного режима в аппарате. В результате моделирования гидродинамического режима внутри биореактора для разных скоростей мешалки были получены профили распределения кинетической энергии турбулентности (рисунки 4, 5).
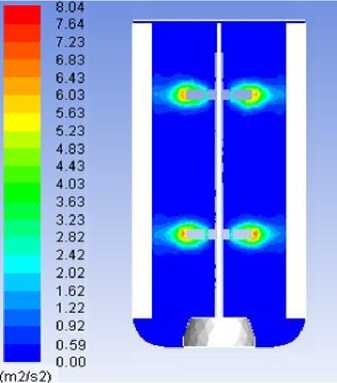
Рисунок 4. Профили распределения кинетической энергии турбулентности в биореакторе при скорости вращения мешалки 250 об/мин
Figure 4. Distribution profiles of the kinetic energy of turbulence in the bioreactor at a stirrer speed of 250 rpm
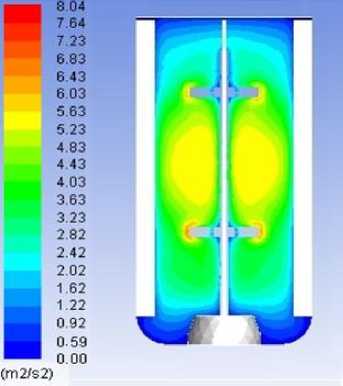
Рисунок 5. Профили распределения кинетической энергии турбулентности в биореакторе при скорости вращения мешалки 750 об/мин
Figure 5. Distribution profiles of the kinetic energy of turbulence in the bioreactor at a stirrer speed of 750 rpm
Процесс культивирования начинался с начальной скорости перемешивания 250 об/мин и был остановлен при скорости вращения 750 об/мин. Из полученных данных видно, что с увеличением скорости вращения мешалки происходит существенное изменение картины потоков в биореакторе.
Максимальная кинетическая энергия турбулентности наблюдается вблизи лопастей мешалки, а в объеме биореактора значения кинетической энергии турбулентности ниже [20]. Как правило, на характеристики турбулентности влияют несколько факторов, включая скорость перемешивания, свойства жидкости и конфигурация крыльчатки мешалки.
Шкала в левой части цветограммы показывает соответствие цветов значениям изменяющейся величины.
При исследовании гидродинамической обстановки в биореакторе были получены скорости движения клеток в объеме биореактора. На основании полученных результатов построена зависимость линейной скорости движения клеток, наблюдаемая около границ мешалки, от скорости вращения мешалки (рисунок 6).
Объемная доля клеток в реакторе составляла α = 0,2.
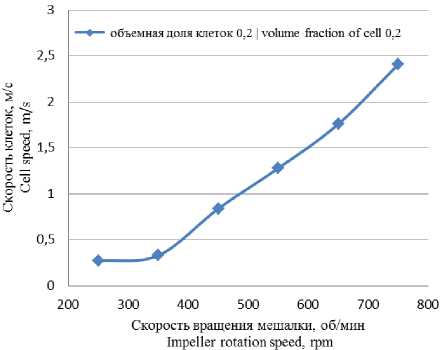
Рисунок 6. Cell movement speeds at different stirrer rotation speeds, (m/s)
Figure 6. Cell movement speeds at different stirrer rotation speeds, (m/s)
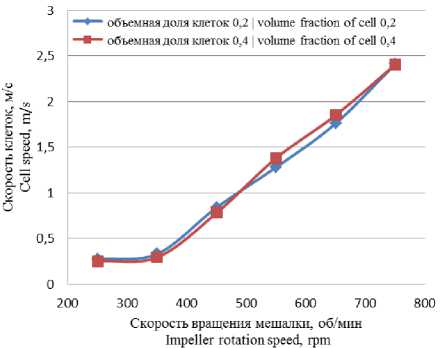
Рисунок 7. Сравнение скоростей клеток при разных объемных долях и при разных скоростях вращения мешалки Figure 7. Comparison of cell velocities at different volume fractions and at different stirrer speeds
Было проведено исследование влияния количества клеток в биореакторе за счет увеличения начальной объемной доли клеток с 0,2 до 0,4. На рисунке 7 приведена зависимость линейной скорости движения клеток при разных объемных долях клеток от скорости вращения мешалки.
Можно сделать вывод, что, начиная с нижнего предела значения скорости вращения мешалки и выше, наблюдается интенсивное перешивание биомассы по всему объему аппарата с объемной долей клеток α = 0,2 и 0,4.
Рабочий объем биореактора достаточно большой и даже при увеличении объёмной доли клеток (т. е. увеличение посевной концентрации приводит к увеличению числа клеток в конце ферментации) линейные скорости клеток меняются незначительно как видно из рисунка 7. Поскольку плотность и вязкость среды и клеток близки, то увеличение объемной доли клеток до α = 0,4 незначительно меняет вязкость системы.
В данном случае возможно проведение процесса в биореакторе данного объема с большей посевной концентрацией клеток (до α = 0,4), что будет способствовать увеличению выхода продукта в конце культивирования.
Заключение
В этом исследовании приведен наглядный пример использования вычислительной гидродинамики CFD для расчета гидродинамической обстановки в биореакторе с мешалкой, работающего в турбулентном режиме. При моделировании CFD использовалась двойная турбинная мешалка Раштона и разные скорости вращения мешалки. Для описания движения потоков и оценки турбулентности в биореакторе периодического действия были использованы многофазная модель Эйлера и модель турбулентности к-Е соответственно, встроенные программный пакет Ansys Fluent. Были определены профили кинетической энергии турбулентности и скорости движения клеток, создаваемые мешалкой из-за турбулентности и градиента скорости. Было проведено исследование кинетики роста клеток за счет увеличения объемной доли клеток в биореакторе. Конфигурация крыльчатки иско-рость вращения мешалки обеспечивали равномерное перемешивание биомассы по всему объему биореактора даже с большей объёмной долей клеток.
Было показано, что CFD-моделирование можно использовать в качестве удобного инструмента для получения подробной информации о биореакторах с мешалкой, что в дальнейшем может способствовать поиску оптимальных условий и масштабированию процесса.
Список литературы Применение вычислительной гидродинамики для моделирования биореакторов с мешалкой в Ansys Fluent
- Li G., Li H., Wei G., He X. et al. Hydrodynamics, mass transfer and cell growth characteristics in a novel microbubble stirred bioreactor employing sintered porous metal plate impeller as gas sparger // Chemical Engineering Science. 2018. V. 192. P. 665-677.
- Schirmer C., Maschke R.W., Pörtner R., Eibl D. An overview of drive systems and sealing types in stirred bioreactors used in biotechnological processes // Appl Microbiol Biotechnol. 2021. V. 105. P. 2225-2242.
- Sharma R., Harrison S.T.L., Tai S.L. Advances in bioreactor systems for the production of biologicals in mammalian cells // ChemBioEng Reviews. 2022. V. 9. № 1. P. 42-62.
- Karthikeyan A., Joseph A., Subramanian R., Nair B.G. Fermenter Design // Industrial Microbiology and Biotechnology. 2022. P. 129-167.
- Wang B., Wang Z., Chen T., Zhao X. Development of novel bioreactor control systems based on smart sensors and actuators // Frontiers in Bioengineering and Biotechnology. 2020. V. 8. P. 7.
- Иванов В.А., Пашкова Е.А., Пестриков С.В. Совершенствование управления фармацевтическим биореактором // Технологии пищевой и перерабатывающей промышленности АПК-продукты здорового питания. 2022. №. 1. С. 137-142.
- Gaugler L., Mast Y., Fitschen J., Hofmann S. et al. Scaling down biopharmaceutical production processes via a single multi compartment bioreactor (SMCB) // Engineering in life sciences. 2022. V. 23. № 1. P. 2100161.
- Минаков Д.В. Мороженко Ю.В., Обрезкова М.В., Шавыркина Н.А., Егорова Е.Ю. Исследование глубинного культивирования грибов рода масленок (Suillus) c целью получения белковых пищевых добавок // Ползуновский вестник. 2020. № 1. С. 32-36.
- Lone S.R., Kumar V., Seay J.R., Englert D.L. et al. Mass Transfer and Rheological Characteristics in a Stirred Tank Bioreactor for Cultivation of Escherichia coli BL21 // Biotechnology and Bioprocess Engineering. 2020. V. 25. P. 766-776.
- Ebrahimi M., Tamer M., Villegas R.M., Chiappetta A. et al. Application of CFD to Analyze the Hydrodynamic Behaviour of a Bioreactor with a Double Impeller // Processes. 2019. V.7. P. 694.
- Villiger T.K., Neunstoecklin B., Karst D.J., Lucas E. et al. Experimental and CFD physical characterization of animal cell bioreactors: From micro - to production scale // Biochemical Engineering Journal. 2018. V. 131. P. 84-94.
- Ebrahimi M., Tamer M., Villegas R.M., Chiappetta A. et al. Application of CFD to analyze the hydrodynamic behaviour of a bioreactor with a double impeller // Processes. 2019. V.7. № 10. P. 694.
- Verma R., Mehan L., Kumar R., Kumar A. et al. Computational fluid dynamic analysis of hydrodynamic shear stress generated by different impeller combinations in stirred bioreactor // Biochemical Engineering Journal. 2019. V. 151. P. 107312.
- Haringa C., Mudde R.F., Noorman H.J. From industrial fermentor to CFD-guided downscaling: what have we learned? // Biochemical Engineering Journal. 2018. V. 140. P. 57-71.
- Vivek V., Eka F.N., Chew W. Mixing studies in an unbaffled bioreactor using a computational model corroborated with in-situ Raman and imaging analyses // Chemical Engineering Journal Advances. 2022. V. 9. P. 100232.
- Ключников А.И., Овсянников В.Ю., Ключникова Д.В., Давыдов А.М. Перспективы методов вычислительной гидродинамики при исследовании мембранных процессов // Вестник ВГУИТ. 2022. T. 84. № 4. С. 32-38.
- Seidel S., Schirmer C., Maschke R.W., Rossi L. et al. Computational fluid dynamics for advanced characterisation of bioreactors used in the biopharmaceutical industry: part I: literature review // Computational Fluid Dynamics - Recent Advances, New Perspectives and Applications. 2023.
- Shafa M., Panchalingam K.M., Walsh T., Richardson T. et al. Computational fluid dynamics modeling, a novel, and effective approach for developing scalable cell therapy manufacturing processes // Biotechnology and Bioengineering. 2019. V. 116. № 12. P. 3228-3241.
- Menshutina N.V., Guseva E.V., Safarov R.R. Boudrant J. Modelling of hollow fiber membrane bioreactor for mammalian cell cultivation using computational hydrodynamics // Bioprocess and Biosystems Engineering. 2020. V. 43. P. 549-567.
- Guler B.A., Deniz I., Demirel Z., Oncel S.S. et al. Computational fluid dynamics modelling of stirred tank photobioreactor for Haematococcus pluvialis production: Hydrodynamics and mixing conditions // Algal Research. 2020. V. 47. P. 101854.


