Природная очаговость инфекционного ринотрахеита крупного рогатого скота в Московской области
Автор: Пчельников А.В., Яцентюк С.П., Красникова М.С., Долинская К.Г.
Статья в выпуске: 4 т.256, 2023 года.
Бесплатный доступ
Целью работы было определение возможной природной очаговости инфекционного ринотрахеита крупного рогатого скота. Активный рандоминизированный мониторинг животноводческих хозяйств Московской области, проведенный в 2020 г., позволил установить хозяйства с активной циркуляцией возбудителя ИРТ КРС. Молекулярно-генетические и серологические исследования материала от диких парнокопытных животных, добытых на территории Московской области в 2019-2022 гг., позволил установить факт циркуляции герпесвируса крупного рогатого скота 1 типа среди этих животных. В результате установлено, что 4 из 5 животноводческих хозяйств, в которых зафиксирована циркуляция полевых штаммов возбудителя ИРТ КРС, находятся в зоне природных очагов этой болезни. Этот факт, а также особенности механизма передачи возбудителя ИРТ КРС между дикими и домашними животными необходимо учитывать при разработке стратегии профилактики и борьбы с этой экономически значимой болезнью.
Ирт, крс, дикие жвачные, пцр, серологические исследования
Короткий адрес: https://sciup.org/142239415
IDR: 142239415 | УДК: 619:616.98:578.831.31:636.2 | DOI: 10.31588/2413_4201_1883_4_256_206
Natural foci of infectious rhinotracheitis of cattle in the Moscow region
The aim of the work was to determine the possible natural foci of infectious rhinotracheitis of cattle. Active rhabdominized monitoring of livestock farms in the Moscow region, conducted in 2020, allowed to establish farms with active circulation of the causative agent of cattle IRT. Molecular genetic and serological studies of the material from wild artiodactyl animals extracted on the territory of the Moscow region in 2019-2022 allowed to establish the fact of circulation of cattle type 1 herpesvirus among these animals. As a result, it was found that 4 out of 5 livestock farms in which the circulation of field strains of the causative agent of cattle is recorded are located in the zone of natural foci of this disease. This fact, as well as the peculiarities of the mechanism of transmission of the causative agent of cattle IRT from wild animals to domestic animals and vice versa, must be taken into account when developing a strategy for the prevention and control of this economically significant disease.
Текст научной статьи Природная очаговость инфекционного ринотрахеита крупного рогатого скота в Московской области
Домашний крупный рогатый скот ( Bos taurus taurus ) (КРС) относится к тому же подотряду Ruminantia отряда парнокопытные ( Artiodactyla ), что и современные лоси, олени и косули, в большом количестве обитающие на Европейской части Российской Федерации. У всех этих животных есть общие возбудители вирусной природы, вызывающие болезни, которые наносят значительный экономический ущерб животноводству. Среди таких возбудителей особое место занимают α-герпесвирусы КРС. В настоящее время исследователи многих стран мира все чаще обращают внимание на изучение циркуляции герпесвируса КРС 1 типа (BoHV-1), возбудителя инфекционного ринотрахеита в популяции диких парнокопытных жвачных животных, а также роли диких животных в передаче этого возбудителя крупному рогатому скоту [5, 4].
В тоже время ряд авторов, занимающихся изучением циркуляции α-герпесвирусов в популяциях диких жвачных животных, утверждают, что значительный антигенный перекрест затрудняет дифференциацию BoHV-1 от антигенно родственных α-герпесвирусов. BoHV-1 входит в кластер близкородственных вирусов семейства Alphaherpesvirinae, включающий, помимо этого вируса еще герпесвирус КРС 5-го типа (BoHV-5), герпесвирус буйвола 1-го типа (BuHV-1), герпесвирус коз 1-го типа
(CpHV-1), герпесвирус оленей 1-го типа (CvHV-1), герпесвирус оленей 2-го типа (CvHV-2) и герпесвирус лосей 1-го типа (ElkHV-1) [7]. Антитела в организме диких животных могут вырабатываться в ответ на инфицирование любым вирусом рассматриваемой группы, а, без учета близкородственных особенностей, могут интерпретироваться, как антитела к BoHV-1 по результатам серологических реакций: реакции нейтрализации (РН) или иммуноферментного анализа (ИФА).
Несмотря на то, что современные принципы ведения животноводства направлены на полное отсутствие непосредственного контакта между КРС и дикими парнокопытными жвачными животными, передача возбудителей указанных болезней между этими животными через факторы передачи возможна [3].
В Российской Федерации этот вопрос до настоящего времени изучен недостаточно.
Авторы настоящей статьи, в рамках проводимых исследований по изучению циркуляции вирусных патогенов КРС в популяции диких парнокопытных животных Московской области, постарались установить теоретическую возможность перекрестной передачи α-герпесвирусов между КРС и дикими парнокопытными жвачными животными.
Материал и методы исследований. Животноводческие хозяйства, в которых циркулирует BoHV-1 были установлены в предыдущих исследованиях [1].
Пробы патологического материала (кусочки паренхиматозных органов, смывы со слизистой оболочки носовой полости, кровь из сердца) отбирались от диких животных, отстрелянных в зимние сезоны охоты 2019-2022 гг. на территории Московской области. Отбор проб проводили посмертно ветеринарными врачами Государственной ветеринарной службы Московской области. Всего было отобрано 626 проб от 177 животных, в том числе: от 137 лосей (Alces alces); 18 косуль (Capreolus capreolus); 3 благородных оленей; 19 животных без информации о виде.
От указанных животных было исследовано 532 образца внутренних органов (носовая перегородка, верхние кольца трахеи, кусочки легкого, сердца, печени, почки), 53 пробы смывов со слизистых и 41 проба сыворотки крови (кровь отбиралась посмертно пункцией полостей сердца).
В ходе пробоподготовки из тканей органов вырезали фрагмент объемом 1 см3, который измельчали на гомогенизаторе Homogenizer type 302 (Mechanika Precyzyjna, Польша) в 10 мл физиологического раствора с добавлением 100 мг стрептомицина и 100 ЕД пенициллина. В дальнейшем гомогенат центрифугировали на центрифуге ОПн-8УХЛ4.2 (Россия) при 3000 об/мин в течение 5 мин; супернатант отбирали и использовали для дальнейших исследований.
Культура клеток. Для репродукции вирусов использовалась перевиваемая культура клеток почки теленка (MDBK).
Вирус. В работе использовался полевой изолят вируса ИРТ КРС «Куйбышев-2006» из коллекции ФГБНУ «Федеральный научный центр – Всероссийский научно-исследовательский институт экспериментальной ветеринарии имени К.И. Скрябина и Я.Р. Коваленко Российской академии наук».
Культивирование клеток. Культивирование проводили в полистироловых культуральных матрасах с площадью роста 75 см2 и невентилируемой крышкой в условиях термостата при 37 °С. В качестве ростовой питательной среды использовали среды Игла DМЕМ («ПанЭко», Россия) с добавлением 7% сыворотки КРС (HyClone, США). Пересев культуры проводили 1 раз в неделю в соотношении 1:4.
Заражение культуры клеток. Заражение культуры клеток проводили после формирования полного монослоя на 1-2-й день после пересева клеток. Ростовую питательную среду сливали. Клеточный монослой дважды отмывали питательной средой Игла DМЕМ. После этого в матрас вносили вируссодержащей материал из расчета 1,0 ТЦД 50 /кл и помещали в термостат при 37 °С на 1 ч. Через 1 ч. содержимое матраса сливали, а в матрас вносили поддерживающую питательную среду (Игла DМЕМ без добавления сыворотки) без предварительного промывания монослоя. После этого матрас помещался в отдельный термостат при 37°С. Цитопатическое действие вирусов учитывали ежедневно визуально под малым увеличением инвертированного микроскопа до отслоения большей части монослоя от субстрата. Вируссодержащую суспензию использовали в дальнейших исследованиях. Определение инфекционного титра вируса проводили по методу Рида и Менча.
Реакция нейтрализации. Реакцию нейтрализации с постоянной дозой вируса 2 lg ТЦД 50 /мл проводили микрометодом, используя полистироловые 96-луночные культуральные планшеты. Каждая проба сыворотки крови исследовалась в двух повторах по три разведения в каждом (1:2 – 1:8). Результаты учитывали через 72 ч. после постановки реакции. Учитывая низкое качество и количество сыворотки в предоставленных пробах, а также невозможность повторного отбора проб у тех же животных, учет результатов реакции проводился качественно (без расчета титра антител в исследуемой сыворотке). Животное считалось серопозитивным при получении положительного результата (отсутствие цитопатического действия вируса) хотя бы в первом разведении сыворотки одного из повторов.
Полимеразная цепная реакция. Выделение нуклеиновых кислот проводили из 100 мкл суспензии органов или смыва со слизистой с помощью набора «РИБО-преп» («АмплиСенс», Россия) по инструкции производителя. ПЦР для выявления ДНК герпесвирусов КРС проводили с использованием тест-системы «РИНОКОР» («АмплиСенс», Россия). Для идентификации родственных α-герпесвирусов проводили амплификацию участка гена gB вирусов с использованием гнездовой ПЦР с праймерами CR30, CR31, CR32, CR33 [0] . Первый раунд с праймерами CR30, CR31 проводили в 25 мкл реакционной смеси, содержащей 2,5× PCR-mix2 blue («АмплиСенс», Россия), 0,25 мМ dNTP, 0,6 мкМ прямого и обратного праймера и 10 мкл выделенной из образца ДНК. Реакцию проводили в амплификаторе «Терцик» («ДНК-технология», Россия) по следующей программе: 5 мин. – 95 °С, 40 циклов (20 сек – 95 °С, 20 сек – 61 °С, 30 сек – 72 °С), 5 мин. – 72 °С. Второй раунд с праймерами CR32, CR33 проводили в аналогичной смеси по программе: 5 мин – 95 °С, 40 циклов (20 сек. – 95 °С, 20 сек. – 63 °С, 20 сек. – 72 °С), 5 мин. – 72 °С с использованием в качестве матрицы 1 мкл реакционной смеси первого раунда.
Секвенирование очищенных ампликонов проводили с использованием набора реагентов BrilliantDye V3.1 на генетическом анализаторе Applied Biosystems 3100 Genetic Analyzer (Life Technologies, США). Полученные нуклеотидные последовательности анализировали с помощью алгоритма BLAST на поисковом интернет-ресурсе National Center for Biotechnology Information ( www.ncbi.nlm.nih.gov ).
Статистическая обработка результатов. Статистическая обработка результатов проводились в программе Microsoft Excel 2016.
Картографический анализ. Карты строили в программе ArcGIS10.8.
Результат исследований. Активный рандомизированный мониторинг животноводческих хозяйств Московской области, проведенный в 2020
г., позволил установить 5 животноводческих хозяйств разных форм собственности, в которых циркулируют полевые штаммы BoHV-1 (Рисунок 1).
Из 177 парнокопытных, добытых на территории Московской области, пробы сыворотки крови отобраны только у 41 животного, в том числе от 36 лосей и 5 косуль. Трудности с отбором были связаны с большим промежутком времени между отстрелом животного и проведенным отбором проб, а также с низкой температурой воздуха в зимний период, что приводило к частичному гемолизу крови, полученному незначительному объему сыворотки и, как следствие, определенными трудностями при ее исследовании в реакции нейтрализации. В образцах сыворотки 19 животных (16 лосей, 3 косули) были детектированы антитела к α-герпесвирусам КРС.
В результате молекулярногенетических исследований (ПЦР) 532 образца патологического материала и 53 проб смывов со слизистых от 177 диких парнокопытных, добытых на территории Московской области, ДНК α-герпесвирусов КРС была выявлена в образцах от 9 животных: в носовых смывах 2 косуль, добытых в 2019 г. на территории г.о. Луховицы; в образцах органов 2 лосей (в образце легкого одного, а также в образцах почки и сердца другого животного), добытых в 2022 г. на территории г.о. Ступино; в носовом смыве 1 косули, добытой в 2022 г. на территории г.о. Серпухов; в образцах 2 косуль, добытых в 2022 г. на территории г.о. Луховицы; в образце 1 лося, добытого в 2022 г. на территории Клинского г.о.; в образце 1 лося, добытого в 2022 г. на территории г.о. Орехово-Зуево.
Анализ нуклеотидных последовательностей фрагмента гена gB, полученных в результате секвенирования продуктов ПЦР с общими для α-герпесвирусов праймерами, подтвердили наличие ДНК BoHV-5 в образце носового смыва от косули и ДНК BoHV-1 в двух пробах органов лосей, отстрелянных в 2022 г. Для остальных проб животных из-за низкого качества образцов не удалось провести идентификацию вирусов герпеса.
животных на территории Московской области представлена на рисунке 2.
Локация добычи указанных
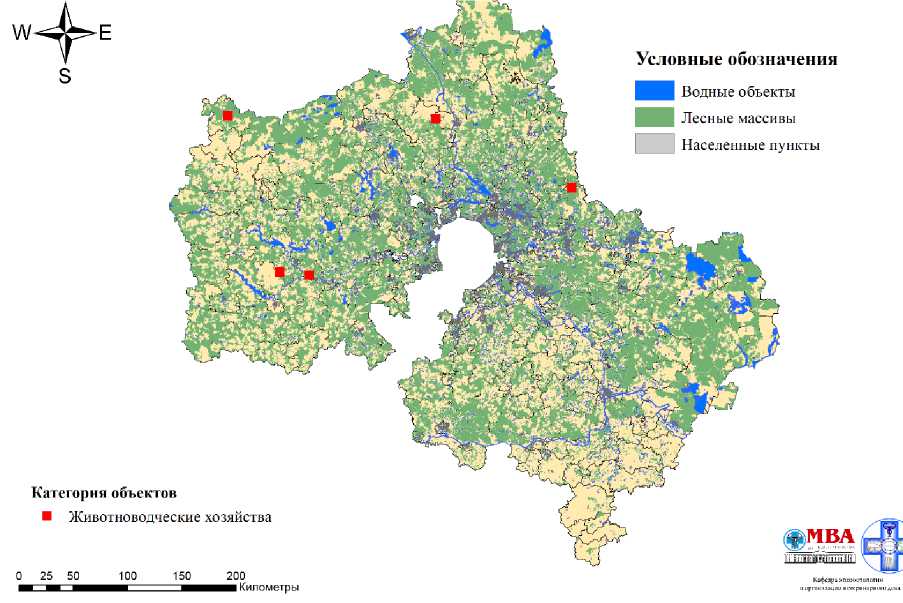
Рисунок 1 – Локация животноводческих хозяйств, в которых зарегистрирована циркуляция полевых штаммов возбудителя ИРТ КРС, на карте Московской области.
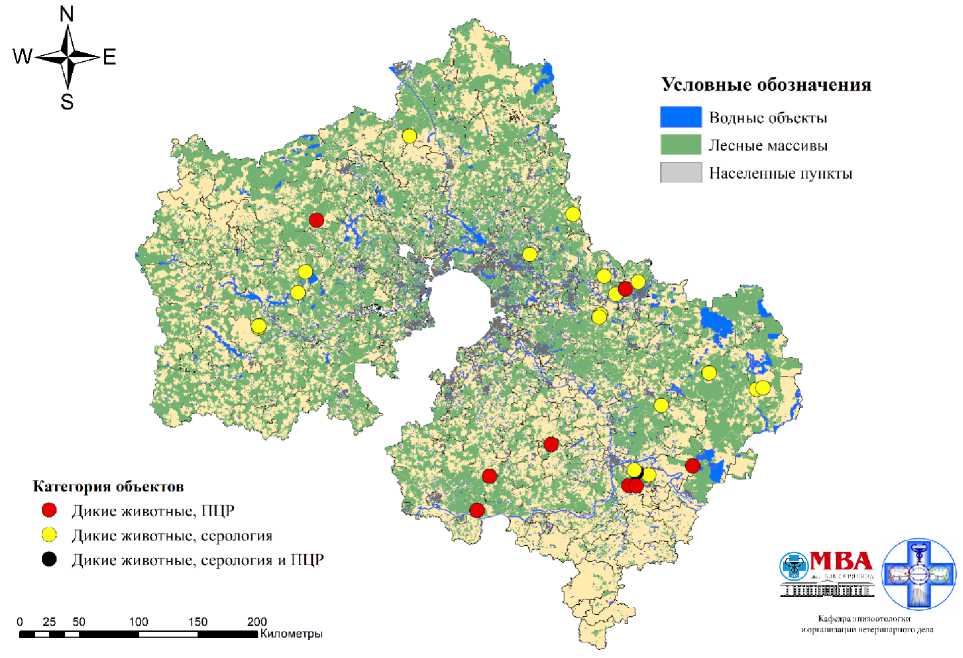
Рисунок 2 – Места добычи диких парнокопытных животных, у которых детектированы геном вируса ИРТ КРС или антитела к нему, на территории Московской области
Наложение локации животноводческих хозяйств, в которых циркулирует BoHV-1, на места добычи диких животных, признанных носителями
α-герпесвирусов, показывает, что 4 из 5 хозяйств находятся в зоне природных очагов α-герпесвирусов (Рисунок 3).
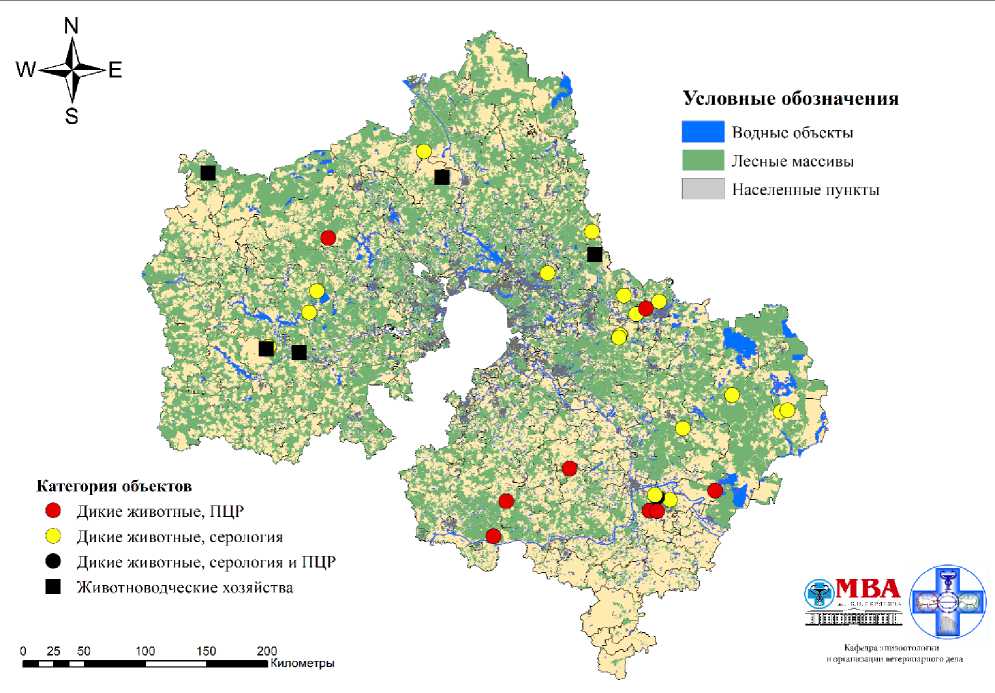
Рисунок 3 – Совмещение геопозиции животноводческих хозяйств с местами отстрела диких животных, носителей вирусов герпеса КРС.
Заключение. Ряд иностранных авторов напрямую указывают на роль диких парнокопытных животных, как природного резервуара возбудителя ИРТ КРС [4].
Нам удалось детектировать геном α-герпесвирусов в различном патологическом материале 9 животных из 177, что составляет 5 % от всей выборки. При анализе рисунка 2 видно, что все указанные животные, за исключением одного, добыты на юге Московской области.
Антитела к вирусу ИРТ КРС детектированы у 19 животных из 41 обследованного. Общая серопревалентность составила 46 %. Большинство из этих 19 животных добыты на юге, юго-востоке и востоке Московской области, 3 животных добыты на западе и 1
– на севере региона. Значительный антигенный перекрест с родственными α-герпесвирусами не позволяет нам утверждать, что все эти животные контактировали непосредственно с возбудителем ИРТ КРС. Тем не менее, факт идентификации генетического материала BoHV-1 в патологическом материале 2 животных подтверждает, что этот возбудитель также циркулирует в популяции диких парнокопытных животных Московской области.
Таким образом мы можем утверждать о наличии на территории Московской области природных очагов ИРТ КРС, носителем возбудителя которого являются дикие парнокопытные животные. На этих же территориях расположены 4 животноводческих хозяйства разной формы собственности (2 крестьянских
(фермерских) хозяйства (КФХ) и 2 мелкотоварные фермы с формой собственности АО), среди животных которых нами ранее зафиксирован факт циркуляции вируса ИРТ КРС.
Мы предполагаем, что взаимная передача α-герпесвирусов между дикими парнокопытными животными и домашним КРС возможен двумя путями:
-
1. КРС, содержащийся в КФХ, в теплый период года выгоняется на пастбища, которые в ночное время могут посещать дикие парнокопытные животные. Устойчивость возбудителя ИРТ КРС во внешней среде достаточна, чтобы обеспечить передачу возбудителя алиментарным путем.
-
2. КРС, содержащийся в мелкотоварных фермах на пастбищах не выпасается, но в теплое время года животные для обеспечения моциона выгоняются в уличные загоны. Кроме того, животноводческие помещения указанных хозяйств не защищены от проникновения насекомых. Хозяйства находятся в непосредственной близости от лесных массивов, в которых были добыты серопозитивные к BoHV-1 дикие животные. В.Н. Сюрин и ряд других авторов утверждают, что в указанных условиях передача возбудителя ИРТ КРС возможна через насекомых [2].
Таким образом факт наличия на территории Московской области природных очагов ИРТ КРС требует пересмотра подходов к профилактике и ликвидации этой болезни в животноводческих хозяйствах Московской области.
Исследование выполнено за счет гранта Российского научного фонда (проект № 22-26-00093, https://rscf.ru/project/22-26-00093/) .
Список литературы Природная очаговость инфекционного ринотрахеита крупного рогатого скота в Московской области
- Пчельников, А. В. Эпизоотическая ситуация по ИРТ КРС на территории Московской и Тверской областей / А. В. Пчельников, С. П. Яцентюк, Е. Р. Сафина // Ветеринария и кормление. - 2021. - № 2. - С. 38-41. DOI: 10.30917/ATT-VK-1814-9588-2021-2-10 EDN: WNDBHU
- Сюрин, В. Н. Вирусные болезни животных / В. Н. Сюрин, А. Я. Самуйленко, Б. В. Соловьев, Н. В. Фомина - М., ВНИТИБП, 1998, 928 с.
- Cripps, J. K.Introduced deer and their potential role in disease transmission to livestock in Australia /j. K. Cripps, C. Pacioni, M. P. Scroggie, A. P. Woolnough, D. S. L. Ramsey // Mammal. - 2019. - V. 49. - P. 60-77. -. DOI: 10.1111/mam.12142
- Lillehaug, A. Antibodies to ruminant alpha-herpesviruses and pestiviruses in Norwegian cervids / A. Lillehaug, T. Vikøren, I. L. Larsen, J. Akerstedt, J. Tharaldsen, K. Handeland //j. Wildl. Dis. - 2003. - V. 39(4). - V. 779-86. -. DOI: 10.7589/0090-3558-39.4.779
- Rola, J. Seroprevalence of bovine herpesvirus 1 related alphaherpesvirus infections in free-living and captive cervids in Poland /j. Rola, M. Larska, W. Socha, J. G. Rola [et al.] // Vet. Microbiol. - 2017. - V. 204. - P. 77-83. -. DOI: 10.1016/j.vetmic.2017.04.006
- Ros, C. Studies of genetic relationships between bovine, caprine, cervine, and rangiferine alphaherpesviruses and improved molecular methods for virus detection and identification / C. Ros, S. Belák //j. Clin. Microbiol. - 1999. - V. 37(5). - P. 1247-53. DOI: 10.1128/JCM.37.5.1247-1253.1999
- Thiry, J.Ruminant alphaherpesviruses related to bovine herpesvirus 1 /j. Thiry, V. Keuser, B. Muylkens, F. Meurens [et al.] // Vet. Res. - 2006. - V. 37(2). - V. 169-90. -:2005052. DOI: 10.1051/vetres


