Профибротические медиаторы в оценке тубулоин-терстициальных изменений при хирургическом лечении больных с мочекаменной болезнью
Автор: Глыбочко П.В., Россоловский Антон Николаевич, Понукалин А.Н., Захарова Н.Б., Маслякова Г.Н., Напшева А.М.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Урология
Статья в выпуске: 3 т.5, 2009 года.
Бесплатный доступ
Целью настоящей работы явилась оценка степени выраженности тубулоинтерстициальных изменений па- ренхимы почек у пациентов с почекаменной болезнью (МКБ) на различных этапах хирургического лечения использованием неинвазивных медиаторов нефрофиброза и ангиогенеза. Проанализированы результаты опе- раций у 65 поциентов мочекаменной болезнью. Определяли содержание молекулярных медиаторов нефрофи- броза в сыворотке крови и моче. Показано, что наиболее информативными неинвазивными маркерами тубу- лоинтерстициального фиброза являются ИЛ12, VEGF в сыворотке крови и экскретирующиеся с мочой ?2 МГ, МСР 1 и NO. Установлено, что у больных с двухсторонним нефролитиазом, на фоне имеющихся выраженных тубулоинтерстициальных повреждений, сохраняющиеся в послеоперационном периоде высокие показатели нефрофиброза могут свидетельствовать о необратимости данных изменений, что ведет к прогрессированию, хронической болезнью почек.
Мочекаменная болезнь, медиаторы нефрофиброза, тубулоинтерстициальные повреждения
Короткий адрес: https://sciup.org/14916941
IDR: 14916941
Profibrotic mediators in assessment of tubulointerstitial changes in surgical treatment of patients with urolithiasis
The aim of present work has been an assessment of degree of tubulointerstitial modifications of kidney parenchyma in patients with urolithiasis in different stages of surgical treatment using non-invasive mediators of nephrofibrosis and angiogenesis. The results of operations of 65 patients have been analysed. The content of nephrofibrosis molecular mediators in blood serum and urine has been determined. It has been shown that the most informative non-invasive mediators of tubulointerstitial fibrosis are IL 12, VEGF in blood serum and b2-microglobulins MG, MCP 1 and NO excreted with urine. Patients with bilateral urolithiasis accompanied by expressive tubulointerstitial damages have had high indices of nephrofibrosis in postoperative period that can indicate irreversibility of these changes, leading to progression of chronic kidney disease.
Текст научной статьи Профибротические медиаторы в оценке тубулоин-терстициальных изменений при хирургическом лечении больных с мочекаменной болезнью
Распространенность мочекаменной болезни (МКБ) в мире прогрессивно увеличивается, и в настоящее время в развитых странах из 10 млн населения 400-500 тыс. человек страдает этим недугом [1]. Вторичный пиелонефрит на фоне МКБ занимает одно из ведущих мест среди заболеваний, приводящих к почечной недостаточности [2].
Основным фактором повреждения почечной паренхимы при МКБ принято считать наличие острой обструкции мочевыводящих путей, клинически проявляющейся почечной коликой [3]. В то же время степень выраженности и длительность обструкции существенно различаются и зависят от многих факторов [4]. Согласно исследованиям отдельных авторов, присутствие камня даже в чашечке нарушает нормальный ритм ее сократительной деятельности, оказывая влияние на уродинамику в целом. Возникающая дискинезия приводит к нарушению микроциркуляции сосочково-чашечной зоны, проявляющемуся отеком, флебостазом, экстравазацией мононуклеарных клеток в интерстиций почки с развитием воспалительных и склеротических изменений. Нарушение уродинамики приводит к изменениям микроциркуляции с последующим развитием воспаления и затем, как его исходу, пролиферативным изменениям как в чашечке, так и в мозговом веществе почки, что еще больше ухудшает их функциональные возможности [5].
На эффективность лечения различных форм нефролитиаза влияет не только степень изменения функции почки в результате нарушения пассажа мочи и перечисленных механизмов, но и интраоперационное повреждение паренхимы при различных видах хирургического лечения больных МКБ [6].
По данным НИИ урологии МЗ и СР РФ [7,8] на 1014 день после операций по поводу коралловидного нефролитиаза у 20% больных сохраняется ухудшение функции почки, которая восстанавливается в зависимости от степени повреждений почечной паренхимы в сроки от 1 до 3 месяцев.
Таким образом, обструкция мочевыводящих путей различной степени выраженности, а также интраоперационное повреждение приводят к ишемии почечной ткани [9], что, по современным данным, ле жит в основе прогрессирования хронической болезни
почек (ХБП), запуская процессы фиброзирования почечной ткани [10]. Наиболее уязвимыми для ишемии при этом являются клетки проксимального отдела ка-нальциевого аппарата. Развитие в дальнейшем протеинурии способствует продукции данными клетками молекул воспаления, вызывающими патологический процесс в интерстиции. В последние десятилетия получено подтверждение первостепенного значения тубулоинтерстициального фиброза, как патоморфо-логической основы прогрессирования почечной недостаточности у больных МКБ [11].
В экспериментальных и клинических исследованиях определен спектр наиболее значимых медиаторов, участвующих в реализации процессов нефрофиброза: хемокины, факторы роста (МСР-1, трансформирующий фактор роста (TGFβ), ряд эндотелиальных факторов) [12]. Кроме того, прогрессирующие заболевания почек приводят к уменьшению числа клубочковых и перитубулярных капилляров, что сопровождается местным нарушением баланса ангиогенных факторов, в том числе снижением экспрессии ангиогенного фактора роста VEGF [13, 14].
Исследований, посвященных динамическому изучению профиброгенных медиаторов в процессе хирургического лечения больных МКБ, практически не представлено [1].
Целью настоящей работы явилась оценка степени выраженности тубулоинтерстициальных изменений паренхимы почек у больных МКБ на различных этапах хирургического лечения с использованием неинвазивных медиаторов нефрофиброза и ангиогенеза.
Материалы и методы исследования. Проанализированы результаты операций у 65 больных МКБ. Контрольную группу составили 20 здоровых добровольцев, сопоставимых по полу и возрасту. Средний возраст пациентов составил 47± 9,4 года. Пациенты были разделены на группы в зависимости от степени выраженности нефролитиаза: 1 группу составили 35 больных с односторонним поражением, во 2 группу, сопоставимую по полу и возрасту, вошли 30 пациентов с двухсторонним процессом. Большинство пациентов обеих групп страдали артериальной гипертензией. По классификации, предложенной экспертами NKF и комитетом K/ DOQI (КDIGO) 2005г., пациенты распределены по стадиям ХБП, при этом большая часть пациентов
2 группы были отнесены к более тяжелой 3 стадии ХБП (р≤0,05) (табл.1).
Все пациенты подвергались оперативному вмешательству. Большей части пациентов выполнялась дистанционная литотрипсия (62%), у 18% больных применены другие малоинвазивные вмешательства. Вместе с тем у 22% пациентов потребовалось открытое оперативное вмешательство в объеме пиелолитотомии, а также нефропиелокаликолитотомии с различными видами дренирующих операций (рис. 1).
Критериями исключения из исследования являлись: возраст старше 60 лет, острый пиелонефрит, блокада мочевыводящих путей с выраженным гидро- и пионефрозом, острая почечная недостаточность, пациенты с 4-5 стадией ХБП, больные с конкрементами мочеточников и нижних мочевыводящих путей, а также пациенты с тяжелой сопутствующей патологией, в том числе выраженной артериальной гипертензией и онкологическими заболеваниями.
Кроме стандартных методов диагностики, включающих лабораторные методы, обзорную и экскреторную урографию, УЗ-сканирование, радионуклидные исследования, пациентам обеих групп определяли содержание наиболее значимых медиаторов нефро-фиброза в сыворотке крови (интерлейкин 6 (ИЛ6), интерлейкин 8 (ИЛ8), интерлейкин 12 (ИЛ12), трансформирующий фактор роста (TGF β), ангиогенный фактор роста (VEGF),оксид азота (NO) и моче: β2

■ ДЛТ
Нефролитолапаксия
■ ЧПНС
■ Открытые операции
Рис.1. Распределение больных по видам хирургического лечения микроглобулин мочи (β2 МГ), моноцитарный хемоат-трактивный протеин-1 (МСР-1), NO).
Исследование проводилось с использованием метода твердофазного иммуноферментного анализа и наборов реактивов. Общепринятым методом оценки синтеза оксида азота (NO) в биологических жидкостях является суммарная оценка нитритов и нитратов [15]. В работе был использован метод непрямой оценки продукции NO по стабильному продукту — нитриту с реактивом Грисса. Концентрации изучаемых медиаторов определяли на дооперационном этапе, на 7-10 сутки и через 1-3 месяца после операции.
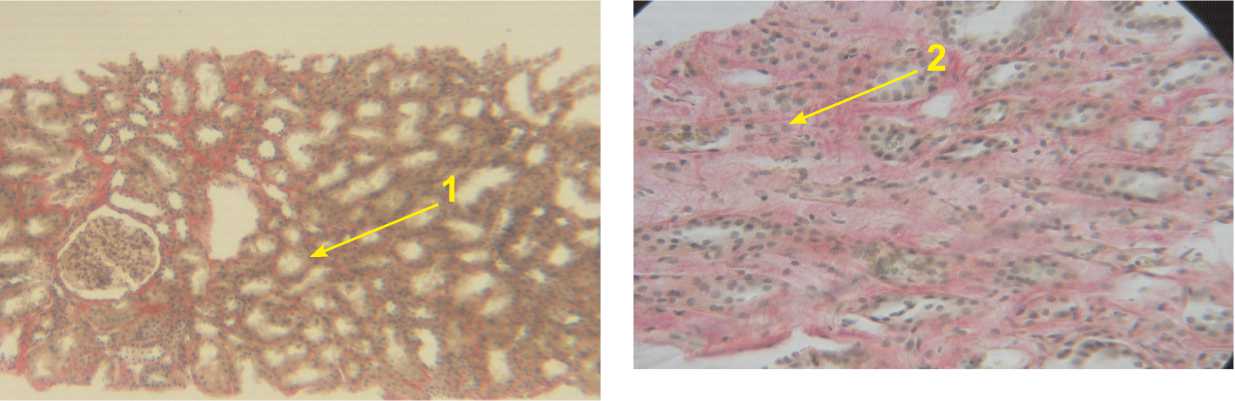
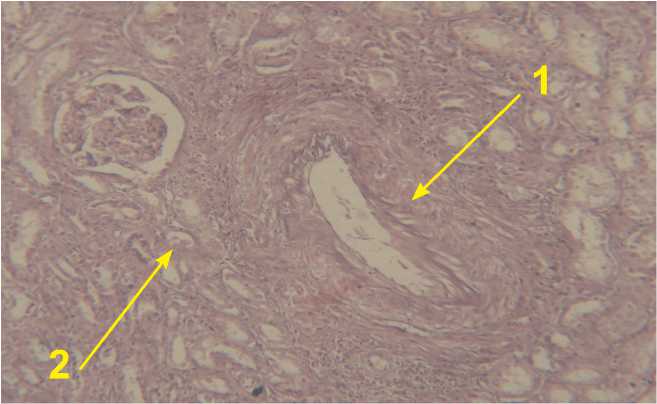
Рис.2. Незначительные тубулоинтерстициальные изменения (изменения составляют <30% объема интерстиция). Окр. пикрофуксиновой смесью по Ван-Гизон. Ув.200.
1 – дистрофия и субатрофия канальцев
2 – очаговый нежно-волокнистый фиброз интерстиция
Таблица 1
Клиническая характеристика пациентов с МКБ
|
Показатель |
1 группа (n=35)(%) |
2 группа (n=30)(%) |
|
Пол м/ж |
20/15 |
16/ 14 |
|
Возраст,г |
47± 9,4 |
51±8,4 |
|
Артериальная гипертензия гипертензияги-пертензия |
32(91,4) |
27 (90) |
|
Изолированные конкременты |
20 (57) |
12(40) |
|
Коралловидный нефролитиаз |
15 (42,8) |
18 (60) |
|
ХБП I (К/DOQI) |
15 (42,8)* |
7(23) |
|
ХБП II |
20 (57) |
14 (47) |
|
ХБП III |
- |
9(30)* |
Примечание: *- достоверность различий при сравнении в группах (р≤0,05 )
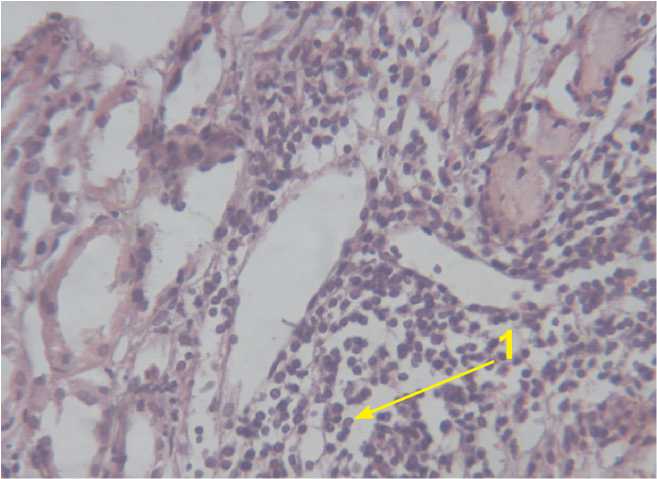
Рис.3. Умеренные тубулоинтерстициальные изменения у пациентов с МКБ Окр. гематоксилин и эозин. Ув.200.
1 — умеренный отек интерстиция и лимфогистиоцитарная инфильтрация

Рис. 6 . Тубулоинтерстициальные изменения у больных МКБ в группах
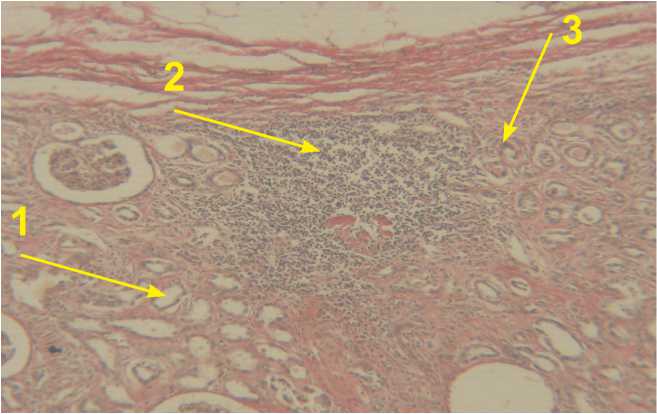
Рис.4. Выраженные тубулоинтерстициальные изменения (> 70%)
Окр. пикрофуксиновой смесью по Ван-Гизон. Ув.200.
1 — уплощение и дегенерация эпителия, атрофия канальцев
2,3 — склероз и лимфогистиоцитарная инфильтрация стромы
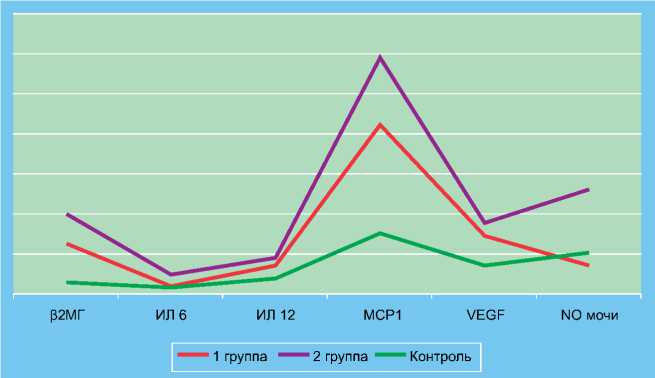
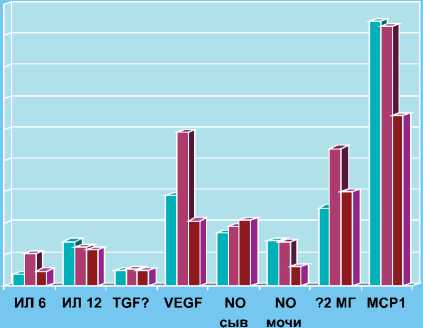
Рис. 7 . Соотношение исследуемых показателей у больных с МКБ и в группе контроля
■ исходно
■ 7-10 сутки
■ 1-3 месяца п/о
Рис. 8 . Динамическая оценка концентрации профибротических медиаторов в послеоперационном периоде у больных с односторонним нефролитиазом
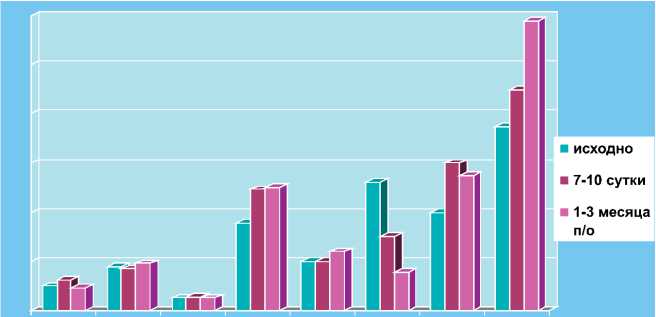
ИЛ6 ИЛ12 TGFP VEGF NO сыв МОмочи ₽ 2 МГ МСР1
Рис. 9. Динамическая оценка концентрации профибротических медиаторов в послеоперационном периоде у больных с двухсторонним нефролитиазом
Рис 5. Выраженные тубулоинтерстициальные изменения (> 70%)
Окр. гематоксилин и эозин. Ув.200.
-
1 — фиброз и утолщение стенок артерий
-
2 — склероз стромы и атрофия канальцев
Для оценки возможности использования исследуемых показателей при МКБ в качестве неинвазивных маркеров неблагоприятного течения заболевания и прогрессирования ХБП, были проанализированы результаты 15 операционных биопсий. Использовалась морфологическая классификация, предложенная В.В.Ставской, С.И.Рябовым, подразделяющая степень тубулоинтерстициальных изменений (ТИИ) на незначительные, умеренные и выраженные (рис. 2–5), составляющие до 30%, от 30 до 70% и более 70% повреждения тубулоинтерстициального аппарата почки соответственно. Незначительные тубулоинтерстициальные изменения выражались в субатрофии канальцев, очаговом нежно-волокнистом фиброзе интерсти-ция и незначительном утолщении стенок артерий и артериол. При прогрессировании процессов нефро-фиброза выявлялись умеренные тубулоинтерстициальные изменения, сопровождающиеся усилением склероза стромы и лимфогистиоцитарной инфильтрации. Выраженные повреждения тубулоинтерстициального аппарата почек также сопровождались диффузной лимфогистиоцитарной инфильтрацией интерстиция на фоне атрофии канальцев, а также фиброза и склерозирования сосудистой стенки.
Статистический анализ данных производился с использованием стандартного пакета программ « STATISTICA 7».
Результаты. Из данных, представленных на рис. 6, следует, что незначительные ТИИ имелись только у пациентов 1 группы (33%), большинство пациентов 1 и 2 групп имели умеренные тубулоинтерстициальные изменения, а у 45% больных с двухсторонним нефролитиазом имелись выраженные ТИИ. При этом именно у пациентов 2 группы отмечалось более выраженное снижение почечных функций, о чем свидетельствует присутствие в этой группе больных с 3 стадией ХБП. При проведении корреляционного анализа получена умеренная корреляция между степенью тубулоинтерстициальных изменений и стадией ХБП (r = 0,5).
Учитывая данные литературы об участии в реализации процессов нефрофиброза целого спектра цитокинов и ростовых факторов, были сопоставлены уровни некоторых медиаторов в изучаемых группах на дооперационном этапе и в контроле. Было выявлено достоверное увеличение концентрации исследуемых показателей у больных МКБ по сравнению с группой контроля (р≤0,05) (рис.7). В то же время при сравнительном анализе уровней профибротических цитокинов в группах больных МКБ показатели во 2 группе оказались достоверно выше всех величин по сравнению с 1 группой (р≤0,05).
Таким образом, сопоставляя данные, полученные при лабораторной диагностике на дооперационном этапе, с результатами морфометрии, можно считать, что исследуемые молекулярные медиаторы допустимо использовать в качестве неинвазивных маркеров нефрофиброза, в частности, при динамической оценки хирургического лечения МКБ.
Для динамической оценки активности процессов нефрофиброза в раннем послеоперационном периоде (на 7-10 сутки) у всех пациентов были определены концентрации профибротических медиаторов в сыворотке крови и в моче (табл.2).
Несмотря на выполненное в полном объеме хирургическое вмешательство, позволяющее в большинстве случаев добиться ликвидации конкрементов, у большинства пациентов обеих групп сохранялся повышенный уровень исследуемых маркеров и даже тенденция к увеличению некоторых из них, что, вероятно, обусловлено активацией процессов фибро — и ангиогенеза на фоне операционной травмы.
Несмотря на то, что тенденция к различию по группам сохранялась на 7-10 сутки после операции, достоверные различия были получены лишь по уровню мочевых показателей и ИЛ 12 (р≤0,05), что может свидетельствовать о наличии локального повреждения на фоне более выраженных исходных изменений у пациентов 2 группы.
Динамическая оценка концентрации профибротических медиаторов у больных МКБ через 7-10 дней после операции
Таблица 2
|
Показатель |
1 группа ( n= 35) |
2 группа (n=30) |
|
ИЛ 6, пг/мл |
10 ±2,3 |
12 ±3,2 |
|
ИЛ 12, пг/мл |
125 ±20,2 |
179 ± 25,4* |
|
TGF β, нг/мл |
5,3 ±0,3 |
5,2 ± 0,25 |
|
VEGF, пг/мл |
491 ± 19,7 |
492 ± 31,4 |
|
NO сыв, мкмоль/л |
19 ± 5, 4 |
20 ± 3,7 |
|
β2 МГ, мкг/мл |
0,4 ± 0,03 |
0,6 ± 0,02* |
|
МСР1 мочи, пг/мл |
830 ±94 |
1202 ±130* |
|
NO мочи, мкмоль/л |
14 ± 3,3 |
30 ± 2,6* |
П р и м еч а н и е : *- достоверность различий при сравнении в группах (р≤0,05 )
Таблица 3
Динамическая оценка концентрации профибротических медиаторов у больных МКБ через 1-3 месяца после операции
|
Показатель |
1 группа ( n= 35) |
2 группа (n=30) |
|
ИЛ 6, пг/мл |
4,7 ±1,3 |
9,2 ±3,2 |
|
ИЛ 12, пг/мл |
114 ±10,2 |
191 ± 20,4* |
|
TGF β, нг/мл |
4,9 ±0,4 |
5,2 ± 0,5 |
|
VEGF, пг/мл |
208 ± 16,7 |
500 ± 21,4* |
|
NO сыв, мкмоль/л |
20,6 ± 3, 2 |
24 ± 3,7 |
|
β2 МГ, мкг/мл |
0,3 ± 0,05 |
0,58 ± 0,04 |
|
МСР1 мочи, пг/мл |
544 ±64 |
1176 ±78* |
|
NO мочи, мкмоль/л |
6,2 ± 2,3 |
15,5 ± 3,6* |
П р и м еч а н и е : *- достоверность различий при сравнении в группах (р≤0,05 )
В то же время через 1-3 месяца после операции у пациентов 1 группы отмечалась тенденция к снижению ряда профибротичеких медиаторов (ИЛ 12, VEGF, NO мочи, МСР1), а у пациентов 2 группы ряд показателей, таких как ИЛ 12, VEGF, NO сыворотки, β2 МГ, МСР1 в моче имел тенденцию к повышению, что, видимо, обусловлено более тяжелыми исходными изменениями почечной паренхимы, возможно, необратимого характера с формированием выраженного тубулоинтерстициального фиброза на фоне активации процессов ангиогенеза (табл.3).
Обсуждение. Таким образом в ходе хирургического лечения больных односторонним нефролитиазом на основании исследуемых маркеров нефрофи-броза, несмотря на результативность большинства оперативных вмешательств, не было получено достоверного подтверждения сокращения выраженности тубулоинтерстициального фиброза (рис.8). А у пациентов с двухсторонним поражением через 1-3 месяца после оперативного вмешательства регистрировалось усиление процессов нефрофиброза, что создает предпосылки для использования у данных пациентов нефропротективной терапии (рис.9).
Выводы. В качестве неинвазивных маркеров тубулоинтерстициального фиброза, являющегося патоморфологической основой ХБП, могут быть использованы такие молекулярные медиаторы, как: ИЛ6, ИЛ12, TGF β, VEGF и NO в сыворотке крови и экскрецию с мочой β2 МГ, МСР1 и NO.
Выполнение оперативного вмешательства, помимо улучшения процессов уро- и гемодинамики приводит к активации процессов нефрофиброза, что требует определения путей воздействия с целью коррекции данного состояния.
У больных с двухсторонним нефролитиазом на фоне имеющихся выраженных тубулоинтерстициальных повреждений, сохраняющиеся в послеоперационном периоде высокие показатели нефрофибро-за могут свидетельствовать о необратимости данных изменений, что ведет к прогрессированию ХБП.
Список литературы Профибротические медиаторы в оценке тубулоин-терстициальных изменений при хирургическом лечении больных с мочекаменной болезнью
- Аляев, Ю.Г. Метафилактика мочекаменной болезни/Ю.Г. Аляев, А.В.Амосов, В.С.Саенко. -М., 2007. -С. 3.
- Иммунологические показатели у больных мочекаменной болезнью и вторичным пиелонефритом/И.И. Казеко, В.А. Жмуров, А.А. Боровский и др.//Урология. -2008. -№1. -С. 11-15.
- Дзеранов, Н.К. Мочекаменная болезнь. Клинические рекомендации/Н.К.Дзеранов, Н.А.Лопаткин. -М., 2007. -С. 29.
- Зубарев, А.В. Диагностический ультразвук. Уро-нефрология. Практическое руководство/А.В.Зубарев, В.Е.Гажонова. -М., 2002. -С.73.
- Есилевский, Ю.М. Реография органов мочеполовой системы/Ю.М. Есилевский. -М., 2004. C.67.
- Казаченко, А.В. Пути профилактики повреждения почек при выполнении нефролитомии или дистанционной литотрипсии по поводу нефролитиаза/А.В.Казаченко, Н.К.Дзеранов, Э.К.Яненко//Урология и нефрология. -1998. -№4. -С. 10-13.
- Камынина, С.А. Результаты оперативного лечения коралловидного нефролитиаза/С.А. Камынина, Э.К.Яненко, Т.В.Обухова//Урология. -2005. -№4. -C. 33-36.
- Лопаткин, Н.А. 15-летний опыт применения ДЛТ в лечении МКБ/Н.А.Лопаткин, Н.К.Дзеранов//Материалы Пленума правления Российского общества урологов. -М., 2003. -С. 5-25.
- Klahr, S. Obstructive nephropathy/S. Klahr//Kidney Int.-1998.-Vol.54. -P. 286-300.
- Fine, L.G. Chronic hypoxia as a mechanism of progression of chronic kidney diseases: from hypothesis to novel therapeutics/L.G. Fine, JT.//Kidney Int. -2008, Jul. 16.
- Pathogenesis of chronic renal failure in the primary glomerulopathies, renal vasculopathies and chronic interstitial nephritides/A. Boble, G.A.Muller, W. Webmann et al.//Kidney Int. 1996; 54:2-92.
- Wada, T. Chemokines:new target molecules in renal diseases/T. Wada, Y.K. Оkoyama Hobayasbi//Clin Exp Neph.-2000.-4; 273-280.
- Шишкин, А.Н. Дисфункция эндотелия у пациентов с прогрессирующими заболеваниями почек/А.Н.Шишкин, Д.В.Кирилюк//Нефрология. -2005; 9: 2: 16-22.
- Gerber H. P. Vascular endothelial growth factor induces expression of the antiapoptotic proteins Bcl-2 and Al in vascular endothelial cells/H.P.Gerber, V. Dixit, N. Ferrara//J Biol Chem. -1998; 273; 13313-13316.
- Nitrite and nitrate determination in plasma: A critical evaluation./H.Моsbage, B. Kok, R. Huzenga et al. Clin Chem. -1995. -Vol. 41. -P. 892-896).


