Прогнозирование эффективности фармакотерапии у больных депрессивными расстройствами на основе генетических показателей
Автор: Вялова Н.М., Симуткин Г.Г., Иванова С.А.
Журнал: Сибирский вестник психиатрии и наркологии @svpin
Рубрика: Биологические исследования
Статья в выпуске: 3 (124), 2024 года.
Бесплатный доступ
Введение. Депрессия как полифакторное, гетерогенное заболевание предопределяется не только неблагоприятными средовыми факторами, но и воздействием многих генов, их взаимовлиянием между собой, что обосновывает целесообразность использования при оценке и прогнозе депрессивной симптоматики генетических методов лабораторной диагностики.
Депрессия, генетика, ремиссия, полиморфизм генов, киназная система, нейротрофическая система, серотонинергическая система
Короткий адрес: https://sciup.org/142243201
IDR: 142243201 | УДК: 616.89-008.454:575.174.015.3:615.214:616-036.66:616-089.17 | DOI: 10.26617/1810-3111-2024-3(124)-28-35
Predicting the effectiveness of pharmacotherapy in patients with depressive disorders based on genetic parameters
Introduction. Depression as a multifactorial, heterogeneous disease is determined not only by unfavorable environmental factors, but also by the impact of many genes, their mutual influence, which justifies the expediency of using genetic methods of laboratory diagnostics in the assessment and prognosis of depressive symptoms.
Текст научной статьи Прогнозирование эффективности фармакотерапии у больных депрессивными расстройствами на основе генетических показателей
Анализ результатов современных эпидемиологических исследований в отношении распространенности большого депрессивного расстройства, дистимии и биполярного аффективного расстройства показывает достаточно высокую встречаемость данных расстройств среди населения в течение жизни: 6,7, 3,6 и 0,8 на 100 человек [1]. Аффективные расстройства, в частности депрессия, являются серьезным экономическим бременем для современного общества и представляют собой причину серьезных нарушений социальной адаптации у соответствующих пациентов [2, 3]. В настоящее время молекулярные и клеточные механизмы, лежащие в основе развития депрессии, мало изучены [4]. Проблема психофармакотерапии депрессивных расстройств является актуальным вопросом психиатрии [5, 6, 7, 8]. Исследования механизмов антидепрессивных препаратов и разработка более эффективных терапевтических средств развиваются медленно [9]. Разработка и внедрение в клиническую практику новых фармакологических средств, их каждодневное назначение базируются на устоявшихся представлениях фармакологов и психиатров о механизмах действия препаратов. Вместе с тем остается насущной проблема недостаточной эффективности современных препаратов, когда эффект плацебо сравним с действием собственно лекарств [10]. Кроме того, клинический ответ на антидепрессивную терапию формируется не ранее чем через 2 недели [11, 12]. Согласно последним данным, около 40% пациентов с депрессией не достигают клинической ремиссии после приема антидепрессантов [8].
В настоящее время предполагается, что генетические факторы могут вносить значительный вклад в развитие депрессивных расстройств, их клинический полиморфизм и в формирование ответа на антидепрессивную психофармакотерапию [13]. По данным литературы, генетические особенности пациентов могут определять от 20 до 95% всех неблагоприятных фармакологических ответов: неэффективность лекарственных средств или нежелательные лекарственные реакции [14, 15, 16].
Внедрение фармакогенетических тестов в клиническую практику позволит индивидуализировано подходить к выбору психотропных препаратов и режима их дозирования, а в некоторых случаях и к тактике ведения пациентов [17, 18]. Подобные подходы лежат в основе персонализированной медицины [19]. Учитывая вышесказанное, проблема прогноза эффективности антидепрессивной терапии является крайне актуальной с точки зрения ведения пациента в ходе лечения и выбора соответствующих лекарственных препаратов и режима дозирования. Разработка методов, позволяющих индивидуализировать психофармакотерапию, является одной из важных задач фундаментальной медицины на современном этапе.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Разработка медицинской технологии прогноза ремиссии у больных депрессивными расстройствами в ходе получаемой психофармакотерапии на основе генетических показателей.
МАТЕРИАЛЫ И МЕТОДЫ
Обследовано 339 пациентов с депрессивными расстройствами (275 женщин и 64 мужчины), проходивших курс лечения в отделении аффективных состояний клиники НИИ психического здоровья Томского НИМЦ. Диагностическая оценка и клиническая верификация проводились врачами-психиатрами. Средний возраст пациентов составил 49,7±11,6 года (возрастной диапазон – от 25 до 70 лет). Исследование проводилось в соответствии с этическими принципами проведения исследований с участием людей. Обязательным являлось наличие информированного согласия от пациентов на проведение лабораторного и генетического исследований и соблюдение врачебных предписаний.
Критерии включения: диагнозы «депрессивный эпизод» (F32) и «рекуррентное депрессивное расстройство» (F33) в соответствии с критериями МКБ-10, повторное обращение за психиатрической помощью, возраст пациентов от 25 до 70 лет, согласие пациента на участие в исследовании.
Критерии исключения: наличие сопутствующих психических расстройств и расстройств поведения, связанных с употреблением психоактивных веществ (F10-F19, МКБ-10), невротических, связанных со стрессом и соматоформных расстройств (F40-F49, МКБ-10), а также сопутствующей соматической патологии в стадии обострения, хронических воспалительных заболеваний.
Оценку тяжести текущего депрессивного эпизода выполняли с использованием шкалы депрессии Гамильтона (17-пунктный вариант, HDRS-17). Согласно количественной балльной оценке по HDRS-17, степень тяжести депрессии оценивалась как легкая (от 8 до 16 баллов), умеренная (от 17 до 23 баллов) и тяжелая (24 балла и более). Оценку наличия/отсутствия ремиссии проводили на 28-й день терапии. Значение балла по HDRS-17 менее или равное 7 интерпретировалось как наличие ремиссии. Большинство обследованных пациентов (n=216, 63,7%) достигли ремиссии, оцененной по шкале Гамильтона на 28-й день. Вместе с тем по итогам терапии у четверти пациентов (n=90, 26,5%) ремиссия отсутствовала. Социальнодемографическая и клиническая характеристики обследованных пациентов с депрессивными расстройствами представлены в таблице 1.
Таблица 1. Социально-демографические и клинические характеристики обследованных пациентов с депрессивными расстройствами
|
Показатель |
Общая выборка |
Пациенты с ремиссией |
Пациенты без ремиссии |
|
Пол (мужчины/женщины) |
64/275 |
38/178 |
17/73 |
|
Возраст, лет |
49,7±11,6 |
49,4±11,5 |
51,3±10,3 |
|
Количество эпизодов |
1,5±1,9 |
1,5±2,0 |
1,5±2,1 |
|
Длительность заболевания, лет |
5,1±7,3 |
4,4±6,5 |
6,2±8,7 |
|
Тяжесть депрессии (легкая/умеренная/тяжелая) |
11/232/33 |
9/165/16 |
1/59/17 |
Предлагаемая технология включает следующие этапы: забор биологического материала (крови натощак из вены), выделение геномной ДНК из венозной крови, генотипирование ДНК.
При поступлении пациента в клинику производилось взятие образца крови из локтевой вены в пробирки фирмы BD Vacutainer с антикоагулянтом
EDTA, нанесенным на внутренние стенки пробирки. Выделение геномной ДНК проводилось стандартным фенол-хлороформным микрометодом с последующим генотипированием высокоточным методом ПЦР в реальном времени с помощью наборов TaqMan1 Validated SNP Genotyping Assay фирмы Life Technologies на приборе QuantStudio 5
(Applied Biosystems, США) (входит в ЦКП «Медицинская геномика» Томского НИМЦ).
Методология анализа заключалась в следующем. На первом этапе проведен анализ ассоциаций генетических маркеров с фактом ремиссии по типу «случай-контроль». Анализ проводили с помощью логистической регрессии, включающей в качестве предикторов генетический полиморфизм (аддитивный эффект), пол, возраст, длительность заболевания, количество депрессивных эпизодов и тяжесть заболевания. По результатам исследования для продолжения работы были выбраны полиморфизмы, p-значение которых не превышало 0,1. Логистическую регрессию применяли для построения трех предиктивных моделей, включающих факторы: 1) генетические, социально-демографические и клинические, 2) генетические, 3) социальнодемографические и клинические. Для всех трех моделей были получены предсказанные значения вероятности ремиссии и таблицы переклассификации, которые использовали для расчетов статистик чувствительности, специфичности, позитивного и негативного предсказательных значений. ROC-анализ включал расчет площади под кривой чувствительности и специфичности (AUC). Все расчеты проводили в программной среде R.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В выборке обследованных пациентов с депрессивными расстройствами социально-демографические и клинические показатели в группах с ремиссией и без ремиссии статистически значимо не отличались (p>0,05), за исключением тяжести течения депрессивного расстройства. Так, у пациентов с отсутствием ремиссии со статистически значимо (p=0,004) более высокой частотой зафиксировано тяжелое течение болезни (соответственно 0,22 и 0,08 у лиц без ремиссии и с ремиссией).
По заключительным результатам ассоциативных генетических исследований разработана новая медицинская технология, представляющая собой генотип-специфический подход к прогнозированию ремиссии у больных депрессивными расстройствами в ходе психофармакотерапии на основе генотипирования ДНК, выделенной из крови.
Всего было изучено 58 однонуклеотидных полиморфизмов генов трех систем: киназной (гены PIP5K2A, SGK1, GSK3B, AKT1 ), нейротрофической (гены BDNF, NGF, NRG1 ) и серотонинергической (гены рецепторов серотонина HTR1A , HTR1B , HTR2A , HTR2C , HTR3A , HTR3B , HTR6 и генов ферментов синтеза и метаболизма серотонина МАО-А , ТPН1 , ТPН2 . Из рассмотрения исключили 4 полиморфных варианта (rs1743940, rs9373085, rs1800042, rs33940208) с частотой редкого аллеля менее 5% и низкой эффективностью генотипирования (<80%).
С помощью статистической модели логистической регрессии была установлена статистически значимая (p<0,05) ассоциация ремиссии с 6 полиморфизмами: rs946961, rs943190 и rs8341 гена нейрональной киназы PIP5KA2 , rs7997012 гена рецептора серотонина HTR2A , rs17326429 гена рецептора серотонина HTR2C , rs3924999 гена NRG1 (рис. 1, табл. 2).
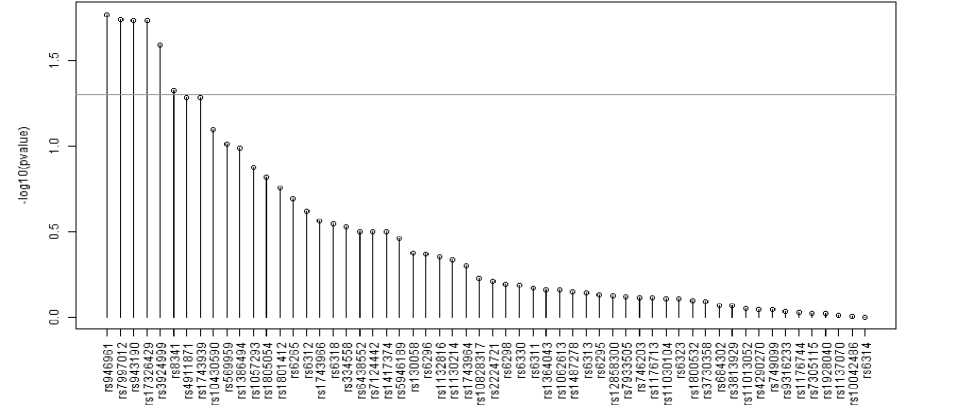
Рисунок 1 . Уровень значимости (р) (-log10) по результатам логической регрессии для отдельных полиморфизмов . Зеленая линия соответствует номинальному уровню значимости (α=0,05)
Для выполнения дальнейшего анализа было выбрано 9 полиморфизмов, p-значение которых не превышало 0,01, а также для которых было проге-нотипировано не менее 100 человек: rs946961 (ген PIP5KA2 ), rs7997012 (ген HTR2A ), rs943190 (ген
PIP5KA2 ), rs17326429 (ген HTR2C ), rs3924999 (ген NRG1 ), rs8341 (ген PIP5KA2 ), rs4911871 (ген HTR2C ), rs10430590 (ген PIP4K2A ), rs569959 (ген HTR2C ).
Т а б л и ц а 2. Результаты логистической регрессии и характеристика исследованных полиморфизмов
|
SNP |
Estimate |
SE |
Z |
P |
OR |
LOWER |
UPPER |
N |
MAF |
|
rs946961 |
0,567 |
0,238 |
2,384 |
0,017 |
1,763 |
1,106 |
2,808 |
188 |
0,4 |
|
rs7997012 |
0,955 |
0,405 |
2,359 |
0,018 |
2,598 |
1,175 |
5,744 |
106 |
0,5 |
|
rs943190 |
0,559 |
0,237 |
2,355 |
0,019 |
1,748 |
1,098 |
2,784 |
189 |
0,47 |
|
rs17326429 |
0,956 |
0,406 |
2,354 |
0,019 |
2,601 |
1,173 |
5,764 |
108 |
0,16 |
|
rs3924999 |
0,679 |
0,305 |
2,227 |
0,026 |
1,971 |
1,085 |
3,581 |
134 |
0,38 |
|
rs8341 |
0,554 |
0,280 |
1,981 |
0,048 |
1,741 |
1,006 |
3,012 |
188 |
0,36 |
|
rs4911871 |
0,714 |
0,368 |
1,942 |
0,052 |
2,043 |
0,993 |
4,200 |
110 |
0,19 |
|
rs1743939 |
1,960 |
1,010 |
1,939 |
0,052 |
7,096 |
0,979 |
51,416 |
54 |
0,1 |
|
rs10430590 |
0,509 |
0,290 |
1,752 |
0,080 |
1,663 |
0,941 |
2,939 |
177 |
0,33 |
|
rs569959 |
0,525 |
0,317 |
1,656 |
0,098 |
1,691 |
0,908 |
3,149 |
111 |
0,32 |
|
rs1386494 |
0,940 |
0,576 |
1,632 |
0,103 |
2,561 |
0,828 |
7,921 |
112 |
0,15 |
|
rs1057293 |
-0,660 |
0,441 |
-1,498 |
0,134 |
0,517 |
0,218 |
1,226 |
133 |
0,12 |
|
rs1805054 |
-0,767 |
0,536 |
-1,431 |
0,152 |
0,464 |
0,162 |
1,328 |
106 |
0,18 |
|
rs1801412 |
0,726 |
0,536 |
1,356 |
0,175 |
2,068 |
0,723 |
5,911 |
109 |
0,07 |
|
rs6265 |
-0,495 |
0,388 |
-1,276 |
0,202 |
0,610 |
0,285 |
1,304 |
107 |
0,21 |
|
rs6312 |
0,721 |
0,614 |
1,174 |
0,240 |
2,057 |
0,617 |
6,854 |
109 |
0,05 |
|
rs1743966 |
-0,325 |
0,297 |
-1,095 |
0,274 |
0,723 |
0,404 |
1,293 |
156 |
0,19 |
|
rs6318 |
0,556 |
0,519 |
1,072 |
0,284 |
1,744 |
0,631 |
4,821 |
111 |
0,15 |
|
rs334558 |
0,852 |
0,815 |
1,046 |
0,296 |
2,344 |
0,475 |
11,577 |
53 |
0,47 |
|
rs6438552 |
0,813 |
0,808 |
1,006 |
0,314 |
2,255 |
0,462 |
11,001 |
53 |
0,48 |
|
rs7124442 |
0,360 |
0,358 |
1,005 |
0,315 |
1,433 |
0,710 |
2,893 |
97 |
0,29 |
|
rs1417374 |
-0,215 |
0,215 |
-1,003 |
0,316 |
0,806 |
0,529 |
1,228 |
186 |
0,43 |
|
rs5946189 |
0,484 |
0,514 |
0,942 |
0,346 |
1,622 |
0,593 |
4,438 |
108 |
0,13 |
|
rs130058 |
-0,406 |
0,506 |
-0,803 |
0,422 |
0,666 |
0,247 |
1,795 |
99 |
0,22 |
|
rs6296 |
0,305 |
0,385 |
0,792 |
0,429 |
1,357 |
0,638 |
2,887 |
112 |
0,29 |
|
rs1132816 |
-0,214 |
0,278 |
-0,768 |
0,442 |
0,808 |
0,468 |
1,393 |
189 |
0,25 |
|
rs1130214 |
-0,867 |
1,182 |
-0,734 |
0,463 |
0,420 |
0,041 |
4,260 |
52 |
0,26 |
|
rs1743964 |
-0,194 |
0,285 |
-0,682 |
0,495 |
0,823 |
0,471 |
1,439 |
154 |
0,36 |
|
rs10828317 |
-0,149 |
0,278 |
-0,537 |
0,591 |
0,862 |
0,500 |
1,484 |
184 |
0,33 |
|
rs2224721 |
-0,202 |
0,403 |
-0,500 |
0,617 |
0,817 |
0,371 |
1,802 |
111 |
0,25 |
|
rs6298 |
-0,182 |
0,390 |
-0,468 |
0,640 |
0,833 |
0,388 |
1,790 |
111 |
0,29 |
|
rs6330 |
-0,349 |
0,754 |
-0,463 |
0,643 |
0,705 |
0,161 |
3,092 |
53 |
0,43 |
|
rs6311 |
0,147 |
0,349 |
0,422 |
0,673 |
1,158 |
0,585 |
2,294 |
112 |
0,33 |
|
rs1364043 |
0,148 |
0,367 |
0,404 |
0,687 |
1,160 |
0,565 |
2,381 |
112 |
0,26 |
|
rs1062613 |
-0,172 |
0,432 |
-0,397 |
0,691 |
0,842 |
0,361 |
1,965 |
101 |
0,22 |
|
rs1487278 |
0,135 |
0,368 |
0,367 |
0,713 |
1,145 |
0,557 |
2,354 |
111 |
0,21 |
|
rs6313 |
-0,124 |
0,340 |
-0,364 |
0,716 |
0,884 |
0,454 |
1,721 |
109 |
0,33 |
|
rs6295 |
-0,119 |
0,351 |
-0,339 |
0,734 |
0,888 |
0,446 |
1,765 |
110 |
0,5 |
|
rs12858300 |
-0,183 |
0,571 |
-0,320 |
0,749 |
0,833 |
0,272 |
2,550 |
109 |
0,07 |
|
rs7933505 |
0,107 |
0,348 |
0,306 |
0,759 |
1,112 |
0,563 |
2,200 |
108 |
0,39 |
|
rs746203 |
0,069 |
0,231 |
0,300 |
0,764 |
1,072 |
0,681 |
1,687 |
186 |
0,47 |
|
rs1176713 |
-0,130 |
0,446 |
-0,291 |
0,771 |
0,878 |
0,366 |
2,107 |
112 |
0,21 |
|
rs11030104 |
-0,106 |
0,366 |
-0,289 |
0,772 |
0,900 |
0,439 |
1,842 |
102 |
0,23 |
|
rs6323 |
0,083 |
0,293 |
0,284 |
0,777 |
1,087 |
0,612 |
1,929 |
110 |
0,34 |
|
rs1800532 |
-0,090 |
0,342 |
-0,263 |
0,792 |
0,914 |
0,467 |
1,787 |
108 |
0,39 |
|
rs3730358 |
-0,282 |
1,184 |
-0,238 |
0,812 |
0,754 |
0,074 |
7,678 |
51 |
0,15 |
|
rs684302 |
0,098 |
0,514 |
0,190 |
0,849 |
1,102 |
0,403 |
3,017 |
109 |
0,15 |
|
rs3813929 |
0,073 |
0,385 |
0,189 |
0,850 |
1,076 |
0,505 |
2,289 |
111 |
0,16 |
|
rs11013052 |
0,051 |
0,349 |
0,147 |
0,883 |
1,053 |
0,531 |
2,088 |
132 |
0,31 |
|
rs4290270 |
0,044 |
0,340 |
0,128 |
0,898 |
1,045 |
0,536 |
2,036 |
111 |
0,39 |
|
rs749099 |
0,043 |
0,334 |
0,128 |
0,898 |
1,044 |
0,542 |
2,007 |
111 |
0,49 |
|
rs9316233 |
-0,045 |
0,462 |
-0,098 |
0,922 |
0,956 |
0,386 |
2,365 |
99 |
0,21 |
|
rs1176744 |
0,048 |
0,540 |
0,088 |
0,930 |
1,049 |
0,364 |
3,025 |
111 |
0,12 |
|
rs7305115 |
-0,025 |
0,347 |
-0,073 |
0,941 |
0,975 |
0,494 |
1,924 |
112 |
0,41 |
|
rs1928040 |
-0,024 |
0,357 |
-0,066 |
0,947 |
0,977 |
0,485 |
1,967 |
112 |
0,36 |
|
rs1137070 |
0,009 |
0,285 |
0,033 |
0,974 |
1,009 |
0,577 |
1,765 |
109 |
0,35 |
|
rs10042486 |
-0,007 |
0,338 |
-0,019 |
0,985 |
0,993 |
0,512 |
1,927 |
111 |
0,49 |
|
rs6314 |
-16,476 |
1386,367 |
-0,012 |
0,991 |
0,000 |
0,000 |
Inf |
98 |
0,06 |
При м е ч а н и е. Estimate ‒ коэффициент логистической регрессии, SE ‒ стандартная ошибка коэффициента логистической регрессии, Z ‒ значение тест-статистики, P ‒ p-значение, OR ‒ отношение шансов, LOWER, UPPER ‒ нижнее и верхнее интервальные значения OR, N ‒ количество индивидов с генотипами, MAF ‒ частота редкого аллеля.
Приведенные в таблице 2 полиморфизмы упорядочены по мере возрастания p-значения. Выделено (жирным шрифтом) 9 полиморфизмов, использованных для построения диагностической модели.
Наилучшие показатели чувствительности, специфичности, ППЗ, НПЗ и AUC получены для диагностической предсказательной модели, включающей как генетические, так и негенетические предикторы (пол, возраст) (табл. 3, рис. 2).
Следующей по эффективности прогнозирования оказалась модель с генетическими факторами. Самые низкие показатели вероятного прогнозирования получены для модели, включающей только негенетические предикторы. Последнее связано с тем, что использованные при разработке модели клинические и демографические предикторы, за исключением тяжести течения, не различаются между группами пациентов с ремиссией и без таковой (табл. 1).
Т а б л и ц а 3. Характеристики моделей предсказания вероятности ремиссии у пациентов с депрессивными расстройствами
|
Статистический показатель |
Модель |
||
|
Все предикторы |
Генетические предикторы |
Негенетические предикторы |
|
|
Чувствительность |
0,78 (0,68, 0,87) |
0,79 (0,71, 0,86) |
0,54 (0,46, 0,63) |
|
Специфичность |
0,78 (0,56, 0,93) |
0,61 (0,42, 0,78) |
0,67 (0,54, 0,79) |
|
Позитивное предсказательное значение |
0,93 (0,83, 0,98) |
0,89 (0,82, 0,94) |
0,80 (0,70, 0,87) |
|
Негативное предсказательное значение |
0,51 (0,34, 0,69) |
0,42 (0,28, 0,58) |
0,39 (0,29, 0,49) |
|
Площадь под кривой чувствительности и специфичности |
0,84 (0,76, 0,93) |
0,74 (0,63, 0,84) |
0,62 (0,53, 0,71) |
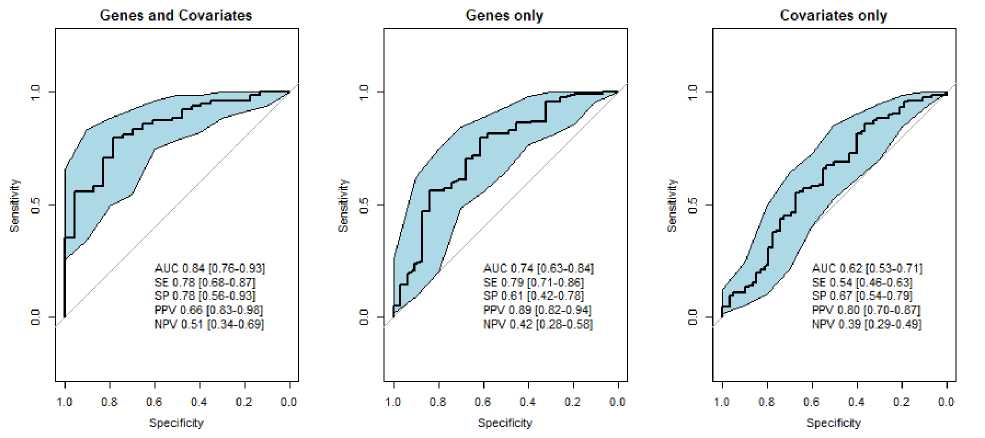
Р и с у н о к 2. Графики кривых чувствительности и специфичности для трех моделей предсказания вероятности ремиссии у пациентов с депрессивными расстройствами
Предлагаемая медицинская технология может использоваться в практическом здравоохранении для прогнозирования ремиссии у больных депрессивными расстройствами на основе генотипирования ДНК, выделенной из крови, до начала лечения и для целенаправленного проведения индивидуальной терапевтической тактики у этой категории больных.
ЗАКЛЮЧЕНИЕ
Таким образом, полученные результаты свидетельствуют о перспективности использования совокупного объединения генетических и негенетических предикторов для предсказания вероят- ности ремиссии. Обобщение результатов уже проведенных исследований и продолжение исследований в этом направлении позволят установить наиболее перспективные сочетания генетических и негенетических факторов с наибольшей предсказательной способностью. Разработанная технология позволит сократить количество дней нетрудоспособности, проведенных пациентом в стационаре, за счет оказания адекватной своевременной медицинской помощи на основе генетического метода определения вероятности формирования ремиссии у больных депрессивными расстройствами.
Список литературы Прогнозирование эффективности фармакотерапии у больных депрессивными расстройствами на основе генетических показателей
- Waraich P, Goldner EM, Somers JM, Hsu L. Prevalence and incidence studies of mood disorders: a systematic review of the literature. Can J Psychiatry. 2004 Feb;49(2):124-38. doi: 10.1177/070674370404900208. PMID: 15065747.
- Краснов В.Н. Проблемы современной диагностики депрессий. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2012. Т. 112, № 11-2. С. 3-10.
- Васильева С.Н., Симуткин Г.Г., Счастный Е.Д., Суровцева А.К., Украинцев И.И., Алтынбеков К.С. Сочетание аффективных расстройств и алкогольной зависимости: клиническое значение коморбидности, социальная адаптация пациентов. Сибирский вестник психиатрии и наркологии. 2022. № 4 (117). С. 14-21. doi:10.26617/1810-3111-2022-4(117)-14-21.
- Счастный Е.Д., Симуткин Г.Г., Лебедева Е.В., Яковлева А.Л., Лосенков И.С., Репин А.Н., Нонка Т.Г. Клинико-динамические и биологические аспекты полиморфизма и эффективности терапии расстройств настроения. Сибирский медицинский журнал. 2018. Т. 33, № 3. С. 86-92. doi:10.29001/2073-8552-2018-33-3-86-92.
- Bauer M, Pfennig A, Severus E, Whybrow PC, Angst J, Möller HJ; World Federation of Societies of Biological Psychiatry. Task Force on Unipolar Depressive Disorders. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of unipolar depressive disorders, part 1: update 2013 on the acute and continuation treatment of unipolar depressive disorders. World J Biol Psychiatry. 2013 Jul;14(5):334-85. doi: 10.3109/15622975.2013.804195. Epub 2013 Jul 3. PMID: 23879318.
- Bauer M, Severus E, Köhler S, Whybrow PC, Angst J, Möller HJ; WFSBP Task Force on Treatment Guidelines for Unipolar Depressive Disorders. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of unipolar depressive disorders. part 2: maintenance treatment of major depressive disorder-update 2015. World J Biol Psychiatry. 2015;16(2):76-95. doi: 10.3109/15622975.2014.1001786. PMID: 25677972.
- Счастный Е.Д., Симуткин Г.Г., Лебедева Е.В., Яковлева А.Л., Лосенков И.С., Левчук Л.А., Сергиенко Т.Н., Муслимова Э.Ф., Репин А.Н., Нонка Т.Г., Иванова С.А. Клинико-биологические факторы полиморфизма и эффективности терапии аффективных расстройств. Сибирский вестник психиатрии и наркологии. 2016. № 4 (93). С. 26-32.
- Cuijpers P, Stringaris A, Wolpert M. Treatment outcomes for depression: challenges and opportunities. Lancet Psychiatry. 2020 Nov;7(11):925-927. doi: 10.1016/S2215-0366(20)30036-5. Epub 2020 Feb 17. PMID: 32078823.
- Duman RS, Aghajanian GK. Synaptic dysfunction in depression: potential therapeutic targets. Science. 2012 Oct 5;338(6103):68-72. doi: 10.1126/science.1222939. PMID: 23042884; PMCID: PMC4424898.
- Иванова С.А., Лосенков И.С., Левчук Л.А., Бойко А.С., Вялова Н.М., Симуткин Г.Г., Бохан Н.А. Депрессивные расстройства: гипотезы патогенеза и потенциальные биологические маркеры. Новосибирск: Изд-во СО РАН, 2018. 199 с.
- Bauer M, Severus E, Möller HJ, Young AH; WFSBP Task Force on Unipolar Depressive Disorders. Pharmacological treatment of unipolar depressive disorders: summary of WFSBP guidelines. Int J Psychiatry Clin Pract. 2017 Sep;21(3):166-176. doi: 10.1080/13651501.2017.1306082. Epub 2017 Apr 3. PMID: 28367707.
- Loonen AJM, Ochi T, Geers LM, Simutkin GG, Bokhan NA, Touw DJ, Wilffert B, Kornetov AN, Ivanova SA. A new paradigm to indicate antidepressant treatments. Pharmaceuticals (Basel). 2021 Dec 10;14(12):1288. doi: 10.3390/ph14121288. PMID: 34959688; PMCID: PMC8705982.
- Corponi F, Fabbri C, Serretti A. Pharmacogenetics and Depression: A Critical Perspective. Psychiatry Investig. 2019 Sep;16(9):645-653. doi: 10.30773/pi.2019.06.16. Epub 2019 Aug 29. PMID: 31455064; PMCID: PMC6761796.
- Середенин С.Б. Лекции по фармакогенетике. М.: Изд-воМИА, 2004. 303 с.
- Evans WE, McLeod HL. Pharmacogenomics ‒ drug disposition, drug targets, and side effects. N Engl J Med. 2003 Feb 6;348(6):538-49. doi: 10.1056/NEJMra020526. PMID: 12571262.
- Kalow W. A pharmacogeneticist's look at drug effects and the drug development process: an overview. Expert Opin Pharmacother. 2005 Jul;6(8):1299-303. doi: 10.1517/14656566.6.8.1299. PMID: 16013980.
- Сычев Д.А., Раменская Г.В., Игнатьев И.В., Кукес В.Г. Клиническая фармакогенетика / под ред. В.Г. Кукеса, В.П. Бочкова. М.: ГЭОТАР-Медиа, 2007. 248 с.
- Иванова С.А. Фармакогенетические подходы к персонализированной антипсихотической терапии больных шизофренией. Психиатрия. 2016. № 1 (69). С. 64-65.
- Kirchheiner J, Fuhr U, Brockmöller J. Pharmacogenetics ‒ based therapeutic recommendations ‒ ready for clinical practice? Nat Rev Drug Discov. 2005 Aug;4(8):639-47. doi: 10.1038/nrd1801. PMID: 16056390.


