Прогнозирование влияния химических активаторов на прочность известково-перлитового вяжущего (ИПВ) методом многоуровневого моделирования
Автор: Танганов Б.Б., Урханова Л.А., Хардаев П.К.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Статья в выпуске: 1 (36), 2012 года.
Бесплатный доступ
Методом многоуровневого моделирования оценены энергии гидратации ионов химических активаторов. Осуществлено математическое прогнозирование прочности ИПВ в зависимости от видов и количества добавок -различных химических активаторов.
Многоуровневое моделирование, предел прочности, известково-перлитное вяжущее
Короткий адрес: https://sciup.org/142142447
IDR: 142142447 | УДК: 691.5:51-7
Forecasting the impact of chemical activators on tensile strength lime-binder perlite method for multilevel modeling
Method for multilevel modeling estimated energy of hydration of ions of chemical activators. Implemented mathematical prediction of strength depending on the types and amounts of additives to different chemical activators.
Текст научной статьи Прогнозирование влияния химических активаторов на прочность известково-перлитового вяжущего (ИПВ) методом многоуровневого моделирования
В работе [1] отмечалось, что единой теории, объясняющей механизм действия микродобавок на твердение силикатных систем, не разработано, и в каждом конкретном случае их действие находит свое истолкование. Однако проведенные исследования показывают, что введение химических добавок даже в небольшом количестве ускоряет твердение бесклинкерных композиций и повышает их прочность в среднем в 2-2,5 раза. Установлено, что рост прочности сопровождается увеличением количества химически связанной воды. Результаты исследования физико-химических свойств вяжущих композиций и расчетов характеристик гидратированных ионов свидетельствуют о том, что количество связанной воды зависит от заряда иона и обратно пропорционально радиусу иона, так как воздействие силового поля ядра на молекулы воды при меньшем радиусе иона распространяется на большее число диполей воды.
Гидратное число n s определяется соотношением [2]:
n s = z i e R s 2/ r i p - 3 к Б Т s R2 / 2 pe (1)
где R s , z i , r i , р, e , Т и к Б - соответственно радиус молекулы воды, заряд и радиус иона, дипольный момент молекулы воды, диэлектрическая проницаемость воды, температура ( К) и константа Больцмана.
Радиус гидратированного иона rsвычисляется по уравнению rs = (25 zpensh2/3 m!LT-; (2)
В таблице 1 представлены некоторые характеристики гидратированных ионов (гидратные числа, массы и радиусы гидратированных ионов), оцененные по уравнениям (1) и (2).
В процессе разработки концепции многочастичных взаимодействий в растворах сильных и слабых электролитов был предложен метод многоуровневого моделирования (ММУМ), позволяющий математически прогнозировать и моделировать те или иные химические и технологические процессы, а также уточнять или оценивать отсутствующие характеристики химических, физических, биологических, медицинских и других систем [2, 3].
Отметим, что в природе (равно как и во всех естественных науках), хотим мы этого или нет, всё взаимосвязано со всем. Например, если мы пытаемся научиться выращивать большие и вкусные помидоры с заданными свойствами, следует не только на эмпирическом или интуитивном уровне, но, главным образом, на теоретически обоснованном уровне рассматривать факторы , связанные с генетической структурой растений, типом почвы, освещенностью, температурой и т.д. Таким образом, при проведении даже типичного эксперимента приходится иметь дело с большим количеством факторов.
Так, методом многоуровневого моделирования был прогнозирован рост камней в печени партии крыс до летального исхода при холелитиазе, а также выдана прогностическая картина накопления алка- лоидов в лекарственных растениях в различных регионах СФО и ДВФО (например, в районах Бурятии и Забайкальском крае) [4, 5].
ММУМ определяется следующей исходной зависимостью, решаемой в последующем системой из n уравнений [6]:
Y = a + b 1 X 1 + b 2 X 2 + ...+ bnXn . (3)
После несложных преобразований найдем, что формула ММУМ с n переменными имеет вид:
Y-y ср = b 1 (X 1 -X 1(ср) +b 2 (X 2 -X 2(ср) +...+b n (X n -X n(ср) ), (4)
причем коэффициенты b 1 , b 2 , ...,b n ММУМ находятся из следующей системы линейных уравнений:
b 1 Σ x 1 2 + b 2 Σ x 1 x 2 + ...+ b n Σ x 1 x n = Σ x 1 y 1 ;
b 1 Σ x 1 x 2 + b 2 Σ x 2 2 + ...+ b n Σ x 2 x n = Σ x 2 y 2 ;
..................
b1Σx1xn + b2Σx2xn + ... + bnΣxn2 = Σxnyn , где приняты нижеследующие обозначения:
Σ x 1 2 = Σ (X 1 -X 1(ср) ); Σ x 1 x 2 = Σ (X 1 -X 1(ср) )(X 2 -X 2(ср) ); Σ x 1 x n = Σ (X 1 -X 1(ср) )(X n -X n(ср) );
Σ x 1 y 1 = Σ (X 1 -X 1(ср) )(Y 1 -Y 1(ср) ); и т.д.
Характеристики гидратированных ионов
Таблица 1
|
Ион |
Радиус иона, rs ⋅ 10 - 8 см |
Масса иона mi |
Гидратное число, n s |
Масса гидратированного иона, ms |
Радиус гидратированного иона, rs ⋅ 10 - 8 см |
Энергия гидратации Еs, кДж/моль (лит.) |
Энергия гидратации Е s по ур.(5), кДж/моль |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
Li+ |
0,78 |
6,9 |
5,33 |
102,87 |
3,96 |
502 |
594,34 |
|
Na+ |
0,98 |
23 |
4,03 |
95,53 |
3,60 |
410 |
359,46 |
|
K+ |
1,33 |
39 |
2,69 |
87,52 |
3,15 |
329 |
350,04 |
|
Mg2+ |
0,78 |
24,3 |
11,70 |
234,90 |
5,14 |
1887 |
2051,83 |
|
Ca2+ |
1,06 |
40,0 |
8,33 |
190,00 |
4,59 |
1569 |
1555,92 |
|
Sr2+ |
1,20 |
87,6 |
7,24 |
217,92 |
4,38 |
1477 |
1252,17 |
|
Ba2+ |
1,38 |
137,3 |
6,16 |
248,18 |
4,15 |
1339 |
927,84 |
|
Zn2+ |
0,83 |
65,4 |
11,97 |
280,86 |
5,18 |
2130 |
2029,18 |
|
Al3+ |
0,57 |
27,0 |
25,11 |
478,93 |
6,63 |
4548 |
4545,93 |
|
Fe3+ |
0,67 |
55,8 |
21,20 |
437,68 |
6,27 |
- |
4001,47 |
|
F– |
1,33 |
19,0 |
2,69 |
67,52 |
3,15 |
423 |
400,37 |
|
Cl– |
1,81 |
35,5 |
1,70 |
66,18 |
2,70 |
330 |
355,73 |
|
Br– |
1,96 |
79,9 |
1,49 |
106,80 |
2,59 |
296 |
309,25 |
|
SO 4 2- |
1,47 |
96,0 |
5,72 |
198,94 |
4,05 |
- |
991,07 |
|
OH– |
1,40 |
17,0 |
2,51 |
62,18 |
3,08 |
- |
288,21 |
|
MnO4– |
2,40 |
157 |
1,03 |
175,54 |
3,30 |
- |
333,65 |
|
NO 3 - |
1,89 |
62,0 |
1,59 |
90,62 |
2,64 |
- |
288,16 |
|
Cr 2 O 7 2- |
2,40 |
216 |
3,10 |
271,80 |
4,16 |
- |
855,54 |
Отметим важный физический смысл коэффициентов в уравнениях ММУМ. Например, коэффициент b 1 в формуле (3) отвечает на вопрос, на сколько единиц в среднем изменяется Y 1 , если X 1 изменяется на одну единицу в предположении, что X 2 при этом сохраняет постоянное значение.
Таким образом, формулы ММУМ позволяют исключить влияние фактора X 2 , корреляционно связанного с фактором X 1 на Y в чистом виде.
Данная идея положена в основу оценки энергий гидратации Е s различных ионов в виде уравнения (5) с соответствующим коэффициентом многоуровневого моделирования.
В таблице 1 также представлены литературные и оцененные величины Е s , систематические значения которых отсутствуют от таких базисных свойств, как радиус и масса иона, гидратное число, масса и радиус гидратированных ионов. Реализация компьютерной программы «ММУМ» [7] приводит к уравнению
Е s = 839,7192 . r i – 1299,3793 . m i – 23175,5342 . n s + 1296,3630. m s + 410,2215 . r s - 2498,6900 (5) с коэффициентом МУМ, равным 0,9992. Приемлемость уравнения (5) к расчету энергий гидратации различных ионов, составляющих химические активаторы для упрочнения ИПВ, подтверждается высоким значением коэффициента МУМ ( К мум ), близким к 1,000. Этот коэффициент выражает тесноту связи между переменными в ММУМ, определяемый по формуле:
Кмум2 = Σ(Yi- Yср)2/Σ(yi - yср)2 , где yi – значения переменной Y, взятые из корреляционной таблицы 1 (колонка 7 – опорные значения), а Yi – значения переменной Y, вычисленные по ММУМ (колонка 8 – по уравнению 5).
Оцененные величины масс m s и энергий гидратации ионов Е s (колонки 5, 7 и 8 в табл. 1) дают возможность определения приведенных масс и энергий гидратации µ s и E s химических активаторов (добавок в ИПВ) (табл. 2).
Таблица 2
Влияние вида, количества и параметров добавок (химических активаторов) на предел прочности ИПВ, МПа
|
Химический активатор |
CaSO 4 ∙2H 2 O |
Ca(NO 3 ) 2 |
CaCl 2 |
CaF 2 |
Fe 2 (SO 4 ) 3 ∙9H 2 O |
Na 2 SO 4 |
K 2 Cr 2 O 7 |
Al(OH) 3 (отходы Авиазавода) |
|
Приведенная масса химического активатора, µs ( г/моль ) |
97,05 |
92,76 |
78,01 |
78,94 |
354,30 |
97,33 |
106,47 |
134,25 |
|
Приведенная энергия гидратации химического активатора , E s ( кДж/моль ) |
605,43 |
363,50 |
524,60 |
537,31 |
2196,15 |
448,73 |
406,65 |
831,07 |
|
Количество добавки мас.% |
σпр, МПа (числитель – эксперимент, знаменатель – теория) |
|||||||
|
0 |
10,0 |
10,0 |
10,0 |
10,0 |
10,0 |
10,0 |
10,0 |
10,0 |
|
0,1 |
- |
- |
- |
- |
- |
- |
18,0 |
- |
|
11,126 |
15,346 |
10,486 |
10,326 |
10,406 |
14,226 |
16,126 |
11,116 |
|
|
0,25 |
- |
31,5 |
12,5 |
20,0 |
12,5 |
4,5 |
24,0 |
6,0 |
|
12,917 |
20,937 |
11,707 |
11,437 |
10,737 |
18,787 |
22,367 |
12,757 |
|
|
0,5 |
10,5 |
28,0 |
16,5 |
36,0 |
25,0 |
22,0 |
27,0 |
9,0 |
|
22,158 |
25,268 |
21,458 |
21,368 |
24,328 |
24,478 |
25,988 |
20,278 |
|
|
1,0 |
12,5 |
34,0 |
15,5 |
21,5 |
21,0 |
27,0 |
25,0 |
7,5 |
|
19,819 |
24,809 |
18,769 |
18,619 |
22,309 |
23,529 |
25,919 |
20,289 |
|
|
2,0 |
15,0 |
- |
- |
- |
- |
- |
- |
- |
|
17,0610 |
26,2310 |
15,3510 |
15,0610 |
15,0610 |
23,8310 |
28,1110 |
17,5210 |
|
|
3,0 |
16,0 |
18,5 |
13,5 |
23,0 |
21,0 |
29,5 |
- |
9,5 |
|
17,1811 |
24,7811 |
15,6911 |
15,4511 |
19,6411 |
22,8111 |
26,3911 |
17,6911 |
|
|
4,0 |
18,0 |
- |
- |
- |
- |
- |
- |
- |
|
16,5112 |
19,8212 |
15,1612 |
15,0912 |
26,7212 |
19,0812 |
21,0412 |
18,0612 |
|
|
5,0 |
21,5 |
12,0 |
9,0 |
22,5 |
35,0 |
19,5 |
- |
9,0 |
|
16,1713 |
15,0813 |
15,0113 |
15,1013 |
33,6113 |
15,6013 |
15,8613 |
18,6713 |
|
|
6,0 |
28,0 |
- |
- |
- |
- |
- |
- |
- |
|
7,0 |
31,0 |
- |
- |
- |
- |
- |
- |
- |
|
8,0 |
35,0 |
- |
- |
- |
- |
- |
- |
- |
Примечание. 6, 7, 8, 9, 10, 11, 12 и 13 – номера уравнений, по которым рассчитаны пределы прочности σ пр , МПа (табл. 2).
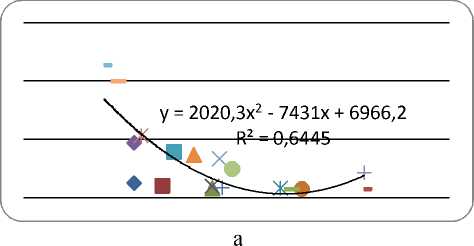
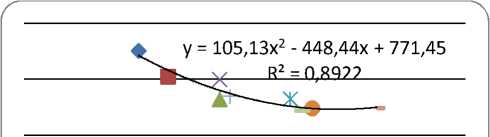
Другим способом оценки энергий гидратации ионов, входящих в состав химических добавок, является графическая зависимость Е s от собственных радиусов r s (рис. 1). Поскольку радиусы многих ионов известны и представлены в справочниках, по ним можно определить соответствующие энергии их взаимодействия с диполями воды (энергии гидратации). Рисунок 1 а соответствует зависимости для 1-, 2- и 3-зарядных, рис. 1 б –для 1-зарядных и 1 в – для 2-зарядных ионов.
В таблице 2 в числителе приведены экспериментальные значения предела прочности ИПВ σ пр , МПа [1]. Видно, что при добавках 0,1; 2,0 и 4,0% (мас.) опытные данные отсутствуют.
ММУМ позволяет теоретически оценивать пределы прочности ИПВ σ пр и рассчитать по уравнению
σпр = а µs + в Esприв + с пределы прочности для всех видов и количеств (до 5,0% мас.) химических активаторов с достаточно высокой вероятностью и надежностью (таблица 2 – знаменатель).
б
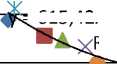
= 615,42x2 - 2697,3x + 3774,9 R² = 0,9249
в
Рис. 1. Взаимосвязь между радиусами ионов химических активаторов (ось абсцисс: r s ⋅ 10 - 8 см – колонка 1 табл. 1) их энергиями гидратации (ось ординат: Е s , кДж/моль – колонка 8 табл. 1):
а – для 1-, 2- и 3-зарядных ионов; б – для однозарядных ионов; в – для двухзарядных ионов
Таблица 3
Коэффициенты уравнения σ пр = а . µ s + в . E sприв + с
|
% добавки |
№ уравнения |
а |
в |
с |
|
0,10 |
6 |
0,11790 |
-0,01952 |
11,50522 |
|
0,25 |
7 |
0,22088 |
-0,03709 |
13,92625 |
|
0,50 |
8 |
0,09878 |
-0,01461 |
21,40911 |
|
1,00 |
9 |
0,32804 |
-0,05174 |
19,00052 |
|
2,00 |
10 |
0,27135 |
-0,04271 |
16,59011 |
|
3,00 |
11 |
0,22899 |
-0,03549 |
16,44431 |
|
4,00 |
12 |
0,13964 |
-0,01616 |
12,74832 |
|
5,00 |
13 |
0,04497 |
0,00369 |
9,56743 |
В таблице 3 представлены коэффициенты уравнения
σ пр = а µs + в E sприв + с для добавок от 0,1 до 5,0% (уравнения 6 – 13).
Анализ пределов прочности ИПВ в зависимости от количества и видов химических активаторов показывает, что некоторые экспериментальные величины имеют аномальные отклонения, что может быть объяснено, скорее всего, ошибкой опыта, а для Al(OH) 3 (отходы Авиазавода) наблюдается значительно меньший (по сравнению с другими активаторами и расчетными величинами) предел прочности, что может быть объяснено присутствием в отходах Авиазавода компонентов, ослабляющих прочность ИПВ.
Таким образом, ММУМ вполне приемлем к прогнозированию математическими методами пределов прочности ИПВ в зависимости от вида и количества химических активаторов.


