Проспективное исследование роли метода интраоперационной люминесцентной спектроскопии в выполнении изолированной профундопластики в гибридной хирургии критической ишемии нижней конечности
Автор: Ваганов А.Г., Кузнецов М.Р., Лисицкий Д.А., Романенко Н.В., Артыков А.Б., Гавриленко А.В.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4 т.39, 2024 года.
Бесплатный доступ
Введение. В настоящее время актуальна разработка новых диагностических критериев оценки состояния глубокой артерии бедра (ГАБ) с целью определения возможностей ее использования в различных гибридных реконструкциях при критической ишемии нижней конечности.Цель: определение показаний к изолированной профундопластике в качестве завершающего этапа проксимальной гибридной реконструкции с помощью метода интраоперационной люминесцентной спектроскопии.Материал и методы. В проспективное открытое нерандомизированное пилотное исследование включены 64 человека, оперированных в ГКБ № 29, с клиническим диагнозом «Облитерирующий атеросклероз артерий нижних конечностей. Стеноз наружной подвздошной артерии. Стено-окклюзионное поражение общей бедренной/поверхностной бедренной артерии. Стеноз глубокой артерии бедра. Хроническая артериальная ишемия III ст.», в объеме проксимальной гибридной реконструкции, включающей изолированную профундопластику. Первую группу (n = 28) составили больные, у которых отмечался стеноз или окклюзия устья глубокой артерии бедра, 2-ю группу (n = 20) - пациенты с диффузным поражением ГАБ, 3-ю группу (n = 16) - пациенты с дистальным типом поражения данной артерии. Первым этапом гибридной операции было выполнено стентирование наружной подвздошной артерии. Выбор дальнейшей интраоперационной тактики происходил в результате оценки анатомии и тяжести поражения глубокой артерии бедра, путем измерения лодыжечно-плечевого и глубокобедренно-подколенного индексов (ГПИ). Всем пациентам интраоперационно проводилась внутрисосудистая люминесцентная спектроскопия по нашей методике с определением люминесцентного коэффициента компенсации (Кл). Срок наблюдения за пациентами составлял 3 мес. Конечной точкой исследования явился тромбоз зоны реконструкции. Для статистической обработки данных при сравнении групп исследования было использовано программное обеспечение SPSS 17.0.Результаты. При сопоставлении полученного Кл отмечена прямая сильная корреляционная связь с предоперационно определенным ГПИ (r = 0,76; p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Гибридные операции на артериях нижних конечностей, критическая ишемия нижних конечностей, люминесцентная спектроскопия, глубокая артерия бедра, изолированная профундопластика, лодыжечно-плечевой индекс, глубокобедренно-подколенный индекс
Короткий адрес: https://sciup.org/149147159
IDR: 149147159 | УДК: 617.58-005.4-089.844-073.584 | DOI: 10.29001/2073-8552-2024-39-4-125-133
A prospective study of the method of intraoperative luminescent spectroscopy in the application of isolated profundoplasty in hybrid surgery of critical ischemia of the lower limb
Introduction. Currently, it is relevant to develop new diagnostic criteria for assessing the condition of the deep femoral artery (DFA), in order to determine the possibilities of its use in various hybrid reconstructions for critical lower limb ischemia.Aim: To determine the indications for isolated profundoplasty as the final stage of proximal hybrid reconstruction using the method of intraoperative luminescence spectroscopy.Material and Methods. The prospective open-label non-randomized pilot study included 64 people operated at City Clinical Hospital No. 29 with a clinical diagnosis of “Obliterating atherosclerosis of the arteries of the lower extremities. Stenosis of the external iliac artery. Steno-occlusive lesion of the common femoral/superficial femoral artery. Stenosis of the deep femoral artery of the thigh. Chronic arterial ischemia of the III st.”, in the volume of proximal hybrid reconstruction, including isolated profundoplasty. The first group (n = 28) consisted of patients who had stenosis or occlusion of the mouth of the deep femoral artery, the second group (n = 20) - had diffuse lesion of the deep femoral artery, the third group (n = 16) - had a distal type of lesion of this artery. The first stage of the hybrid operation was stenting of the external iliac artery. The choice of further intraoperative tactics occurred as a result of an assessment of the anatomy and severity of the lesion of the deep femoral artery, by measuring the ankle-shoulder and hip-popliteal indices. All patients underwent intravascular luminescent spectroscopy intraoperatively using our technique to determine the luminescent compensation coefficient (CI). The follow-up period was 3 months. The end point of the study was thrombosis of the reconstruction zone. The SPSS 17.0 software was used for statistical data processing when comparing study groups.Results. When comparing the obtained CI, a direct strong correlation was noted with a preoperatively determined hip-popliteal index (r = 0.76; at p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Проспективное исследование роли метода интраоперационной люминесцентной спектроскопии в выполнении изолированной профундопластики в гибридной хирургии критической ишемии нижней конечности
Глубокая артерия бедра (ГАБ) в условиях бедренно-подколенной окклюзии может стать ключевым сосудом, от которого будет зависеть артериальное наполнение подколенно-берцового артериального сегмента нижней конечности [1]. В условиях проксимальной гибридной реконструкции принципиально важной становится оценка компенсаторных возможностей ГАБ с целью определения вариантов открытой реконструкции в области бифуркации общей бедренной артерии (ОБА) [2–5].
Механизмы адаптации, имеющиеся у ГАБ, определяются ее анатомическими особенностями строения. Устье ГАБ располагается на задней стенке ОБА или поверхностной бедренной артерии (ПБА). ГАБ, проходя по задней стенке ПБА и располагаясь латеральнее бедренной вены, в самом начале рассыпается на множество ветвей, которые и формируют многочисленные коллатерали между голенью и бедром. Важно отметить, что ГАБ является артерией эластического типа, вследствие чего позже всех и в меньшей степени подвергается атеросклеротическому поражению [6]. Чаще всего отмечается поражение устья ГАБ, наблюдающееся в 74% случаев. Дистальная часть артерии поражается в 12% случаев. Диффузное поражение может наблюдаться в 14% случаев. Наиболее часто встречается стеноз ГАБ (39–64% случаев), окклюзия наблюдается лишь в 4–16% случаев [2]. При возникновении бедренно-подколенной окклюзии основная масса крови поступает в ГАБ, что вызывает ее компенсаторные изменения в виде расширения диаметра просвета, увеличения длины основного артериального ствола. По своей сути ГАБ является естественным бедренно-подколенным шунтом – своеобразным буфером, обеспечивающим функционирование конечности в критических условиях протяженного атеросклеротического поражения бедренных артерий [4]. Вопрос изолированной реваскуляризации ГАБ в составе проксимальной гибридной реконструкции в условиях бедренно-подколенной окклюзии при многоуровневом атеросклеротическом поражении нижней конечности является дискутабельным [5–6]. Это происходит в связи с тем, что отсутствуют достаточно четкие прогностические критерии результатов данных вмешательств, опирающиеся на индивидуальные морфофункциональные особенности ГАБ на фоне атеросклеротического поражения [7–11]. В настоящее время основным диагностическим методом, позволяющим определить показания к изолированной реваскуляризации ГАБ, является ультразвуковая допплерография с посегментарным измерением индекса регионального систолического давления (ИРСД) в пораженной конечности. Последний представляет собой соотношение давления в определенном региональном бассейне конечности (верхней, средней, нижней трети бедра, верхней трети голени, области голеностопного сустава) к систолическому давлению в плечевой артерии. ИРСД позволяет судить о развитии коллатерального кровообращения на бедре, косвенно оценивает функциональные особенности ГАБ [12]. Особое значение имеет также вычисление глубокобедренно-подколенного индекса (ГПИ), который является отношением разницы систолического артериального давления на бедре и голени к систолическому давлению на бедре. По своей сути ГПИ является градиентным индексом между буферной системой ГАБ и подколенной артерией. При ГПИ до 0,3 эффект от изолированной профундопластики считается ощутимым, при ГПИ в диапазоне от 0,3 до 0,5 – сомнительным, а при ГПИ более 0,5 – однозначно отрицательным [13]. Разработка новых диагностических критериев выбора изолированной профундопластики будет способствовать комплексному определению показаний к данному вмешательству в рамках проксимальной гибридной реконструкции.
Цель исследования: оценка возможности применения метода интраоперационной люминесцентной спектроскопии в определении показаний к изолированной про-фундопластике в качестве завершающего этапа проксимальной гибридной реконструкции.
Материал и методы
В проспективное открытое нерандомизированное пилотное исследование включены 64 человека, оперированных в сосудистом отделении ГКБ № 29, с клиническим диагнозом «Облитерирующий атеросклероз артерий нижних конечностей. Стеноз наружной подвздошной артерии (НПА). Стено-окклюзионное поражение общей бе-дренной/поверхностной бедренной артерии (ОБА/ПБА). Стеноз ГАБ. Хроническая артериальная ишемия (ХАИ) III ст.», в объеме проксимальной гибридной реконструкции, в качестве открытого этапа которой выступала изолированная профундопластика. Отбор пациентов и наблюдение за ними осуществлялись в 2023 г. и в 1 квартале 2024 г. Все участники были разделены на 2 группы в зависимости от анатомии поражения ГАБ. Первую группу ( n = 28) составили больные со стенозом или окклюзией устья ГАБ; 2-ю группу ( n = 20) – пациенты с диффузным поражением ГАБ; 3-ю группу ( n = 16) – пациенты с установленным дистальным типом поражения ГАБ.
У всех пациентов отмечались различные варианты стено-окклюзивного поражения ОБА и ПБА в сочетании со стенозом НПА. Первым этапом гибридной операции было выполнено стентирование НПА. Выбор интраоперационной тактики в отношении второго этапа гибридной операции (профундопластики) происходил в результате оценки анатомии и тяжести поражения ГАБ, а также степени развития коллатералей на бедре и голени по имеющимся КТ-ангиограммам, путем измерения лодыжечно-плечевого индекса (ЛПИ), а также вычисления ГПИ.
Критерии включения пациентов в группу исследования:
-
1. Наличие у пациентов болей покоя, дистанция перемежающейся хромоты не более 25 м; характеризующихся отсутствием некрозов на нижней конечности.
-
2. Наличие стеноза или окклюзии ОБА или ПБА в сочетании с гемодинамически значимым поражением ГАБ и окклюзионно-стенотическим поражением НПА.
-
3. Невозможность многоуровневой открытой или эндоваскулярной реконструкции.
-
4. Отсутствие гемодинамически значимых стенозов и окклюзий дистального русла на оперированной конечности.
Критерии исключения из группы исследования:
-
1. Отсутствие у пациентов болей покоя, дистанция перемежающейся хромоты от 25 до 200 м, наличие некрозов и язв на нижней конечности.
-
2. Отсутствие сочетанного поражения подвздошных и бедренных артерий, гемодинамически значимые окклюзии дистального русла оперированной конечности.
-
3. Возможность применения в конкретной клинической ситуации эндоваскулярной реваскуляризации подвздошно-бедренного сегмента либо многоэтажной открытой реконструкции.
-
4. Наличие подострого атеротромбоза артерий нижних конечностей.
Срок наблюдения за пациентами составлял 3 мес. Конечной точкой исследования явился тромбоз зоны реконструкции. Возраст пациентов составил 60 (57; 62) лет. Большинство респондентов в каждой группе исследования были представлены мужчинами (1-я группа – 92,8%, 2-я группа – 90,0%, 3-я группа – 93,8%). Все пациенты были сопоставимы по спектру сопутствующей патологии, курению (табл.1).
Таблица 1. Спектр сопутствующей патологии у пациентов, включенных в группы исследования
Table 1. The spectrum of concomitant pathology in patients included in the study groups
Всем пациентам интраоперационно проводилась внутрисосудистая лазерная фотолюминесцентная спектроскопия по представленной ниже методике. После завер- шения эндартерэктомии из ОБА в устье ГАБ вводилась металлическая насадка диаметром 2–3 мм, соединенная с оптоволоконным выходом. Последний совмещал в себе источник лазерного излучения и воспринимающее устройство для снятия сигнала люминесценции. Электрод помещался в стерильный рукав и в дальнейшем соединялся со стойкой, схема которой представлена на рисунке 1.


Рис. 1. Вид установки для люминесцентной спектроскопии (А – общий вид, Б – (слева направо) эксимерный лазер, спектрометр, фильтр для очистки сигнала)
Fig. 1. Type of installation for luminescent spectroscopy (A – general view, B – (from left to right) excimer laser, spectrometer, filter for signal purification)
В проведенном исследовании был применен метод лазер-индуцированной ультрафиолетовой фотолюми-несцентной спектроскопии с использованием прибора, состоявшего из источника лазерного излучения (эксимерный лазер XeCl), миниспектрометра, который является средством регистрации этого сигнала. Доставка излучения и снятие показаний индуцированной люминесценции проводились с использованием двух кварцевых волокон, смонтированных в одном электроде, диаметром сердцевины 450 мкм. Накачка осуществлялась на длине волны импульсного излучения эксимерного лазера XeCL 308 нм на протяжении 20 с. Спектр люминесценции фиксировался в диапазоне от 350 до 780 нм, с шагом 10 нм, в течение 20 с.
Необходимо отметить, что каждый элемент или химическое соединение имеет уникальный спектр свече- ния при накачке лазером на определенной длине волны [14]. Особенностью данного метода является высокая чувствительность измерения для конкретного вещества. Кроме того, согласно литературным источникам, существуют соединения, поглощающие люминесцентный сигнал. В частности, такими веществами являются гемопорфирины. Ими осуществляется резорбция излучения на частоте 450 нм. Таким образом, чем ниже амплитуда свечения на данной частоте, тем выше степень развития коллатерального кровотока. Поскольку измерения проводились на перекрытом кровотоке, поглощение сигнала на данной длине волны определяется количеством крови, оставшейся в коллатералях, и прямо пропорционально степени их развития.
Вторым аспектом, изученным нами в ходе исследования, было определение спектральных характеристик сосудистой стенки в зависимости от ее плотности и степени содержания в ней кальция. Прежде чем приступать к сравнению амплитуды люминесценции, мы определили ее спектральную характеристику для чистого кальция, взяв за ориентир человеческий ноготь с содержанием Са, по данным масс-спектрометрии, в 6000 мкг/г. После получения спектра люминесцентного свечения для Са, а также для бляшек, где его содержание было минимальным (контроль), мы определяли длину волны, характерную для кальциевого пика люминесценции. Она соответствовала 380 нм (рис. 2).
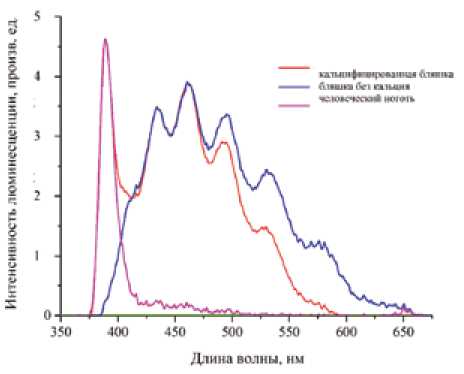
Рис. 2. Характеристика кальциевого пика люминесцентного сигнала, полученного от разных объектов
Fig. 2. Characteristics of the calcium peak of the luminescent signal received from different objects
В дальнейшем рассчитывался люминесцентный коэффициент компенсации (Кл) по формуле (1):
к =—
S380’ (1), где S 380 – амплитуда люминесценции на длине волны 380 нм (пик кальция), S 450 – амплитуда люминесценции на длине волны 450 нм (пик гемопорфиринов).
Оценку пациентов, участвовавших в исследовании, проводили по следующим критериям: длительность второго этапа гибридной реконструкции, объем интраоперационной кровопотери, время наступления послеоперационных осложнений и их связь с показателями люминесценции, а также с уровнем ГПИ и ЛПИ. В позд- нем послеоперационном периоде при ежемесячном осмотре регистрировали количество рецидивов критических ишемий, тромботических осложнений, повторных операций, а также ампутаций. Объективно оценивали уровни ЛПИ, ГПИ путем выполнения ультразвуковой допплерографии.
Таблица 2. Различия Кл в подгруппах с разными диапазонами значений лодыжечно-плечевого и глубокобедренно-подколенного индексов
Table 2. Differences in Cl in subgroups with different value ranges of ankle-brachial and deep femoropopliteal indices
|
Показатель |
Значение |
1-я группа |
2-я группа |
3-я группа |
р |
|
ГПИ |
0,1–0,2 |
0,26 (0,24; 0,29) |
0,28 (0,24; 0,30) |
0,27 (0,26; 0,34) |
0,13 |
|
0,2–0,3 |
0,32 (0,25; 0,35) |
0,32 (0,29; 0,40) |
0,27 (0,23; 0,36) |
0,16 |
|
|
0,3–0,4 |
0,51 (0,46; 0,54) |
0,55 (0,51; 0,61) |
0,54 (0,52; 0,58) |
0,12 |
|
|
ЛПИ |
0,2–0,3 |
0,64 (0,54; 0,67) |
0,52 (0,59; 0,67) |
0,58 (0,52; 0,54) |
0,12 |
|
0,3–0,4 |
0,33 (0,31; 0,37) |
0,35 (0,30; 0,38) |
0,28 (0,20; 0,39 ) |
0,23 |
|
|
0,4 и более |
0,12 (0,11; 0,14) |
0,16 (0,15; 0,17) |
0,18 (0,16; 0,20) |
0,43 |
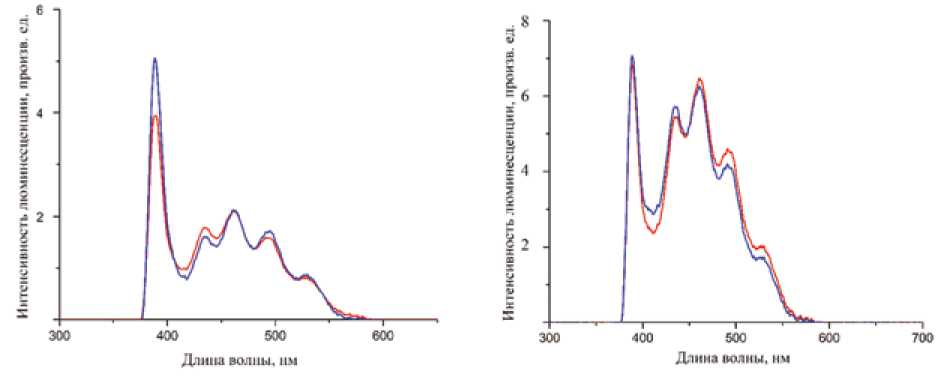
Рис. 3. Спектральные характеристики люминесценции, полученные при внутрисосудистом измерении в ГАБ в группах исследования (А – пациент с тромботическими осложнениями, Б – пациент с неосложненным течением послеоперационного периода)
Fig. 3. Spectral characteristics of luminescence obtained by intravascular measurement in deep femoral artery in the study groups (A – patient with thrombotic complications, B – patient with uncomplicated course of the postoperative period)
Для статистической обработки данных использовали программное обеспечение SPSS 17.0. Количественные показатели представлены медианой и межквартильным интервалом, Me ( Q 1; Q 3). Проверку нормальности распределения количественных показателей проводили по критерию Шапиро – Уилка. Статистическую значимость различий количественных показателей между тремя независимыми группами оценивали по критерию Краске-ла – Уоллиса. Для оценки корреляционной зависимости между количественными показателями использовали коэффициент корреляции Спирмена. Различия категориальных показателей между независимыми группами оценивали с помощью χ 2 -критерия Пирсона. Критический уровень значимости при проверке статистических гипотез составлял р = 0,05.
Результаты
Технический успех операции наблюдался у всех респондентов. Пациенты исследуемых групп были сопоставимы по длительности операции (1-я группа – 96,5 (94; 107,5) мин; 2-я группа – 97 (94,5; 107,5) мин; 3-я группа – 99 (97; 110,5) мин), величине интраоперационной кровопотери (1-я группа – 243 (234; 254) мл; 2-я группа – 265,5 (263,5; 273) мл; 3-я группа – 265 (263,5; 272,5) мл).
Периоперационных осложнений также отмечено не было. При сопоставлении полученного коэффициента люминесценции, полученного по результатам интраоперационной внутрисосудистой люминесцентной спектроскопии, в группах исследования установлена прямая сильная корреляционная связь между Кл и предоперационно определенным ГПИ ( r = 0,76; при p < 0,005), а также обратная по направленности сильная корреляционная связь между предоперационным ЛПИ и Кл ( r = –0,81; при р < 0,001) (табл. 2, рис. 3).
У 25 (89,3%) пациентов 1-й группы, 18 (90,0%) пациентов 2-й группы и у 15 (93,8%) пациентов 3-й группы послеоперационный период протекал без тромботических осложнений. Средний ГПИ у данных респондентов составил 0,30 (0,25; 0,34); а рассчитанный интраоперационно Кл – в среднем 0,32 (0,26; 0,41). Вне зависимости от варианта анатомического поражения ГБА респонденты, участвующие в исследовании, были сопоставимы по приведенным значениям.
При оценке тромботических осложнений у 6 пациентов в группах исследования среднее время их возникновения в группах исследования было сопоставимо и составляло 46 (42; 50) ч. Медиана ГПИ у таких пациентов была равна 0,43 (0,42; 0,45); Кл = 0,53 (0,52; 0,55).
При оценке пациентов с ГПИ в интервале от 0,3 до 0,4; который предполагает неблагоприятные исходы изолированной профундопластики, были оценены 4 пациента с тромботическими осложнениями в раннем послеоперационном периоде и 3 пациента, у которых таких осложнений не отмечено. При соотнесении Кл у данных категорий респондентов отмечается статистическая значимость различий показателей: Кл (без осложнений) = 0,46 (0,43; 0,50); Кл (осложненный) = 0,59 (0,58; 0,60); р < 0,05. Все исследуемые пациенты с ГПИ от 0,3 и 0,4 относились к представителям 1-й и 2-й групп исследования. У пациентов с дистальным типом поражения ГАБ во всех случаях ГПИ был больше 0,5; Кл = 0,62 (0,59; 0,66).
В исследование после выписки были включены лица с неосложненным течением раннего послеоперационного периода. Результаты изучения отдаленного послеоперационного периода в течение 3 мес. представлены в таблице 3.
По количеству рецидивов перемежающейся хромоты, тромботических осложнений и ассоциированных с ними повторных сосудистых операций группы исследования были сопоставимы. При изучении предоперационного ГПИ у пациентов с поздними тромбозами зон реконструкции установлено, что 75% их них имели значение данного показателя в интервале от 0,3 до 0,4 (пациенты с данными осложнениями входили в 1-ю и 2-ю группы исследования); остальные 25% имели значение выше 0,5 (все пациенты из 3-й группы исследования).
У пациентов с неосложненным течением отдаленного послеоперационного периода ГПИ в интервале от 0,3 до 0,4 имел место лишь в 15,2% случаев. При сопоставлении Кл у представителей 1-й и 2-й групп исследования, имевших ГПИ в диапазоне от 0,3 до 0,4, но отличавшихся исходами позднего послеоперационного периода, отмечалась статистическая значимость различий показателей: Кл (без осложнений) = 0,44 (0,43; 0,46); Кл (осложненный) = 0,61 (0,60; 0,62); р < 0,05.
Таблица 3. Основные показатели эффективности отдаленного послеоперационного периода
Table 3. The main performance indicators of the long-term postoperative period
|
Группа исследования |
1-я группа ( n = 25) |
2-я группа ( n = 20) |
3-я группа ( n = 15) |
р |
|
Количество рецидивов перемежающейся хромоты, % |
8,0 |
5,0 |
6,7 |
0,15 |
|
Количество тромботических осложнений, % |
8,0 |
5,0 |
6,7 |
0,16 |
|
Количество повторных сосудистых операций |
4,0 |
5,0 |
6,7 |
0,14 |
|
Количество ампутаций |
0 |
0 |
0 |
– |
|
Летальность |
0 |
0 |
0 |
– |
Обсуждение
ГАБ является важнейшим анатомическим сосудистым образованием, от которого в условиях полной бедренно-подколенной окклюзии зависит кровоснабжение всей нижней конечности. Данная биологическая роль предо- пределена ГАБ особенностями ее строения, возможностью формирования множественных коллатералей на голени и бедре. При наличии достаточных компенсаторных возможностей ГАБ выполнение изолированной профундопластики в составе гибридной реконструкции по поводу многоуровневого атеросклеротического поражения артерий нижних конечностей у тяжелых комор-бидных пациентов позволяет снизить объем операции при сопоставимых результатах реваскуляризации конечности. Наше исследование показало, что комплексный многофункциональный подход к определению показаний к изолированной профундопластике может способствовать повышению эффективности данной методики. Ультразвуковые методы определения градиентов давлений между буферной системой ГАБ и подколенной артерией, а также между верхней и нижней конечностями (ИРСД) позволяют определить степень развития коллатерального кровотока на нижней конечности, косвенно оценив функциональный потенциал ГАБ.
Наше исследование продемонстрировало эффективность профундопластики при ГПИ до 0,3 и отрицательный результат – при ГПИ более 0,5, что, несомненно, является ценным диагностическим критерием в выборе хирургической стратегии при планировании проксимальной гибридной реконструкции. Для уточнения показаний к изолированной профундопластике нами был применен метод внутрисосудистой люминесцентной спектроскопии. Было доказано, что оценка амплитуды люминесценции на длине волны 380 нм соответствует плотности сосудистой стенки, коррелирующей с содержанием в ней кальция. Чем выше сила свечения на частоте 380 нм, тем выше плотность ГАБ и ниже ее эластичность и растяжимость при перенаправлении в ее русло больших объемов крови вследствие бедренно-подколенной окклюзии.
Оценка амплитуды люминесценции на длине волны 450 нм показывает степень резорбции полученного сигнала гемопорфиринами в сосудистом русле. При измерениях в условиях интраоперационно остановленного кровообращения данная амплитуда соответствует количественному содержанию крови в коллатералях голени и бедра. Применение метода интраоперационной внутрисосудистой люминесцентной спектроскопии позволило уточнить тактику при ГПИ, находящейся в «серой зоне» от 0,3 до 0,4; где прогностический результат во многом не предсказуем.
Соотношение спектральных характеристик сосудистой стенки, зависящих от тяжести атеросклеротического поражения и степени редукции люминесцентного сигнала коллатеральной сосудистой сетью на бедре и голени, позволило диалектически изучить компенсаторные возможности ГАБ в режиме интраоперационного мониторинга. Определена сильная корреляционная зависимость между ультразвуковыми градиентными показателями систолического сегментарного давления и люминесцентным коэффициентом компенсации ГАБ. Как в раннем, так и в позднем послеоперационном периоде уточнены параметры Кл, на которые можно ориентироваться при формировании окончательной интраоперационной тактики в случае ГПИ от 0,3 до 0,4. Так, при Кл в коридоре 0,44–0,46 возможно выполнение изолированной профун-допластики, а при Кл = 0,59–0,61 данное вмешательство может сочетаться с возникновением тромботических осложнений в послеоперационном периоде. Кроме того, определена возможность использования данных закономерностей при стенозе устья ГАБ и диффузном поражении ее ствола.
Заключение
Исходя из вышесказанного, можно сделать вывод, что внутрисосудистая люминесцентная спектроскопия является важным методом уточнения интраоперационной возможности выполнения изолированной профун-допластики в дополнение к предоперационной оценке степени ГПИ. Выяснено, что при ГПИ в диапазоне 0,3–
0,4; при Кл в коридоре 0,44–0,46 возможно выполнение изолированной профундопластики, а при Кл = 0,59–0,61 высок риск тромботических осложнений после данного вмешательства. Необходимо отметить, что для проверки полученных выводов требуется проведение дальнейших исследований на большей выборке пациентов. Данные исследования также будут способствовать определению чувствительности и специфичности метода интраопера-цонной внутрисосудистой люминесцентной спектроскопии и ее широкому практическому применению.
Список литературы Проспективное исследование роли метода интраоперационной люминесцентной спектроскопии в выполнении изолированной профундопластики в гибридной хирургии критической ишемии нижней конечности
- Гавриленко А.В., Котов А.Э., Лепшоков М.К. Результаты профундопластики у пациентов с критической ишемией нижних конечностей. Хирургия. Журнал им. Н.И. Пирогова. 2017;(9):17-22. https://doi.org/10.17116/ hirurgia2017917-22.
- Фаталиев Г.Б., Шубин А.А., Сидорова А.В. Традиционные и гибридные вмешательства при поражении подвздошных артерий и путей оттока. Грудная и сердечно-сосудистая хирургия. 2023;3(65):320-326. https://doi.org/10.24022/0236-2791-2023-65-3-320-326.
- Темрезов М.Б., Коваленко В.И., Темерезов Т.Х., Бахметьев А.С., Лойко В.С., Рудаков М.О. Гибридная хирургия в лечении пациентов с облитерирующим атеросклерозом артерий нижних конечностей. Трансляционная медицина. 2020;7(1):33-38. (In Russ.). https://doi.org/10.18705/2311-4495-2020-7-1-33-38.
- Куликович Ю.К., Лызиков А.А., Каплан М.Л., Коваленко А.А., Усенкова В.В. Отдаленные результаты профундопластики у пациентов с атеросклеротическим поражением артерий нижних конечностей в зависимости от состояния дистального русла. Проблемы здоровья и экологии. 2023;20(3):46-52. https://doi.org/10.51523/2708-6011.2023-20-3-06.
- Бокерия Л.А., Аракелян В.С., Папиташвили В.Г., Цурцумия Ш.Ш. Результаты изолированной профундопластики в сравнении с дистальным шунтированием у больных с сахарным диабетом и трофическими язвами. Кубанский научный медицинский вестник. 2020;27(2):38-48. https://doi.org/10.25207/1608-6228- 2020-27-2-38-48.
- Русин В.И., Корсак В.В., Русин В.В., Горленко Ф.В., Добош В.М. Ангиоархитектоника и морфометрия глубокой артерии бедра. Новости хирургии. 2019;27(6):615-621. https://doi.org/10.18484/2305-0047.2019.6.615
- Фаталиев Г.Б., Аракелян В.С., Шубин А.А., Сидорова А.В. Сравнение различных видов гибридных вмешательств при поражении подвздошных артерий и артерий ниже паховой складки. Грудная и сердечно-сосудистая хирургия. 2023;5(65):572-578. https://doi.org/10.24022/0236-2791-2023-65-5-572-578.
- Бокерия Л.А., Аракелян В.С., Папиташвили В.Г., Цурцумия Ш.Ш. Отдаленные результаты проксимальных и дистальных реконструкций у пациентов с диффузным поражением артерий нижних конечностей и сахарным диабетом. Вестник Российского университета дружбы народов. 2021;25(4):271-281. https://doi.org/10.22363/2313-0245-2021-25-4-271-28.
- Vos A., Vink A., Kockelkoren R., Takx R.A.P., Celeng C., Mali W., et al. Radiography and computed tomography detection of intimal and medial calcifications in leg arteries in comparison to histology. J. Pers. Med. 2022;12(5):711. https://doi.org/10.3390/jpm12050711 28.
- Vos A., de Jong P.A., Verdoorn D., Mali W., Bleys R., Vink A. Histopathological characterization of intimal lesions and arterial wall calcification in the arteries of the leg of elderly cadavers. Clin. Anat. 2021;34(6):835- 841. https://doi.org/10.1002/ca.23701 29.
- McDermott M.M., Kramer C.M., Tian L., Carr J., Guralnik J.M., Polonsky T., et al. Plaque composition in the proximal superficial femoral artery and peripheral artery disease events. JACC Cardiovasc Imaging. 2017;10(9):1003-1012. https://doi.org/10.1016/j.jcmg.2016.08.012.
- Жане А.К., Пичугин А.Г., Напсо Х.Р., Жане Д.А. Реконструкция глубокой бедренной артерии в хирургическом лечении больных с хронической артериальной недостаточностью нижних конечностей. Кубанский научный медицинский вестник. 2013;(4):51-54.
- Гавриленко А.В., Котов А.Э., Лепшоков М.К. Эффективность профундопластики при хирургическом лечении пациентов с критической ишемией нижних конечностей. Кардиология и сердечно-сосудистая хирургия. 2019;12(4):296-301. https://doi.org/10.17116/kardio201912041296.
- Гусева И.А., Рогаткин Д.А., Бувалая Е.С. Анализ люминесценции в мутных биологических средах. Альманах клинической медицины. 2017;45(2):163-169. https://doi.org/10.18786/2072-0505-2017-45-2-163-169.


