Простое слепое проспективное рандомизированное мультицентровое исследование эффективности и безопасности сиролимус-доставляющего коронарного стента «Калипco» по сравнению с эверолимус-доставляющим стентом XiencePrime: дизайн и обоснование клинического исследования «ПАТРИOТ»
Автор: Прохорихин Алексей Андреевич, Верин В.В., Осиев А.Г., Ганюков В.И., Протопопов А.В., Демин В.В., Абугов С.А., Байструков В.И., Гражданкин И.О., Пономарев Д.Н., Кретов Е.И.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Протокол исследования
Статья в выпуске: 4 т.20, 2016 года.
Бесплатный доступ
Цель Оценить безопасность и эффективность сиролимус-покрытого стента «Калипсо» в сравнении с эверолимус- покрытым стентом Xience Prime у пациентов, нуждающихся в коронарной реваскуляризации. Методы Простое слепое проспективное рандомизированное мультицентровое исследование пациентов, которым показана коронарная реваскуляризация методом чрескожной транслюминальной коронарной ангиопластики со стентированием. Набор в исследование составит 610 человек. Пациентам выполнят стандартную реваскуляризацию в условиях рандомизации 2 : 1 с использованием стентов «Калипсо» («Ангиолайн») и Xience Prime (Abbott). Период наблюдения составит 12 мес. Группе из 122 (20%) человек к 12-месячному сроку наблюдения проведут контрольную количественную коронарографию. Выводы Дизайн исследования «ПАТРИОТ» составлен таким образом, чтобы доказать безопасность и эффективность первого российского сиролимус-доставляющего стента «Калипсо».
Ишемическая болезнь сердца, реваскуляризация, коронарный стент
Короткий адрес: https://sciup.org/142140774
IDR: 142140774 | DOI: 10.21688-1681-3472-2016-4-96-101
Prospective randomized, single-blind, multicenter control clinical study of sirolimus-eluting coronary stent “Calypso” vs everolimus-eluting coronary stent “Xience Prime”: design and rationale for “PATRIOT” trial
Aim. This study is aimed at evaluating the efficacy and safety of sirolimus-eluting coronary stent “Calypso” in comparison with everolimus-eluting coronary stent “Xience Prime” in patients with ischemic heart disease. Methods. This is a prospective, randomized, single-blind multicenter clinical trial in patients undergoing coronary revascularization with coronary stenting. Seven clinical sites in Russia will enroll 610 patients with coronary artery disease. Patients suitable for coronary stenting will be randomized in group 1 (n=406) to receive coronary stent “Calypso” (“Angioline”, and group 2 (n=204) to receive coronary stent Xience Prime (Abbott). Clinical follow-up will continue for 1 year. By the end of follow-up, a quantitative coronary angiography will be performed in 122 patients (20 %). Conclusion. A randomized trial “PATRIOT” is designed to prove the efficacy and safety of sirolimus-eluting coronary stent “Calypso” in comparison with everolimus-eluting coronary stent “Xience Prime” in patients with ischemic heart disease.
Текст научной статьи Простое слепое проспективное рандомизированное мультицентровое исследование эффективности и безопасности сиролимус-доставляющего коронарного стента «Калипco» по сравнению с эверолимус-доставляющим стентом XiencePrime: дизайн и обоснование клинического исследования «ПАТРИOТ»
Ангиопластика в сочетании со стентированием — эффективный и безопасный метод реваскуляризации миокарда при ишемической болезни сердца с различными типами поражений [1, 2]. К недостаткам метода относятся рестеноз и тромбоз стента, которые исследователи компенсируют совершенствованием дизай- на устройств, полимерных и лекарственных покрытий. Внедрение стентов с лекарственным покрытием в клиническую практику привело к значительному повышению эффективности эндоваскулярной коррекции коронарной патологии [3, 4]. Одной из проблем первого поколения стентов было несовершенство характеристик биосовместимости полимера, что приводило
Статья доступна по лицензии Creative Commons Attribution 4.0.
к аллергическим реакциям и воспалению в месте имплантации. Эти процессы в сочетании с незавершенной эндотелизацией страт стента вызывали ранний или поздний тромбоз стента [5]. Новое поколение стентов привело к значительному сокращению тромботических осложнений [6, 7].
Другая проблема — недоступность эндоваскулярных методов лечения, особенно для пациентов с острым коронарным синдромом. Если в европейских странах в среднем на 1 млн населения ежегодно выполняют 1 870 стентирований, то в России в 2015 г. на 1 млн населения всего провели 941 процедуру. Это связано как с недостаточным количеством центров, оказывающих данный вид высокотехнологической медицинской помощи, так и с ограниченным финансированием, не позволяющим выполнять достаточное количество стентирований всем нуждающимся [8].
В связи с этим оптимизация стоимости коронарного стентирования — актуальная задача в помощи пациентам с острым коронарным синдромом. Коронарные стенты российского производства при сравнимом с западными аналогами соотношении «эффективность – безопасность» и меньшей цене могут решить эту проблему.
Цель исследования: сравнить покрытый сиролиму-сом стент «Калипсо» со стентом Xience Prime, покрытым эверолимусом.
Методы
Система коронарного стента «Калипсо »
Каркас стента изготовлен из сплава кобальта и хрома, имеет матричную конструкцию. Основой для лекарственного покрытия в стенте «Калипсо» является биорезорбируемая композиция сополимеров DL-лактида с гликолидом. Лекарственным агентом покрытия стента используют сиролимус (рапамицин). Концентрация лекарственного вещества — 150 мг/см2.
Система коронарного стента Xience Prime
Коронарный стент Xience Prime обладает одними из самых высоких показателей безопасности и эффективности, подтвержденными крупными рандомизированными исследованиями [9–12]. Стент изготовлен из кобальтохромового сплава с постоянным биосовмес-тимым покрытием. Антипролиферативный компонент лекарственного покрытия представлен препаратом эве-ролимус. Концентрация лекарственного вещества — 100 мг/см2.
Гипотеза и популяция исследования
Гипотеза исследования заключается в том, что стент «Калипсо» не менее эффективный и безопасный, чем стент Xience Prime. Результаты определят измерением разницы частоты нежелательных явлений у пациентов, рандомизированных в группы стентов «Калипсо» (основная) и Xience Prime (контрольная). В исследование
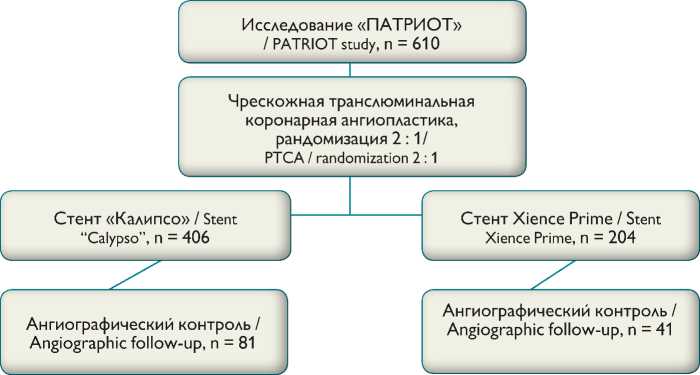
Дизайн исследования «ПАТРИОТ» “PATRIOT” study design
войдут пациенты, которым показана коронарная реваскуляризация методом чрескожной транслюминальной коронарной ангиопластики со стентированием. Запланированное количество пациентов — 610 человек. Учитывая частоту комбинированной конечной точки при имплантации стентов Xience Prime 6,5% [9], порог non-inferiority 5,3%, рассчитали, что в исследование необходимо включить 554 пациента (369 и 185 участников в основной и контрольной группах соответственно) для получения статистической достоверности при уровнях ошибки первого и второго типа, равных 0,05 и 0,20 соответственно. С целью компенсации незавершенных наблюдений размер выборки увеличен на 10% от расчетного, таким образом, в исследование включат 610 пациентов (406 и 204 в основной и контрольной группах соответственно).
Дизайн исследования
Простое слепое многоцентровое рандомизированное (non-inferiority) исследование пациентов, которых в ежедневной клинической практике направляют на стентирование коронарных артерий (рисунок). В исследование войдут пациенты старше 18 лет, подписавшие информированное согласие, которым показана имплантация стента с лекарственным покрытием для лечения стабильной ишемической болезни сердца или острого коронарного синдрома. Пациентов включат в исследование при поражении коронарной артерии с референсным диаметром артерии от 2,5 до 4,5 мм и стенозом более 50%.
Протокол исследования не предусматривает ограничения, связанные с длиной поражения, числом целевых поражений и количеством имплантированных стентов [13]. Одним из критериев исключения будет инфаркт миокарда с элевацией сегмента ST. Исследование рассмотрит локальный этический комитет каждого учреждения, в котором пройдет исследование. Критерии отбора/неотбора и критерии включения/исключения пациентов в исследование «ПАТРИОТ» представлены ниже.
Критерии отбора Критерии неотбора
Возраст пациента более 18 лет
Пациенты обоего пола
Подписанное информированное согласие
Показания для реваскуляризации ангиопластикой со стентированием
Целевое поражение локализовано в коронарной артерии >2,5 и <4,5 мм
Возраст пациента более 75 лет
Беременность, кормление грудью, если женщины детородного возраста не используют эстроген-прогестиновые или прогестиновые контрацептивные препараты или внутриматочные контрацептивные средства или женщины, использующие эстроген-прогестиновые или прогестиновые контрацептивные препараты или внутриматочные контрацептивные средства, прекратят их применение в течение срока, соответствующего планируемой продолжительности исследования
Пациенты, не толерантные к приему антикоагулянтов/дезагрегантов
Тяжелая клапанная патология, требующая в течение 1 года оперативного вмешательства
Скорость клубочковой фильтрации менее 30 мл/мин
Анемия менее 100 г/л
Тромбоцитопения
Онкология
Продолжающееся кровотечение
Госпитализация по поводу сердечной недостаточности как основного диагноза в последние 12 мес.
ЧТКА/стентирование или АКШ в анамнезе
Фракция выброса ЛЖ <30%
Острый коронарный синдром с подъемом сегмента ST
Критерии включения Критерии исключения
Целевое поражение локализовано в коронарной артерии >2,5 и <4,5 мм
Поражение коронарных артерий, требующее проведения аортокоронарного шунтирования
Плановое стадийное ЧТКА и/или стентирование за исключением случаев незапланированного стадийного ЧТКА и/или стентирования в течение 4 нед. после целевой процедуры (по причине чрезмерной длительности процедуры, предельного объема используемого контрастного вещества и т. д.) целевыми стентами
Примечание. ФК по NYHA — функциональный класс по классификации Нью-йоркской ассоциации сердца; ЧТКА — чрескожная транслюминальная коронарная ангиопластика; АКШ — аортокоронарное шунтирование; ЛЖ — левый желудочек
Рандомизация
Включение и рандомизацию выполнят с использованием электронной системы IWRS. После анализа данных коронарографии и в случае соответствия критериям включения и отсутствия критериев исключения пациентов рандомизируют в соотношении 2 : 1 в группы стентов «Калипсо» и Xience Prime соответственно. Далее пациентам проведут стандартную коронарную реваскуляризацию с использованием стента согласно результатам рандомизации ( рисунок ).
Период наблюдения и конечные точки
Общий период наблюдения пациентов составит 12 мес. Состояние пациентов оценят при помощи амбулаторного приема или телефонного контакта через 3, 6, 9 и 12 мес. Во время контакта с пациентом проанализируют параметры безопасности и эффективности стентов. Группе из 122 (20%) человек к 12-месячному сроку наблюдения выполнят контрольную коронарографию с целью количественного анализа коронарографии для измерения поздних изменений просвета сосуда.
Первичные конечные точки: осложнение, связанное с целевым поражением в течение 1 года, определяемое как кардиогенная смерть, инфаркт миокарда, связанный с целевой артерией; реваскуляризация целевого поражения по клиническим показаниям.
Вторичные конечные точки включают отдельные компоненты первичной точки: смерть по любой причине, инфаркт миокарда, реваскуляризацию целевого сосуда по клиническим показаниям, любую реваскуляризацию целевого сосуда, любую реваскуляризацию целевого поражения, тромбоз стента (определенный, вероятный, возможный). Ко вторичным конечным точкам также относятся поздняя потеря диаметра просвета стентированного сосуда, успех имплантации устройства, лечения поражения и процедуры.
Статистический анализ
Нулевая гипотеза будет тестироваться путем построения одностороннего 95%-го доверительного интервала для разницы рисков неблагоприятного события (комбинированная первичная точка) «тест» (стент «Калипсо») минус «контроль» (стент Xience Prime). Нулевая гипотеза не меньшей эффективности стента «Калипсо» в сравнении со cтентом Xience Prime будет отклонена, если верхняя граница одностороннего (95%) доверительного интервала для разницы рисков составит менее 5,3%. Отдельные компоненты комбинированной первичной точки будут описаны как номинальные величины по визитам исследования и группам терапии и в целом по группам терапии за все время исследования (событие считается случившимся, если произошло хотя бы один раз на любом из визитов). Сравнение групп терапии будет производится для событий за время исследования (произошло хотя бы один раз). Для сравнения групп будет использован permutation test. В остальных случаях бинарные качественные признаки будут сравнивать с применением точного теста Фишера. Качественные признаки с количеством категорий более двух — с помощью ординарной логистической регрессии. Межгрупповые сравнения количественных переменных выполнят с помощью теста Стьюдента для несвязанных выборок или U-критерия Манна – Уитни. Внутригрупповые сравнения качественных признаков выполнят с применением теста Мак-Не-мара. Количественные признаки на этапах исследования оценят с помощью теста Фридмана, теста Стьюдента для связанных выборок или смешанных регрессионных моделей. Статистическая значимость будет установлена при вероятности ошибки первого типа менее 5%. Все анализы будут выполнены с применением языка статистического программирования R (R Core Team (2015). R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. Режим доступа: .
Заключение
Дизайн исследования «ПАТРИОТ» составлен таким образом, чтобы продемонстировать не меньшую безопасность и эффективность первого российского сироли-мус-доставляющего стента «Калипсо». Дополнительный ангиографический анализ субпопуляции исследования направлен на изучение отдаленных результатов взаимодействия комплекса «стент – сосуд».
Финансирование
Спонсор исследования — компания-производитель стента «Калипсо» ОАО «Ангиолайн».
Список литературы Простое слепое проспективное рандомизированное мультицентровое исследование эффективности и безопасности сиролимус-доставляющего коронарного стента «Калипco» по сравнению с эверолимус-доставляющим стентом XiencePrime: дизайн и обоснование клинического исследования «ПАТРИOТ»
- Kinnaird T., Kwok C.S., Narain A., Butler R., Ossei-Gerning N., Ludman P., Moat N., Anderson R., Mamas M.A. Meta-Analysis of Percutaneous Coronary Intervention With Drug-Eluting Stent Versus Coronary Artery Bypass Grafting for Isolated Proximal Left Anterior Descending Coronary Disease//Am. J. Cardiol. 2016. Vol. 118. No. 8. P. 1171-1177. https://dx.doi.o DOI: rg/10.1016/j.amjcard.2016.07.030
- Кузнецов В.А., Бессонов И.С., Пушкарев Г.С., Мусихина Н.А., Гультяева Е.П., Зырянов И.П., Горбатенко Е.А., Сапожников С.С. Проспективный регистр чрескожных коронарных вмешательств: опыт Тюменского кардиологического центра//Патология кровообращения и кардиохирургия. 2015. Т. 19. № 3. С. 80-86.
- Holmes D.R. Jr., Leon M.B., Moses J.W., Popma J.J., Cutlip D., Fitzgerald P.J., Brown C., Fischell T., Wong S.C., Midei M., Snead D., Kuntz R.E. Analysis of 1-Year Clinical Outcomes in the SIRIUS Trial: A Randomized Trial of a Sirolimus-Eluting Stent Versus a Standard Stent in Patients at High Risk for Coronary Analysis of 1-Year Clinical Outcomes in the SIRIUS Trial: A Randomized Trial of a Coronary Restenosis//Circulation. 2004. Vol. 109. No. 5. P. 634-640.
- Осиев А.Г., Мироненко С.П., Кретов Е.И., Бирюков А.В., Ёлкина Д.С., Коледа Н.В., Крестьянинов О.В. Сравнительная клинико-ангиографическая оценка отдаленных результатов коронарного стентирования у больных ишемической болезнью сердца при использовании стентов с различным лекарственным покрытием//Патология кровообращения и кардиохирургия. 2012. Т. 16. № 2. С. 45-51.
- Jensen L.O., Thayssen P., Christiansen E.H., Maeng M., Ravkilde J., Hansen K.N., Hansen H.S., Krusell L., Kaltoft A., Tilsted H.H., Berencsi K., Junker A., Lassen J.F.; SORT OUT IV Investigators. Safety and Efficacy of Everolimus-Versus Sirolimus-Eluting Stents: 5-Year Results From SORT OUT IV//J. Am. Coll. Cardiol. 2016. Vol. 67. No. 7. P. 751-62. http://dx.doi.o DOI: rg/10.1016/j.jacc.2015.11.051
- Leon M.B., Kandzari D.E., Eisenstein E.L., Anstrom K.J., Mauri L., Cutlip D.E., Nikolsky E., O'Shaughnessy C., Overlie P.A., Kirtane A.J., McLaurin B.T., Solomon S.L., Douglas J.S. Jr., Popma J.J.; ENDEAVOR IV Investigators. Late Safety, Efficacy, and Cost-Effectiveness of a Zotarolimus-Eluting Stent Compared With a Paclitaxel-Eluting Stent in Patients With De Novo Coronary Lesions 2-Year Follow-Up From the ENDEAVOR IV Trial (Randomized, Controlled Trial of the Medtronic Endeavor Drug Eluting Coronary Stent System Versus the Taxus Paclitaxel-Eluting Coronary Stent System in De Novo Native Coronary Artery Lesions)//JACC Cardiovasc. Interv. 2009. Vol. 2. No. 12. P. 1208-1218.
- Natsuaki M., Kozuma K., Morimoto T., Kadota K., Muramatsu T., Nakagawa Y., Akasaka T., Igarashi K., Tanabe K., Morino Y., Ishikawa T., Nishikawa H., Awata M., Abe M., Okada H., Takatsu Y., Ogata N., Kimura K., Urasawa K., Tarutani Y., Shiode N., Kimura T.; NEXT Investigators. Biodegradable Polymer Biolimus-Eluting Stent Versus Durable Polymer Everolimus-Eluting Stent//J. Am. Coll. Cardiol. 2013. Vol. 62. No. 3. P. 181-190. http://dx.doi.o DOI: rg/10.1016/j.jacc.2013.04.045
- Бокерия Л.А., Алекян Б.Г. Рентгенэндоваскулярные диагностика и лечение заболеваний сердца и сосудов Российской Федерации -2015 год. М.: НЦССХ им. А.Н. Бакулева, 2016. 22 с.
- Beijk M.A., Neumann F.J., Wiemer M., Grube E., Haase J., Thuesen L., Hamm C., Veldhof S., Dorange C., Serruys P.W., Piek J.J. Two-year results of a durable polymer everolimus-eluting stent in de novo coronary artery stenosis (The SPIRIT FIRST Trial)//Eurointervention. 2007. Vol. 3. No. 2. P. 206-212.
- Serruys P.W., Ruygrok P., Neuzner J., Piek J.J., Seth A., Schofer J.J., Richardt G., Wiemer M., Carné D., Thuesen L., Boone E., Miquel-Herbert K., Daemen J. A randomised comparison of an everolimus-eluting coronary stent with a paclitaxel-eluting coronary stent: the SPIRIT II trial//Eurointervention. 2006. Vol. 2. No. 3. P. 286-294.
- Stone G.W., Midei M., Newman W., Sanz M., Hermiller J.B., Williams J., Farhat N., Caputo R., Xenopoulos N., Applegate R., Gordon P., White R.M., Sudhir K., Cutlip D.E., Petersen J.L.; SPIRIT III Investigators. Randomized comparison of everolimus-eluting and paclitaxel-eluting stents two-year clinical follow-up from the clinical evaluation of the Xience V Everolimus Eluting Coronary Stent System in the treatment of patients with de novo native coronary artery lesions (SPIRIT) III Trial//Circulation. 2009. Vol. 119. No. 5. P. 680-686. http://dx.doi. org/10.1161/CirculationAHA.108.803528
- Costa M., Kereiakes D., Smith R., Wu K., Yu X., Cannon L., Wang J., Sudhir K. TCT-608 Two-Year Outcomes after Implantation of XIENCE PRIME and XIENCE PRIME Long Lesion Stents in Patients with Coronary Artery Disease: Results of the SPIRIT PRIME Multicenter Pivotal Clinical Trial//J. Am. Coll. Cardiol. 2012. Vol. 60. No. 17 (Suppl.). B176-B177. http://dx.doi.o DOI: rg/10.1016/j.jacc.2012.08.645
- Осиев А.Г., Редькин Д.А., Марченко А.В., Гранкин Д.С., Верещагин М.А., Бирюков А.В., Кретов Е.И., Зубарев Д.Д., Крестьянинов О.В., Ибрагимов Р.У., Байструков В.И. Оценка эффективности эндоваскулярного лечения больных ишемической болезнью сердца со стенозом ствола левой коронарной артерии//Международный журнал интервенционной кардиоангиологии. 2009. № 19. С. 52.


