Протезирование аортального клапана полнопроточным механическим протезом «МедИнж-СТ» и современной двустворчатой моделью: сравнение непосредственных результатов
Автор: Лепилин М.А., Цеханович В.Н., Шарифулин Р.М., Богачев-Прокофьев А.В.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Приобретенные пороки сердца
Статья в выпуске: 2 т.28, 2024 года.
Бесплатный доступ
Актуальность. Механические протезы клапанов сердца при всем многообразии моделей имеют общий недостаток: их форма и особенности строения запирающих элементов создают препятствие току крови. В основе конструкции механического протеза «МедИнж-СТ» (ЗАО НПП «МедИнж», Пенза, Россия) лежит принцип полнопроточности, что должно увеличить эффективную площадь отверстия клапана при сохранении тех же размеров импланта. Результаты применения данного типа протезов недостаточно изучены. В литературе имеются единичные публикации без сравнения с другими моделями. Цель. Сравнить непосредственные результаты протезирования аортального клапана полнопроточным и стандартным механическими протезами. Методы. В ретроспективное исследование включили 246 пациентов, перенесших протезирование аортального клапана механическим протезом с 2015 по 2021 г. Стандартный двустворчатый протез «МедИнж-2» имплантировали 134 пациентам, полнопроточный протез «МедИнж-СТ» — 112 больным. Для устранения исходных различий между группами провели псевдорандомизацию (propensity score matching). Первичная конечная точка — уровень транспротезного градиента. Результаты. После псевдорандомизации получили 2 группы по 90 человек в каждой. Госпитальная летальность в группах «МедИнж-СТ» и «МедИнж-2» составила 2,2 и 6,7 % соответственно (р = 0,178). В раннем послеоперационном периоде не выявили различий между группами в ремоделировании полости левого желудочка. В группе «МедИнж-СТ» отметили значимо более низкие транспротезные градиенты (средние градиенты 12,6 и 16,1 мм рт. ст., р < 0,001). Эффективная площадь отверстия протеза была больше в группе «МедИнж-СТ» (2,04 и 1,89 см2, p < 0,001). Заключение. Механический клапан «МедИнж-СТ» безопасен при хирургической коррекции аортальных пороков. Его гемодинамическую эффективность подтверждают значимо более низкий уровень транспротезного градиента и бóльшая эффективная площадь отверстия клапана в сравнении со стандартным двустворчатым механическим протезом.
Механический протез, полнопроточный механический протез клапана сердца, порок аортального клапана, протезирование аортального клапана
Короткий адрес: https://sciup.org/142241022
IDR: 142241022 | DOI: 10.21688/1681-3472-2024-2-62-72
Aortic valve replacement with the MedInzh-ST full-flow mechanical implant and modern bicuspid model: comparison of short-term results
Introduction: Mechanical heart valves prostheses have certain disadvantages related to impeding blood flow due to their shape and the design principle of the locking elements. The design of the new model of mechanical prostheses is based on the principle of full flow, which enables to increase the effective area of the valve opening and retain the identical dimensions of the implant. The results of using this type of prosthesis have not been sufficiently studied. Objective: The study aimed to compare the short-term results of aortic valve replacement with the mechanical full-flow prosthesis and with the standard mechanical prosthesis. Methods: The retrospective study included 246 patients who underwent aortic valve replacement with mechanical prosthesis over the period from 2015 to 2021. The MedInzh-2 classical bicuspid valve was implanted in 134 patients, and the new full-flow prosthesis was used in 112 patients. A pseudorandomization procedure (Propensity score matching) was performed to equalize the groups. The level of the transprosthetic gradient was used as the primary endpoint. Results: Propensity score matching resulted into forming two groups of 90 patients each. Hospital mortality in the MedInzh-ST group and the MedInzh-2 group amounted to 2.2% and 6.7%, respectively (Р = 0.178). In the early postoperative period, no differences in the processes of left ventricular cavity remodeling were found between the groups. In the MedInzh-ST full-flow prosthesis group, significantly lower values of transprosthetic gradients were revealed (mean gradients 12.6 versus 16.1 mm Hg, P < 0.001). The effective prosthetic orifice area was statistically higher in the full-flow implant group (2.04 versus 1.89 cm2, P < 0.001). Conclusion: Application of the MedInzh-ST mechanical valve proved to be safe at surgical correction of aortic valve diseases. The prosthesis was hemodynamically effective that was confirmed by a significantly lower level of transprosthetic gradient and a larger effective valve orifice area in comparison to the standard bicuspid mechanical prosthesis.
Текст научной статьи Протезирование аортального клапана полнопроточным механическим протезом «МедИнж-СТ» и современной двустворчатой моделью: сравнение непосредственных результатов
Цитировать: Лепилин М.А., Цеханович В.Н., Шарифулин Р.М., Богачев-Прокофьев А.В. Протезирование аортального клапана полнопроточным механическим протезом «МедИнж-СТ» и современной двустворчатой моделью: сравнение непосредственных результатов. Патология кровообращения и кардиохирургия. 2024;28(2):62-72. https://doi.
How to cite: Lepilin M.A., Tsekhanovich V.N., Sharifulin R.M., Bogachev-Prokophiev A.V. Aortic valve replacement with the MedInzh-ST full-flow mechanical implant and modern bicuspid model: comparison of short-term results. Patologiya krovoobrashcheniya i kardiokhirurgiya = Circulation Pathology and Cardiac Surgery. 2024;28(2):62-72. (In Russ.) https://doi. org/10.21688/1681-3472-2024-2-62-72
M.A. Lepilin,
V.N. Tsekhanovich,
R.M. Sharifulin,
A.V. Bogachev-Prokophiev,
Ежегодно от заболеваний сердечно-сосудистой системы умирает больше людей, чем от любой другой причины [1]. Наряду с высокой распространенностью ишемической болезни сердца в развитых странах растет количество пациентов с приобретенными пороками клапанов. Согласно крупным эпидемиологическим исследованиям, распространенность в общей популяции пороков сердечных клапанов умеренной и выраженной степеней составляет около 2,5 %. С увеличением возраста пациентов этот показатель значительно возрастает [2].
Дегенеративные пороки аортального клапана — самая частая причина аортального стеноза и аортальной регургитации в развитых странах [3; 4]. Наиболее распространенный способ хирургического лечения приобретенных пороков аортального клапана — протезирование. Каждый год в России выполняется около 11 тысяч операций по замене клапанов сердца, их них 60 % — на аортальном клапане [5]. Замена пораженного аортального клапана механическим протезом — стандартная процедура в хирургии приобретенных пороков. Структурная долговечность протеза и минимизация осложнений при соблюдении адекватного уровня антикоагуляции делают эту методику безопасной и эффективной. По данным проспективных рандомизированных исследований, 10-летняя свобода от клапан-ассоциированных осложнений варьирует от 85,5 до 92 % [6–8].
Главным недостатком протезирования клапанов сердца механическими протезами является необходимость в пожизненном приеме антикоагулянтов. Современные двустворчатые механические клапаны конструктивно обеспечивают минимальный контакт крови с элементами протеза, но не исключают тромбоз протеза и тромбоэмболические осложнения. В рандомизированных исследованиях, сравнивающих современные механические клапаны, не выявлены клинические преимущества той или иной модели [9; 10].
Разработка модели механического клапана, которая нивелирует риск тромботических событий, является приоритетным направлением. Новый отечественный механический клапан «МедИнж-СТ» (ЗАО НПП «МедИнж», Пенза) имеет оригинальную конструкцию створок и запирательного элемента. Шарнирные узлы протеза расположены на противоположных сторонах опорного кольца клапана, что обеспечивает централизацию потока крови. Результаты применения данного протеза недостаточно изучены. Имеются единичные публикации без сравнения с другими моделями. Цель данной работы — проанализировать непосредственные результаты протезирования аортального клапана полнопроточным протезом «МедИнж-СТ» в сравнении с современной моделью двустворчатого импланта.
Методы
Провели ретроспективный анализ результатов лечения пациентов, перенесших протезирование аортального клапана с 2015 по 2021 г. Работа одобрена этическим комитетом ФГБОУ ВО «Омский государственный медицинский университет» Минздрава России (протокол № 81 от 26.09.2021 г.).
В исследование включили 246 пациентов, которым был имплантирован механический двустворчатый клапан «МежИнж-2» (n = 134) или полнопроточный протез «МедИнж-СТ» (n = 112). Критерии включения: возраст старше 18 лет; выраженный порок аортального клапана; перенесенная операция по замене аортального клапана с использованием полнопроточного механического протеза «МедИнж-СТ» или двустворчатого механического протеза «МедИнж-2». Критерии исключения: протезирование других клапанов; снижение систолической функции левого желудочка до уровня менее 35 %; наличие конкурирующего заболевания или сопутствующей патологии, значимо влияющих на прогноз и качество жизни пациента после операции (онкологическое заболевание, терминальная стадия хронической болезни почек и др.).
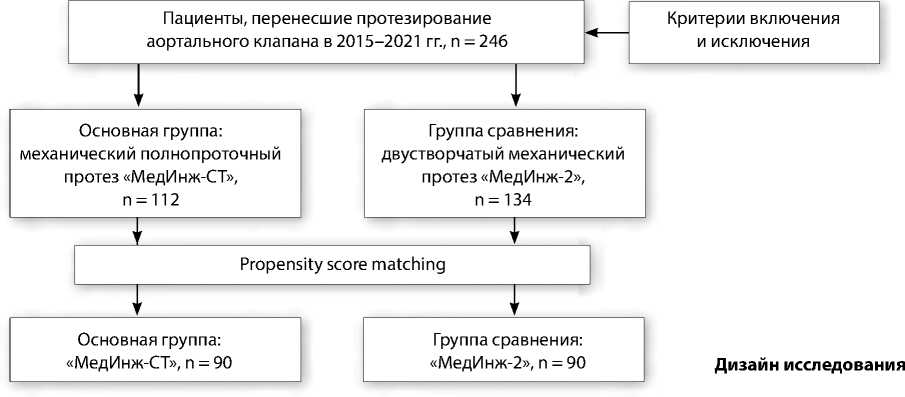
Первичной конечной точкой исследования являлся уровень транспротезного градиента на протезированном аортальном клапане через 12 мес. после операции. Для устранения исходных различий между группами применили метод подбора групп по индексу соответствия (псевдорандомизация, англ. propensity score matching, PSM). Дизайн исследования представлен на рисунке.
Хирургическая техника
Во всех случаях применяли стандартную технику протезирования аортального клапана. Хирургический доступ осуществляли через срединную стернотомию. Операции выполняли в условиях нормотермического искусственного кровообращения по схеме правое предсердие – восходящая аорта. Использовали селективную антеградную кардиоплегию холодовым кристаллоидным раствором. Доступ к аортальному клапану осуществляли через косо-поперечную аортотомию. Имплантацию клапана проводили супра- и интрааннулярным способом на П-образных швах с использованием синтетических прокладок.
Обследование в послеоперационном периоде
Для оценки параметров левого желудочка (конечный диастолический размер, конечный систолический размер, конечный диастолический объем, фракция выброса левого желудочка), функции механического протеза (уровень пикового и среднего градиентов, степень регургитации, эффективная площадь отверстия клапана) при выписке из стационара выполняли трансторакальную эхокардиографию. Эффективную площадь отверстия клапана вычисляли при допплер-эхокардиографии с помощью уравнения непрерывности. Анализировали частоту встречаемости пациент-протезного несоответствия. Критерием пациент-протезного несоответствия средней степени считали значение индексированной эффективной площади отверстия 0,66–0,85 см2/м2, выраженного — ≤ 0,65 см2/м2.
Всем пациентам с полнопроточным протезом «МедИнж-СТ» при выписке проводили лабораторную оценку маркеров гемолиза. Исследовали уровень лактатдегидрогеназы, количество ретикулоцитов, уровень гаптоглобина.
Статистический анализ
Статистическую обработку осуществляли с помощью программы Stata/MP 13.0 (StataCorp LP, Кол-ледж-Стейшен, США). Нормальность распределения непрерывных признаков проверяли с помощью визуальной оценки гистограмм. Количественные данные представлены как среднее ± стандартное отклонение (при нормальном распределении); медиана и 25-й, 75-й процентили (при распределении, отличающемся от нормального). Категориаль- ные данные представлены в виде абсолютных чисел и относительных частот. Показатель propensity score, определяемый как вероятность попадания пациента в группы протезирования аортального клапана стандартным или полнопроточным протезом, рассчитывали для каждого пациента с использованием множественного логистического регрессионного анализа. Переменные, включенные в анализ propensity score, перечислены в табл. 1.
Для PSM-анализа проводили сопоставление ближайшего соседа без возвращения с соотношением групп 1:1 с ограничением внутрипарного расстояния (caliper) по вероятностям (raw propensity score) 0,15. Баланс базовых характеристик после сопоставления оценивали в терминах абсолютных стандартизированных разностей, которые вычисляли как абсолютные стандартизированные разности средних для непрерывных переменных и абсолютные разности пропорций для бинарных переменных. Переменную считали сбалансированной, если абсолютная стандартизированная разность была < 0,1. Межгрупповое сравнение параметров до проведения PSM выполняли с помощью t-критерия для независимых групп, критериев Манна – Уитни (для непрерывных и порядковых данных) и хи-квадрат (для номинальных данных). Для сравнения групп по количественным признакам после PSM использовали t-критерий для зависимых переменных и критерий Уилкоксона. Для сравнения групп по бинарным признакам применяли условную логистическую регрессию. Для выявления предикторов госпитальной летальности в когорте после PSM провели логистический регрессионный анализ. Статистически значимыми считали различия данных при р < 0,05.
|
Табл. 1. Дооперационная характеристика пациентов |
||||||||
|
Показатель |
До propensity score matching |
После propensity score matching |
||||||
|
МедИнж-2, n = 128 |
МедИнж-СТ, n = 110 |
АСР, % |
p |
МедИнж-2, n = 90 |
МедИнж-СТ, n = 90 |
АСР, % |
p |
|
|
Пол мужской, n (%) |
77 (60,2) |
89 (80,9) |
20,7 |
< 0,001 |
67 (74,4) |
69 (76,7) |
2,3 |
0,932 |
|
Возраст, лет |
57,7 ± 10,9 |
57,9 ± 10,7 |
1,6 |
0,904 |
57,9 ± 10,5 |
58,5 ± 11,3 |
5,3 |
0,736 |
|
Вес, кг |
78,3 ± 14,8 |
84,3 ± 14,5 |
40,8 |
0,002 |
81,5 ± 13,4 |
81,4 ± 13,3 |
1,0 |
0,937 |
|
Рост, см |
168,3 ± 9,4 |
172,5 ± 7,8 |
47,9 |
< 0,001 |
171,1 ± 7,9 |
171,5 ± 7,6 |
4,4 |
0,739 |
|
ИМТ, кг/м² |
27,6 ± 4,91 |
28,4 ± 5,01 |
15,5 |
0,235 |
27,9 ± 4,63 |
27,8 ± 4,90 |
3,0 |
0,829 |
|
S поверхности тела, м2 |
1,91 ± 0,21 |
2,0 ± 0,19 |
48,0 |
< 0,001 |
1,96 ± 0,18 |
1,96 ± 0,17 |
0,3 |
0,996 |
|
Гемодинамический вариант порока, n (%): |
||||||||
|
стеноз |
77 (60,2) |
64 (58,2) |
2,0 |
0,758 |
54 (60,0) |
54 (60,0) |
0 |
0,923 |
|
недостаточность |
51 (39,8) |
46 (41,8) |
36 (40,0) |
36 (40,0) |
||||
|
Дисфункция протеза, n (%) |
5 (3,9) |
0 |
3,9 |
0,037 |
1 (1,1) |
0 |
1,1 |
> 0,999 |
|
III–IV ФК NYHA, n (%) |
61 (47,7) |
71 (64,5) |
16,8 |
0,009 |
48 (53,3) |
52 (57,8) |
4,5 |
0,764 |
|
ФП, n (%) |
24 (18,8) |
20 (18,2) |
0,6 |
0,911 |
18 (20,0) |
16 (17,8) |
2,2 |
0,655 |
|
Митральная недостаточность ≥ 2 степени, n (%) |
32 (25,0) |
21 (19,1) |
5,9 |
0,277 |
22 (24,4) |
19 (21,1) |
3,3 |
0,532 |
|
АГ, n (%) |
95 (74,2) |
80 (72,7) |
1,5 |
0,795 |
68 (75,6) |
64 (71,1) |
4,5 |
0,794 |
|
ОНМК в анамнезе, n (%) |
12 (9,4) |
7 (6,4) |
3,0 |
0,394 |
7 (7,8) |
5 (5,6) |
2,2 |
0,773 |
|
ИБС, n (%) |
47 (36,7) |
47 (42,7) |
6,0 |
0,346 |
38 (42,2) |
38 (42,2) |
0 |
0,909 |
|
ПИКС, n (%) |
19 (14,8) |
16 (14,5) |
0,3 |
0,949 |
13 (14,4) |
11 (12,2) |
2,2 |
0,838 |
|
ХОБЛ, n (%) |
36 (28,1) |
35 (31,8) |
3,7 |
0,639 |
31 (34,4) |
29 (32,2) |
2,2 |
0,897 |
|
ХПН, n (%) |
24 (18,8) |
22 (20,0) |
1,2 |
0,808 |
18 (20,0) |
15 (16,7) |
3,3 |
0,728 |
|
Заболевания щитовидной железы, n (%) |
10 (7,8) |
2 (1,8) |
6,0 |
0,036 |
5 (5,6) |
2 (2,2) |
3,4 |
0,449 |
|
ФВ ЛЖ, % |
58,1 ± 10,1 |
57,8 ± 8,2 |
3,3 |
0,800 |
57,7 ± 10,0 |
57,9 ± 8,29 |
3,2 |
0,831 |
|
КДР ЛЖ, см |
5,51 ± 0,92 |
5,67 ± 0,89 |
17,6 |
0,178 |
5,54 ± 0,91 |
5,60 ± 0,85 |
6,7 |
0,641 |
|
КСР ЛЖ, см |
3,81 ± 0,85 |
3,92 ± 0,85 |
13,1 |
0,315 |
3,84 ± 0,85 |
3,87 ± 0,81 |
2,9 |
0,845 |
|
КДО ЛЖ, мл |
153,9 ± 59,1 |
163,1 ± 60,9 |
15,3 |
0,240 |
155,9 ± 59,6 |
158,5 ± 57,6 |
4,3 |
0,765 |
|
ИКДО ЛЖ, мл/м² |
81,4 ± 31,9 |
82,3 ± 31,9 |
2,8 |
0,829 |
79,8 ± 31,2 |
81,6 ± 31,3 |
5,5 |
0,709 |
|
КСО ЛЖ, мл |
67,2 ± 35,8 |
71,3 ± 40,8 |
10,8 |
0,405 |
68,7 ± 36,5 |
68,7 ± 39,3 |
0,1 |
0,997 |
|
ММ ЛЖ, г |
349,2 ± 87,7 |
335,3 ± 116,8 |
3,5 |
0,794 |
305,5 ± 84,5 |
317,8 ± 113,1 |
3,1 |
0,383 |
|
ИММ ЛЖ, г/м2 |
181,9 ± 45,9 |
167,8 ± 58,2 |
7,4 |
0,581 |
156,0 ± 42,2 |
162,7 ± 59,2 |
3,5 |
0,341 |
|
Средний градиент на АоК, мм рт. ст. |
40,4 ± 26,0 |
38,2 ± 26,6 |
8,5 |
0,515 |
39,2 ± 24,4 |
39,2 ± 27,0 |
0,2 |
0,990 |
|
Фиброзное кольцо, мм |
23,2 ± 0,25 |
23,7 ± 0,15 |
24,6 |
0,065 |
23,6 ± 2,35 |
23,6 ± 1,55 |
1,6 |
0,912 |
|
Синусы, мм |
34,3 ± 0,47 |
36,3 ± 0,46 |
41,9 |
0,001 |
35,4 ± 4,86 |
35,8 ± 4,64 |
9,1 |
0,492 |
|
Восходящая аорта, мм |
37,2 ± 0,56 |
38,9 ± 0,54 |
29,7 |
0,023 |
38,1 ± 5,55 |
38,5 ± 5,74 |
6,7 |
0,673 |
Примечание. АГ — артериальная гипертензия; АоК — аортальный клапан; АСР — абсолютная стандартизированная разность; ИБС — ишемическая болезнь сердца; ИКДО — индексированный конечный диастолический объем; ИММ — индексированная масса миокарда; ИМТ — индекс массы тела; КДО — конечный диастолический объем; КДР — конечный диастолический размер; КСО — конечный систолический объем; КСР — конечный систолический размер; ЛЖ — левый желудочек; ММ — масса миокарда; ОНМК — острое нарушение мозгового кровообращения; ПИКС — постинфарктный кардиосклероз; ФК NYHA — функциональный класс хронической сердечной недостаточности по классификации Нью-Йоркской ассоциации кардиологов (англ. New York Heart Association); ФВ — фракция выброса; ФП — фибрилляция предсердий; ХОБЛ — хроническая обструктивная болезнь легких; ХПН — хроническая почечная недостаточность; S — площадь. Данные представлены как n (%) или как M ± SD.
Результаты
До процедуры PSM группы не были сбалансированы по антропометрическим параметрам (рост, вес, площадь поверхности тела). В группе «МедИнж-2» было больше пациентов с дисфункцией ранее имплантированного механического клапана. У пациентов в группе «МедИнж-СТ» отметили исходно больший размер восходящего отдела аорты. Кроме того, больные не были сопоставимы по тяжести сердечной недостаточности по классифика- ции Нью-Йоркской ассоциации кардиологов (англ. New York Heart Association). После PSM сформировали 2 группы по 90 пациентов, сбалансированные по основным дооперационным демографическим и клиническим характеристикам (табл. 1).
По структуре сопутствующих вмешательств группы достоверно не различались. В группе «МедИнж-СТ» отмечены меньшие длительность искусственного кровообращения и общая продолжительность операции (табл. 2).
Табл. 2. Операционные результаты
|
Показатель |
До propensity score matching |
После propensity score matching |
||||
|
МедИнж-2, n = 128 |
МедИнж-СТ, n = 110 |
p |
МедИнж-2, n = 90 |
МедИнж-СТ, n = 90 |
p |
|
|
Время окклюзии аорты, мин |
76,0 [62,5; 99,5] |
71,0 [59,0; 92,0] |
0,1062 |
78,5 [62,0; 100,0] |
71,0 [60,0; 92,0] |
0,1734 |
|
Время искусственного кровообращения, мин |
105,0 [87,0; 128,5] |
94,0 [79,0; 126,0] |
0,0422 |
107,5 [88,0; 134,0] |
93,5 [80,0; 127,0] |
0,0634 |
|
Длительность операции, мин |
253,3 ± 77,6 |
234,2 ± 47,6 |
0,0261 |
261,4 ± 81,7 |
232,8 ± 47,7 |
0,0065 |
|
Посадочный размер протеза, мм |
22,2 ± 1,8 |
22,7 ± 1,4 |
0,0081 |
22,5 ± 1,7 |
22,6 ± 1,3 |
0,7635 |
|
Сопутствующие вмешательства, n (%): |
||||||
|
Коронарное шунтирование |
25 (19,5) |
27 (24,6) |
0,3523 |
19 (21,1) |
23 (25,6) |
0,4516 |
|
Протезирование / экзопротезирование аорты |
5 (3,9) |
13 (11,8) |
0,0223 |
4 (4,4) |
10 (11,1) |
0,6186 |
|
Пластика митрального клапана |
5 (3,9) |
0 |
0,0373 |
3 (3,3) |
0 |
> 0,9996 |
|
Радиочастотная фрагментация предсердий |
2 (1,6) |
1 (0,91) |
0,6533 |
2 (2,2) |
0 |
> 0,9996 |
|
Отделяемое по дренажам, мл |
350,0 [300,0; 450,0] |
300,0 [250,0; 400,0] |
0,0102 |
350,0 [300,0; 450,0] |
300,0 [250,0; 400,0] |
0,0144 |
|
Искусственная вентиляция легких, ч |
8,2 ± 2,0 |
8,1 ± 1,2 |
0,7591 |
8,3 ± 2,2 |
8,3 ± 1,1 |
0,8225 |
|
Пребывание в ОРИТ, сут. |
4,2 ± 1,1 |
4,3 ± 1,1 |
0,5301 |
4,2 ± 1,2 |
4,3 ± 1,1 |
0,4345 |
|
Осложнения раннего послеоперационного периода, n (%): |
||||||
|
Госпитальная летальность |
12 (9,4) |
2 (1,8) |
0,0143 |
6 (6,7) |
2 (2,2) |
0,1786 |
|
Потребность в инотропной поддержке |
65 (50,8) |
57 (51,8) |
0,8733 |
54 (60) |
46 (51,1) |
0,2606 |
|
Рестернотомия, гемостаз |
11 (8,6) |
7 (6,4) |
0,5173 |
7 (7,8) |
6 (6,7) |
0,7636 |
|
Инфаркт миокарда |
2 (1,6) |
0 |
0,5013 |
2 (1,1) |
1 (1,1) |
0,5716 |
|
Острое нарушение мозгового кровообращения |
1 (0,78) |
0 |
> 0,9993 |
1 (1,1) |
0 |
> 0,9996 |
Список литературы Протезирование аортального клапана полнопроточным механическим протезом «МедИнж-СТ» и современной двустворчатой моделью: сравнение непосредственных результатов
- Nishimura R.A., Otto C.M., Bonow R.O., Carabello B.A., Erwin J.P. 3rd, Guyton R.A., O'Gara P.T., Ruiz C.E., Skubas N.J., Sorajja P., Sundt T.M. 3rd, Thomas J.D., Anderson J.L., Halperin J.L., Albert N.M., Bozkurt B., Brindis R.G., Creager M.A., Curtis L.H., DeMets D., Guyton R.A., Hochman J.S., Kovacs R.J., Ohman E.M., Pressler S.J., Sellke F.W., Shen W.-K., Stevenson W.G., Yancy C.W.; American College of Cardiology/American Heart Association. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Thorac Cardiovasc Surg. 2014;148(1):e1-e132. PMID: 24939033. https://doi.org/10.1016/j.jtcvs.2014.05.014
- Nkomo V.T., Gardin J.M., Skelton T.N., Gottdiener J.S., Scott C.G., Enriquez-Sarano M. Burden of valvular heart diseases: a population-based study. Lancet. 2006;368(9540):1005-1011. PMID: 16980116. https://doi.org/10.1016/S0140-6736(06)69208-8
- Pawade T.A., Newby D.E., Dweck M.R. Calcification in aortic stenosis: The skeleton key. J Am Coll Cardiol. 2015;66(5):561-577. PMID: 26227196. https://doi.org/10.1016/j.jacc.2015.05.066
- Rajamannan N.M., Evans F.J., Aikawa E., Grande-Allen K.J., Demer L.L., Heistad D.D., Simmons C.A., Masters K.S., Mathieu P., O'Brien K.D., Schoen F.J., Towler D.A., Yoganathan A.P., Otto C.M. Calcific aortic valve disease: not simply a degenerative process: A review and agenda for research from the National Heart and Lung and Blood Institute Aortic Stenosis Working Group. Executive summary: Calcific aortic valve disease-2011 update. Circulation. 2011;124(16):1783-1791. PMID: 22007101; PMCID: PMC3306614. https://doi.org/10.1161/CIRCULATIONAHA.110.006767
- Астапов Д.А., Демидов Д.П., Семенова Е.И. Протезирование аортального клапана бескаркасным биологическим протезом. Хирургия. Журнал им. Н.И. Пирогова. 2016;(5):4-12. https://doi.org/10.17116/hirurgia201654-12 Astapov D.A., Demidov D.P., Semenova E.I. Aortic valve replacement with stentless bioprosthesis. Khirurgiya. Zhurnal im. N.I. Pirogova = Pirogov Russian Journal of Surgery. 2016;(5):4-12. (In Russ.) https://doi.org/10.17116/hirurgia201654-12
- Toole J.M., Stroud M.R., Kratz J.M., Crumbley A.J. 3rd, Bradley S.M., Crawford F.A. Jr, Ikonomidis J.S. Twenty-five year experience with the St. Jude medical mechanical valve prosthesis. Ann Thorac Surg. 2010;89(5):1402-1409. PMID: 20417752. https://doi.org/10.1016/j.athoracsur.2010.01.045
- Lund O., Nielsen S.L., Arildsen H., Ilkjaer L.B., Pilegaard H.K. Standard aortic St. Jude valve at 18 years: performance profile and determinants of outcome. Ann Thorac Surg. 2000;69(5):1459-1465. PMID: 10881823. https://doi.org/10.1016/s0003-4975(00)01191-7
- Khan S.S., Trento A., DeRobertis M., Kass R.M., Sandhu M., Czer L.S., Blanche C., Raissi S., Fontana G.P., Cheng W., Chaux A., Matloff J.M. Twenty-year comparison of tissue and mechanical valve replacement. J Thorac Cardiovasc Surg. 2001;122(2):257-269. PMID: 11479498. https://doi.org/10.1067/mtc.2001.115238
- Bryan A.J., Rogers C.A., Bayliss K., Wild J., Angelini G.D. Prospective randomized comparison of CarboMedics and St. Jude Medical bileaflet mechanical heart valve prostheses: ten-year follow-up. J Thorac Cardiovasc Surg. 2007;133(3):614-622. PMID: 17320553. https://doi.org/10.1016/j.jtcvs.2006.08.075
- Murday A.J., Hochstitzky A., Mansfield J., Miles J., Taylor B., Whitley E., Treasure T. A prospective controlled trial of St. Jude versus Starr Edwards aortic and mitral valve prostheses. Ann Thorac Surg. 2003;76(1):66-73; discussion 73-74. PMID: 12842515. https://doi.org/10.1016/s0003-4975(03)00118-8
- Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия – 2015. Болезни и врожденные аномалии системы кровообращения. М.: НЦССХ им А.Н. Бакулева, 2016. 208 с. Bokeriya L.A., Gudkova R.G. Cardiovascular surgery – 2015. Diseases and congenital anomalies of the circulatory system. Moscow: Bakulev National Medical Research Center for Cardiovascular Surgery Publ.; 2016. 208 p. (In Russ.)
- Рогулина Н.В., Горбунова Е.В., Кондюкова Н.В., Одаренко Ю.Н., Барбараш Л.С. Сравнительная оценка качества жизни реципиентов механических и биологических протезов при митральном пороке. Российский кардиологический журнал. 2015;(7):94-97. https://doi.org/10.15829/1560-4071-2015-7-94-97 Rogulina N.V., Gorbunova E.V., Kondyukova N.V., Odarenko Yu.N., Barbarash L.S. Comparison of the life quality with mechanical and biological mitral prostheses. Russian Journal of Cardiology. 2015;(7):94-97. (In Russ.) https://doi.org/10.15829/1560-4071-2015-7-94-97
- Celiento M., Filaferro L., Milano A.D., Anastasio G., Ferrari G., Bortolotti U. Single center experience with the Sorin Bicarbon prosthesis: a 17-year clinical follow-up. J Thorac Cardiovasc Surg. 2014;148(5):2039-2044. PMID: 24332112. https://doi.org/10.1016/j.jtcvs.2013.11.015
- Tominaga R., Kurisu K., Ochiai Y., Tomita Y., Masuda M., Morita S., Yasui H. A 10-year experience with the Carbomedics cardiac prosthesis. Ann Thorac Surg. 2005;79(3):784-789. PMID: 15734377. https://doi.org/10.1016/j.athoracsur.2004.08.067
- Молчанов А.Н., Идов Э.М., Хрущев И.В., Гамзаев А.Б., Ананьев Д.А., Цеханович В.Н., Богачев-Прокофьев А.В., Чернов И.И., Дробот Д.Б., Глумсков А.Б., Евдокимов С.В. Результаты протезирования аортального клапана полнопроточным механическим протезом «МедИнж-СТ». Медицинский альманах. 2018;(1):105-108. Molchanov А.N., Idov E.М., Khruschev I.V., Gamzaev А.B., Ananiev D.А., Tsekhanovich V.N., Bogachev-Prokofiev А.V., Chernov I.I., Drobot D.B., Glumskov А.B., Evdokimov S.V. Results of aortic valve replacement with “MedInzh-ST” full-flow prosthetic cardiac valve. Medicinskij almanah = Medical Almanac. 2018;(1):105-108. (In Russ.)
- Biancari F., Martin M., Bordin G., Vettore E., Vinco G., Anttila V., Airaksinen J., Vasques F. Basic data from 176 studies on the immediate outcome after aortic valve replacement with or without coronary artery bypass surgery. J Cardiothorac Vasc Anesth. 2014;28(5):1251-1256. PMID: 24290746. https://doi.org/10.1053/j.jvca.2013.07.020
- Magovern J.A., Pennock J.L., Campbell D.B., Pae W.E., Bartholomew M., Pierce W.S., Waldhausen J.A. Aortic valve replacement and combined aortic valve replacement and coronary artery bypass grafting: predicting high risk groups. J Am Coll Cardiol. 1987;9(1):38-43. PMID: 3491844. https://doi.org/10.1016/S0735-1097(87)80079-7
- Энгиноев С.Т., Зеньков А.А., Чернов И.И., Джамбиева М.Н., Рамазанова Н.Э., Баев Д.Ю., Хассан М.М., Болурова А.М., Колесников В.Н. Непосредственные и среднесрочные результаты имплантации механического протеза «МедИнж-2» в аортальной позиции: десятилетний опыт одного центра. Креативная хирургия и онкология. 2024;14(1):20-28. https://doi.org/10.24060/2076-3093-2024-14-1-20-28 Enginoev S.T., Ziankou A.A., Chernov I.I., Dzhambieva M.N., Ramazanova N.E., Baev D.Yu., Hassan M.M., Bolurova A.M., Kolesnikov V.N. Immediate and mid-term results of implanting a MedInzh-2 mechanical prosthesis in the aortic position: ten-year experience of one center. Creative Surgery and Oncology. 2024;14(1):20-28. (In Russ.) https://doi.org/10.24060/2076-3093-2024-14-1-20-28
- Chambers J., Roxburgh J., Blauth C., O'Riordan J., Hodson F., Rimington H. A randomized comparison of the MCRI On-X and CarboMedics Top Hat bileaflet mechanical replacement aortic valves: early postoperative hemodynamic function and clinical events. J Thorac Cardiovasc Surg. 2005;130(3):759-764. PMID: 16153925. https://doi.org/10.1016/j.jtcvs.2005.02.057
- Jawitz O.K., Wang T.Y., Lopes R.D., Chavez A., Boyer B., Kim H., Anstrom K.J., Becker R.C., Blackstone E., Ruel M., Thourani V.H., Puskas J.D., Gerdisch M.W., Johnston D., Capps S., Alexander J.H., Svensson L.G. Rationale and design of PROACT Xa: A randomized, multicenter, open-label, clinical trial to evaluate the efficacy and safety of apixaban versus warfarin in patients with a mechanical On-X Aortic Heart Valve. Am Heart J. 2020;227:91-99. PMID: 32693197; PMCID: PMC7484170. https://doi.org/10.1016/j.ahj.2020.06.014
- Базылев В.В., Глумсков А.Б., Евтюшкин И.А., Идов Э.М., Молчанов А.Н., Богачев-Прокофьев А.В., Салегин А.В., Чигинев В.А., Гамзаев А.Б., Ананьев Д.А., Козлов А.В., Сакович В.А., Дробот Д.Б., Тарасов Д.Г., Чернов И.И., Цеханович В.Н. Среднесрочные результаты клинического исследования аортальных полнопроточных механических протезов клапанов сердца «МедИнж-СТ». Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сердечно-сосудистые заболевания. 2016;17(S6):27. Bazylev V.V., Glumskov A.B., Yevtyushkin I.A., Idov E.M., Molchanov A.N., Bogachev-Prokophiev A.V., Salegin A.V., Chiginev V.A., Gamzayev A.B., Ananyev D.A., Kozlov A.V., Sakovich V.A., Drobot D.B., Tarasov D.G., Chernov I.I., Tsekhanovich V.N. Mid-term results of clinical studies of aortic full-flow mechanical heart valve prostheses “MedInzh-ST”. The Bulletin of Bakoulev Center. Cardiovascular Diseases. 2016;17(S6):27. (In Russ.)
- Абдульянов И.В., Вагизов И.И., Каипов А.Э. Клинические результаты протезирования клапанов сердца двустворчатым полнопроточным механическим протезом «МедИнж-СТ». Ангиология и сосудистая хирургия. Журнал им. академика А.В. Покровского. 2020;26(4):141-148. https://doi.org/10.33529/ANGIO2020419 Abdulyanov I.V., Vagizov I.I., Kaipov A.E. Clinical results of cardiac valve repair with bicuspid full-flow mechanical prosthesis “MedEng-ST”. Angiology and Vascular Surgery. 2020;26(4):141-148. (In Russ.) https://doi.org/10.33529/ANGIO2020419


