Пузырно-влагалищные свищи: современные концепции диагностики и лечения
Автор: Сучков Денис Александрович, Шахалиев Р.А., Шкарупа Д.Д., Шкарупа А.Г., Кубин Н.Д., Гаджиев Н.К., Шульгин А.С.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Урогинекология
Статья в выпуске: 2 т.15, 2022 года.
Бесплатный доступ
Введение. Пузырно-влагалищный свищ (ПВС) - это патологическое сообщение между мочевым пузырем и влагалищем. В связи с отсутствием общих подходов к выбору тактики лечения, времени его начала и послеоперационному ведению больных, заболевание не теряет своей актуальности и остается одной из наиболее серьезных проблем современной урогинекологии. Материалы и методы. Поиск данных выполнялся с использованием базы PubMed, поисковой системы Google Scholar и научной электронной библиотеки России eLibrary.ru. Результаты и обсуждение. ПВС - наиболее частая форма мочеполовых свищей. В развитых странах формирование ПВС в основном является следствием хирургической травмы или перенесенной лучевой терапии. В развивающихся странах большинство ПВС имеют акушерскую этиологию. Существуют различные классификации ПВС, однако, нет единой, подходящей для прогнозирования эффективности лечения и отдаленных результатов независимо от их этиологии. Лечение ПВС при помощи длительного дренирования мочевого пузыря следует проводить только при небольших, доброкачественных, несформированных ПВС. Основным методом лечения ПВС является хирургическое вмешательство. Оно может быть выполнено с использованием абдоминального и влагалищного доступа. Положительный результат (закрытие свища) достигается в среднем в 90,8% случаев, независимо от примененного доступа. Лечение постлучевых свищей более затруднительно и сопряжено с высоким процентом неудач. Заключение. При всем многообразии методов лечения ПВС, идеального способа до сих пор не существует. Это связано с большим вариативным разнообразием ПВС, отсутствием единых подходов к лечению данной патологии и недостаточным количеством исследований, позволяющих сравнить различные методы хирургического лечения.
Пузырно-влагалищный свищ, урогенитальный свищ, мочеполовой свищ, диагностика, фистулопластика
Короткий адрес: https://sciup.org/142235314
IDR: 142235314 | DOI: 10.29188/2222-8543-2022-15-2-148-161
Vesico-vaginal fistulas: modern concepts of diagnosis and treatment
Introduction. Vesicovaginal fistula (VVF) is a pathological communication between the urinary bladder and the vagina. The lack of common approaches to the treatment choice, its timing and postoperative management of patients makes this disorder one of the challenges of modern urogynecology. Materials and methods. Relevant publications were searched using the PubMed database, the Google Scholar search system, and the scientific electronic library eLibrary.ru. Results. VVF is the most common form of urogenital fistulas. In developed countries, the formation of VVF mainly are the result of surgical trauma or radiation therapy, but in developing ones the majority of VVF have an obstetric etiology. There are different classifications of VVF; however, there is no overall accepted one that is suitable for predicting treatment efficacy and long-term outcomes regardless of etiology of VVF. Treatment of VVF with long-term bladder drainage should be performed only for small, benign and unformed VVF. Surgical closure of VVF is the primary method of treatment. Surgery can be performed using abdominal and vaginal access. Regardless of the access, a positive result (closure of the fistula) on average is achieved in 90,8% of cases. The treatment of post-radiation fistulas is more challenged and associated with a high failure rate. Conclusion. Despite of the variety of VVF treatment options, unfortunately, there is no the perfect one yet due to the variability of VVF ethiology, the lack of unified curative approaches and the shortage of studies comparing different therapies.
Текст обзорной статьи Пузырно-влагалищные свищи: современные концепции диагностики и лечения
Пузырно-влагалищный свищ (ПВС) – это патологическое сообщение между мочевым пузырем и влагалищем (рис. 1).
В связи с отсутствием общих подходов к выбору тактики лечения, времени его проведения и послеопе рационному ведению больных, данное заболевание не теряет своей актуальности на протяжении многих лет и остается одной из наиболее серьезных проблем совре менной реконструктивной урогинекологии [1, 2].
Постоянное неконтролируемое выделение мочи из половых путей зачастую приводит к социальной деза даптации пациенток, стигматизации и изоляции в об ществе [3].
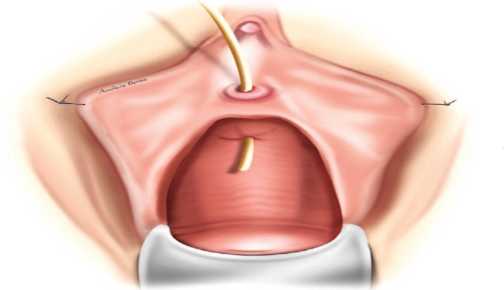
Рис. 1. Пузырно-влагалищный свищ с проведенным в его просвет мочеточниковым катетером
Fig. 1. Vesico-vaginal fistula with a ureteral catheter inserted into its lumen
Hillary и соавт. в своем обзоре сообщают, что 83,2% слу чаев ПВС в развитых странах имеют хирургическую этиологию, среди них 62,7% – после гистерэктомии.
В развивающихся странах 95,2 % случаев ПВС имеют акушерскую этиологию (чаще всего в результате затяжных затрудненных родов – дистоции), в 9% слу чаев – после кесарева сечения и в 2% – после инстру ментального родоразрешения [4].
В России и странах СНГ 40,54% мочеполовых сви щей имеют хирургическую этиологию, 58,91% – яв ляются следствием лучевой терапии и 3,59% связаны с акушерскими причинами. На долю пузырно-влагалищ ных свищей приходится 71,41% всех случаев [6].
Этиология и патогенез
Среди причин возникновения мочеполовых сви щей можно выделить следующие: акушерские, хирурги ческие, лучевые, онкологические, травматические, а также осложненения инфекций влагалища и нижних мочевыводящих путей.
Истинные акушерские свищи
В основе патогенеза «истинных» акушерских ПВС, то есть возникших в результате родовой деятельности, а не ятрогенного воздействия при родоразрешении лежит длительная ишемия в результате сдавления пе редней стенки влагалища и мочевого пузыря между та зовыми костями и головкой плода, приводящая к некрозу тканей (рис. 2) [7, 8].
МАТЕРИАЛЫ И МЕТОДЫ
Произведен поиск и анализ релевантных публика ций с использованием базы PubMed (https://pubmed. , поисковой системы Google Scholar , научной электронной библиотеки России , по ключевым словам: «пузырно-влагалищный свищ», «урогенитальный свищ», «мочеполовой свищ», «vesicovaginal fis-tula», «urogenital fistula», «genitourinary fistula». Отобрано 70 источников, на основании которых представлена информация об эпидемиологии,этиологии, патогенезе, классификации, диагностике и лечении пузырно-влагалищных свищей.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
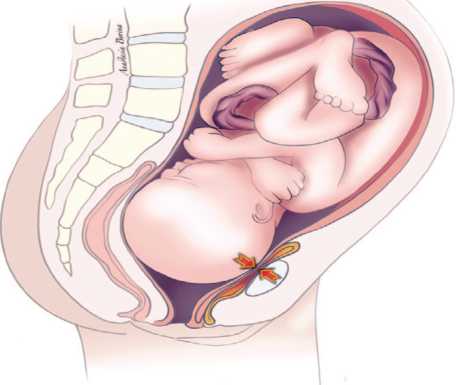
Рис. 2. Cдавление передней стенки влагалища и мочевого пузыря между тазовыми костями и головкой плода
Fig. 2. Compression of the anterior vaginal wall and bladder between the pelvic bones and the fetal head
Эпидемиология
ПВС – наиболее частая форма мочеполовых свищей [4, 5]. По оценкам различных авторов, более трех миллионов женщин в развивающихся странах живут с нелечеными ПВС. Только в Африке ежегодно выявляется от 30 000 до 130 000 новых случаев [3].
В развитых странах формирование мочеполовых свищей, в основном, является следствием хирургической травмы или перенесенной лучевой терапии. C.J.
Неправильное предлежание и несоответствие раз меров таза роженицы с предлежащей частью плода яв ляется основным фактором развития затрудненных родов [9].
Осложненные длительные роды должны быть раз решены путем выполнения кесарева сечения, но в раз вивающихся странах и отдаленных регионах своевре менный доступ к неотложной акушерской помощи часто затруднен [10]. В таких условиях роды могут продолжаться до 4-5 дней без медицинской помощи, что приводит к безусловной гибели плода от удушья [11]. Через 1-2 дня мертвый плод мацерируется и меняет свою форму в тазу матери настолько, что может быть самостоятельно изгнан роженицей через влагалище. Через несколько дней некротизированные ткани секвестрируются, оставляя на своем месте свищ между мочевым пузырем и влагалищем [3].
Ятрогенные акушерские свищи
При выполнении кесарева сечения основными факторами риска, приводящими к повреждению моче вого пузыря, могут быть спаечные процессы, вызван ные ранее перенесенным кесаревым сечением или хирургическими вмешательствами на тазовых органах, повторные роды, наличие крупного плода (массой более 4 кг), так как он требует большего разреза на матке и проведения оперативного родоразрешения по экстренным показаниям (рис. 3) [12].
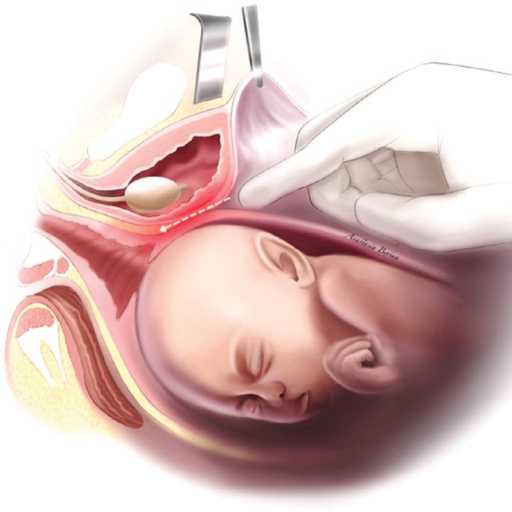
Рис. 3. Зона возможного повреждения стенки мочевого пузыря при выполнении кесарева сечения
Fig. 3. Area of possible bladder wall injury during cesarean section
Хирургические свищи
К факторам риска образования хирургических ПВС относятся предшествующие операции на органах малого таза, наличие очагов эндометриоза и злокачественных новообразований, перенесенная лучевая терапия, а также изменения нормальных анатомических взаимоотношений органов а этой области (например, при большой миоме матки). Все вышеперечисленные факторы риска повышают вероятность ятрогенного повреждения стенки мочевого пузыря и влагалища, в следствие чего может образоваться урогенитальный свищ [4, 7].
Важно отметить, что ятрогенное повреждение мочевого пузыря, с последующим формированием мочеполовых фистул, может произойти во время любой операции на органах малого таза, но лидирую щей причиной возникновения ПВС после хирургических вмешательств является гистерэктомия [4].
Данные анализа 343 771 выполненных гистерэктомий, проведенного P. Hilton и соавт., свидетельствуют, что каждая 788 операция осложнялась ПВС. Частота их возникновения зависела от типа операции и показаний к ней. Наибольшее количество наблюдалось после радикальной гистерэктомии по поводу рака шейки матки, наименьшее – после влагалищной гистерэктомии при пролапсе органов малого таза [13].
Рассматривая механизмы формирования ПВС при гистерэктомиии можно выделить следующие сценарии. Нераспознанное повреждение мочевого пузыря во время гистерэктомии приводит к образованию ури-номы или мочевого затека.Затем моча идет по пути наименьшего сопротивления и стекает через линию шва культи влагалища образуя патологическое сообщение между мочевым пузырем и влагалищем. Второй возможный механизм – это некроз тканей вследствие сдавления из-за неправильно наложенных швов между культей влагалища и мочевым пузырем, либо наложение зажима на стенку мочевого пузыря с последующим формированием свища [3].
Лучевые и онкологические свищи
Рост онкогинекологической заболеваемости и ее выявляемости приводит к увеличению случаев использования лучевой терапии и, соответственно, к росту количества осложнений со стороны органов мочеполовой системы.
История лучевой терапи при онкогинекологиче-ской патологии берет начало с 1903 г., когда Margaret Abigail Cleaves сообщила о первом успешном внутри-полостном применении радия у пациентки с раком шейки матки.
Первые упоминания о лучевых повреждениях органов мочевыделительной системы встречаются в работах Heyneman (1914), Г.Н. Берман (1926) и W. Schmidt (1926).
В 1961 году на ХII конгрессе международного общества урологов в Рио-де-Жанейро активно обсуждался вопрос о влиянии лучевой терапии на органы мочевой системы [14].
В настоящее время, несмотря на меньшую агрессивность методов лучевой терапии, проблема постлучевых свищей остается актуальной [15]. По данным ретроспективного анализа U. Maier и соавт. из 10 709 пациенток, перенесших лучевую терапию, урологические осложнения наблюдались у 133. У 35 из них были ПВС [16].
В свою очередь, по данным C.J. Hillary и соавт., в развитых странах, из общего числа пациенток с урогенитальными фистулами, 13% проходили курсы лучевой терапии (с предшествующей радикальной операцией или без нее). В развивающихся странах эта цифра составляет 0,2% [4]. Отрицательные эффекты лучевой экспериментальная и клиническая урология № 2 2 0 2 2 терапии наблюдаются, когда разница в чувствительно сти к облучению между опухолевой и нормальной тка нью невелика, а также при несоблюдении норм лучевой нагрузки [17].
Оценка уровня лучевой нагрузки, приводящего к изменению в тканях и формированию свищей, прове дена в нескольких исследованиях.
Д.Ю. Пушкарь и соавт. провели анализ 216 про оперированных пациентов с постлучевыми свищами. Из-за различных стандартов лучевой терапии, приме няемых в течение последних 40 лет, разделить этих па циентов на группы по схемам лечения не представлялось возможным. По данным авторов 86,1% женщин (186 пациентов) получили кумулятивную дозу облуче ния 40–60 гр. Еще 26 женщин (12,0%) имели общую
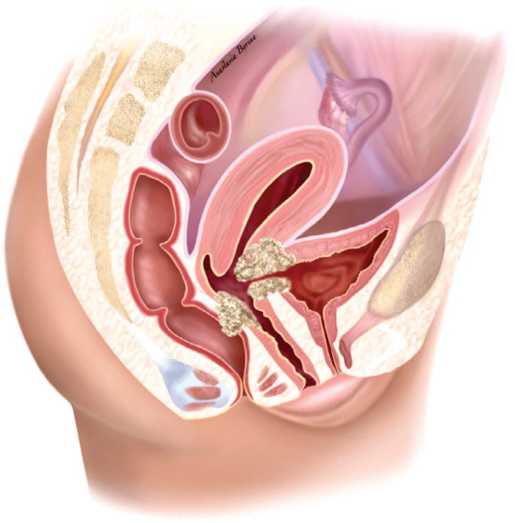
Рис. 4. Формирование ПВС в результате распада опухоли шейки матки
Fig. 4. Formation of VVF as a result of cervical tumor necrosis дозу облучения менее 40 гр. У 4 (1,85%) больных луче вой режим остался неясным [15].
В исследовании U. Maier и соавт. 35 пациенток с постлучевыми ПВС, ранее проходили курсы комбини рованной лучевой терапии с средней кумулятивной дозой облучения 67,5 Гр [16].
Последствия радиационного облучения наблю даются как в процессе лечения, так и после него. ПВС могут формироваться в течение 2-3 лет после оконча ния курса лучевой терапии. Латентный период может быть и более продолжительным [18].
В основе патогенеза лучевого поражения мочевого пузыря лежит фиброз подслизистого и мышечного слоев [17]. В тканях развивается хроническое воспале ние с изменением мелких сосудов (облитерирующий эндартериит), которое приводит к нарушению микро циркуляции, ишемии тканей, некрозу эпителия и в ко нечном итоге – формированию свища [19].
Говоря об истинных онкологических причинах, ПВС формируются в результате опухолевого распа да при местно-распространенных формах злокачествен ных новообразований органов малого таза (рис. 4) [20].
По данным метаанализа C.J. Hillary и соавт., в раз вивающихся странах мочеполовые свищи онкологиче ского генеза встречаются в 0,1% (14/10398 случаев), а в развитых странах, среди анализируемых случаев, онко логические свищи не наблюдались (0/2055 случаев) [4].
Классификация
Предложены различные классификации пузырно влагалищных свищей, однако, к сожалению, нет еди ной, подходящей для прогнозирования эффектив ности лечения и отдаленных результатов независимо от этиологии [21].
В качестве основы для планирования лечения пу зырно-влагалищные свищи подразделяют на простые и сложные (табл. 1) [22, 23].
Таблица 1. Классификация ПВС по уровню сложности
Table 1. Classification of VVF by level of difficulty
|
Простой свищ Simple fistula |
Сложный свищ Complex fistula |
|
Небольшой размер (<0,5 см) Small size (<0,5 cm) |
Большой размер (≥2,5 см) Large size (≥2,5 cm) |
|
Одиночный Single |
Множественные свищи Multiple fistulas |
|
Не связан с лучевой терапией Not associated with radiotherapy |
Связан с лучевой терапией Associated with radiotherapy |
|
Не связан с злокачественным новообразованием Not associated with malignancy |
Связан с злокачественным новообразованием Associated with malignancy |
|
Рецидивирующий свищ Previously failed fistula repairs |
|
|
Связан с хроническим заболеванием Associated with a chronic disease |
|
|
Свищ размером 0,5–2,5 см считается промежуточным A fistula sized 0,5–2,5 cm is considered as intermediate |
|
В 2004 г. J. Goh и соавт. предложили классификацию (рис. 5), выделяющую 4 основных типа свищей в зависимости от расположения относительно наружного отверстия уретры, их подтипы, включающие размер свища, длину и емкость влагалища, а также осложняющие факторы [24]. Классификация достаточно полно отражает характеристики пузырно-влагалищных свищей и позволяет прогнозировать риски осложнений (вовлечение интрамуральных отделов мочеточников в патологический процесс, риск их интраоперационной травмы, вероятность возникновения послеоперационного недержания мочи).
В качестве интерпретации данной классификации и ее клинического использования J.Goh приводит сле-дующе примеры. При свище типа 2ВI устья мочеточников могут находиться в непосредственной близости к краю свища, в связи с чем требуется их предварительная визуализация и стентирование. Пациентки со свищем типа 3АII имеют высокий риск послеоперационного недержания мочи в связи с вовлечением в патологический процесс области средней трети уретры, повреждение которой может приводить к инконтиненции [24].
Диагностика
Самопроизвольное подтекание мочи из половых путей, как проявление ПВС появляется в среднем через 7–12 дней после операции на органах малого таза, но может возникнуть и в более поздние сроки – до 6 недель после нее. После лучевой терапии форми рование свища происходит более длительно – от не скольких месяцев до нескольких лет [25].
Влагалищный осмотр в кресле,в большинстве случаев, позволяет визуализировать ПВС. При его вы полнении необходимо определить количество свище вых отверстий, их размер, локализацию, состояние краев свища, тканей, вовлеченных в патологический процесс, оценить глубину влагалища, его емкость и растяжимость. В свище и непосредственной близости к нему могут наблюдаться конкременты, шовный ма териал, фрагменты сетчатых имплантатов [26]. Диаг ностическую сложность при осмотре могут представ лять свищи после ранее выполненной экстирпации матки, в виду их небольшого диаметра, складчатости стенки влагалища, расположения в куполе влагалища в области рубца [27]. Важно обратить внимание на то что на ранней стадии формирования свища, его паль пация может быть неинформативна. При осмотре с по мощью зеркала слизистая влагалища, окружающая свищевое отверстие, может выглядеть как небольшая гиперемированная грануляционная область без види мого отверстия [25].
Типы ПВС относительно расстояния от наружного отверстия уретрыVVF types relative to the distance from the external urethral orifice
Размер ПВС VVF size
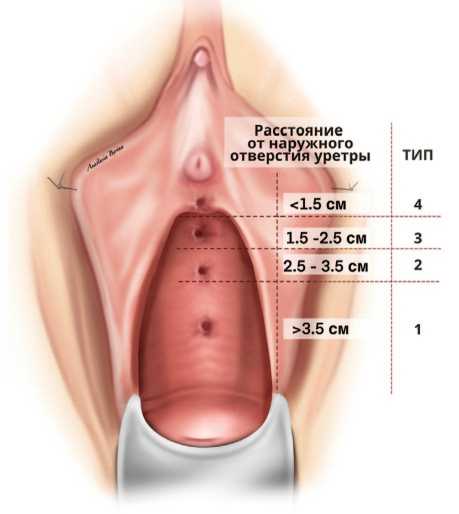
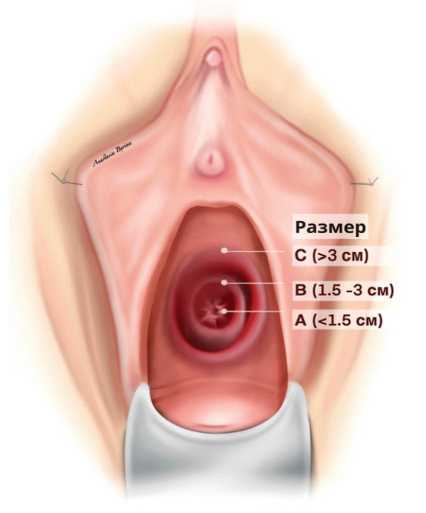
Осложняющие факторы, Complicated factors
-
I. Отсутствие или минимальный фиброз (вокруг свища/влагалища) и/или длина влагалища >6 см, нормальная емкость влагалища.
The absence of minimal fibrosis (around the fistula/vagina) and/or vaganal more less than 6 cm, normal capacity of vagina.
-
II. Умеренный или выраженный фиброз (вокруг свища/влагалища) и/или уменьшение длины/ёмкости влагалища.
Moderate or severe fibrosis (around the fistula/vagina) and/or decrease of vaginal lenth/capacity.
-
III. Особые случаи (постлучевые свищи, вовлечение мочеточников, рецидивные свищи).
Special cases (postradiation fistulas, ureters involvement, reccurent fistulas).
Рис. 5. Классификация ПВС по J. Goh
-
Fig. 5. J. Goh сlassification of VVF
Важным диагностическим методом является проба с красителями [28]. Мочевой пузырь через катетер заполняют раствором метиленового синего или индигокармина. Затем пациентку просят натужиться или покашлять. При этом может наблюдаться выделение раствора из свища. При отсутствии адекватной визуализации, а также сомнительных случаях, во влагалище вводят марлевые тампоны. Через 2 часа они удаляются. Синяя окраска тампона указывает на наличие ПВС и его локализацию. Дополнительный пероральный прием феназопиридина помогает при выявлении уретеро-влагалищных свищей. Оранжевый цвет на тампоне подтверждает присутствие свища. Обязательным условиям для установления диагноза является выполнение цистоскопического исследования. Оно позволяет подтвердить наличие и количество ПВС, оценить их размер, расположение относительно устьев мочеточников и внутреннего отверстия уретры [29].
При сложностях идентификации небольших свищей можно попробовать провести мочеточниковый катетер или струну-проводник через предполагаемый свищевой канал, для определения его точной локализации [22].
При больших свищевых отверстиях, с целью адек ватного заполнения полости мочевого пузыря, во вла галище раздувается баллон катетера Фолея [29].
При свищах, образовавшихся вследствие лучевой терапии, особенно при подозрении на рецидив новообразования, следует провести биопсию краев свища [22, 25].
Немаловажным в диагностике ПВС являются лучевые методы исследований, одним из которых яв ляется вагиноцистография – рентгенологическое иссле дование, позволяющее определить локализацию свища, емкость мочевого пузыря, вовлечение мочеточников и кишечника в патологический процесс [26].
При диагностике ПВС нужно обращать внимание на возможное вовлечение мочеточников в патологиче ский процесс. В 10% случаев ПВС сочетаются с моче точниково-влагалищными свищами [30]. В связи с этим,оценка состояния верхних мочевых путей яв ляется обязательной.
К методам, позволяющим оценить верхние моче выводящие пути, относят ультразвуковое исследование (УЗИ) почек, экскреторную урографию и компьютер ную томографию (КТ) урографию [26]. При подозрении на мочеточниковый свищ выполняется ретроградная уретеропиелография. В случае сложности визуализа ции устьев мочеточников выполняется хромоцистоско пия. Наличие мочеточникового свища также может быть подтверждено в сомнительных случаях с исполь зованием тампонов (методика описана выше).
Фистулография позволяет визуализировать сви щевой канал со сложным топографо-анатомическим расположением (например, при прохождении свища через полость абсцесса). Для этого используется моче точниковый катетер,через который в свищевой ход вводится рентгенконтрастный препарат [14, 29].
Традиционные рентгенографические методы дают ограниченную анатомическую и функциональную информацию (особенно при сложных, комбинированных формах свищей) и в настоящее время вместо них все чаще выполняют на КТ- и магнитно-резонансные томографические (МРТ)-контрастные исследования [31].
Такие методы как комбинированная одномоментная вагино-цистоскопия, трансвагинальная сонография с доплерографией,несмотря на свою диагностическую ценность, являются оператор-зависимыми и выполняются редко [32, 33].
Лечение
Катетеризация мочевого пузыря
Лечение ПВС при помощи длительного дренирования следует проводить только при небольших, доброкачественных, несформированных (не имеющих эпителизированного канала) ПВС [25].
На фоне длительного (от 2 до 8 недель) дренирования мочевого пузыря уретральным катетером с одновременным приемом антихолинергических препаратов, может наблюдаться самостоятельное закрытие свищевого отверстия. По данным P. Hilton, из 348 пациенток с мочеполовыми свищами, его спонтанное закрытие произошло у 24 (6,9%) из них после 6-8 недель дренирования мочевого пузыря уретральным катетером. Ни у одной пациентки с постлучевыми свищами не удалось достичь спонтанного его закрытия [2].
В исследовании K. Waaldijk из 1716 пациенток с акушерскими свищами, на фоне длительного дренирования мочевого пузыря самопроизвольное закрытие наблюдалось у 264 (15,4%) [34].
Применение коагуляционных методов
При небольших (менее 2-3 мм) сформированных свищах (т.е. при наличии эпителизированного свищевого канала), трансуретральная электрокоагуляция доступной слизистой свищевого канала, совместно с катетеризацией мочевого пузыря в течение 2–4 недель может привести к его закрытию.
В ретроспективных наблюдениях M. Stovsky и соавт. отметили эффективность данного метода у 11 из 15 женщин (73%) [35].
Об использовании гольмиевого лазера при лечении ПВС сообщили P.N. Dogra и соавт. Лечение было успешным у 7 из 8 пациенток с диаметром свища менее 3 мм при среднем сроке наблюдения 47 месяцев [36].
Обращают на себя внимание условия использования энергий. У пациентов с истонченной пузырно-влагалищной перегородкой, большим свищевым отверстием или выраженным воспалением вокруг свищевого канала коагуляция не только не даст положительного эффекта, но и может привести к увеличению диаметра свищевого канала [22].
Применение клеевых композиций
Первое описание успешного применения фибринового клея при лечении пузырно-влагалищных свищей было опубликовано в 1979 г. В результате введения клея в свищевой канал происходит ингибирование тромболизиса, что способствует миграции и агрегации фибробластов в заживляющую соединительную ткань [37]. Терапевтический эффект обеспечивается также за счет гелеобразной консистенции фибринового клея,кото-рая создает эффект «пробки», закрывающей свищевой канал до его заживления [38]. Фибриновый клей также может быть использован как материал для покрытия линии швов, с целью лучшего заживления тканей после фистулопластики.
L.A. Evans и соавт. описывают положительные результаты у 18 из 19 пациенток [39]. M.K. Shirvan и соавт. сообщили о полном закрытии свищей у 11 из 12 пациентов при использовании обогащенной тромбоцитами плазмы (PRP) и фибринового клея, вводимых в свищевой канал [40].
Также имеются данные о использовании цианакрилатного клея в качестве вспомогательного средства для заживления тканей [41]. Однако в связи c отсутствием в литературе рандомизированных исследований, оценивающих применение адгезивных материалов, их практическое использование остается ограниченным.
Хирургические методы
Учитывая низкую эффективность консервативных мероприятий,основным методом лечения больных с пузырно-влагалищными свищами является хирургический. Важно отметить, что эффективность операции по устранению свища напрямую зависит от соблюдения базовых принципов хирургии данной патологии (табл. 2) [42].
Таблица 2. Базовые принципы хирургического лечения ПВС Table 2: Basic principles of VVF surgical treatment
Базовые принципы хирургического лечения ПВС Basic principles of surgical VVF treatment
Соблюдение сроков выполнения хирургического вмешательства Compliance with surgical timelines
Адекватное дренирование мочевыводящих путей
Adequate urinary tract drainage
Профилактика и купирование инфекционных процессов
Treatment and prevention of infection
Достаточная диссекция тканей мочевого пузыря и влагалища вокруг свища
Sufficient dissection of bladder and vaginal tissues around the fistula
Удаление некротизированных тканей
Removal of necrotic tissues
Удаление инородных тел, синтетических материалов в области свища
Removal of foreign bodies, synthetic materials from the fistula area
Многослойное, герметичное ушивание дефекта без избыточного натяжения
Multiple-layer, watertight closure, tension-free sutures
Непересекающиеся линии швов
Non-overlapping suture lines
Использование рассасывающегося шовного материала
Use of absorbable suture material
Тщательный гемостаз
Hemostasis
При необходимости, использование васкуляризованных, здоровых тканевых лоскутов
If necessary, use vascularized, healthy tissue flaps
Время выполнения оперативного лечения
Сроки выполнения фистулопластки могут варьировать в зависимости от этиологического фактора свища, сроков его выявления, состояния окружающих тканей. В случае выявленного интраоперационного повреждения стенки мочевого пузыря незамедлительное ушивание дефекта, во всех случаях дает положительный результат [43].
При своевременной диагностике ятрогенные свищи могут быть прооперированы на ранней стадии (в пределах 72 часов) после операции до того, как исчезнут условия для немедленного закрытия дефекта [44].
При выявлении неосложненного ПВС в более поздние сроки,часть авторов придерживается безотлагательного хирургического вмешательства, однако чаще применяется отсроченное лечение [22, 34]. Наиболее подходящим временем закрытия свища является 8–12 недель после его образования [5, 30].
Для успешного выполнения операции, свищ должен быть сформирован, не иметь признаков активного воспаления, некроза и инкрустации [25].
При осложненных свищах, например, возникших после затрудненных родов, наиболее подходящим временем для оперативного лечения является срок 3-6 месяцев после его образования, а для лучевой терапии этот срок составляет 6–12 месяцев. Общий алгоритм диагностики и лечения ПВС представлен на рисунке 6 [45].
Выбор доступа
Выполнение фистулопластики возможно влагалищным и абдоминальным доступом. Следует отметить, что выбор доступа чаще всего основан на индивидуальных характеристиках свища и предпочтениях хирурга [46]. В связи с этим невозможно оценить их преимущества относительно друг друга. В настоящее время нет данных рандомизированных исследований, сравнивающих абдоминальный и влагалищный доступ [19].
По данным C. J. Hillary, в исследованиях, которые оценивали доступ, суммарно 6300/7676 (82%) операций были выполнены трансвагинально [19].
Независимо от того, является доступ влагалищным или абдоминальным, положительный результат (закрытие свища) достигается в среднем в 90,8% слу чаев (94,6% в высокоразвитых странах, 87,0% в развивающихся).
В тех исследованиях, где был указан хирургический доступ, показатель эффективности для влагалищной пластики свища составил 260/286 (90,9%) и 210/250 (84,0%) – для абдоминальной.
Опять же, следует подчеркнуть, что эти серии включают нерандомизированные когорты, поэтому прямое сравнение результатов является неправомерным [4].
В России, по данным Л.В. Тихоновой и соавт. эффективность хирургического лечения ПВС составила 84%, что в целом несколько ниже мировых данных,
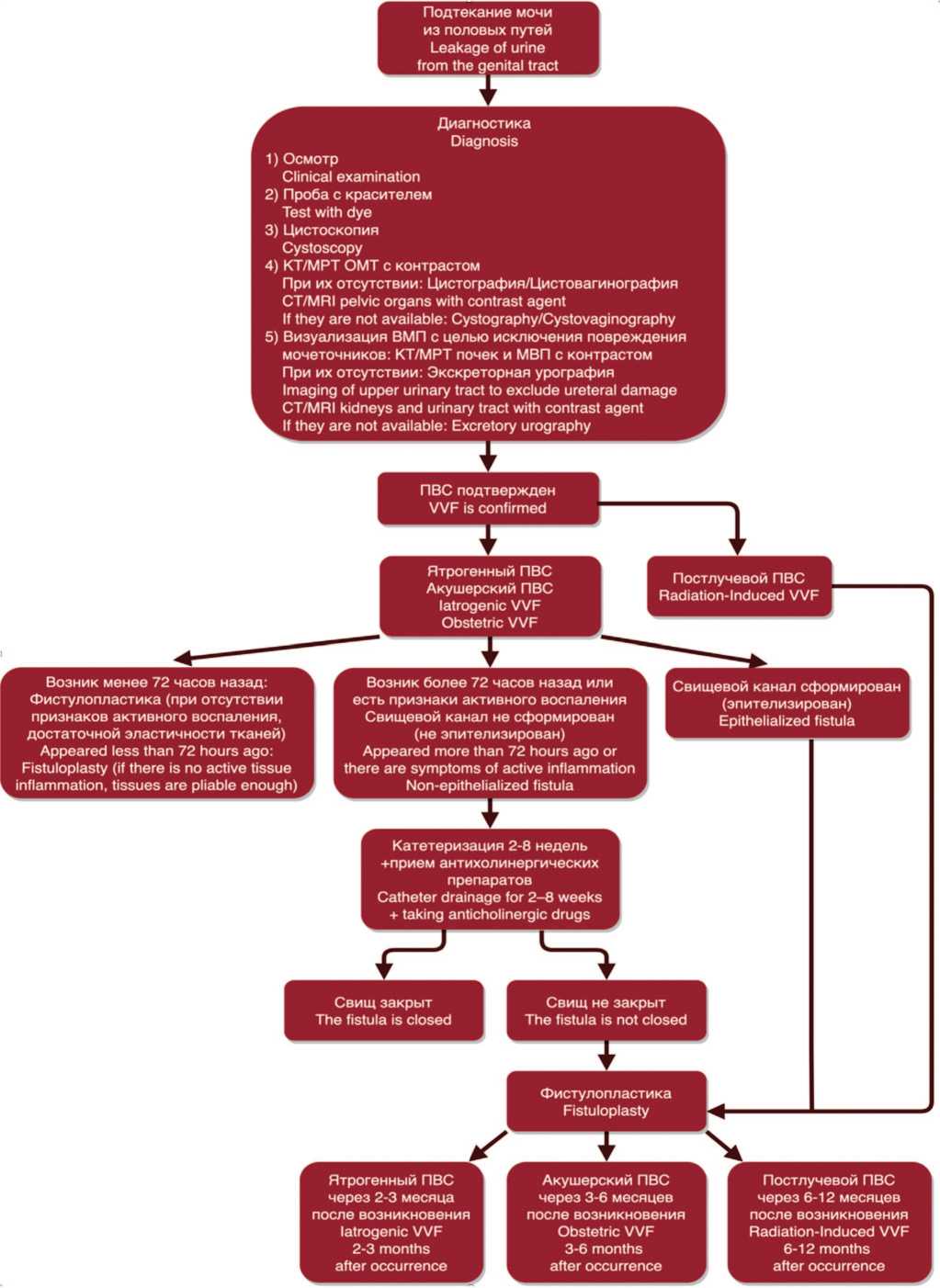
Рис. 6. Алгоритм диагностики и лечения ПВС
Fig. 6. Algorithm for the diagnosis and treatment of VVF
КТ, CT — компьютерная томография, computed tomography; МРТ, MRI — магнитно-резонансная томография, magnetic resonance imaging;
ОМТ — органы малого таза, pelvic organs; ВМП — верхние мочевыводящие пути, upper urinary tract;
МВП — мочевыводящие пути , urinary tract; ПВС, VVF — пузырно-влагалищный свищ, vesico-vaginal fistula.
приведенных в литературе. Однако при детальном рассмотрении этот факт легко объясняется тем, что в анализе почти 60% случаев составляют постлучевые свищи, лечение которых изначально более затруднительно и сопряжено с высоким процентом неуспеха [6].
Д. Ю. Пушкарь и соавт. описали самую большую серию постлучевых ПВС, включающую 210 пациенток, которым была выполнена фистулопластика влагалищ ным доступом. Положительный результат после пер вичной операции был достигнут у 48,1% (n=101) пациенток. Эффективность второй операции, выпол ненной у 98 пациенток, составила 39,8% (39/98). Третья операция была выполнена 42 пациенткам. Ее эффек тивность составила 52,4% (22/42); 19 пациенток пере несли более трех операций. Успешное закрытие свища было достигнуто в 35,0% (7/19). В совокупности у 169 пациенток из 210 свищ был закрыт (80,4%) [15].
Влагалищный доступ
Первая фистулопластика влагалищным доступом была описана в 1663 году H. Roonhuyse, который осве жил края свища и затем сблизил их заостренными ле бяжьими перьями.
Первую успешную пластику ПВС с использова нием техники H. Roonhuyse выполнил J. Fatio в 1675 году.
В 1838 году, используя свинцовые швы, J.P. Met tauer стал первым хирургом в США, заявившим об ус пешном закрытии ПВС.
В 1852 году J. Sims описал метод, который заклю чался в освежении краев свища трансвагинальным до ступом и его ушивании с использованием серебряной нити. Однако в серии своих операций он добился успеха только с 30-й попытки.
В 1854 году G.Simon описал метод кольпоклейзиса при лечении ПВС, популяризованного W. Latzko в 1942 году.
В 1861 году M. Collis предложил метод расщепления (расслоения), при котором после освежения краев свища,выполняется отделение стенки влагалища от мочевого пузыря и их раздельное ушивание [42].
Влагалищный доступ имеет ряд преимуществ перед абдоминальным: меньший болевой синдром, снижение кровопотери, сокращение продолжительности операции и длительности пребывания в стационаре [47].
Однако он может быть выполнен только при условии отсутствия вовлечения устьев мочеточников в патологический процесс [14].
-
A. Geik и соавт., сравнив методы хирургического доступа у 53 женщин с ПВС диаметром от 15 до 20мм, сообщили, что положительные результаты операций, выполненных влагалищным доступом, практически не отличались от операций,выполненных абдоминальным доступом: 100% (25/25) против 96,4% (27/28), но продолжительность пребывания в стационаре и частота осложнений были ниже в первом случае [48].
Методика операции показана на рисунке 7. После визуализации фистулы, для удобства экспозиции, в ее канал устанавливается зонд или тонкий катетер Фолея. Далее выполняется циркулярный разрез парасвищевых тканей. Его возможно дополнить U-образным разрезом
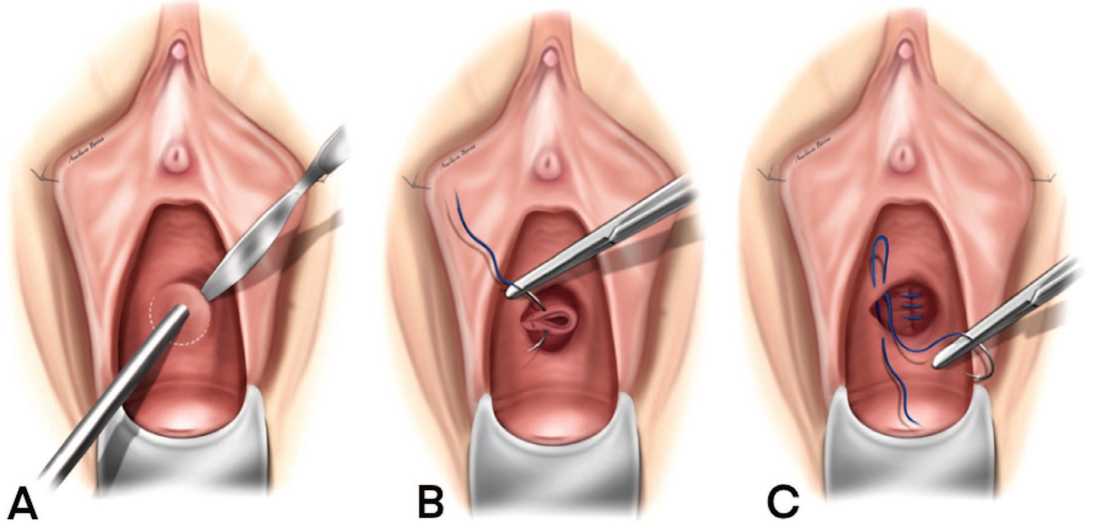
Рис. 7. Пластика пузырно-влагалищного свища влагалищным доступом
(A) В свищевой канал установлен зонд для удобства экспозиции; циркулярный разрез парасвищевых тканей. (B) Выполнена диссекция окружающих тканей; свищевой канал иссечен; первый ряд швов на ткани мочевого пузыря. (C) Второй ряд швов на перивезикальную фасцию; третий ряд швов на ткани передней стенки влагалища.
Fig. 7. Transvaginal repair of vesicovaginal fistula
A) Surgical probe in the fistula providing retraction; circular incision of the parafistula tissues. (B) Dissection of the surrounding tissues was performed; the fistula canal is excised; the first layer of sutures to the bladder tissues. (C) The second layer of sutures to the perivesical fascia; third layer of sutures to the tissue of the anterior vaginal wall.
передней стенки влагалища с формированием лоскута, позволяющим избежать избыточного натяжения тканей при их сопоставлении и пересечения линий накладываемых швов [42]. После чего, тупым и острым способом выполняется широкая мобилизация тканей влагалища и мочевого пузыря с иссечением краев свища в пределах здоровых тканей, или без иссечения (метод Füth). Ушивание дефекта производится трехрядно (дефект мочевого пузыря, перивезикальная фасция, рана передней стенки влагалища), рассасывающейся нитью Викрил 2/0, 3/0, без натяжения [29, 49].
В единственном рандомизированном исследова нии, сравнивающим результаты фистулопластик без иссечения и с иссечением свищевого канала,не было отмечено разницы эффективности того или иного ме тода. Однако у пациенток с послеоперационным реци дивом ПВС, диаметр свищевого отверстия становился больше исходного в группе, где производилось иссече ние свищевого канала [50].
Также необходимо отметить, что при иссечении свищевого канала желательно не использовать активно методы электрохирургического гемостаза, так как это может привести к некрозу коагулированных тканей, препятствующему их адекватному заживлению [51].
При топографической близости фистулы к устьям мочеточников, для профилактики их травмы, выпол няется интраоперационная установка мочеточниковых стентов [29].
У пациенток с постгистерэктомическими ПВС, альтернативным методом является фистулопластика по Латцко. Она подразумевает частичный кольпоклейзис. Производится широкое элипсовидное иссечение и мо билизация тканей влагалища вокруг свища, без во влечения тканей мочевого пузыря. Далее выполняется ушивание свищевого отверстия в несколько слоев, и облитерирующее сшивание передней и задней стенок влагалища [46].
Показатели успешного закрытия свищей с исполь зованием данного метода составляют от 89% до 100% [44].
При свищах большого диаметра и/или изменен ных лучевой терапией ригидных тканях, сопоставить края дефекта обычными швами обычно не представ ляется возможным. В таких случаях используются раз личные тканевые лоскуты,компенсирующие дефицит тканей [52].
Использование васкуляризованной жировой ткани большой половой губы и поверхностных мышц урогени тальной диафрагмы (луковично-губчатой и седалищно пещеристой) в качестве лоскута, было описано Martius в 1928 году. Позже метод был многократно модифициро ван, и в настоящее время выполняется без мышечной ткани [53] (рис. 8).
В обзоре S. Malde и соавт. успешное закрытие свища зарегистрировано у 95% из 43 пациенток, кото рым была проведена данная операция [54].
В 1993 г. S. Raz и соавт. предложили использовать в качестве лоскута брюшину. В серии из 11 пациентов эффективность операции составила 82% [55].
K.S. Eilber и соавт. за 10-летний период выпол нили 83 операции с использованием перитонеального лоскута. Метод оказался эффективным в 96% случаев (80/83) [51].
В качестве интерпозиционного лоскута также возможно использование тонкой мышцы бедра (m. gracilis). О первом опыте использования данного ме тода в 1928 году сообщил J.H. Garlock [56]. Описаны модификации перемещения данного лоскута:через за
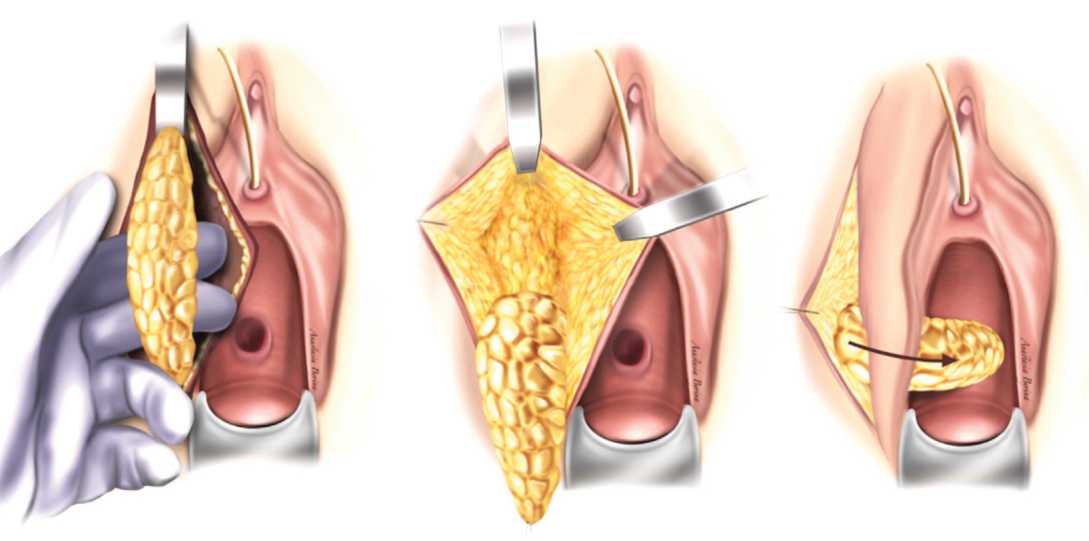
Рис. 8. Пластика пузырно-влагалищного свища с использованием васкуляризованного лоскута из жировой ткани большой половой губы (по Martius) Fig. 8. Plasty of the vesicovaginal fistula using a vascularized fatty tissue flap of the labia majora (according to Martius)
пирательную мембрану, и, ставшее ныне стандартным, подкожное проведение [57, 58].
По данным D. Bolbandi и соавт., свищ удалось закрыть у 13 из 14 пациенток, прооперированных данным способом [59].
Также описывают успешное использование лоскута портняжной мышцы (m. sartorius) и ягодичного кожного лоскута [29, 60].
Важно обратить внимание на то, что трансвагинальные методы выполнения фистулопластик,в виду своей эффективности и универсальности, должны быть в арсенале каждого хирурга, занимающегося лечением ПВС.
Абдоминальный доступ
О первой успешной фистулопластике абдоминальным (чреспузырным) доступом сообщил в 1888 г. F. Trendelenburg. Во время операции он выполнил чреспузырное освежение краев свища и его и ушивание с установкой цистостомического дренажа в конце операции.
-
V. O'Conor и J. Sokol популяризировали абдоминальный доступ благодаря своей методике,которая заключается в продольном рассечении мочевого пузыря до свища, иссечении свищевого канала в пределах здоровых тканей, широкой диссекции тканей мочевого пузыря от влагалища и их раздельным ушиванием (рис. 9) [42].
Показания к абдоминальному доступу
-
• вовлечение мочеточников в патологический процесс или наличие мочеточниково-влагалищного свища;
-
• сочетание ПВС с пузырно-кишечными свищами;
-
• необходимость выполнения кишечной пластики мочевого пузыря;
-
• невозможность выполнения фистулопластики из влагалищного доступа (например, при узком вла галище, которое не позволяет получить доступ к де фекту) [49].
Лапароскопические/роботизированные операции
Малоинвазивные методики, совершив револю цию в урологии, не обошли стороной и хирургию сви щей.
С 1994 г. для закрытия ПВС применяется лапаро скопический доступ, а в 2005 году впервые была вы полнена роботизированная пластика ПВС [61, 62].
Фистулопластики при данных доступах могут осуществляться как чреспузырно, так и внепузырно. В мета-анализе J.R. Miklos и соавт. был проведен обзор 44 работ (опубликованных в период с января 1994 г. по март 2014 г.), в которых оценивались как лапаро скопические,так и роботизированные операции по закрытию ПВС.Эффективность хирургического за крытия свищей составляла от 80 до 100% с периодом наблюдения от 1 до 74 месяцев. Эффективность чрес пузырных и внепузырных методик оценена 95,89% и 98,04%, соответственно [63].
Показания к лапароскопическому/роботизиро ванному методу аналогичны открытым операциям. В сравнении с традиционной «открытой» операцией,ла пароскопичсекие методы улучшают визуализацию операционного поля,обеспечивают более прецизион ный гемостаз,уменьшают хирургическую травму и послеоперационный болевой синдром,а также дли тельность пребывания в стационаре и период реаби литации [62, 63].
В работе B. Ghosh и соавт. сравнили 2 группы па циенток, перенесших лапароскопическую и открытую фистулопластику при диаметре свищей менее 3 см, и обнаружили меньшие кровопотерю,количество дней
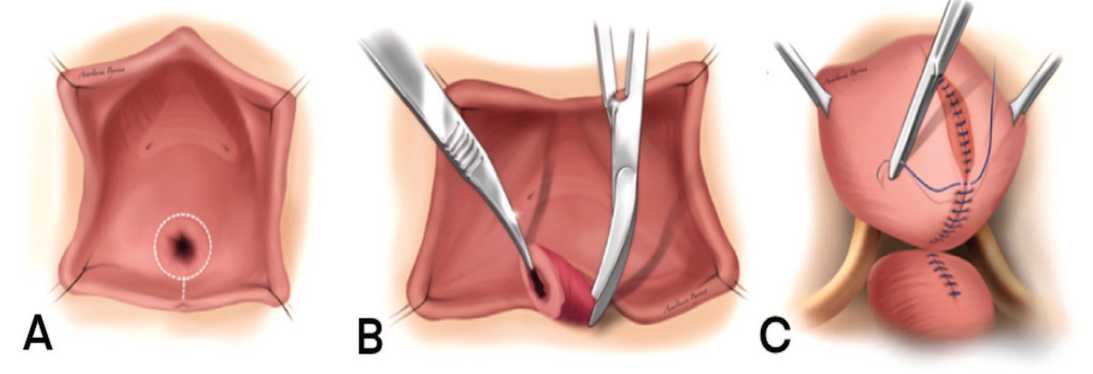
Рис. 9. Пластика пузырно-влагалищного свища абдоминальным доступом
(А) Продольное рассечение мочевого пузыря до свища.
(В) Иссечение свищевого канала в пределах здоровых тканей; диссекция тканей мочевого пузыря от влагалища.
(С) Раздельное ушивание раны мочевого пузыря и влагалища.
Fig. 9. Plasty of the vesicovaginal fistula by abdominal access
(A) Longitudinal dissection of the bladder to the fistula.
(B) Excision of the fistula canal within healthy tissue; dissection of the bladder tissue from the vagina.
(C) Separate suturing of the bladder and vaginal wound.
пребывания в стационаре и потребность в анальгетиках, а также более быстрое удаление катетера Фолея (11,5 дней против 27 дней) в группе пациентов, перенесших лапароскопическую фистулопластику [64].
К плюсам абдоминального доступа следует отнести оптимальные условия для перемещения сальника между стенкой мочевого пузыря и влагалища, что имеет важное значение для успешного выполнения фи-стулопластики [52].
В 1937 г. W. Walters впервые использовал большой сальник при закрытии пузырно-влагалищного свища [65]. Широкое распространение метод получил благодаря I. Kiricuta, который описал все плюсы оментопла-стики [66].
D.H. Evans и соавт. провели ретроспективный анализ 37 пациенток с ПВС, которым в одном учреждении была выполнена фистулопластика абдоминальным доступом. У 29 пациенток с ПВС не связанными с онкологическим процессом и его лечением 10 из 10 операций (100%) были успешными при использовании сальникового лоскута по сравнению с 12 из 19 операций (63%), когда он не использовался. У восьми пациенток с ПВС,образовавшимися в следствие лечения онкологического процесса репродуктивных органов,в 2 случая (100%) свищи были успешно закрыты с использованием сальникового лоскута. Среди остальных шести пациенток,оперированных без сальникового лоскута, закрытия свища удалось добиться только у четверых [67].
При невозможности использования большого сальника, в качестве лоскута можно использовать брюшину, миофасциальный лоскут прямой мышцы живота или перисигмоидной жировой ткани [52].
J. Hadzi-Djokic и соавт. в качестве интерпозицион- ной ткани у 2 пациенток использовали буккальный лоскут с положительным результатом [68].
A. Abou-Elela и соавт. использовали ротационный лоскут мочевого пузыря и гемостатическую матрицу FloSeal для закрытия ПВС абдоминальным доступом у 20 пациенток, и продемонстрировали 100% эффектив ность при длительном наблюдении [69].
Несмотря на наличие альтернативных вариантов, ни один из них не обладает такими уникальными ре генеративными свойствами как большой сальник [52].
Снижение емкости мочевого пузыря менее 100 мл и его растяжимости (комплаентности), обширные де фекты мочевого пузыря с вовлечением мочепузырного треугольника, устьев мочеточников, шейки мочевого пузыря являются показанием для выполнения аугмен тационной цистопластики, формирования ортотопи ческого мочевого пузыря из сегмента подвздошной кишки (операция Studer, Hautmann, Camey, HemiKock) или суправезикальной деривации мочи с фор мированием илеокондуита по Bricker [14, 70].
ВЫВОДЫ
При всем многообразии методов лечения ПВС, идеального способа, к сожалению, до сих пор не суще ствует. Это связано с большим вариативным разнооб разием ПВС,отсутствием единых подходов к лечению данной патологии и недостаточным количеством ис следований,позволяющих сравнить те или иные ме тоды хирургического лечения.
Проведение рандомизированных исследований, а также совершенствование методов диагностики и воз можных хирургических пособий должны улучшить уровень оказываемой помощи таким пациенткам.
ЛИТЕ РАТУ РА/RE FERENCE S
Список литературы Пузырно-влагалищные свищи: современные концепции диагностики и лечения
- Frajzyngier V, Ruminjo J, Barone MA. Factors influencing urinary fistula repair outcomes in developing countries: a systematic review. Am J Obstet Gynecol 2012;207(4):248-58. https://doi.org/10.1016/j.ajog.2012.02.006.
- Hilton P. Urogenital fistula in the UK: a personal case series managed over 25 years. BJUInt 2012;110(1):102-10. https://doi.org/10.1111/j.1464-410X.2011.10630.x.
- Wall LL. Obstetric vesicovaginal fistula as an international public-health problem. Lancet 2006;368(9542):1201-9. https://doi.org/10.1016/S0140-6736(06)69476-2.
- Hillary CJ, Osman NI, Hilton P, Chapple CR. The aetiology, treatment, and outcome of urogenital fistulae managed in well- and low-resourced countries: a systematic review. Eur Urol 2016;70(3):478-92. https://doi.org/10.1016/j.eururo.2016.02.015.
- Malik MA, Sohail M, Malik MT, Khalid N, Akram A. Changing trends in the etiology and management of vesicovaginal fistula. Int J Urol 2018;25(1):25-9. https://doi.org/10.1111/iju.13419.
- Тихонова Л.В., Касян Г.Р., Пушкарь Д.Ю., Григорьев Н.А. Систематический обзор современное русскоязычное литературы по урогенитальным свищам у женщин. Урология 2020(6):137-141.. [Tikhonova L.V., Kasyan G.R., Pushkar D.Yu., Grigoriev N.A. A systematic review of modern Russian-language literature on urogenital fistulas in women. Urologiya=Urology 2020(6):137-141. (In Russian)]. https://dx.doi.org/10.18565/urology.2020.6.137-141.
- Garthwaite M, Harris N. Vesicovaginal fistulae. Indian J Urol 2010;26(2):253-6. https://doi.org/10.4103/0970-1591.65400.
- Arrowsmith SD. Genitourinary reconstruction in obstetric fistulas. J Urol 1994;152(2 Pt 1):403-6. https://doi.org/10.1016/s0022-5347(17)32749-0.
- Neilson JP, Lavender T, Quenby S, Wray S. Obstructed labour. Br Med Bull 2003(67):191-204. https://doi.org/10.1093/bmb/ldg018.
- De Brouwere V, Dubourg D, Richard F, Van Lerberghe W. Need for caesarean sections in west Africa. Lancet 2002;359(9310):974-975. https://doi.org/10.1016/s0140-6736(02)07993-x.
- Wall LL, Arrowsmith SD, Briggs ND, Browning A, Lassey A. The obstetric vesicovaginal fistula in the developing world. Obstet Gynecol Surv 2005;60(7 Suppl 1):S3-S51. https://doi.org/10.1097/00006254-200507001-00002.
- Gungorduk K, Asicioglu O, Celikkol O, Sudolmus S, Ark C. Iatrogenic bladder injuries during caesarean delivery: a case control study. J Obstet Gynaecol 2010;30(7):667-70. https://doi.org/10.3109/01443615.2010.486086.
- Hilton P, Cromwell DA. The risk of vesicovaginal and urethrovaginal fistula after hysterectomy performed in the English National Health Service — a retrospective cohort study examining patterns of care between 2000 and 2008. BJOG 2012;119(12):1447-54. https://doi.org/10.1111/j.1471-0528.2012.03474.x.
- Кан Д.В. Руководство по акушерской и гинекологической урологии. М.: Медицина, 1986; 488 с. [Kan D.V. Guide to obstetric and gynecological urology. M.: Meditsina, 1986; 488 p. (in Russian)].
- Pushkar DY, Dyakov VV, Kasyan GR. Management of radiation-induced vesicovaginal fistula. Eur Urol 2009;55(1):131-7. https://doi.org/10.1016/j.eururo.2008.04.044.
- Maier U, Ehrenböck PM, Hofbauer J. Late urological complications and malignancies after curative radiotherapy for gynecological carcinomas: a retrospective analysis of 10,709 patients. J Urol 1997;158(3 Pt 1):814-7. https://doi.org/10.1097/00005392-199709000-00033.
- Berthrong M. Pathologic changes secondary to radiation. World J Surg 1986;10(2):155-70. https://doi.org/10.1007/BF01658133.
- Руководство по урологии. Под ред. Н.А. Лопаткина. М.: Медицина, 1998(3):672 с. [Urology manual. Ed. N.A. Lopatkin. M.: Meditsina, 1998(3):672 p. (in Russian)].
- Hillary CJ, Chapple CR. The choice of surgical approach in the treatment of vesico-vaginal fistulae. Asian J Urol 2018;5(3):155-9. https://doi.org/10.1016/ j.ajur.2018.01.002.
- Penalver M, Angioli R. Urinary diversion. Chapter 11. In: Glenn HW, editor. Urogynecologic surgery, 2nd edn. Philadelphia: Lippincott Williams & Wilkins, 2000;193-206 р.
- Capes T, Stanford EJ, Romanzi L, Foma Y, Moshier E. Comparison of two classification systems for vesicovaginal fistula. Int Urogynecol J 2012;23(12):1679-85. https://doi.org/10.1007/s00192-012-1671-9.
- Stamatakos M, Sargedi C, Stasinou T, Kontzoglou K. Vesicovaginal fistula: diagnosis and management. Indian J Surg 2014;76(2):131-6. https://doi.org/10.1007/ s12262-012-0787-y.
- Angioli R, Penalver M, Muzii L, Mendez L, Mirhashemi R, Bellati F, , et al. Guidelines of how to manage vesicovaginal fistula. Crit Rev Oncol Hematol 2003;48(3):295-304. https://doi.org/10.1016/s1040-8428(03)00123-9.
- Goh JT. A new classification for female genital tract fistula. Aust N Z J Obstet Gynaecol. 2004;44(6):502-504. https://doi.org/10.1111/j.1479-828X.2004.00315.x
- Ghoniem GM, Warda HA. The management of genitourinary fistula in the third millennium. Arab J Urol 2014;12(2):97-105. https://doi.org/10.1016/j.aju.2013.11.006.
- Елисеев Д.Э., Алексеев Б.Я., Качмазов А.А., Гурбанов Ш.Ш., Огай Д.С., Холодова Ж.Л., Абакумов Р.С., Черникова Е.Н. Оптимизация диагностики мочеполовых и кишечно-влагалищных свищей. Экспериментальная и клиническая урология 2017(4):82-90. [Eliseev D.E., Alekseev B.Y., Kachmazov A.A., Gurbanov S.S., Ogay D.S., Kholodova J.L., Abakumov R.S., Chernikova E.N. Optimization of diagnostics of urogenital and intestine-vaginal fistulas. Eksperimentalnaya i klinicheskaya urologiya = Experimental and clinical urology 2017(4):82-90. (In Russian)].
- Matthew P. Rutman, Larissa V. Rodrigues, Raz S. Vesicovaginal fistula: vaginal approach. In: Raz S., Rodriguez LV, editors. Female urology, 3rd ed. Philadelphia: Elsevier Saunders 2008;794-801 р.
- Moir JC. Personal experiences in the treatment of vesicovaginal fistulas. Am J Obstet Gynecol 1956;71(3):476-91. https://doi.org/10.1016/0002-9378(56)90476-8.
- Пушкарь Д.Ю., Касян Г.Р. Ошибки и осложнения в урогинекологии. М.: ГЭО-ТАР-Медиа, 2017;384 с. [Pushkar D.Yu., Kasyan G.R. Errors and complications in urogynecology. M.:GEOTAR-Media, 2017;384 p. (in Russian)].
- El-Azab AS, Abolella HA, Farouk M. Update on vesicovaginal fistula: a systematic review. Arab J Urol 2019;17(1):61-8. https://doi.org/10.1080/2090598X.2019.1590033.
- Tonolini M. Elucidating vaginal fistulas on CT and MRI. Insights I maging 2019;10(1):123. https://doi.org/10.1186/s13244-019-0812-9.
- Andreoni C, Bruschini H, Truzzi JC, Simonetti R, Srougi M. Combined vaginoscopy-cystoscopy: a novel simultaneous approach improving vesicovaginal fistula evaluation. J Urol 2003;170(6 Pt 1):2330-2. https://doi.org/10.1097/01. ju.0000096343.03276.75.
- Volkmer BG, Kuefer R, Nesslauer T, Loeffler M, Gottfried HW. Colour Doppler ultrasound in vesicovaginal fistulas. Ultrasound Med Biol 2000;26(5):771-5. https://doi.org/10.1016/s0301-5629(00)00210-6.
- Waaldijk K. The immediate management of fresh obstetric fistulas. Am J Obstet Gynecol 2004;191(3):795-9. https://doi.org/10.1016Zj.ajog.2004.02.020.
- Stovsky MD, Ignatoff JM, Blum MD, Nanninga JB, O'Conor VJ, Kursh ED. Use of electrocoagulation in the treatment of vesicovaginal fistulas. J Urol 1994;152(5 Pt 1):1443-4. https://doi.org/.1016/s0022-5347(17)32441-2.
- Dogra PN, Saini AK. Laser welding of vesicovaginal fistula — outcome analysis and long-term outcome: single-centre experience. Int Urogynecol J 2011;22(8):981-4. https://doi.org/10.1007/s00192-011-1389-0.
- Pettersson S, Hedelin H, Jansson I, Teger-Nilsson AC. Fibrin occlusion of a vesicovaginal fistula. Lancet 1979;1(8122):933. https://doi.org/10.1016/ s0140-6736(79)91422-3.
- Kumar U, Albala DM. Fibrin glue applications in urology. Curr Urol Rep 2001;2(1):79-82. https://doi.org/10.1007/s11934-001-0029-5.
- Evans LA, Ferguson KH, Foley JP, Rozanski TA, Morey AF. Fibrin sealant for the management of genitourinary injuries, fistulas and surgical complications. J Urol 2003;169(4):1360-2. https://doi.org/10.1097/01.ju.0000052663.84060.ea.
- Shirvan MK, Alamdari DH, Ghoreifi A. A novel method for iatrogenic vesicovagi-nal fistula treatment: autologous platelet rich plasma injection and platelet rich fibrin glue interposition. J Urol 2013;189(6):2125-9. https://doi.org/10.1016/ j.juro.2012.12.064.
- Muto G, D'Urso L, Castelli E, Formiconi A, Bardari F. Cyanoacrylic glue: a minimally invasive nonsurgical first line approach for the treatment of some urinary fistulas. J Urol 2005;174(6):2239-43. doi:10.1097/01.ju.0000181809.51544.20.
- Gopal H. Badlani, Dirk J.M.K. De Ridder, Jayadev Reddy Mettu and Eric S. Rovner. Urinary tract fistulae. In: Alan Partin, Craig Peters, Louis Kavoussi, Roger Dmo-chowski, Alan Wein, editors. Campbell Walsh Wein Urology, 12th ed. Philadelphia: Elsevier, 2020; eBook. XIII/129.
- Satitniramai S, Manonai J. Urologic injuries during gynecologic surgery, a 10-year review. J Obstet Gynaecol Res 2017;43(3):557-63. https://doi.org/10.1111/jog.13238.
- Walters MD, Karram MM. Urogynecology and reconstructive pelvic surgery. 3rd ed. Philadelphia: Elsevier Mosby, 2007;616 р.
- Rovner ES. Urinary tract fistulae. In: AJ Wein, editor-in-chief, LR Kavoussi, AC Novick, AW Partin, CA Peters, editors. Campbell-Walsh Urology. 10th ed. Philadelphia: Elsevier Saunders, 2012;2222-52 р.
- Latzko W. Postoperative vesicovaginal fistulas: genesis and therapy. Am J Surg 1942;58(2):211-28. https://doi.org/10.1016/s0002-9610(42)90009-6.
- Theofanides MC, Sui W, Sebesta EM, Onyeji I, Matulay JT, Chung DE. Vesicovaginal fistulas in the developed world: an analysis of disease characteristics, treatments, and complications of surgical repair using the ACS-NSQIP database. Neurourol Urodyn 2017;36(6):1622-8. https://doi.org/10.1002/nau.23167.
- Gedik A, Deliktas H, Celik N, Kayan D, Bircan MK. Which surgical technique should be preferred to repair benign, primary vesicovaginal fistulas? Urol J 2015;12(6):2422-7.
- Лоран О. Б., Пушкарь Д. Ю., Касян Г. Р. Урогенитальные свищи. Методические рекомендации №15. М.: АБВ-пресс, 2019;32 с. [Loran O.B., Pushkar D.Yu., Kasyan G.R. Urogenital fistulas. Methodological recommendations № 15. M.:ABV-press, 2019;32 p. (in Russian)].
- Shaker H, Saafan A, Yassin M, Idrissa A, Mourad MS. Obstetric vesico-vaginal fistula repair: should we trim the fistula edges? A randomized prospective study. Neu-rourol Urodyn 2011;30(3):302-5. https://doi.org/10.1002/nau.20995.
- Eilber KS, Kavaler E, Rodriguez LV, Rosenblum N, Raz S. Ten-year experience with transvaginal vesicovaginal fistula repair using tissue interposition. J Urol 2003;169(3):1033-6. https://doi.org/10.1097/01.ju.0000049723.57485.e7.
- Cohen BL, Gousse AE. Current techniques for vesicovaginal fistula repair: surgical pearls to optimize cure rate. Curr Urol Rep 2007;8(5):413-8. https://doi.org/10.1007/s11934-007-0040-6.
- Sajjadi SG, Hortvath OP, Kalmar K. Martius flap: historical and anatomical considerations. Eur J Plast Surg 2012;35(10):711-6. https://doi.org/10.1007/ s00238-012-0742-y.
- Malde S, Spilotros M, Wilson A, Pakzad M, Hamid R, Ockrim J, et al. The uses and outcomes of the Martius fat pad in female urology. World J Urol 2017;35(3):473-8. https://doi.org/10.1007/s00345-016-1887-2.
- Raz S, Bregg KJ, Nitti VW, Sussman E. Transvaginal repair of vesicovaginal fistula using a peritoneal flap. J Urol 1993;150(1):56-9. https://doi.org/10.1016/ s0022-5347(17)35396-x.
- Garlock JH.The cure of an intractable vesicovaginal fistula by use of a pedicled muscle graft. Surg Gynecol Obstet 1928(47):255-60.
- Ingelman-Sundberg A. Pathogenesias and operative treatment of urinary fistulas in irradiated tissue. In: Youssef AF, editor. Gynecological urology. Springfield, III: Charles C Thomas, 1960;263-279 p.
- Hamlin RH, Nicholson EC. Reconstruction of urethra totally destroyed in labour. Br Med J 1969;2(5650):147-50. https://doi.org/10.1136/bmj.2.5650.147.
- Bolbandi D, Raghuveer, Agarwal M. Role of gracilis muscle transfer in complex vesico vaginal fistula. Indian J Applied Research 2016;6(8):10-1.
- Byron RL Jr, Ostergard DR. Sartorius muscle interposition for the treatment of the radiation-induced vaginal fistula. Am J Obstet Gynecol 1969;104(1):104-7. https://doi.org/10.1016/s0002-9378(16)34147-3.
- Nezhat CH, Nezhat F, Nezhat C, Rottenberg H. Laparoscopic repair of a vesicovaginal fistula: a case report. Obstet Gynecol 1994;83(5 Pt 2):899-901.
- Melamud O, Eichel L, Turbow B, Shanberg A. Laparoscopic vesicovaginal fistula repair with robotic reconstruction. Urology 2005;65(1):163-6. https://doi.org/10.1016/j.urology.2004.09.052.
- Miklos JR, Moore RD, Chinthakanan O. Laparoscopic and robotic-assisted vesicovaginal fistula repair: a systematic review of the literature. J Minim Invasive Gynecol 2015;22(5):727-36. https://doi.org/10.1016/j.jmig.2015.03.001.
- Ghosh B, Wats V, Pal DK. Comparative analysis of outcome between laparoscopic versus open surgical repair for vesico-vaginal fistula. Obstet Gynecol Sci 2016;59(6):525-9. https://doi.org/10.5468/ogs.2016.59.6.525.
- Walters W. An omental flap in transperitoneal repair of recurring vesicovaginal fistulas. Surg Gynecol Obstet 1937(64):74-5.
- Kiricuta I, Berariu T. The simplified technic of treatment by omentoplasty of irradiated and injured large vesico-vaginal fistulas. Apropos of 130 surgical cases. J Urol (Paris) 1988;94(4):205-9.
- Evans DH, Madjar S, Politano VA, Bejany DE, Lynne CM, Gousse AE. Interposition flaps in transabdominal vesicovaginal fistula repairs: are they really necessary? Urology 2001;57(4):670-4. https://doi.org/10.1016/s0090-4295(01)00933-5.
- Hadzi-Djokic J, Pejcic T, Stamenkovic V, Petrovic M, Acimovic M. Buccal mucosal graft interposition in the treatment of recurrent vesicovaginal fistula: a report on two cases. Taiwan J Obstet Gynecol 2015;54(6):773-5. https://doi.org/10.1016/ j.tjog.2015.10.008.
- Abou-Elela A, Alfaiomy H, Torky H, Reyad E, Azazy S. The use of rotational bladder flap and hemostatic matrix sealant (FloSeal): a modified transabdominal approach to repair supratrigonal and complex vesicovaginal fistula. Surg Technol Int 2012(22):44-8.
- Лоран О.Б., Серегин А.В., Довлатов З.А. Современные подходы к лечению постлучевых урогенитальных свищей у женщин: обзор литературы. Экспериментальная и клиническая урология 2015(4):42-45. [Loran O.B., Seregin A.V., Dovlatov Z.A. Modern approach to therapy of the postradiation urogenital fistula in female patients: literature review. Eksperimentalnaya i klinicheskaya urologiya=Exper-imental and clinical urology 2015(4):42-45. (in Russian)].


