Радиочастотная импульсная абляция спинальных ганглиев в лечении послеоперационного корешкового болевого синдрома
Автор: Волков Иван Викторови, Карабаев Игорь Шамансурович, Пташников Дмитрий Александрович, Коновалов Николай Александрович, Поярков Константин Александрович
Журнал: Гений ортопедии @geniy-ortopedii
Статья в выпуске: 3, 2018 года.
Бесплатный доступ
Актуальность. Частота встречаемости корешкового болевого синдрома без хирургически значимого субстрата компрессии составляет 4,8-10,2 % в структуре «синдрома неудачных операций» на позвоночнике. Импульсная радиочастотная абляция (ИРЧА) с успехом применяется для лечения некоторых видов нейропатического болевого синдрома, возможности применения в случаях постоперационной радикулопатии изучены недостаточно. Цель. Оценить возможности использования ИРЧА в сочетании с эпидуральной блокадой (ЭБ) для лечения корешкового болевого синдрома после оперативных вмешательств по поводу дегенеративно-дистрофических заболеваний пояснично-крестцового отдела позвоночника. Материалы и методы. Выполнено проспективное нерандомизированное открытое исследование. Включено 56 пациентов с послеоперационным корешковым болевым синдромом. 22 пациентам основной группы (ОГ) выполнялась ИРЧА спинальных ганглиев в сочетании с ЭБ, 34 пациентам контрольной группы (КГ) - только трансфораминальная ЭБ. Положительным результатом считалось снижение болевого синдрома по цифровой шкале (NRS-11) на 50 % или на 4 балла и/или снижение индекса Освестри (ODI) на 20 %, и/или снижение индекса беспокойства радикулопатии (SBI) на 8 баллов от исходных значений с сохранением эффекта в течение 6 и более месяцев. Оценивалась и сравнивалась динамика снижения исследуемых показателей, проводился поиск значимых прогностических факторов. Результаты. Положительные результаты вмешательств получены у 18 пациентов (81,82 %) ОГ и 19 пациентов (55,88 %) КГ, p = 0,045. Произошло достоверное снижение всех индексов, снижение SBI в ОГ было достоверно ниже, чем в контрольной, p = 0,021. Значимых осложнений и побочных эффектов не было. Наличие аллодинии/гиперпатии было основным негативным прогностическим фактором в ОГ и КГ с отношением шансов 0,79 при 95 % доверительном интервале (0,735-0,897) и 0,82 (0,780-0,929) соответственно. Заключение. Применение ИРЧА спинальных ганглиев в сочетании с ЭБ является более эффективной методикой по сравнению с изолированной ЭБ для лечения послеоперационного корешкового болевого синдрома.
Дегенеративно-дистрофические заболевания позвоночника, корешковый болевой синдром, эпидуральная блокада, импульсная радиочастотная абляция, синдром оперированного позвоночника
Короткий адрес: https://sciup.org/142213575
IDR: 142213575 | УДК: 616.711.9-044.342-007.17-009.7-089:615.846 | DOI: 10.18019/1028-4427-2018-24-3-349-356
Текст научной статьи Радиочастотная импульсная абляция спинальных ганглиев в лечении послеоперационного корешкового болевого синдрома
Корешковый болевой синдром – основная хирургическая мишень в хирургии дегенеративно-дистрофических заболеваний позвоночника (ДДЗП). Сохранение или возобновление радикулярной боли после успешно выполненной операции без очевидного субстрата для повторного вмешательства составляет основу так на-
зываемого «синдрома неудачной операции на позвоночнике» (FBSS). Частота встречаемости FBSS определяется разными авторами в диапазоне 10–40 %, в зависимости от выбора методологии оценки, исходной патологии и вида оперативного вмешательства [1–5]. Общепринятые подходы к терапии хронической корешковой боли после операции отсутствуют, большинство неинвазивных методов имеют слабую доказательную базу и поддерживаются ограниченным количеством работ невысокого уровня [6, 7]. Интервенционные методы показывают достоверно лучшие результаты, и неэффективность именно интервенционных методов лечения боли является критерием постановки диагноза FBSS и показанием к выполнению нейромодуляции [8, 9, 10], в настоящий момент времени работами 1–2 класса подтверждена эффективность эпидурального введения глюкокортикостероидов и чрезкожного адгезиолиза [11, 12]. Импульсная радио- частотная абляция (ИРЧА) является методом лечения боли, в основе которого лежит ультраструктурное воздействие тока высокой частоты на безмиелиновые нервные волокна с моделированием прохождения болевого импульса. Исследования различного уровня демонстрируют эффективность метода для лечения болевого синдрома различной этиологии, в том числе и радикулопатии [13–17], при этом количество работ, посвященных лечению корешковой боли после оперативного лечения, невелико, результаты противоречивы, в большинстве случаев совместно исследовались пациенты и без операции в анамнезе [18–22].
Цель настоящего исследования – оценить возможности использования ИРЧА спинальных ганглиев в сочетании с эпидуральной блокадой (ЭБ) для лечения корешкового болевого синдрома после оперативных вмешательств по поводу дегенеративно-дистрофических заболеваний пояснично-крестцового отдела позвоночника.
МАТЕРИАЛЫ И МЕТОДЫ
В данной работе проводится анализ подгруппы пациентов из основного исследования, посвященного диагностике и лечению болевых синдромов после оперативного лечения ДДЗП поясничного отдела позвоночника, которое выполнялось в период 2012–2017 гг. В рамках основного исследования 310 пациентов обследовалось и прослеживалось проспективно. Подгруппа пациентов с послеоперационным корешковым болевым синдромом, удовлетворяющих выбранным критериям соответствия, составила 56 человек. 22 пациентам основной группы выполнялась ИРЧА спинальных ганглиев в сочетании с ЭБ, 34 пациентам контрольной группы – только ЭБ трансфораминальным доступом. Для анализа отбирались пациенты, первично или повторно оперированные на одном или нескольких уровнях по поводу грыж межпозвонковых дисков (МПД) или дегенеративного стеноза позвоночного канала в объеме дискэктомии/декомпрессии или декомпрессии с задним межтеловым спондилодезом и транспедикулярной фиксацией, с радикулярным болевым синдромом.
Критерии включения
-
1. Радикулярный болевой синдром, сохраняющийся после вмешательства или появившийся в пределах 1 года после него.
-
2. Уровень болевого синдрома - 4 и более баллов по цифровой шкале боли (NRS-11) и/или 8 балла и более по индексу беспокойства, причиняемого радикулопатией, и/или нарушение жизнедеятельности 20 % и более по индексу Освестри (ODI).
-
3. Отсутствие очевидных факторов компрессии по данным послеоперационной магнитно-резонансной (МРТ) и/или компьютерной (КТ) томографии, а также мелографии в виде неполностью удаленной грыжи МПД или устраненного стеноза, неправильного положения транспедикулярных финтов или миграции межтелового имплантата. Эпидуральный фиброз к факторам компрессии не относился. Наличие и степень компрессии корешка оценивалась по классификации C.S. Pfirrman et al. [23], стеноза позвоночного канала – по классификации С. Schizas et al. [24], фораминального стеноза – по S. Lee et.al. [25], допускалась перфорация медиальной стенки корня дуги и выстояние винта в канал не более 4 мм, исходя из рекомендаций обзора E.J. Woo, M.N. DiCuccio [26].
-
4. Отсутствие снижения болевого синдрома (как минимум на 50 % или 4 балла по шкале NRS-11, 20 % ODI,
-
5. При преимущественной локализации боли в нижней конечности выше колена, боли, связанной с движением, наличием хронической боли в спине, для исключения других возможных механизмов формирования болевого синдрома ряду пациентов проводилась однократная тестовая блокада межпозвонковых суставов и/или крестцово-подвздошных сочленений 0,2 % раствором ропивака-ина под флюороскопическим контролем. При снижении болевого синдрома на 50 % и более по шкале NRS-11 пациенты исключались из дальнейшего анализа.
8 баллов SBI) на фоне приема хотя бы одного препарата из группы антидепрессантов или антиконвульсантов, рекомендованных для лечения нейропатической боли, в адекватных дозировках в течение 1 месяца.
Критерии исключения
Наличие хронической боли в спине в качестве ведущего клинического синдрома, радикулопатия без болевого синдрома, крайне выраженный болевой синдром, грубый неврологический дефицит, признаки инфекционного процесса.
Исходы исследования
Основные исходы . Инструментами оценки предоперационного состояния и исходов вмешательств были индексы NRS-11 и SBI для определения интенсивности болевого синдрома и индекс ODI для оценки нарушений жизнедеятельности. Достижение пациентом положительного результата было основным исследуемым исходом настоящего исследования. Положительным результатом считалось снижение индекса NRS-11 на 50 % или на 4 балла, и/или снижение индекса ODI на 20 %, и/или снижение индекса SBI на 8 баллов от исходных значений с сохранением эффекта в течение 6 и более месяцев. Пациенты обследовались в течение года с контролем через 6 и 12 месяцев с момента процедуры. При наличии факта выполнения других интервенционных процедур и/или повышения дозы противоболевых препаратов, а также при утрате контакта с пациентом в течение первых 6 месяцев результат считался отрицательным. Оценка основных исходов проводилась при телефонном опросе, по электронной почте или при амбулаторном визите через 6 и 12 месяцев после выполнения процедуры.
Дополнительные исходы. Проводился анализ динамики исследуемых индексов NRS-11, ODI и SBI до и через 6 месяцев после процедуры. Для поиска факторов, влияющих на положительный исход интервенций, учитывались и анализировались следующие показатели: возраст, пол, количество и объем операций по по- воду данной патологии в анамнезе, наличие аллодинии или гиперпатии, наличие неврологического дефицита, длительность болевого синдрома перед вмешательством, уровень и количество пораженных корешков.
Описание медицинского вмешательства
Все вмешательства проводились одним исследователем в условиях операционной, оборудованной передвижным рентгеновским аппаратом с С-дугой, в положении больного лежа на животе под местной анестезией с мониторингом витальных функций. Под флюороскопическим контролем в косой проекции пункционная игла или игла для абляции устанавливалась и проводилась в зону между верхушкой верхнего суставного отростка нижележащего позвонка и корнем дуги вышележащего позвонка (рис. 1). В боковой проекции кончик иглы должен был занять положение в задне-верхнем квадранте межпозвонкового отверстия (рис. 2), в прямой – не далее медиальной педикулярной линии (рис. 3). При последующей эпидурографии оценивалось распространение контраста, при отсутствии адекватного контрастирования эпидурального пространства или при внутрисосудистом распространении производилось изменение положения иглы (рис. 4). С учетом возможных особенностей распределения контрастного вещества и вводимых после препаратов в виде краниального или каудального распространения
(рис. 4), при монорадикулярном синдроме трансфораминальный доступ осуществлялся на двух уровнях – на уровне патологии и ниже, при бирадикулярном – на трех уровнях. При патологии на уровне LV-SI для выделения S1 корешка доступ осуществлялся через первое крестцовое отверстие (рис. 5), для выполнения ИРЧА спинального ганглия S1 – через hiatus sacralis с использованием эпидурального электрода (рис. 6), что связано с анатомическими особенностями строения крестца и технической сложностью достижения спинального ганглия через крестцовое отверстие. В основной группе в иглу устанавливался электрод для абляции и проводилась сенсорная и моторная стимуляция с пороговыми значениями 0,5 В и 1,0 В соответственно, для дополнительной верификации позиционирования рядом с целевым нервом, в случае превышения указанных порогов стимуляции, положение иглы корректировалось. Импульсная радиочастотная абляция проводилась в течение 10 минут с параметрами: напряжение 65 В, длительность импульса 5 мс, частота 5 Гц, лимит температуры 42 °С, в конце процедуры через каждую иглу проводилось эпидуральное введение суммарно 5–8 мл 0,2 % раствора ропивакаина и 1 мл суспензии, содержащей 40 мг триамцинолона ацетонида. В контрольной группе проводилось только эпидуральное введение указанных препаратов.
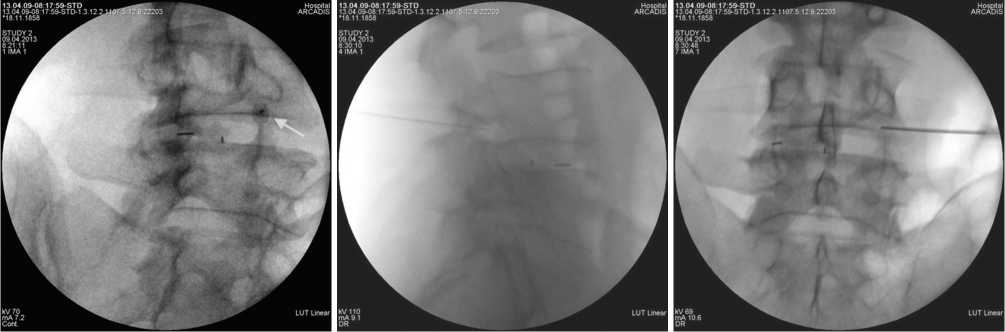
Рис. 2. Интраоперационная рентгенограмма поясничного отдела позвоночника в боковой проекции. Кончик пункционной иглы расположен в верхненаружном квадранте межпозвонкового отверстия LIV-V
Рис. 3. Интраоперационная рентгенограмма поясничного отдела позвоночника в прямой проекции. Кончик пункционной иглы расположен в межпозвонковом отверстии LIV-V справа по медиальной педикулярной линии
Рис. 1. Интраоперационная рентгенограмма поясничного отдела позвоночника в косой проекции. Пункционная игла (помечена стрелкой) расположена в зоне между верхушкой верхнего суставного отростка LV и корнем дуги LIV справа
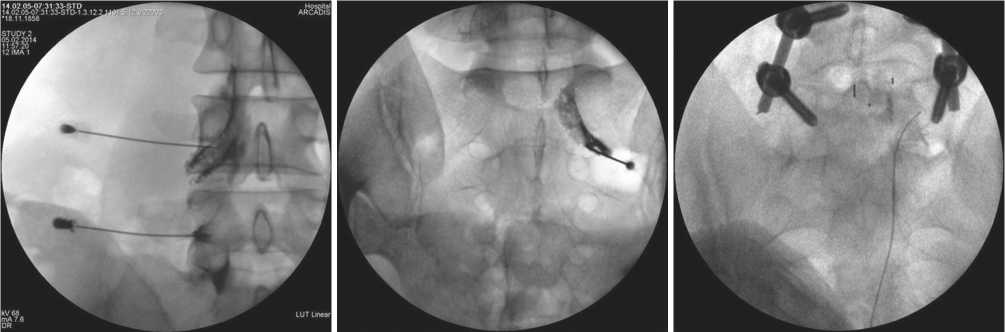
Рис. 4. Интраоперационная рентгенограмма поясничного отдела позвоночника в прямой проекции. Эпидурография и возможные пути распределения контрастного вещества
Рис. 5. Интраоперационная рентгенограмма поясничного отдела позвоночника в прямой проекции. Пункция первого крестцового отверстия и распространение контраста вдоль корешка S1
Рис. 6. Интраоперационная рентгенограмма поясничного отдела позвоночника в прямой проекции. Эпидуральный электрод заведен через hiatus sacralis и расположен в проекции спинального ганглия S1 слева
После процедуры пациенты могли продолжать прием противоболевых препаратов, в случае эффективности проведенного лечения рекомендовалось ступенчатое снижение дозы антиконвульсантов/антидепрессантов не ранее, чем через 1 месяц после вмешательства, на половину используемой дозы 1 раз в неделю до полной отмены или до появления болевого синдрома.
Статистическая обработка данных
Проверка соответствия эмпирических законов распределения исследуемых показателей показала достоверное отличие большинства из них от теоретического закона нормального распределения по критерию Шапиро-Уилка (р < 0,05). В соответствии с этим для статистического описания показателей использовались медиана и межквартильный интервал (Ме [25 %; 75 %]), а для проверки статистических гипотез – непараметрические методы анализа. Оценка значимости различий количественных и качественных показателей между группами проводилась, соответственно, по критериям U Манна-Уитни и χ2 Пирсона, при малом количестве ожидаемых значений в таблице сопряженности использовался точный тест Фишера. Оценка значимости различий количественных и качественных показателей до и после лечения внутри групп – по критерию T Уилкоксона и тесту Мак-Немара. Для выявления статистической связи между показателями проводился корреляционный анализ с использованием коэффициента ранговой корреляции ρ Спирмена. Для выявления предикторов исхода проводился бинарный логистический анализ с определением отношения шансов (ОШ) с доверительным интервалом (ДИ) 95 %.
Этическая экспертиза . Исследование одобрено локальным этическим комитетом, все пациенты, включенные в исследование, дали письменное информированное согласие.
РЕЗУЛЬТАТЫ
Из 310 пациентов с болевыми синдромами после оперативного лечения ДДЗП поясничного отдела позвоночника у 91 пациента (29,36 %) имела место боль в нижней конечности без очевидного субстрата компрессии по данным нейровизуализации. При выполнении тестовых блокад для дифференциальной диагностики у 26 пациентов (28,57 %) достигнуто купирование болевого синдрома, на фоне коррекции консервативного лечения положительный эффект достигнут у 9 пациентов (9,89 %), в итоге, у 56 пациентов выполнены интервенционные вмешательства, все они прослежены в течение года после процедуры и включены в окончательный анализ.
В таблице 1 представлено распределение выделенных групп пациентов перед вмешательством по исследуемым характеристикам, достоверных различий между группами не выявлено. Для обеих групп необходимо отметить высокий процент пациентов с остаточной радикулопатией после двух и более вмешательств (46,63 % суммарно), и наиболее частое страдание L5 корешка (58,93 %).
Положительные результаты вмешательств, исходя из заданных критериев, получены у 18 пациентов (81,82 %) основной группы и 19 пациентов (55,88 %) контрольной группы, различия достоверны, p = 0,045. Спустя год после вмешательства положительный эффект сохранялся у 16 пациентов основной группы (72,73 %) и 15 пациентов (44,12 %) контрольной, различия достоверны, p = 0,048. В контрольной группе 10 пациентам, у которых отмечался достаточный, но кратковременный эффект от ЭБ (не менее 2-х недель), в дальнейшем выполнена ИРЧА с положительным эффектом в 7 случаях.
Динамика изменений анализируемых показателей представлена в таблице 2. Произошло достоверное снижение всех индексов после вмешательства. При межгрупповом анализе различия по индексам NRS-11 и ODI до и после вмешательства недостоверны. При этом медиана индекса SBI в основной группе было достоверно ниже, чем в контрольной, p = 0,021.
В обеих группах осложнений вмешательств, побочных эффектов от введения препаратов зарегистрировано не было.
Наличие аллодинии и/или гиперпатии было основным фактором риска негативных результатов в обеих группах, с ОШ 0,79 при 95 % ДИ (0,735–0,897) в основной и ОШ 0,82 при 95 % ДИ (0,780–0,929) в контрольной.
Таблица 1
Характеристики исследуемых групп пациентов перед вмешательством
|
Признак |
ОГ (n = 22) |
КГ (n = 34) |
р* |
|
Возраст, Ме [25 %;75 %] |
47,5 [38; 60,5] |
35 [34,25; 60] |
0,860 |
|
Мужчины |
14 (63,64 %) |
14 (41,18 %) |
0,171 |
|
Женщины |
8 (36,36 %) |
20 (58,82 %) |
|
|
Дискэктомия |
2 (9,09 %) |
2 (5,88 %) |
0,103 |
|
Декомпрессия |
3 (13,64 %) |
4 (11,76 %) |
|
|
Декомпрессия+стабилизация |
9 (40,91 %) |
16 (47,06 %) |
|
|
Декомпрессия + стабилизация более 3-х сегментов |
8 (36,36 %) |
12 (35,29 %) |
|
|
Повторная операция в анамнезе |
12 (54,55 %) |
14 (41,18 %) |
0,414 |
|
Аллодиния/гиперпатия |
5 (22,73 %) |
9 (26,47 %) |
0,752 |
|
L3 корешок |
– |
1 (2,94 %) |
0,811 |
|
L4 корешок |
3 (13,64 %) |
3 (8,82 %) |
|
|
L5 корешок |
13 (59,09 %) |
20 (58,82 %) |
|
|
S1 корешок |
6 (27,27 %) |
10 (29,42 %) |
|
|
Бирадикулярная симптоматика |
2 (0,09 %) |
5 (1,47 %) |
0,417 |
* – уровень значимости различий между группами.
Таблица 2
Изменения медиан исследуемых показателей NRS-11, ODI и SBI после вмешательства
|
Показатель |
Группа |
Сроки наблюдения |
p* |
|
|
до лечения |
после лечения |
|||
|
NRS-11 |
ОГ |
6 [4,25; 6] |
4,5 [2; 6] |
< 0,001 |
|
КГ |
6 [5; 7] |
4 [3; 7,75] |
0,004 |
|
|
p** |
0,261 |
0,725 |
||
|
ODI |
ОГ |
49,5 [36; 56,5] |
28,5 [16,75; 47,75] |
0,02 |
|
КГ |
40,5 [33,25; 49] |
33 [14,75; 48] |
0,045 |
|
|
p** |
0,135 |
0,294 |
||
|
SBI |
ОГ |
15 [13,25; 17,75] |
5,5 [3,25; 11] |
0,019 |
|
КГ |
14 [11; 17] |
12 [7; 15,75] |
0,031 |
|
|
p** |
0,507 |
0,021 |
||
* – уровень значимости различий внутри группы до и после лечения; ** – уровень значимости различий между группами.
ОБСУЖДЕНИЕ
По данным метаанализа работ, посвященных FBSS [27], частота встречаемости корешкового болевого синдрома без очевидного субстрата компрессии составляет 4,8–10,2 % среди всех послеоперационных проблем. Частота встречаемости эпидурального фиброза, по данным того же исследования, достигает 34 %, и, если не рассматривать фиброз в качестве самостоятельного фактора компрессии наряду с резидуальным стенозом или грыжей МПД, то встречаемость радикулярной боли будет еще выше. Связь между клиническими исходами спинальных вмешательств и выраженностью эпидурального фиброза по данным МРТ в настоящий момент не доказана, равно как и значение методов его профилактики [28–31], поэтому в настоящей работе выраженность рубцового процесса не учитывалась. Частота встречаемости некомпрессионного корешкового болевого синдрома составила 11,46 % среди пациентов с различными болевыми синдромами и/или патологическими состояниями после хирургии ДДЗП поясничного отдела. Стоит отметить, что на этапе отбора из 91 пациента с болью в нижней конечности 26 было исключено по результатам положительных тестовых блокад или других потенциальных генераторов псевдорадикулярной боли.
Эффективность эпидуральных блокад подтверждена одним рандомизированным контролируемым исследованием [32], у 59 % пациентов отмечен положительный результат в виде снижения болевого синдрома на 50 % в течение первого года. Среди недостатков исследования – большое количество повторных инъекций (в среднем 4 в год), использование наименее выгодного анатомически каудального доступа и признание результата положительным при продолжительности эффекта хотя бы в течение 3-х недель. V. Wilde с со-авт. [33] на основании анализа 5 работ делают вывод о недостаточности доказательств эффективности ЭБ при лечении послеоперационного болевого синдрома. В настоящем исследовании в контрольной группе удовлетворительные результаты достигнуты при ЭБ у 55,88 % пациентов при однократной инъекции с продолжительностью эффекта 6 месяцев, у 44,12 % эффект сохранялся в течение года. Позитивные отличия могут быть связаны с трансфораминальным путем введения стероидов – гораздо ближе к зоне предполагаемого воспаления по сравнению с каудальным путем с достижением более высокой концентрации препарата. Значение селективности введения косвенно подтверждает и анализ результатов применения чрез-кожного адгезиолиза – вмешательства с селективной катетеризацией эпидурального пространства гибким рентгенпозитивным катетером и введением через него стероида в комбинации с гиалуронидазой и гипертоническим растворам хлорида натрия. Процедура демонстрировала большую эффективность по сравнению с каудальной блокадой, однако на результат в большей степени влияло именно позиционирование катетера в вентральном эпидуральном пространстве, а не использование ферментов и агрессивных растворов [34].
Эффективность использования ИРЧА для лечения радикулярной боли подтверждена рандомизированным исследованием [35] с двойным слепым контролем и плацебо-процедурой при патологии шейного отдела позвоночника. Во многих проспективных [18, 21, 22] и ретроспективных [20, 36–39] исследованиях получены довольно противоречивые результаты – количество пациентов с удовлетворительными исходами не превышало 50 %, отсутствовали достоверные различия в динамике исследуемых индексов по сравнению с контрольной группой, худшие результаты были у пациентов с FBSS. При этом стоит отметить, что во все упомянутые исследования были включены пациенты с разнообразной патологией, включая хирургически значимые состояния в виде грыж МПД и дегенеративного стеноза, для которых неэффективность консервативного лечения является ожидаемой клинической ситуацией. Для оценки результатов традиционно использовались шкала боли и индекс Освестри, последний разработан, в первую очередь, для измерения нарушения жизнедеятельности при боли в спине, а не радикулопатии. В ряде исследований высокого уровня, посвященных сравнению результатов хирургии и терапии в лечении грыж МПД, дегенеративного стеноза и спондилолистеза [40], достоверных различий в этих показателях между группами после лечения не выявлено, различия были только в индексе SBI, специально разработанном для оценки радикулопатии. В патогенезе радикулопатии воспаление является признаваемым всеми ведущим компонентом, а использование кортикостероидов является очевидным патогенетическим компонентом лечения. Исключение использования стероидов при селекции пациентов на ИРЧА или отбор на основании неэффективности ЭБ может негативно влиять на ожидаемый результат. Сочетание ЭБ и ИРЧА исследовалось в работе W. Koh с соавт. [22] и было достоверно более эффективно, чем изолированная ЭБ.
Более высокие результаты (81,8 % положительных результатов в течение 6 месяцев, сохранение эффекта в течение года у 72,73 % пациентов), полученные в проведенном исследовании, могут быть объяснены особенностями его организации на основании данных, полученных при литературном поиске. Включались пациенты только после исключения хирургического субстрата корешкового болевого синдрома, с дополнительным исключением других механизмов и источников боли в спорных случаях при помощи тестовых блокад.
ЗАКЛЮЧЕНИЕ
Исходя из результатов проведенного исследования, импульсная радиочастотная абляция и эпидуральное введение стероидов являются эффективными и безопасными методиками для лечения послеоперационного корешкового болевого синдрома при условии отсутствия хирургически значимых субстратов компрессии. При- менение ИРЧА в сочетании с ЭБ является более эффективной методикой по сравнению с изолированной ЭБ, что подтверждается достоверными различиями в количестве пациентов с удовлетворительными результатами (81,82 % и 55,88 %, p = 0,045), а также большим снижением индекса SBI после вмешательства, p = 0,021.
Ограничения исследования
Основными ограничениями исследования являются отсутствие рандомизации и малое количество наблюдений, открытый дизайн. Совместное использование ИРЧА и ЭБ не позволяют полностью оценить роль импульсной абляции, фоновый прием медикаментов, разрешенный в настоящем исследовании, уменьшает «чистоту» эксперимента и требует организации исследований более высокого уровня, где основной проблемой станет поиск пациентов, с учетом относительно небольшого их числа. Тем не менее, продемонстрированная эффективность ИРЧА в сочетании с ЭБ на фоне отсутствия значимых осложнений и побочных эффектом позволяет рекомендовать этот метод для лечения послеоперационного корешкового болевого синдрома.
Список литературы Радиочастотная импульсная абляция спинальных ганглиев в лечении послеоперационного корешкового болевого синдрома
- Chan C.W., Peng P. Failed back surgery syndrome//Pain Med. 2011. Vol. 12, No 4. P. 577-606. DOI: 10.1111/j.1526-4637.2011.01089.x.
- Thomson S. Failed back surgery syndrome -definition, epidemiology and demographics//Br. J. Pain. 2013. Vol. 7, No 1. P. 56-59. DOI: 10.1177/2049463713479096.
- Neuropathic pain after spinal surgery/J.H. Cho, J.H. Lee, K.S. Song, J.Y. Hong//Asian Spine J. 2017. Vol. 11, No 4. P. 642-652. DOI: 10.4184/asj.2017.11.4.642.
- An analysis of reasons for failed back surgery syndrome and partial results after different types of surgical lumbar nerve root decompression/A. Bokov, A. Isrelov, A. Skorodumov, A. Aleynik, A. Simonov, S. Mlyavykh//Pain Physician. 2011. Vol. 14, No 6. P. 545-557.
- Диагностика и лечение болевого синдрома после операций по поводу грыж межпозвонковых дисков пояснично-крестцового отдела позвоночника/О.Н. Тюлькин, В.В. Щедренок, К.И. Себелев, О.В. Могучая//Вестник хирургии им. И.И. Грекова. 2010. Т. 169, № 4. С. 55-57.
- Treatment Outcomes for Patients with Failed Back Surgery/J.H. Cho, J.H. Lee, K.S. Song, J.Y. Hong, Y.S. Joo, D.H. Lee, C.J. Hwang, C.S. Lee//Pain Physician. 2017. Vol. 20, No 1. P. E29-E43.
- Treatment Options for Failed Back Surgery Syndrome Patients With Refractory Chronic Pain: An Evidence Based Approach/K. Amirdelfan, L. Webster, L. Poree, V. Sukul, P. McRoberts//Spine. 2017. Vol. 42, No Suppl. 14. P. S41-S52. DOI: 10.1097/BRS.0000000000002217.
- Spinal cord stimulation versus conventional medical management for neuropathic pain: a multicentre randomised controlled trial in patients with failed back surgery syndrome/K. Kumar, R.S. Taylor, L. Jacques, S. Eldabe, M. Meglio, J. Molet, S. Thomson, J. O'Callaghan, E. Eisenberg, G. Milbouw, E. Buchser, G. Fortini, J. Richardson, R.B. North//Pain. 2007. Vol. 132, No 1-2. P. 179-188. DOI: 10.1016/j.pain.2007.07.028.
- Spinal cord stimulation versus re-operation in patients with failed back surgery syndrome: an international multicenter randomized controlled trial (EVIDENCE study)/R.B. North, K. Kumar, M.S. Wallace, J.M. Henderson, J. Shipley, J. Hernandez, N. Mekel-Bobrov, K.N. Jaax//Neuromodulation. 2011. Vol. 14, No 4. P. 330-335. DOI: 10.1111/j.1525-1403.2011.00371.x.
- Clinical Evidence for Spinal Cord Stimulation for Failed Back Surgery Syndrome (FBSS): Systematic Review/L. Kapural, E. Peterson, D.A. Provenzano, P. Staats//Spine. 2017. Vol. 42, No Suppl. 14. P. S61-S66. DOI: 10.1097/BRS.0000000000002213.
- A comparative effectiveness evaluation of percutaneous adhesiolysis and epidural steroid injections in managing lumbar post surgery syndrome: a randomized, equivalence controlled trial/L. Manchikanti, V. Singh, K.A. Cash, V. Pampati, S. Datta//Pain Physician. 2009. Vol. 12, No 6. P. E355-E368.
- Assessment of effectiveness of percutaneous adhesiolysis and caudal epidural injections in managing post lumbar surgery syndrome: 2-year follow-up of a randomized, controlled trial/L. Manchikanti, V. Singh, K.A. Cash, V. Pampati//J. Pain Res. 2012. Vol. 5. P. 597-608 DOI: 10.2147/JPR.S38999
- Pulsed radiofrequency: current clinical and biological literature available/A. Cahana, J. van Zundert, L. Macrea, M. van Kleef, M. Sluijter//Pain Med. 2006. Vol. 7, No 5. P. 411-423 DOI: 10.1111/j.1526-4637.2006.00148.x
- Chua N.H., Vissers K.C., Sluijter M.E. Pulsed radiofrequency treatment in interventional pain management: mechanisms and potential indications -a review//Acta Neurochir. (Wien). 2011. Vol. 153, No 4. P. 763-771 DOI: 10.1007/s00701-010-0881-5
- Заболотский Д.В., Портнягин И.В. Применение импульсной радиочастотной абляции при лечении тяжелого хронического болевого синдрома после эндопротезирования плечевого сустава (клинический случай)//Травматология и ортопедия России. 2015. № 4 (78). С. 126-130.
- Егоров О.Е., Евзиков Г.Ю. Лечение больного с радикулопатическим болевым синдромом с применением импульсной радиочастотной невротомии заднего ганглия корешка спинномозгового нерва. Клиническое наблюдение и обзор литературы//Неврологический журнал. 2015. Т. 20, № 1. С. 28-33.
- Генов П.Г., Смирнова О.В., Тимербаев В.Х. Успешное применение импульсной радиочастотной абляции ганглиев спинномозговых нервов при лечении пациента с хронической нейропатической болью в культе ампутированной конечности//Регионарная анестезия и лечение острой боли. 2016. Т. 10, № 1. С. 60-64.
- Radiofrequency lesioning of dorsal root ganglia for chronic lumbosacral radicular pain: a randomised, double-blind, controlled trial/J.W. Geurts, R.M. van Wijk, H.J. Wynne, E. Hammink, E. Buskens, R. Lousberg, J.T. Knape, G.J. Groen//Lancet. 2003. Vol. 361, No 9351. P. 21-26.
- Hussain A.M., Afshan G. Use of pulsed radiofrequency in failed back surgery syndrome//J. Coll. Physicians Surg. Pak. 2007. Vol. 17, No 6. P. 353-355 DOI: 06.2007/JCPSP.353355
- Pulsed radiofrequency in lumbar radicular pain: clinical effects in various etiological groups/D. Abejón, S. Garcia-del-Valle, M.L. Fuentes, J.I. Gómez-Arnau, E. Reig, J. van Zundert//Pain Pract. 2007. Vol. 7, No 1. P. 21-26 DOI: 10.1111/j.1533-2500.2007.00105.x
- Pulsed radiofrequency treatment of the lumbar dorsal root ganglion in patients with chronic lumbar radicular pain: a randomized, placebo-controlled pilot study/H. Shanthanna, P. Chan, J. McChesney, L. Thabane, J. Paul//J. Pain Res. 2014. Vol. 7. P. 47-55 DOI: 10.2147/JPR.S55749
- Treatment of chronic lumbosacral radicular pain using adjuvant pulsed radiofrequency: a randomized controlled study/W. Koh, S.S. Choi, M.H.Karm, J.H. Suh, J.G. Leem, J.D. Lee, Y.K. Kim, J. Shin//Pain Med. 2015. Vol. 16, No 3. P. 432-441 DOI: 10.1111/pme.12624
- MR image-based grading of lumbar nerve root compromise due to disk herniation: reliability study with surgical correlation/C.W. Pfirrmann, C.Dora, M.R. Schmid, M. Zanetti, J. Hodler, N. Boos//Radiology. 2004. Vol. 230, No 2. P. 583-588 DOI: 10.1148/radiol.2302021289
- Qualitative grading of severity of lumbar spinal stenosis based on the morphology of the dural sac on magnetic resonance images/C. Schizas, N. Theumann, A. Burn, R. Tansey, D. Wardlaw, F.W. Smith, G. Kulik//Spine. 2010. Vol. 35, No 21. P. 1919-1924 DOI: 10.1097/BRS.0b013e3181d359bd
- A practical MRI grading system for lumbar foraminal stenosis/S. Lee, J.W. Lee, J.S. Yeom, K.J. Kim, H.J. Kim, S.K. Chung, H.S. Kang//AJR Am. J. Roentgenol. 2010. Vol. 194, No 4. P. 1095-1098 DOI: 10.2214/AJR.09.2772
- Woo E.J., DiCuccio M.N. Clinically significant pedicle screw malposition is an underestimated cause of radiculopathy//Spine J. 2018. Vol. 18, No 7. P. 116-1171 DOI: 10.1016/j.spinee.2017.11.006
- Clancy C., Quinn A., Wilson F. The aetiologies of Failed Back Surgery Syndrome: A systematic review//J. Back Musculoskelet. Rehabil. 2017. Vol. 30, No 3. P. 395-402 DOI: 10.3233/BMR-150318
- Outcome following lumbar disc surgery: the role of fibrosis/D.B. Almeida, M.N. Prandini, Y. Awamura, M.L. Vitola, M.P. Simião, J.B. Milano, K.C. Bordignon, M.P. Ache, R. Ramina//Acta Neurochir. (Wien). 2008. Vol. 150, No 11. P. 1167-1176 DOI: 10.1007/s00701-008-0131-2
- Волков И.В. Влияние дренирования и пластики эпидурального пространства на результаты поясничных дискэктомий//Вестник хирургии им. И.И. Грекова. 2008. Т. 167, № 2. С. 61-63.
- Rankine J.J. The postoperative spine//Semin. Musculoskelet. Radiol. 2014. Vol. 18, No 3. P. 300-308 DOI: 10.1055/s-0034-1375571
- Peridural scar and its relation to clinical outcome: a randomised study on surgically treated lumbar disc herniation patients/K. Rönnberg, B. Lind, B. Zoega, G. Gadeholt-Göthlin, K. Halldin, M. Gellerstedt, H. Brisby//Eur. Spine J. 2008. Vol. 17, No 12. P. 1714-1720 DOI: 10.1007/s00586-008-0805-8
- Fluoroscopic caudal epidural injections in managing post lumbar surgery syndrome: two-year results of a randomized, double-blind, active-control trial/L. Manchikanti, V. Singh, K.A. Cash, V. Pampati, S. Datta//Int. J. Med. Sci. 2012. Vol. 9, No 7. P. 582-591 DOI: 10.7150/ijms.4672
- Systematic review of management of chronic pain after surgery/V. Wylde, J. Dennis, A.D. Beswick, J. Bruce, C. Eccleston, N. Howells, T.J. Peters, R. Gooberman-Hill//Br. J. Surg. 2017. Vol. 104, No 10. P. 1293-1306 DOI: 10.1002/bjs.10601
- Percutaneous adhesiolysis in the management of chronic low back pain in post lumbar surgery syndrome and spinal stenosis: a systematic review/Ii.S. Helm, R.M. Benyamin, P. Chopra, T.R. Deer, R. Justiz//Pain Physician. 2012. Vol. 15, No 4. P. E435-E462.
- Pulsed radiofrequency adjacent to the cervical dorsal root ganglion in chronic cervical radicular Pain: a double blind sham controlled randomized clinical trial/J. van Zundert, J. Patijn, A. Kessels, I. Lamé, H. van Suijlekom, M. van Kleef//Pain. 2007. Vol. 127, No 1-2. P. 173-182 DOI: 10.1016/j.pain.2006.09.002
- Teixeira A., Grandinson M., Sluijter M.E. Pulsed radiofrequency for radicular pain due to a herniated intervertebral disc -an initial report//Pain Pract. 2005. Vol. 5, No 2. P. 111-115 DOI: 10.1111/j.1533-2500.2005.05207.x
- Percutaneous pulsed radiofrequency applied to the L-2 dorsal root ganglion for treatment of chronic low-back pain: 3-year experience/H.K. Tsou, S.C. Chao, C.J. Wang, H.T. Chen, C.C. Shen, H.T. Lee, Y.S. Tsuei//J. Neurosurg. Spine. 2010. Vol. 12, No 2. P. 190-196 DOI: 10.3171/2009.9.SPINE08946
- Percutaneous pulsed radiofrequency in the treatment of cervical and lumbar radicular pain/S.C. Chao, H.T. Lee, T.H. Kao, M.Y. Yang, Y.S. Tsuei, C.C. Shen, H.K. Tsou//Surg. Neurol. 2008. Vol. 70, No 1. P. 59-65 DOI: 10.1016/j.surneu.2007.05.046
- Pulsed radiofrequency treatment adjacent to the lumbar dorsal root ganglion for the management of lumbosacral radicular syndrome: a clinical audit/K. van Boxem, J. van Bilsen, N. de Meij, A. Herrler, F. Kessels, J. van Zundert, M. van Kleef//Pain Med. 2011. Vol. 12, No 9. P. 1322-1330 DOI: 10.1111/j.1526-4637.2011.01202.x
- Comparative effectiveness evidence from the Spine patient outcomes research trial: surgical versus nonoperative care for spinal stenosis, degenerative spondylolisthesis, and intervertebral disc herniation/A.N. Tosteson, T.D. Tosteson, J.D. Lurie, W. Abdu, H. Herkowitz, G. Andersson, T. Albert, K. Bridwell, W. Zhao, M.R. Grove, M.C. Weinstein, J.N. Weinstein//Spine. 2011. Vol. 36, No 24. P. 2061-2068 DOI: 10.1097/BRS.0b013e318235457b


