Раневое покрытие на основе коллагенламиновой матрицы
Автор: Саганов Владислав Павлович, Балханов Юрий Содномович, Эрдынеева Елена Базыровна, Бодоев Александр Васильевич, Синицына Татьяна Юрьевна
Журнал: Вестник Бурятского государственного университета. Медицина и фармация @vestnik-bsu-medicine-pharmacy
Статья в выпуске: 1, 2022 года.
Бесплатный доступ
Заживление ран остается серьезной клинической проблемой. Одним из новых направлений регенеративной медицины является применение клеточных технологий в областях поражений кожного покрова. Клеточные технологии должны решать следующие задачи: восстановление поврежденного строения и функции кожного покрова, стимуляции регенеративных процессов заживления и создании микроокружения для усиления потенциала собственных тканей и клеток. Наиболее эффективным методом в лечении ран является использование тканеинженерных матриц, состоящих из дермального и эпидермального компонентов, для полноценного замещения поврежденных участков ткани. Нами исследована одна из конструкций, композитный материал, содержащий коллаген и ламинин. Пациентка, ДЗ: Вульгарная пузырчатка, распространенная форма. Анемия средней степени тяжести. Диагноз выставлен с 2016 г. В течение заболевания периодические обострения до 2-3 раз в год, последнее обострение с июня 2019 г. Находилась на госпитализации без особой положительной динамики, на суточной дозировке преднизолона: 40 мг/сутки. В сентябре этого года проводилось наложение на пораженные участки кожи раневого покрытия NovoSkin, в течение трех недель в ходе лечения произошла полная эпителизация, с уменьшением дозировки преднизолона до 10 мг/сутки. Новый биосовместимый коллаген-ламининовый ранозаживляющий материал, основанный на комбинации полимерной подложки и продукта синтеза кератиноцитов кожи человека, при этом лишенный клеточной составляющей, отличается сравнительной простотой изготовления, длительностью сроков хранения, может быть рекомендован к внедрению.
Коллаген, ламинин, ранозаживление, тканеинженерные конструкции
Короткий адрес: https://sciup.org/148326720
IDR: 148326720 | УДК: 616-001:616.5 | DOI: 10.18101/2306-1995-2022-1-15-24
Wound healing with collagen-laminin matrix
Wound healing remains a serious clinical problem. The most important and rapidly developing area of modern regenerative medicine is the use of cell technologies. The task of cellular technologies in this case is to completely restore the structure and function of the skin, to stimulate regenerative processes and create a microenvironment to realize the potential of one's own tissues and cells. The most effective method for treating wounds is the use of tissue-engineered structures, consisting of dermal and epidermal components, for full replacement of damaged skin areas. One of the constructions, a composite material containing collagen and laminin have been examined.Patient, DZ: Pemphigus vulgaris, common form. Moderate anemia. The diagnosis has been made since 2016. During the course of the disease, periodic exacerbations up to 2-3 times a year, the last exacerbation has been since June 2019, The patient was hospitalized without much positive dynamics, on a daily dosage of prednisolone: 40 mg / day. In September of this year, a NovoSkin wound covering was applied to the affected skin areas; within 3 weeks during the treatment, complete epithelialization occurred, with a decrease in the dosage of prednisolone to 10 mg / day.The developed biocompatible collagen-laminin wound healing material based on a combination of a polymer substrate and a human keratinocyte synthesis product, while devoid of a cellular component, is characterized by comparative ease of manufacture and a long shelf life, which makes it possible to recommend the design for implementation.
Текст научной статьи Раневое покрытие на основе коллагенламиновой матрицы
Несмотря на существующие достижения в области регенеративной медицины, заживление ран кожи остается актуальной проблемой. Для полноценного замещения поврежденных участков кожи необходимо использование тканеинженерных конструкций, состоящих из эпидермального и дермального компонентов кожи. Использование биологически активных стимулирующих средств с направленным действием на процессы регенерации и эпителизации является очень действенным способом заживления ран, в том числе вызванных ожогами [1]. В настоящее время использование материалов основывается на биодеградации полимеров: альгинатов, коллагена, желатина, хитозана, фиброинов шелка, полиэфиров бактериального происхождения — полиоксибутиратов и их сополимеров [2]. Данные материалы биосовместимы и выполняют роль эффективных биостимуляторов. Сегодня предложены коллагенсодержащие препараты, которые в качестве антисептического компонента содержат в себе метронидазол либо доксициклин или хлоргексидин биглюконат [3]. Коллаген, являясь белком соединительной ткани, играет важную роль в осуществлении репаративных свойств. Заживление любой раны — это восстановление соединительной ткани кожи тела. Основным компонентом в процессах заживления кожных покровов тела является коллаген [4]. Причиной усиления коллагеном роста соединительной ткани будет стимуляция продуктов его распада. Важным преимуществом разрабатываемых средств на основе коллагена является их способность к биоадгезии при контакте с тканями организма и его последующей биодеградации.
В наши дни в качестве перевязочного материала разработаны коллагеновые губки, в сочетании с эластинами, фибронектинами и гликозаминогликанами, обладающие способностью впитывать экссудат покровной ткани и защищать от механических повреждений и присоединения вторичной бактериальной инфекции. Данное покрытие стимулирует дермальное и эпидермальное ранозаживле-ние кожных покровов тела [5, 6].
Кожные покровы являются наиболее обширным органом человека по измеряемой поверхности тела. Расположение кожи на границе наружной и внутренней сред определяет ее защитные, барьерные и другие функции. Кожные покровы защищают организм от неблагоприятных воздействий внешней среды, защищают от действия патогенных микробов и вирусов, а также кожа позволяет получать осязательную информацию, воспринимать термические и механические действия посредством осязания покровов тела. Отдельные повреждения составляющих элементов кожных покровов при травме или заболеваниях могут приводить к тяжелым последствиям вплоть до смертельного исхода. Поэтому развива- ются следующие направления науки, такие как тканевая инженерия и регенеративная медицина, одна из целей которых — разработка новых способов регенерации поврежденных тканей и органов, в том числе кожи [7]. Сегодня предполагается создание новых искусственных биологически совместимых средств, которые выступают в качестве раневых покрытий нового поколения и служат основой для получения новых эквивалентов кожи, которые обладают свойством замещать поврежденные участки тканей.
Цель исследования
Объектом исследования являются коллаген-ламининовые матрицы для образования тканеинженерных конструкций. Цель работы — разработка коллагенламининовой матрицы для задач тканевой инженерии. Одно из действий регенеративной медицины будут клеточные технологии. Цель в данном случае не только в трансплантации живых клеток в поврежденные ткани, но и в репарации структуры и свойств кожи, в усилении восстановительных процессов и создании окружения для реализации всех свойств тканей и клеток. Чтобы решить данные задачи, применяются способы тканевой инженерии [8]. Эти методы решают задачи регенеративной медицины и рассматривают вопросы качества жизни человека, повышения ее длительности за счет восстановления строения и функций тканей и органов.
Одним из способов, направленных на восстановление поврежденных или утраченных тканей, служит применение тканеинженерных конструкций, созданных на основе клеточных технологий. Большинство исследований направлено на изготовление растворов коллагена и дальнейшее его использование в приготовлении лекарственных средств. Коллаген — основной белок соединительной ткани, имеющий важные биохимические свойства, главной из которых является репаративная [9]. Коллаген интересен еще и тем, что имеет свойства вновь образованных полимеров (прочность, эластичность, способность формировать различные структуры и др.), а также функции природных полимеров (способность к биодеградации и образованию обратимых комплексов с лекарственными средствами, тем самым пролонгируя их действие).
Материалы и методы
Коллаген первого типа выделяется из сухожилий хвостов крыс. С этой целью берутся взрослые крысы линии Вистар весом от 300 грамм, содержащиеся в условиях вивариев при лабораториях, без инфицирования, влияния паразитов и т. д. Хвосты крыс отделяются после умерщвления животных, хвосты можно хранить в течение нескольких лет в морозильной камере при t̊°-20 °С. Перед выделением коллагена крысиные хвосты вначале отмывают при помощи моющих средств и стерилизуют в 70%-ном этиловом спирте в течение 24 часов перед экстрагированием коллагена. Все манипуляции проводятся в стерильных условиях. Кожу с хвоста крысы снимают при помощи скальпеля и пинцета и далее крысиный хвост разрезается на порции по 2–3 см. Полученные таким образом куски хвоста инкубируются в 70%-ном этиловом спирте в течение 15 минут. Затем сухожилия извлекают из крысиных хвостов и расщепляют на тонкие волокна и помещают в сосуд со стерильным раствором 0,1%-ной ледяной уксусной кислоты. При этом коллаген начинает экстрагироваться в раствор практически сразу, в этом случае раствор приобретает вязкость и окраску по типу синевато- опалесцирующей дымки. Для получения необходимой концентрации и консистенции раствора сухожилия с одного хвоста следует помещать в 100–150 мл раствора. Затем раствор инкубируют при t°+4°С в течение одного месяца. Потом раствор коллагена центрифугируют (при комнатной температуре 1 час при 1500g≈4000 об./мин при радиусе ротора 10 см) для осаждения нерастворенных волокон коллагена. Образовавшийся раствор сливают в стерильные емкости для консервации. Концентрацию полученного раствора определяют, выпарив в суховоздушном термостате водную фракцию и определив вес осадка. Раствор коллагена можно считать нормальным при концентрации коллагена не ниже 1мг/мл (обычно получается 3–5 мг/мл).
Полимеризация коллагена происходит быстро, в течение 3–5 минут, поэтому все процедуры необходимо проводить вовремя, желательно на льду, для этого следует нейтрализовать кислый раствор. Добавив необходимые ингредиенты и смешав их, чашку Петри с коллагеновым гелем ставят в инкубатор с t°+37 °C на несколько часов.
Следующим этапом является процесс высаживания клеток на поверхность полученной пленки: на коллагеновый гель высаживают клетки линии HaCaT в плотности 10–40 тысяч клеток на 1 см². Клетки линии HaCaT являются имморта-лизованными кератиноцитами человека, они хорошо культивируются и широко используются в научных исследованиях.
После достижения необходимой плотности клеток получившийся коллагенламининовый матрикс фиксируют в 4%-ном параформальдегиде в течение 24 часов при t°+4 °С. При этом все белки композиции соединяются между собой, образуя нерастворимый комплекс, а клетки инактивируются. После необходимой фиксации трансплант отмывается от формальдегида при помощи стерильного раствора фосфатно-солевого буфера (PBS), 3 раза по 15 минут с покачиванием на орбитальном шейкере. Далее проводят этап децеллюлирования матрикса. Готовый матрикс можно хранить в течение одного месяца при t°+4 °С в растворе PBS либо два года в высушенном состоянии, замораживая при t°-20 °С.
Полученная конструкция представляет устойчивую белковую композицию, которая состоит из коллагена первого типа и ламинина базальной мембраны. Коллаген составляет основу транспланта, ламинин закрывает ее в виде базальной мембраны. Матрикс стерильный, лишен какой-либо клеточной составляющей.
В настоящее время используются новые препараты в медицине, способные выполнять нужные функции и разлагаться на простые составляющие, выводиться организмом в определенное время, не оказывая токсическое действие на организм в целом. Большинство травм и заболеваний, связанных с ранением кожи, создают долгосрочную основу для спроса на биосовместимые и биодеградируемые медицинские материалы 1 . Поэтому средства, применяемые как тканеинженерные конструкции, должны иметь свойства, в основе которых лежит биосовместимость. Многие полимеры естественного происхождения обладают высокой биологической активностью, усиливают восстановление тканей без проявления новообразований соединительной ткани в месте повреждения [10].
Для разработки новых кожных покрытий применяют коллаген, ламинины и другие компоненты внеклеточного матрикса, которые обладают высокой биосовместимостью и способны оказывать определенное действие на соприкасающиеся ними клетки [11]. Ламинины — семейство крупных адгезивных гликопротеинов, которые являются главными компонентами базальных мембран и способны выполнять ряд функций. Основной задачей ламинина являются связывание клеток и моделирование клеточного поведения.
Апробация полученного ранозаживляющего матрикса
Пациентка: Б. 55 лет ДЗ: Вульгарная пузырчатка, распространенная форма. Анемия средней степени тяжести. Диагноз выставлен в 2016 г. В течение заболевания периодические обострения до 2–3 раз в год, последнее обострение с июня 2019 г. Находилась на госпитализации с 08.07 до 26.09.2019 г. без особой положительной динамики, на суточной дозировке преднизолона: 40 мг/сутки. На рисунке 1 показано состояние до наложения коллагенламиновой матрицы. В июле и августе проводилось наложение на пораженные участки кожи раневого покрытия NovoSkin, в течение трех недель. На рисунке 2 показано начало эпителиза-ции от 19.07.19 г. после наложения коллагенламиновой матрицы, на рисунке 3 повторное наложение коллагенламиновой матрицы от 23.07.2019 г., на рисунке 4 показан результат на 2-й день наложения коллагенламиновой матрицы.
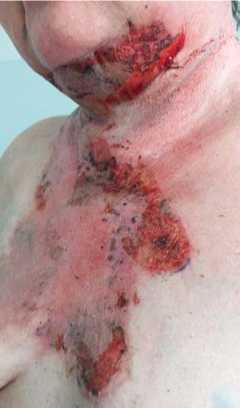
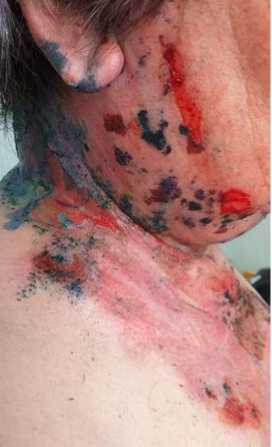
Рис. 1. До наложения коллагенламиновой матрицы
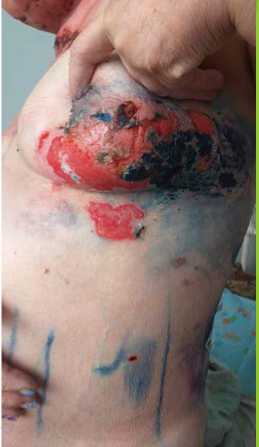
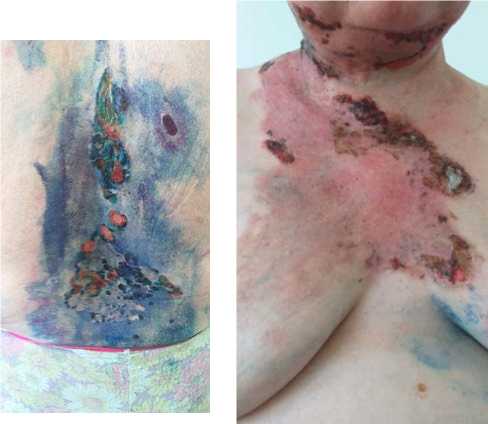
Рис. 2. На 3-й день после наложения коллагенламиновой матрицы
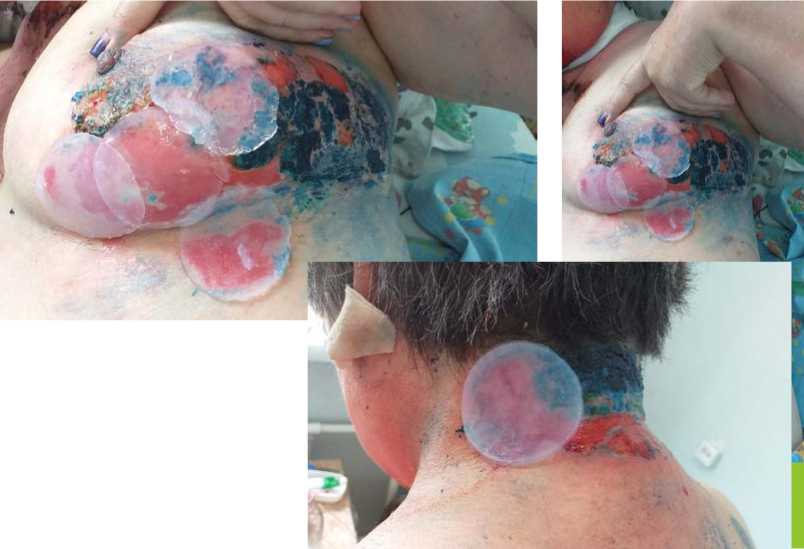
Рис. 3. Повторное наложение коллагенламиновой матрицы
В. П. Саганов, Ю. С. Балханов, Е. Б. Эрдынеева, А. В. Бодоев, Т. Ю. Синицына. Раневое покрытие й
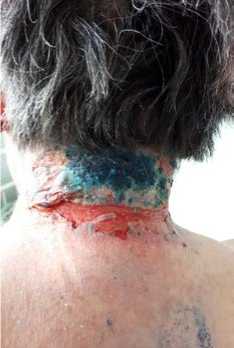
Рис. 4. На 2-й день после повторного наложения коллагенламиновой матрицы
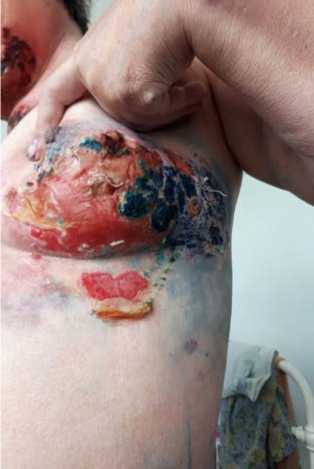
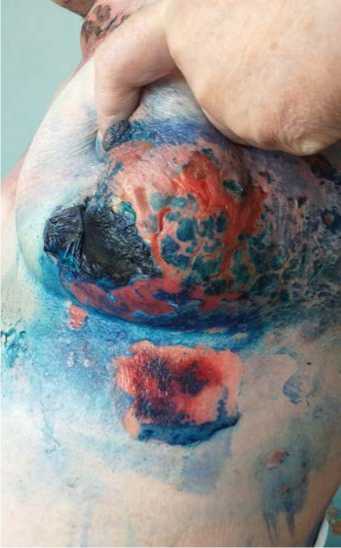
Рис. 5. На 7-й день повторного наложения коллагенламиновой матрицы
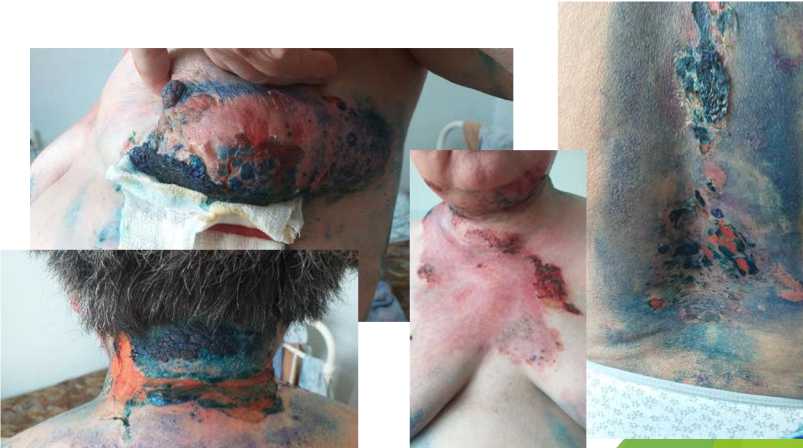
Рис. 6. На 11-й день после повторного наложения коллагенламиновой матрицы
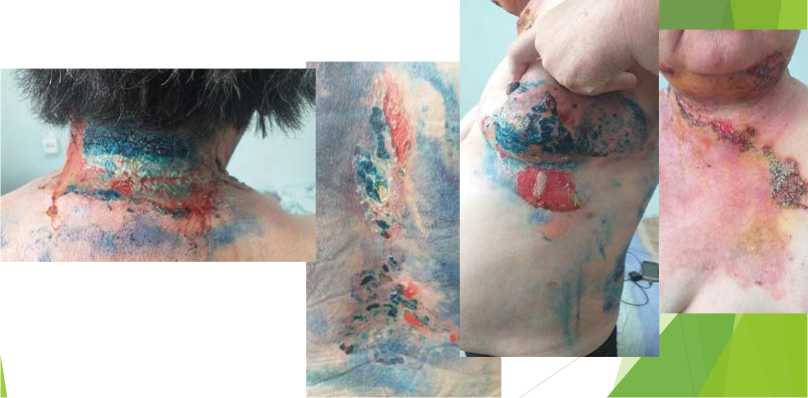
Рис. 7. На 17-й день после повторного наложения коллагенламиновой матрицы
На рисунке 5 показан результат на 7-й день наложения повязки. На рисунке 6 результат эпителизации от 02.08.2019 г., на 11-й день наложения повязки, на рисунке 7 — результат от 08.08.2019 г., на 17-й день наложения повязки.
Через две недели произошла практически полная эпителизация раневой поверхности. В ходе лечения произошло уменьшение дозировки преднизолона до 10 мг/сутки.
Заключение
Нами получены результаты по заживлению поврежденных участков кожи, которые свидетельствуют о том, что создана новая репаративная тканеинженерная конструкция, обладающая эффективностью и высокой скоростью заживления ран, благодаря целенаправленному росту регенерирующих тканевых структур. Анализируя изложенное, можно отметить, что посредством ламинина и коллагена подтверждается активное положительное влияние на процессы заживления. Разработанный биологический материал и нетоксичная коллагенламининовая композиция направлены на регенерацию раны в комбинации с полимерной подложкой и продуктом синтеза кератиноцитов организма человека, при этом клеточный компонент удален. Новый продукт отличается простым способом изготовления и длительным сроком хранения. Все это позволяет рекомендовать полученную тканеинженерную конструкцию к внедрению в производство.
Список литературы Раневое покрытие на основе коллагенламиновой матрицы
- Погодин И. Е., Кулакова К. В. Применение разработанных коллагенсодержащих пленочных покрытий для восстановления кожного покрова при поверхностных ожогах // Кубанский научный медицинский вестник. 2016. № 6(1361). С. 102. Текст: непосредственный.
- Биологические свойства пленок из регенерированного фиброина шелка / Л. А. Сафонова, М. М. Боброва, О. И. Агапова [и др.] // Современные технологии в медицине. 2015. Т. 7, № 3. С. 6-14. Текст: непосредственный.
- Шагидулин М. Ю., Онищенко Н. А., Крашенинников М. Е. Трансплантация гепатоцитов как метод лечения почечной недостаточности: экспериментальный и клинический опыт // Вестник трансплантологиии искусственных органов. 2010. № 12(4). С. 53-60. URL: https://doi.org/10.15825/1995-1191-2010-4-53-60. Текст: электронный.
- Баранов Е., Буравский А., Третьяк С. Лечение трофических язв с использованием цветодиодной фототерапиии стволовых клеток // Наука и инновации. 2019. № 2. С. 70-75. URL: https://doi.org/10.29235/1818-9857-2019-2-70-75. Текст: электронный.
- Новые биорезорбируемые микроносители на основе фиброина шелка / О. И. Агапова, Д. А. Куликов, А. В. Куликов [и др.] // Бюллетень экспериментальной биологии и медицины. 2015. Т. 16. № 10. С. 497-502. Текст: непосредственный.
- Клеточные технологии и тканевая инженерия в лечении длительно незаживающих ран / Ю. С. Винник, А. Б. Салмина, А. И. Дробушевская, О. В. Теплякова // Вестник экспериментальной и клинической хирургии. 2011. Т. 4, № 2. С. 392-394. Текст: непосредственный.
- Культуры клеток в заместительной терапии. Биопрепараты. Профилактика, диагностика, лечение / Е. М. Петручук, Н. В. Шалунова, Ю. В. Олефир [и др.]. 2017. № 17(4). С. 197-206. Текст: непосредственный.
- Дремина Н. Н., Трухан И. С., Шурыгина И. А. Клеточные технологии в травматологии: от клетки до тканевой инженерии // Acta Biomedica Scientifica (East Siberian Biomedical Journal). 2020. № 5(6). С. 66-76. Текст: непосредственный.
- Tissue-engineered skin constructs and application of stem cells for creation of skin equivalents (review) / A. V. Meleshina, A. S. Bystrova, O. S. Rogovaya at al. // Sovremennyetehnologii v medicine. 2017. Vol. 9(1). P. 198-218.
- Применение клеточных технологий в комплексном лечении незаживающих трофических язв нижних конечностей / И. В. Гилевич, Э. Н. Шубров, С. Б. Богданов [и др.] // Пластическая хирургия и эстетическая медицина. 2020. № 3. С. 53-60. Текст: непосредственный.
- Использование клеточных технологий для восстановления повреждений кожи при ожоговой травме / Д. Я. Алейник, В. Л. Зорин, И. И. Еремин [и др.] // Современные проблемы науки и образования. 2015. № 4. С. 84-86. Текст: непосредственный.


