Ранние предикторы развития затяжного плеврального выпота после лобэктомии: проспективное исследование
Автор: Шагдалеев Р.Ф., Власов А.П.
Журнал: Московский хирургический журнал @mossj
Рубрика: Онкология
Статья в выпуске: 1 (95), 2026 года.
Бесплатный доступ
Цель. Определить ранние клинико-функциональные и плевральные предикторы развития затяжного плеврального выпота (ЗПВ) у пациентов после лобэктомии и оценить их прогностическую значимость. Материалы и методы. Проведено проспективное одноцентровое исследование, включившее 168 пациентов, перенесших лобэктомию с системной медиастинальной лимфодиссекцией в ГУЗ «Областной онкологический диспансер» г. Ульяновска в период с 01.06.2024 по 01.11.2025. В анализ включены клинико-демографические данные, показатели функции внешнего дыхания, результаты общего и биохимического анализа крови, а также характеристики плевральной жидкости на 2-е и 4–5-е сутки после операции. ЗПВ определяли при сохранении плеврального дренажа более 5 суток при отсутствии признаков гнойно-воспалительных осложнений. Статистический анализ выполняли с использованием логистической регрессии и ROC-анализа. Полученные результаты. Частота развития ЗПВ составила 29,2 % (49/168). По данным статистического анализа с риском ЗПВ ассоциировались больший рост пациента (p=0,012), курение (p=0,002), более высокие значения ПОС и ФЖЕЛ (%), а также повышенный уровень белка, нейтрофилов, лимфоцитов и объёма плеврального отделяемого на 2-е сутки (p<0,001). В многофакторной модели независимыми предикторами ЗПВ стали: абсолютное количество нейтрофилов в плевральной жидкости на 2-е сутки (AOR=1,94), концентрация белка плеврального экссудата (AOR=1,082), факт курения (AOR=2,92), ФЖЕЛ (%) (AOR=1,021), при этом наличие атеросклероза сосудов нижних конечностей ассоциировалось со снижением риска ЗПВ (AOR=0,34). Построенная модель продемонстрировала высокую прогностическую точность (AUC=0,832; 95 % ДИ: 0,756–0,908; чувствительность 70,8 %; специфичность 83,6 %). Выводы. Затяжной плевральный выпот после лобэктомии развивался почти у трети пациентов и тесно связан с ранними признаками воспалительно-экссудативного ответа в плевральной полости, а также с курением и функциональными особенностями дыхательной системы. Оценка состава плевральной жидкости и ключевых клинических параметров уже на 2-е сутки после операции позволяет надёжно стратифицировать риск ЗПВ и индивидуализировать послеоперационную тактику дренирования и наблюдения.
Лобэктомия, затяжной плевральный выпот, прогностические факторы, логистическая регрессия
Короткий адрес: https://sciup.org/142247250
IDR: 142247250 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2026-1-132-139
Early predictors of prolonged pleural effusion after lobectomy: a prospective study
Introduction. To identify early clinical, functional and pleural predictors of prolonged pleural effusion (PPE) after lobectomy and to assess their prognostic value. Materials and methods. This prospective single-centre study included 168 patients who underwent lobectomy with systematic mediastinal lymph node dissection at the Ulyanovsk Regional Oncology Dispensary between 1 June 2024 and 1 November 2025. Clinical and demographic data, pulmonary function parameters, complete blood count and biochemical markers, as well as pleural fluid characteristics on postoperative days 2 and 4–5 were analysed. PPE was defined as the need to maintain a pleural drain for more than 5 days in the absence of purulent complications. Logistic regression and ROC analysis were used for statistical assessment. Results. The incidence of PPE was 29,2 % (49/168). In univariate analysis, taller height (p=0,012), smoking (p=0,002), higher peak expiratory flow (PEF) and forced vital capacity (FVC, % predicted), as well as increased pleural protein, neutrophil and lymphocyte counts and higher pleural fluid volume on day 2 (all p<0,001) were associated with PPE. In multivariable logistic regression, independent predictors of PPE were pleural neutrophil count on day 2 (AOR=1,94), pleural protein concentration (AOR=1,082), smoking (AOR=2,92) and FVC (% predicted) (AOR=1,021), whereas peripheral lower limb atherosclerosis was associated with a reduced risk of PPE (AOR=0,34). The resulting model demonstrated high discriminative ability (AUC=0,832; 95 % CI: 0,756–0,908; sensitivity 70,8 %; specificity 83,6 %). Conclusion. Prolonged pleural effusion after lobectomy occurs in nearly one-third of patients and is strongly related to early markers of inflammatory exudative response in the pleural space, smoking status and functional respiratory characteristics. Early assessment of pleural fluid composition and key clinical parameters on postoperative day 2 allows reliable risk stratification for PPE and may guide individualized postoperative drainage management and clinical surveillance.
Текст научной статьи Ранние предикторы развития затяжного плеврального выпота после лобэктомии: проспективное исследование
Затяжной плевральный выпот (ЗПВ) остаётся одним из частых и клинически значимых осложнений после анатомических резекций лёгкого. По данным современных исследований, после анатомических резекций по поводу рака лёгкого доля пациентов с послеоперационным плевральным выпотом достигает нескольких процентов (около 3,8 % среди всех послеоперационных осложнений), при этом именно «крупный» выпот (например, >400 мл/сут на 2-е сутки) встречается примерно у четверти пациентов после лобэктомии и нередко задерживает удаление дренажей, продлевая сроки госпитализации [1, 2]. Затяжной выпот ассоциируется с повышенным риском инфекционных осложнений и может соседствовать с остаточным плевральным пространством и/или персистирующей утечкой воздуха, что усугубляет послеоперационное восстановление и функциональные исходы лёгкого [3, 4]. На этом фоне актуальна разработка валидированных прогностических моделей, позволяющих раннее выявление пациентов высокого риска и персонификацию послеоперационной тактики дренирования, респираторной поддержки и наблюдения [5, 6].
Предикторы затяжного плеврального выпота гетерогенны и отражают как предоперационный функциональный резерв лёгких, так и выраженность послеоперационного воспаления и особенности анатомической резекции. В предшествующих работах показана связь возраста, ХОБЛ (хронической обструктивной болезни легких) и локализации/объёма резекции (в т.ч. нижнедолевой лобэктомии) с риском значимого выпота на 2-е сутки, а сниженные показатели дыхательной функции (например, ОФВ1<40 % предсказанного) и активное курение ассоциированы с более высокими частотами послеоперационных лёгочных осложнений [2, 7]. Ранние биомаркеры плеврального воспаления – повышение белка и содержания нейтрофилов в плевральной жидкости – физиологически отражают преобладание экссудативного компонента по критериям Light и дисбаланс фильтрации/резорбции по Старлингу и лимфатического дренажа плевры, что может поддерживать персистирование выпота [8].
Поскольку критериев затяжного плеврального выпота в настоящее время так же не существует, рядом авторов опытным путем принято считать, что его пороговым значением являются 5 сутки, а диапазон нахождения дренажа в плевральной полости может варьировать от 3 до 15 суток при отсутствии гнойно-воспалительных осложнений [9, 10].
Настоящее исследование выполнено с целью выявления предикторов развития затяжного плеврального выпота после лобэктомии.
Материалы и методы
Проведён статистический анализ проспективной базы данных 168 пациентов, перенесших лобэктомию по поводу рака лёгкого в ГУЗ «Областной онкологический диспансер» г. Ульяновска в период с 01.06.2024 по 01.11.2025.
Критерии включения в исследовани е:
-
1. Выполненная лобэктомия с системной медиастинальной лимфодиссекцией.
-
2. Сохранение герметичности лёгочной ткани в течение первых 24 часов после операции.
-
3. Полное расправление лёгкого по данным рентгенографии органов грудной клетки в первые 24 часа после операции.
-
4. Отсутствие инфицированного плеврального выпота.
-
5. Отсутствие хилоторакса.
Критерии исключения:
-
1. Отсутствие герметичности по дренажу в течение 24 часов после лобэктомии.
-
2. Цитологически верифицированный злокачественный плеврит.
-
3. Наличие в анамнезе хирургических вмешательств на органах грудной клетки.
-
4. Необходимость повторного вмешательства в раннем послеоперационном периоде (реторакоскопия, реторакотомия).
Стадирование опухолевого процесса осуществляли в соответствии с классификацией TNM 8-го пересмотра, утверждённой Международным союзом по борьбе с раком (UICC).
Для оценки воспалительных изменений выполнялись следующие исследования:
-
1. В общем анализе крови определяли: количество лейкоцитов, уровень гемоглобина, число нейтрофилов и лимфоцитов, а также количество тромбоцитов.
-
2. Рассчитывали нейтрофильно-лимфоцитарный индекс (НЛИ) и тромбоцитарно-лимфоцитарный индекс (ТЛИ). Эти показатели оценивались до операции, а также на 1-е и 4–5-е сутки после хирургического вмешательства.
-
3. В биохимическом анализе крови измеряли концентрацию общего белка, креатинина, мочевины, С-реактивного белка и фибриногена. Исследования проводились до операции, а также на 1-е и 4–5-е сутки после неё.
-
4. В плевральной жидкости на 2-е и 4–5-е сутки после операции определяли: уровень общего белка, количество лейкоцитов и нейтрофилов. Объём плеврального отделяемого фиксировали на 2-е, 4–5-е сутки и в день удаления дренажа.
Послеоперационное ведение плевральной полости.
Все пациенты проходили плановое предоперационное обследование в соответствии с рекомендациями Ассоциации онкологов России (АОР).
Видео-ассистированная лобэктомия выполнялась из многопортового доступа. Торакотомия осуществлялась стандартно – в 4-м или 5-м межреберье (боковой или переднебоковой доступ). Плевральная полость дренировалась одним дренажом, который устанавливался в 8-е межреберье по задней подмышечной линии с проведением в купол плевральной полости. Дренирование осуществляли по методу Бюлау без применения активной аспирации с первых суток.
Ежедневно регистрировали объём плеврального отделяемого по дренажу. Рентгенографию органов грудной клетки выполняли в первые сутки после операции, а далее – по клиническим показаниям. Состав плевральной жидкости анализировали на 2-е и 4–5-е сутки, либо в день удаления дренажа (в зависимости от того, какое из событий наступало раньше), с определением количества лейкоцитов, общего белка, числа нейтрофилов и лимфоцитов. Антибактериальная терапия проводилась в соответствии с рекомендациями Совета по контролю антимикробной терапии (СКАТ).
В отделении, где проводилось исследование, действуют стандартизированные критерии удаления плеврального дренажа, которые были соблюдены у всех включённых пациентов:
-
• полное расправление лёгкого по данным рентгенографии органов грудной клетки на 1-е сутки после операции;
-
• отсутствие сброса воздуха по дренажу;
-
• суточный объём плеврального отделяемого не более 100 мл к моменту планируемого удаления дренажа.
Анализ статистических данных.
Сравнение долей при анализе четырёхпольных таблиц сопряжённости проводилось с использованием критерия χ² Пирсона (при ожидаемых частотах более 10) или точного критерия Фишера (при ожидаемых частотах менее 10).
Построение прогностической модели вероятности развития исхода осуществляли методом логистической регрессии. В качестве меры объяснённой вариабельности модели использовали коэффициент R² Найджелкерка. Для оценки диагностической значимости количественных признаков при прогнозировании исхода применялся ROC-анализ; оптимальное пороговое значение (cut-off) определяли по максимальному значению индекса Юдена.
Все статистические расчёты выполнялись с использованием программного обеспечения StatTech v. 4.04 (ООО «Статтех», Россия).
Результаты
Частота развития ЗПВ у пациентов после лобэктомии в нашем исследовании составила 29,2 % (49/168).
Основные клинические параметры исследуемых пациентов представлены в таблице 1.
Таблица 1
Клинические характеристики пациентов в зависимости от наличия затяжного плеврального выпота
Clinical characteristics of patients depending on the presence of prolonged pleural effusion
Table 1
|
Показатель / Variable |
Без затяжного выпота / Without prolonged pleural effusion (n = 119) |
С затяжным выпотом / With prolonged pleural effusion (n = 49) |
p |
|
|
Рост, см / Height, cm (Me, Q1–Q3) |
169 (162–173,5) |
175 (165–178) |
0,012 |
|
|
Пол/ Sex |
Мужской/ Male |
71 (59,7 %) |
37 (75,5 %) |
0,051 |
|
Женский/ Female |
48 (60,3 %) |
12 (24,5 %) |
||
|
ХОБЛ / COPD, n (%) |
Да / Yes |
9 (7,6 %) |
9 (18,4 %) |
0,054 |
|
Нет / No |
110 (92,4 %) |
40 (81,6 %) |
||
|
Сахарный диабет / Diabetes mellitus, n (%) |
Да / Yes |
14 (11,8 %) |
2 (4,1 %) |
0,155 |
|
Нет / No |
105 (98,2 %) |
47 (95,9 %) |
||
|
Курение (активное/в анамнезе) / Smoking (current or former), n (%) |
Да / Yes |
49 (41,2 %) |
33 (67,3 %) |
0,002 |
|
Нет / No |
70 (38,8 %) |
16 (32,7 %) |
||
|
Ожирение / Obesity, n (%) |
Да / Yes |
46 (38,7 %) |
18 (36,7 %) |
0,816 |
|
Нет / No |
73 (61,3 %) |
31 (63,3 %) |
||
По результатам статистического анализа клинических параметров исследуемых пациентов были определены следующие значимые предикторы: рост (p=0,012), курение (p=0,002).
Показатели функции внешнего дыхания представлены в таблице 2.
Таблица 2
Показатели функции внешнего дыхания в зависимости от наличия выпота
Table 2
Pulmonary function parameters depending on the presence of pleural effusion
|
Показатель / Parameter |
Без выпота / Without effusion (Me, Q1–Q3) |
С выпотом / With effusion (Me, Q1–Q3) |
p |
|
ОФВ1 / FEV₁ (n) |
2,33 (1,06–3,72) |
2,61 (1,96–2,95) |
0,517 |
|
ОФВ1 / FEV₁ (%) |
83 (70–98) |
80 (65–91) |
0,247 |
|
Индекс Тиффно / Tiffeneau index (%) |
92 (77–95) |
79 (75–95) |
0,184 |
|
ПОС / PEF (n) |
5,06 (2–12) |
8,23 (3,48–12) |
0,019 |
|
ПОС / PEF (%) |
75,6 (58–96,5) |
82 (49,2–92) |
0,834 |
|
ЖЕЛ / VC (n) |
3,06 (2–7) |
3,55 (2,6–3,9) |
0,872 |
|
ЖЕЛ / VC (%) |
80,0 (61–95,1) |
79,0 (73–94) |
0,514 |
|
ФЖЕЛ / FVC (n) |
2,76 (2–7) |
3,27 (2,52–3,76) |
0,450 |
|
ФЖЕЛ / FVC (%) |
77 (62,3–95) |
94 (81,7–103) |
<0,001 |
Из представленных показателей достоверно различались значения ПОС (n) (p=0,019) и ФЖЕЛ (%) (p<0,001).
Основные лабораторные параметры плевральной жидкости исследуемых пациентов на 2 сутки представлены в таблице 3.
Таблица 3
Клинические характеристики пациентов в зависимости от наличия затяжного плеврального выпота
Clinical characteristics of patients depending on the presence of prolonged pleural effusion
Table 3
|
Показатель / Parameter |
Без выпота / Without prolonged effusion (Me, Q1–Q3) |
С выпотом / With prolonged effusion (Me, Q1–Q3) |
p |
|
Белок плевральный, г/л / Pleural protein, g/L |
24,56 (18,81–29,84) |
28,80 (24,73–30,24) |
<0,001 |
|
Ne# плевральный, ×10⁹/л / Pleural neutrophils, ×10⁹/L |
0,31 (0,06–0,76) |
2,50 (0,24–3,00) |
<0,001 |
|
Ne % / Neutrophils %, |
44,22 (35,7–64,6) |
62,9 (56–67,3) |
0,002 |
|
Лимфоциты / Lymphocytes, ×10⁹/л |
0,32 (0,03–0,54) |
0,70 (0,50–1,50) |
<0,001 |
|
Лимфоциты / Lymphocytes, % |
44,0 (29,1–54,1) |
25,8 (22–34) |
0,001 |
|
Объём плеврального отделяемого, мл / Pleural fluid volume, mL |
200 (111–285) |
300 (250–400) |
<0,001 |
На 2-е сутки у пациентов с выпотом отмечалось повышение уровня белка (p<0,001) и нейтрофильного компонента в плевральной жидкости (p<0,001), а также количество лимфоцитов в выпоте (p<0,001) и увеличенный объем плевральной жидкости (p<0,001), что указывает на воспалительно-экссудативный характер выпота.
При проведении многофакторного статистического анализа была разработана модель логистической регрессии, представленная в таблице 4.
Таблица 4 Прогностическая модель развития затяжного плеврального выпота
Table 4
Clinical characteristics of patients depending on the presence of prolonged pleural effusion
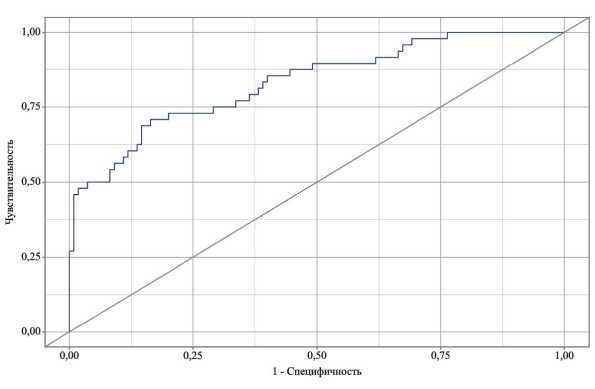
Рис. 1. ROC-кривая модели логистической регрессии
Fig 1. ROC Curve of the Logistic Regression Model
|
Предиктор / Predictor |
COR (95 % ДИ) |
p |
AOR (95 % ДИ) |
p |
|
Ne# плеврал 2 сут / Pleural neutrophil count on day 2 |
1,97 (1,50–2,60) |
<0,001 |
1,94 (1,43–2,64) |
<0,001 |
|
Белок плевральный 2 сут, г/л / Pleural protein on day 2, g/L |
1,085 (1,04–1,14) |
0,001 |
1,082 (1,03–1,14) |
0,004 |
|
Курение (да) / Smoking (yes) |
2,78 (1,37–5,66) |
0,005 |
2,92 (1,23–6,90) |
0,015 |
|
Атеросклероз сосудов ног (да) / Lower limb atherosclerosis (yes) |
0,39 (0,17–0,88) |
0,024 |
0,34 (0,12–0,92) |
0,034 |
|
ФЖЕЛ / FVC (%) |
1,023 (1,008–1,039) |
0,003 |
1,021 (1,003–1,040) |
0,020 |
Площадь ROC-кривой полученной модели составила 0,83, представлена на рисунке 1
Оценка вероятности P является статистически значимым предиктором выпота (AUC = 0,832; 95 % ДИ: 0,756 – 0,908, p < 0,001). Чувствительность и специфичность полученной прогностической модели составили 70,8 % и 83,6 %, соответственно. Необходимо отметить, что наличие атеросклероза сосудов нижних конечностей оказалось независимым фактором снижения риска выпота.
Обсуждение
В нашем анализе затяжной плевральный выпот после лобэктомии ассоциировался, прежде всего, с ранними характеристиками плеврального экссудата: повышением концентрации белка и количества нейтрофилов в плевральной жидкости на 2-е сутки, а также с большим суточным объёмом плеврального отделяемого. Такое «воспалительно-экссудативное» поведение полости согласуется с классическими критериями Light и современными представлениями о балансе фильтрации и резорбции по Старлингу в пострезекционном остаточном пространстве. В обзорах по физиологии плевры после резекций подчёркивается, что при повышенной проницаемости сосудистой/плевральной поверхности формируется устойчивый градиент, поддерживающий накопление жидкости; ранняя высокая дренажная продукция отражает именно этот сдвиг баланса. Концепция использования объёма дренажной жидкости (порог ~400 мл/сут на 2-е сутки) как предиктора «крупного» выпота уже применялась при построении аггрегированных шкал риска после лобэктомии и подтверждала клиническую значимость ранней экссудации для задержки удаления дренажей и увеличения сроков госпитализации [2, 11].
Выявленная связь более высокого роста пациента с большей вероятностью ЗПВ заслуживает отдельного комментария. Абсолютные лёгочные объёмы (ФЖЕЛ/ЖЕЛ, ОФВ₁) физиологически возрастают с ростом, что отражено в уравнениях GLI 2012 и других референсных рядах; даже небольшое увеличение роста на 1 % повышает предсказанные ОФВ₁/ ФЖЕЛ на ~1–3 % в популяционных моделях. Лица большего роста имеют большую площадь париетальной и висцеральной плевры; при равном уровне воспалительного стресса это может увеличивать суммарный фильтрационный поток в плевральную полость и, как следствие, объём отделяемого на ранних сроках, что косвенно продлевает сроки дренирования. Такое механистическое объяснение согласуется с данными по плевральной механике после резекций: объём «остаточного» плеврального пространства и способность остаточной легочной ткани к расправлению определяют баланс между фильтрацией и лимфатической резорбцией [12].
Интерпретация спирометрических показателей требует учёта антропометрии. В нашей когорте абсолютные значения ОФВ₁ (л) и ФЖЕЛ (л) у пациентов с ЗПВ были несколько выше, что, вероятно, связано с бóльшим средним ростом в этой группе; при корректировке на референсные величины различия по ОФВ₁ (%) нивелировались, тогда как ФЖЕЛ (%) сохранила связь с риском осложнения. Это согласуется с тем, что предсказуемые значения объёмов лёгких пропорциональны росту и возрастают как степенная функция длины тела; использование процентa от должного снижает искажение, связанное с антропометрией, и лучше отражает функциональный резерв дыхания, релевантный исходам после резекции лёгкого [13].
Курение в нашей модели осталось самостоятельным фактором риска ЗПВ. Патофизиологически табачный дым поддерживает хроническое воспаление и эндотелиальную дисфункцию, усиливая проницаемость сосудистой стенки и склонность к экссудации; у пациентов, продолжающих курить к моменту операции, частота послеоперационных лёгочных осложнений и длительность госпитализации выше, чем у некурящих или бросивших курить заранее. Это коррелирует с выводами проспективных и ретроспективных исследований по торакальной хирургии [14].
Необычно наблюдавшийся обратный эффект диагностиро ванного атеросклероза артерий нижних конечностей (АНК) на риск ЗПВ можно рассматривать как правдоподобную, но пока гипотетическую, модификацию капиллярной фильтрации. Хронический атеросклероз и АНК ассоциированы с системной эндотелиальной дисфункцией и уменьшением капиллярной плотности в тканях конечностей; сходные феномены описаны и при коронарной микрососудистой дисфункции. Теоретически более жёсткая, менее проницаемая микрососудистая сеть может снижать конвективную фильтрацию через плевру и ограничивать объём пострезекционного экссудата — что согласуется с современными представлениями о роли воспаления и эндотелия в атеро-генезе. Альтернативно, у больных с атеросклерозом сосудов чаще применяется рестриктивная инфузионная тактика и более ранняя диуретическая поддержка, что снижает гидростатическую нагрузку на плевру. Эти механистические объяснения требуют проспективной проверки на большем количестве исследуемых, но направление поиска подтверждается данными фундаментальных и клинических обзоров по атеросклерозу и микрососудистой дисфункции [15].
Таким образом, немногочисленные исследования по поиску предикторов затяжного плеврального выпота после лобэктомии подтверждают значимое влияние воспалительного компонента и изменение проницаемости плевры на развитие данного осложнения, а также выявляет новые, ранее не обнаруживаемые маркеры.
Выводы
Затяжной плевральный выпот отмечен почти у трети пациентов после лобэктомии (29,2 %) и ассоциирован с выраженным воспалительным ответом в плевральной полости и рядом клинико-функциональных особенностей. Построенная модель логистической регрессии позволяет надёжно стратифицировать риск развития ЗПВ уже в первые 48 часов после операции и может быть использована для индивидуализации послеоперационного ведения, оптимизации тактики дренирования и мониторинга пациентов после лобэктомии.


