Разнообразие микробных сообществ мелководных и прибрежных экосистем озера Байкал в летний период 2021-2022 гг
Автор: Зайцева С.В., Дагурова О.П., Цыренова Д.Д.
Журнал: Природа Внутренней Азии @nature-inner-asia
Рубрика: Биология
Статья в выпуске: 4 (26), 2023 года.
Бесплатный доступ
Структура микробного сообщества мелководных прибрежных участков тесно взаимосвязана с экологическими условиями и гидрохимическими параметрами, а также быстро меняется в ответ на негативные изменения экологического состояния водоемов, определяемые гидрологическими колебаниями. Исследована таксономическая структура микробных сообществ воды прибрежных мелководных участков оз. Байкал в период повышенной водности. На уровне филумов доминировали Proteobacteria, Actinobacteriota, Bacteroidota, Firmicutes, Cyanobacteria, Verrucomicrobiota и Deinococcota, составляя от 98,55 до 99,46 % общего микробного разнообразия. Выявлено значительное сходство таксономического состава микробных сообществ воды прибрежных мелководных участков оз. Байкал в определенные летние месяцы 2021-2022 гг. Сходные микробные сообщества формировались в июне 2021-2022 гг.; в июле 2022 г. на участках Энхалук и Сухая; в августе 2022 г. на участках Горячинск и Сухая.
Микробная экология, озеро байкал, изменение уровня воды, микробное сообщество, гидрохимические параметры озера
Короткий адрес: https://sciup.org/148328094
IDR: 148328094 | УДК: 579.2(517.3) | DOI: 10.18101/2542-0623-2023-4-12-22
Diversity of microbial communities in shallow water and coastal ecosystems of lake Baikal in the summer period of 2021-2022
The article reviews the structure of the microbial community in shallow coastal areas that is closely related to environmental conditions and hydrochemical parameters, and it rapidly transforms in response to negative changes in the ecological state of water bodies, determined by hydrological fluctuations. We have studied the taxonomic structure of microbial communities in the water of shallow coastal areas of Lake Baikal during periods of increased water levels. At the phylum level, Proteobacteria, Actinobacteriota, Bacteroidota, Firmicutes, Cyanobacteria, Verrucomicrobiota, and Deinococcota dominated, accounting for 98.55 to 99.46 % of the total microbial diversity. Significant similarities in the taxonomic composition of microbial communities in the water of shallow coastal areas of Lake Baikal were found in certain summer months of 2021-2022. Similar microbial communities were formed in June 2021/22; in July 2022 at the Enkhaluk and Sukhaya sites; and in August 2022 at the Goryachinsk and Sukhaya sites.
Текст научной статьи Разнообразие микробных сообществ мелководных и прибрежных экосистем озера Байкал в летний период 2021-2022 гг
Влияние изменения уровня воды на микробные сообщества озер — один из наименее исследованных аспектов в знаниях об экологии пресных водоемов. Негативные изменения, связанные с гидрологическими колебаниями, могут оказывать сильное влияние на микробный состав и функционирование микробных сообществ воды и донных отложений и, следовательно, изменять биогеохимические циклы и потоки энергии в экосистеме [Weise et al., 2016; Ren et al., 2019]. Микробное сообщество тесно связано с экологическими условиями и гидрохимическими параметрами, а также способно быстро реагировать на негативные изменения экологического состояния водоемов, связанные с изменчивостью гидрологических и физико-химических характеристик [Li et al., 2017; Liu et al., 2019; Wang et al., 2021]. Прибрежная зона в озерных экосистемах особенно затронута увеличением колебаний уровня воды [Zohary and Ostrovsky, 2011; Evtimova & Donohue 2014] и экологические последствия изменения уровня, вероятно, будут наибольшими именно в мелководных прибрежных зонах [Wantzen et al., 2008]. В прибрежной зоне оз. Байкал особо выделяют заплесковую зону — район побережья, подверженный значительному воздействию ветро-волновой активности [Тимошкин и др. 2011]. Верхней границей зоны на пологом восточном побережье оз. Байкал принято считать границу максимального влияния ветро-волновой активности. Увеличение колебаний уровня воды отражается на гидрохимических и микробиологических показателях качества прибрежных и интерстициальных (воды из лунок) вод заплесковой зоны [Тимошкин и др., 2011]. Мелководные прибрежные участки озер тесно связаны с наземными экосистемами за счет поступления значительного количества аллохтонного органического вещества. На границе раздела суша и вода водный режим в значительной степени контролирует микробную трансформацию углерода и во время эпизодических гидрологических потоков может происходить интенсификация биогеохимических процессов [McClain et al., 2003; Gerull et al., 2011]. Были предложены соответствующие концептуальные схемы воздействия изменений уровня воды на микробные сообщества прибрежной зоны Байкала и выявлены некоторые возможные негативные изменения в структуре микробных сообществ прибрежных экосистем, связанные с гидрологическими колебаниями [Борисова и др., 2022]. Целью данного исследования было определить таксономическое разнообразие микробных сообществ воды мелководных участков оз. Байкал в многоводный период.
Материалы и методы исследования
Исследования были проведены в летние месяцы 2021–2022 гг., которые по значению уровня оз. Байкал характеризуются как многоводный период. Пробы были отобраны на участках восточного побережья с протяженными песчаными пляжами и с характерными гидрологическими и климатическими условиями. Участок у с. Гремячинск — это часть побережья, расположенная вне заливов и бухт в средней котловине оз. Байкал, с условиями, характерными для протяженной части восточного побережья озера. Типичным участком бухт восточного побережья можно рассматривать исследуемый участок у с. Горячинск. Участки у сел Энхалук и Сухая в дельте р. Селенги характерны для дельтовых прибрежных террасных участков. Пробы были отобраны в 1 м от уреза воды. Для проведения молекулярных исследований отбирали пробы воды объемом 1 л, фильтровали через мембранные фильтры (диаметр пор — 0,22 мкм) до забития. Выделение ДНК, создание библиотек ДНК для секвенирования согласно рекомендациям Illumina Sample Preparation Guide и секвенирование на платформе MiSeq («Illumina», США) проводились на оборудовании центра коллективного пользования «Геномные технологии, протеомика и клеточная биология» федерального государственного бюджетного учреждения «Всероссийский НИИ сельскохозяйственной метеорологии». Для амплификации использовали набор праймеров Ferier_F515: 5’-GTGCCAGCMGCCGCGGTAA-3’ и Ferier_R806: 5’-GGACTACVSGG GTATCTAAT-3’. Для биоинформационного анализа применяли программы QIIME version 1.9.1 и SILVA [Quast et al., 2013].
Статистическую и математическую обработку данных выполняли в программе XLSTAT (Addinsoft, Франция) и пакета программ MatLab (MatWorks, США). Анализ главных координат (PCoA) проводился в пакете MatLab11 с кластеризацией образцов по первым двум главным координатам. Предварительная обработка данных для стандартизации проводилась согласно рекомендациям Zuur et al. [2007]. Относительная численность микробных таксонов суммировалась на уровне филу-мов, классов, семейств и родов и включала только те микробные таксоны, которые представляли >1% общего микробного разнообразия хотя бы в одном образце. Микробные филумы, классы, семейства и рода с относительной численностью <1% во всех образцах были сгруппированы как «другие» соответственно.
Результаты и обсуждение
За последние пять лет уровень оз. Байкал характеризовался значительными перепадами (рис. 1). В 2018–2019 гг. показатели притока были в пределах средней водности [Бычков, Никитин, 2022], однако зимой-весной 2018 г. были отмечены низкие значения уровня в озере 455,73–455,94 м. Внутригодовая амплитуда (dH) превышала допустимые 0,85 м и составляла 1,09 м. В 2019 г. диапазон регулирования 456–457 м ТО соблюдался.
В 2020 г. при среднем годовом притоке, который соответствует обеспеченности 25 % и является верхней границей средней водности или нижней границей многоводного года по классификации Росстата, при высоких притоках в августе и сентябре, несмотря на повышенные расходы через Иркутскую ГЭС, уровень озера повысился до 457,07 м ТО [Бычков, Никитин, 2022]. Затем в 2021 г. наступил многоводный период, средний годовой приток имел обеспеченность 3–4 % и в третьей декаде сентября уровень озера достиг отметки 457,23 м ТО [Бычков, Никитин, 2022]. При этом негативные последствия отмечались как на восточном побережье оз. Байкал, так и в нижнем бьефе Иркутской ГЭС [Плюснин, Перязева, 2022]. В 2022 г. диапазон регулирования по постановлению № 234 [2001] 456–457 м ТО соблюдался.
Таксономическое разнообразие микробных сообществ воды прибрежных мелководных участков в летний период значительно варьировало (рис. 2).
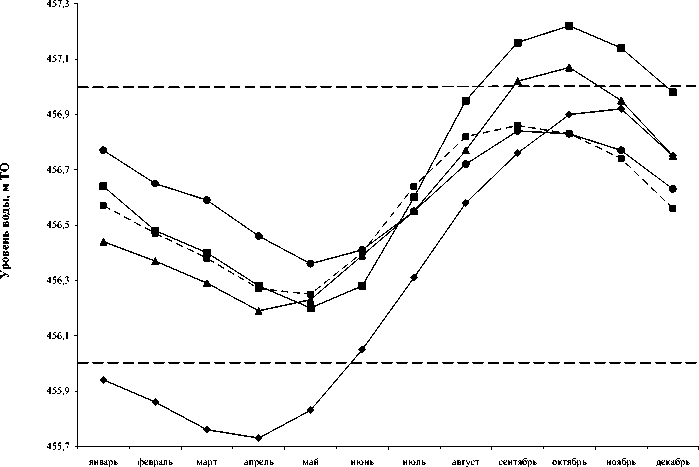
Рис. 1. Динамика изменений уровня оз. Байкал 2018-2022 гг. Представлены данные на первое число каждого месяца. Предельные значения уровня по постановлению № 234 [2001].
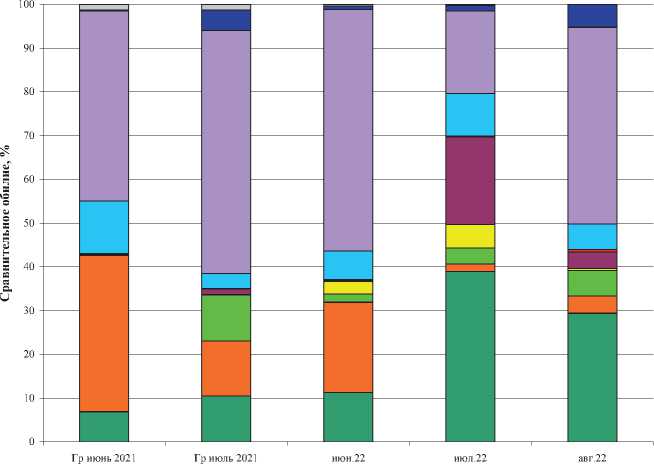
□ Другие
□ Verrucomicrobiota
□ Gammaproteobacteria
□ Alphaproteobacteria
□ Planctomycetota
□ Firmicutes
□ Deinococcota
□ Cyanobacteria
□ Bacteroidota
□ Actinobacteriota
Рис. 2. Таксономическое разнообразие микробных сообществ воды в летний период 2021–2022 гг.
На уровне филумов доминировали Proteobacteria , Actinobacteriota , Bacteroi-dota , Firmicutes , Cyanobacteria , Verrucomicrobiota и Deinococcota (от филума с наибольшей численностью далее по уменьшению), составляя от 98,55 до 99,46 % общего микробного разнообразия. Наиболее представленными среди протеобак-терий были Gammaproteobacteria (19–56 % общего разнообразия). Среди многочисленных представителей этого класса можно выделить семейство Comamona-daceae , которые достигали обилия до 27,5 % в июне 2021 г. Кроме них, в микробных сообществах доминировали гамма-протеобактерии родов Acinetobacter (4–38 %), Pseudomonas (до 17,5 %), Polynucleobacter (до 1,9 %), а в июльских пробах 2021 г. в микробных сообществах отмечено значительное количество (до 3,75 %) неклассифицированных представителей семейства Enterobacteriaceae , что свидетельствует об интенсивном антропогенном влиянии. Из представителей Alphaproteobacteria практически во всех пробах присутствовал р. Sphingomonas , который составлял до 9 % микробного разнообразия в июне 2021 г. Бактерии р. Brevundimonas составляли 10,9 % в микробном сообществе на участке Сухая в июле 2022 г. и 4,7 % на участке Горячинск в конце августа 2022 г. Филум Actinobacteriota в микробных сообществах в 2022 г. был в основном представлен неклассифицированными на уровне рода бактериями семейства Micrococcaceae (2–22 %) и кладой hgcI (0,5–5,5 %). Летом 2021 г. преобладали типичные пресноводные актинобактерии клады hgcI (0,5–5,5 %). Из представителей филума Bacte-roidota доминировали рода: Flavobacterium , Pseudarcicella , Sediminibacterium и Algoriphagus , однако их сравнительное обилие значительно варьировало. Интересно отметить, что в воде в июне 2021 г. отсутствовали представители филума Cyanobacteria , хотя в июльских пробах в составе микробного сообщества доминировали цианобактерии (до 10,5 %), представленные р. Cyanobium PCC-6307. Летом 2022 г. сравнительное обилие цианобактерий варьировало от 1,8 в июне до 6,9 % в августе, достигая максимального разнообразия и обилия в воде у с. Горя-чинск, отмечались токсичные цианобактерии Aphanizomenon NIES81 и Dolicho-spermum NIES41, которые способны формировать обильные цианобактериальные цветения [Cao et al. 2014]. Ранее сообщалось, что представители рода Dolichospermum NIES41 вызывали бурное цветение в литоральных участках в южной части Байкала в июле-августе 2019 г. [Белых и др., 2020].
Альфа-разнообразие микробных сообществ оценивали через индекс разнообразия Шеннона. Микробные сообщества воды мелководных участков были достаточно разнообразными. Индекс Шеннона варьировал от 3,63 до 3,86 летом 2021 г. и от 3,12 до 4,1 в летних пробах 2022 г. Наибольший индекс разнообразия был получен для микробного сообщества у с. Сухая в конце августа 2022 г. Для оценки бета-разнообразия микробных сообществ на уровне родов был проведен анализ главных координат (PCoA) с кластеризацией образцов по первым двум главным координатам. Анализ включал данные по 43 родам бактерий, которые представляли >1% общего микробного разнообразия хотя бы в одном образце (рис. 3).
Бактерии Nocardioides , unclassified_ Micrococcaceae , Exiguobacterium , Marmo-ricola , Phycicoccus , unclassified_ Intrasporangiaceae , Deinococcus и Sediminibacte-rium имели наибольший вклад в распределение по первой главной координате (РСо1). Актинобактерии группы CL500-29 и клады hgcI, веррукомикробии
Luteolibacter , цианобактерии Cyanobium PCC-6307, протеобактерии Comamo-nadaceae , Methylobacterium-Methylorubrum , Acinetobacter и Sphingomonas , а также представители филума Bacteroidota бактерии р. Pseudarcicella и Flavobacterium в большей степени определяли распределение по второй главной координате (РСо2). По результатам проведенного анализа можно сделать заключение о формировании сходных микробных сообществ в прибрежных мелководных участках в определенные летние месяцы: июнь 2021/июнь 2022; в июле 2022 г. на участках Энхалук и Сухая; в августе 2022 г. на участках Горячинск и Сухая; пробы ‘Гремячинск июль 2021’ и ‘Горячинск2 август 2022’ образовывали отдельный кластер на графике главных координат (рис. 3).
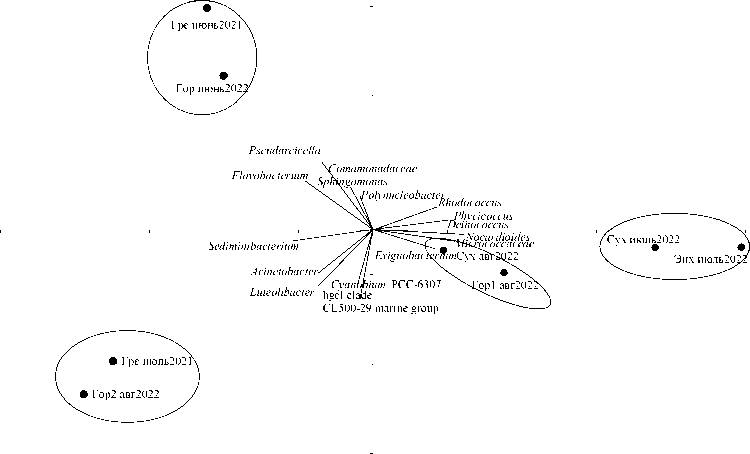
РСо1 28%
Рис. 3. Анализ главных координат (PCoA) с кластеризацией образцов по первым двум главным координатам
Сходный состав микробных сообществ выявлен в июньских пробах прибрежной воды в 2021 г. и 2022 г. Топ 10 таксонов (>1 % сравнительного обилия) в пробе ‘Гремячинск июнь 2021’ составляли unclassified_Comamona-daceae (27,8 %), Flavobacterium (23,4 %), Sphingomonas (9,0 %), Pseudarcicella (9,0 %), Pseudomonas (5,3 %), Acinetobacter (4,1 %), Polynucleobacter (1,9 %), unclassified_Oxalobacteraceae (1,4 %), Methylobacterium-Methylorubrum (1,2 %) и Sediminibacterium (1,2 %). Бактерии семейства Comamonadaceae представлены метаболически разнообразными водными и почвенными микроорганизмами, которые включают аэробных органотрофов, анаэробных денитрификаторов, водородокисляющих и Fe3+-восстанавливающих бактерий, фотоавтотрофных и фотогетеротрофных бактерий [Decleyre et al., 2015] и, возможно, свидетельствуют о распространении почвенных микроорганизмов при изменении гидрологических условий. Большинство Flavobacterium являются хемоорганотрофами и способны использовать сложные органические вещества в качестве источника углерода [Parulekar et al., 2017]. Кроме того, показано разнообразие и высокое обилие Flavobacterium в эвтрофных озерах и выявлены взаимосвязи их распространения с цианобактериальными цветениями и трофностью пресных водоемов [Eiler, Bertilsson 2007; Parulekar et al., 2017; Özbayram et al., 2020]. Flavobacterium (29 %) и бактерии семейства Comamonadaceae (14 %) доминировали в микробном сообществе прибрежной воды в крупном пресном озере Сапанджа (Турция) во время интенсивного цианобактериального цветения [Özbayram et al 2020]. Напротив, бактерии р. Pseudarcicella, которые составляли 9 % микробного разнообразия в прибрежном мелководье оз. Байкал в июне 2021 г., рассматриваются некоторыми исследователями как значимый индикатор благополучного состояния пресноводных экосистем [Li et al., 2017; Salmaso et al., 2018; Guo et al., 2021]. Flavobacte-rium (9,5 %), бактерии семейства Comamonadaceae (6,7 %) и Pseudarcicella (2,2 %) сохраняли свое доминирующее положение и в составе микробного сообщества прибрежной воды оз. Байкал в июне 2022 г. Другими доминирующими таксонами в этой пробе были рода: Acinetobacter (22,6 %), Stenotrophomonas (14,9 %), Comamonas (5,5 %), Empedobacter (4,2 %), unclassified_Enterobacteriaceae (3,7 %), Deinococcus (2,8 %), Methylobacterium-Methylorubrum (2,8 %), Rhodoluna (2,5 %), unclassified_Micrococcaceae (2,2 %), Flectobacillus (1,4 %) и Aphanizomenon NIES81 (1,4 %). Обращает на себя внимание присутствие значительного количества последовательностей, связанных с потенциально токсичными цианобактериями Aphanizomenon NIES81, и доминирование р. Stenotrophomonas, некоторые представители которого способны к деградации микроцистинов, образуемых во время цианобактериального цветения [Yang et al., 2014]. Высокое относительное обилие р. Stenotrophomonas (6,4%) также было определено в пробе ‘Гор2’ в конце августа 2022 г. В оз. Байкал цианобактерии, продуцирующие цианотоксины группы сакситоксина и микроцистина выявляются с 2010 г. в планктоне прибрежной зоны около пос. Турка, в Баргузинском и Чивыркуйском заливах [Belykh et al., 2017]. В планктоне этих мелководных районов выявлены Aphanizomenon flosa-quae, Dolichospermum flosaquae, D. lemmermannii, D. macrosporum, D. solitarium, D. mucosum, D. planctonicum, D. smithii, Gloeotrichia echinulata, Merismopedia sp., Microcystis sp., M. aeruginosa, Chamaesiphon sp., Phormidium sp., Tolypothrix sp. [Белых и др., 2020]. Микроскопический и генетический анализ обрастаний, отобранных в 2014–2017 гг. с различных субстратов, выявил массовое развитие бентосных цианобактерий с доминированием видов Symplocastrum sp., Tychonema sp., Tolypothrix distorta, Pseudanabaena spp., Oscillatoria curviceps, Kamptonema formosum, Leptolyngbya spp., а также содержащие гены синтеза цианотоксинов [Belykh et al., 2017]. Массовое увеличение биомассы фитопланктона в мелководных прибрежных участках, способное оказать существенное влияние на круговорот питательных веществ и устойчивость экосистемы озера Байкал, выявлялось в условиях маловодного периода 2014–2017 гг. [Борисова и др., 2022]. Доминирование цианобактерий в микробных сообществах прибрежной воды оз. Байкал может служить индикатором неблагоприятных изменений при изменении уровня.
Выводы
-
1. Были выявлены особенности таксономического состава бактериальных сообществ мелководных прибрежных участков оз. Байкал в многоводный период. На уровне филумов доминировали Proteobacteria , Actinobacteriota , Bacteroidota , Firmicutes , Cyanobacteria , Verrucomicrobiota и Deinococcota . Среди представителей самого многочисленного класса Gammaproteobacteria можно выделить семейство Comamonadaceae , которые присутствовали во всех образцах и достигали максимума в июне 2021 г. Кроме них, в микробных сообществах доминировали рода Acinetobacter (4–38 %), Flavobacterium (0,3–23,4 %), unclassified_ Micrococcaceae (до 22 %), Exiguobacterium (до 15,5 %), Pseudomonas (до 17,5 %) и Cyanobium PCC-6307 (до 10 %). Альфа-разнообразие микробных сообществ различалось незначительно.
-
2. Важным фактором структуры микробных сообществ воды в период многоводья является значительное количество микроорганизмов семейства Comamona-daceae , занимающих до 27 % общего микробного разнообразия, что, возможно, обусловлено распространением почвенных бактерий в прибрежных мелководных участках при повышении уровня воды.
-
3. Представители филума Cyanobacteria не были выявлены в составе микробного сообщества воды в июне 2021 г. Цианобактерии р. Cyanobium PCC-6307 доминировали (до 10,5 %) в июльских пробах. Летом 2022 г. сравнительное обилие цианобактерий варьировало от 1,8 до 6,9 %, достигая максимального разнообразия и обилия в воде у с. Горячинск, где отмечались токсичные цианобактерии Aphanizomenon NIES81 и Dolichospermum NIES41.
-
4. Выявлено значительное сходство таксономического состава микробных сообществ воды прибрежных мелководных участков оз. Байкал в определенные летние месяцы 2021–2022 гг.
Список литературы Разнообразие микробных сообществ мелководных и прибрежных экосистем озера Байкал в летний период 2021-2022 гг
- Белых О.И., Федорова Г.А., Кузьмин А.В. и др. Микроцистины в цианобактериальных биопленках литорали озера Байкал. Вестник биологических наук Московского университета . 2017 год; 72: 225–231. DOI: 10.3103/S0096392517040022
- Цао Х., Шимура Й., Масанобу К., Инь Й. Проект последовательности генома цианобактерии, образующей токсичное цветение, Aphanizomenon flos-aquae NIES-81. Геномные объявления. 2014 г.; 2(1):e00044-14. DOI: 10.1128/геномA00044-14
- Деклейр Х., Хейлен К., Ван Колен К. и Виллемс А. Диссимиляционное восстановление азота в приливных отложениях устья умеренного пояса: мелкомасштабная гетерогенность и новые восстановители нитрат-аммония. Передний. Микробиол. 2015 г.; 6: 1124. DOI: 10.3389/fmicb.2015.01124.
- Эйлер А., Бертилссон С. Цветение флавобактерий в четырех эвтрофных озерах: связь динамики популяций пресноводного бактериопланктона с наличием ресурсов. Прикладная и экологическая микробиология. 2007 г.; 73: 3511–3518. DOI:10.1128/АЕМ.02534-06
- Евтимова В.В., Донохью И. Количественная оценка экологической реакции на усиленные колебания уровня воды в стоячих водах: экспериментальный подход. Журнал прикладной экологии. 2014 г.; 51: 1282–1291. DOI: 10.1111/1365-2664.12297.
- Герулл Л., Фроссар А., Гесснер М.О., Мутц М. Изменчивость гетеротрофного метаболизма в малых речных коридорах раннего сукцессионного водораздела. Дж. Геофиз. Рез. Биогеология. 2011 г.; 116: Г0201210. DOI: 1029/2010JG001516
- Го Д., Лян Дж., Чен В. и др. Анализ бактериального сообщества двух соседних пресноводных озер, происходящих из одного озера. Пол. Дж. Энвайрон. Стад. 2021 год; 30: 111–117. DOI: 10.15244/pjoes/119094
- Ли З., Лу Л., Го Дж. и др. Реакция пространственно-временной динамики сообщества бактериопланктона на эксплуатацию крупномасштабного водохранилища: пример водохранилища «Три ущелья», Китай. Научный представитель 2017; 7: 42469. DOI: 10.1038/srep42469.
- Лю Дж., Чен Ю., Ли М. и др. Колебания уровня воды являются ключевыми для таксономических сообществ и функциональных групп фитопланктона в озере Поянге. Экол. Индия, 2019 г.; 104: 470–478. DOI: 10.1016/j.ecolind.2019.05.021
- Макклейн М.Э., Бойер Э.В., Дент К.Л. и др. Биогеохимические горячие точки и горячие моменты на стыке наземных и водных экосистем. Экосистемы. 2003 г.; 6: 301–312. DOI: 10.1007/s10021-003-0161-9
- Озбайрам Э.Г., Кокер Л., Акчаалан Р. и др. Состав бактериального сообщества озера Сапанджа во время цветения цианобактерий. Водные науки и инженерия. 2020; 35 (2): 52–56. DOI: 10.26650/ASE2020652073
- Парулекар Н.Н., Колекар П., Дженкинс А. и др. Характеристика бактериального сообщества, связанного с цветением фитопланктона в эвтрофном озере в Южной Норвегии, с использованием анализа последовательности ампликона гена 16S рРНК. ПЛОС ОДИН. 2017 год; 12(3): e0173408. DOI: 10.137/журнал. поне.0173408
- Кваст С., Прюсс Э., Йылмаз П. и др. Проект базы данных генов рибосомальной РНК SILVA: улучшенная обработка данных и веб-инструменты. Нукл. Кислоты Рез. 2013; 41: Д590–Д596.
- Жэнь З., Цюй С., Чжан М., Ю Ю. и Пэн В. Отличительные бактериальные сообщества во влажные и засушливые сезоны во время сезонных колебаний уровня воды в крупнейшем пресноводном озере (озере Поян) в Китае. Передний. Микробиол. 2019 год; 10: 1167. DOI: 10.3389/fmicb.2019.01167.
- Салмазо Н., Альбанезе Д., Капелли К. и др. Разнообразие и циклические сезонные переходы бактериального сообщества большого и глубокого периальпийского озера. Микробная экология. 2018 год; 76: 125–143. DOI: 10.1007/s00248-017-1120-x.
- Ван С., Ян Г., Цзюньцзе Дж. и др. Уровень воды как ключевой контролирующий регулятор, связанный с изменениями питательных веществ и валовой первичной продуктивности в большой пойменно-озерной системе (озеро Поян), Китай. Журнал гидрологии. 2021 год; 599:126414 DOI: 10.1016/j.j Hydrol.2021.126414.
- Ванцен К.М., Ротхаупт К.-О., Мёртл М. и др. Экологические последствия колебаний уровня воды в озерах: актуальная проблема. Гидробиология. 2008 г.; 613: 1–4. DOI: 10.1007/с10750-008-9466-1
- Вайзе Л., Ульрих А., Мореано М. и др. Изменения уровня воды влияют на круговорот углерода и состав микробного сообщества в отложениях озера. ФЭМС Микробиология Экология. 2016 г.; 92(5): fiw035. DOI: 10.1093/femsec/fiw035
- Ян Ф., Чжоу Ю., Инь Л. и др. Микроцистин-деградирующая активность местного бактериального штамма Stenotropomonas acidaminiphila MC-LTH2, выделенного из озера Тайху. ПЛОС ОДИН. 2014 г.; 9(1): e86216. DOI: 10.1371/journal.pone.0086216
- Зохарий Т. и Островский И. Экологические последствия чрезмерных колебаний уровня воды в стратифицированных пресноводных озерах. Внутренние воды. 2011 г.; 1 (1): 47–59. DOI: 10.5268/IW-1.1.406
- Зуур А.Ф., Иено Э.Н., Смит Г.М. Анализ экологических данных. Нью-Йорк: Спрингер, 2007, стр. 672.
- Токсин-продуцирующие цианобактерии в озере Байкал и водоемах Байкальского региона (обзор) / О. И. Белых, И. В. Тихонова, А. В. Кузьмин [и др.] // Теоретические проблемы экологии. 2020. № 1. С.21–27. DOI: 10.25750/1995-4301-2020-1-021-027. Текст: непосредственный.
- Концептуальные схемы изменений уровня озера Байкал на биоту прибрежных экосистем / Н. Г. Борисова, О. А. Аненхонов, С. В. Зайцева [и др.] // География и природный ресурс. 2022. № 5. С. 133–142. DOI: 10.15372/GIPR20220514. Текст: непосредственный.
- Бычков И. В., Никитин В. М. Современные проблемы регулирования уровня озера Байкал // География и природные ресурсы. 2022. № 5. С. 13–24. DOI: 10.15372/ГИПР20220502. Текст: непосредственный.
- Плюснин А. М., Перязева Е. М. Воздействие подъема уровня Байкала на инженерные сооружения прибрежных поселений // География и природные ресурсы. 2022. № 5. С. 74–82. DOI: 10.15372/GIPR20220508ю Текст: непосредственный.
- О предельных значениях уровней воды в озере Байкал при прекращении хозяйственной и иной деятельности: постановление правительства Российской Федерации от 26 марта 2001 г. № 234 // Собрание законодательства РФ. 2001. № 14. 1366 с. Текст: непосредственный.
- Тимошкин О. А., Сутурин А. Н., Бондаренко Н. А. [и др.] Биология прибрежной зоны озера Байкал. Сообщение 1. Заплесковая зона: первые результаты междисциплинарных исследований, направляющих для экосистемы // Изв. Иркут. гос. ун-та. Сер. Биология. Экология. 2011. Т. 4, № 4. С. 75–110. Текст: непосредственный.


