Разработка и получение ДНК-иммуногена на основе генов SARS-СоV-2
Автор: Рябченкова А.А., Чирак Е.Р., Чирак Е.Л., Колмаков Н.Н., Копать В.В., Духовлинов И.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 4 (98) т.85, 2023 года.
Бесплатный доступ
В связи с развитием пандемии и необходимостью массовой вакцинации разработка вакцин нового поколения против коронавирусной инфекции COVID19 является важнейшей задачей медицины и биотехнологии. Ввиду распространенности COVID19, все еще актуально создание безопасной и протективной вакцины, особенно стимулирующей Т-клеточный иммунный ответ. В работе представлены разработка и получение ДНК-иммуногена на основе плазмидной ДНК, кодирующей гибридный белок, содержащий иммуногенные фрагменты структурных белков β-коронавируса SARS-СоV2. В результате методами генной инженерии была создана векторная конструкция на основе плазмидной ДНК, кодирующей гибридный белок, содержащий наиболее иммуногенные участки структурных белков M, S, N, E β-коронавируса SARS-СоV2, для транзиентной экспрессии в клетках млекопитающих; методом электропорации был создан штамм E.coli - продуцент ДНК-иммуногена; разработан метод очистки рекомбинантной плазмидной ДНК на основе последовательного постадийного процесса: данная методика позволила получить 100 мг ДНК-иммуногена рСМV3Таg3а-СVVV3 в растворе с концентрацией 1 мг/мл (100 мл), соответствующих установленным в Государственной Фармакопее РФ (ОФС.1.7.1.0013.18 ДНК-вакцины) параметрам качества - полученный результат стабильно воспроизводится в лабораторных условиях; были отработаны методики контроля качества плазмидной ДНК и проверена экспрессия гибридного белка методом Вестерн-блоттинга. Было показано, что антиген СVVV3 специфически связывается с иммуноглобулинами IgG из кроличьих сывороток после иммунизации ДНК-иммуногеном рСМV3Таg3А-СVVV3. Доля суперспирализованной плазмидной ДНК в образце ДНК-иммуногена рСМV3Таg3а-СVVV3 составила 85,64%, содержание эндотоксинов - менее 25 ЕЭ/мг; концентрация остаточных белков штамма-продуцента в растворе 1 мг/мл ДНК-иммуногена рСМV3Таg3А-СVVV3 составила менее 100нг на 1 мл (мг суммарной рекомбинантной ДНК).
Sars-соv 2, днк-иммуноген, гибридный белок, экспрессия
Короткий адрес: https://sciup.org/140304455
IDR: 140304455 | УДК: 640 | DOI: 10.20914/2310-1202-2023-4-96-101
Development and production of DNA-immunogen based SARS-СоV-2genes
Due to the development of the pandemic and the need for mass vaccination, the development of next-generation vaccines against COVID 19 coronavirus infection is a major challenge for medicine and biotechnology. Due to the prevalence of COVID 19, it is still urgent to develop a safe and protective vaccine, especially one that stimulates T-cell immune response. This work presents the design and production of a DNA immunogen based on plasmid DNA encoding a hybrid protein containing immunogenic fragments of structural proteins of SARS-CoV 2 β-coronavirus. As a result, a vector construct based on plasmid DNA encoding a hybrid protein containing the most immunogenic parts of structural proteins M, S, N, E of SARS-CoV 2 β-coronavirus was created by genetic engineering methods for transient expression in mammalian cells; a strain of E. coli, a producer of DNA-coronavirus β-coronavirus, was created by electroporation. coli, a DNA-immunogen producer; a method of purification of recombinant plasmid DNA was developed on the basis of a sequential step-by-step process: this method allowed to obtain 100 mg of DNA-immunogen pCMV 3Tag 3a-CVVVV3 in a solution with a concentration of 1 mg/mL (100 ml), which corresponds to the concentration established in the State Pharmacopoeia of the Russian Federation (OFS.1.7.1.0013.0013.1). .7.1.0013.18 DNA-vaccines) quality parameters - the obtained result is stably reproduced in laboratory conditions; methods of plasmid DNA quality control were worked out and expression of hybrid protein was tested by Western blotting. The CVVV3 antigen was shown to bind specifically to IgG immunoglobulins from rabbit sera after immunization with pCMV 3Tag 3A-CVVVV3 DNA-immunogen. The proportion of superhelicalized plasmid DNA in the sample of DNA-immunogen pCMV 3Tag 3A-CVVVV3 was 85.64 %, the content of endotoxins was less than 25 U/mg; the concentration of residual proteins of the strain-producer in a solution of 1 mg/ml of DNA-immunogen pCMV 3Tag 3A-CVVVV3 was less than 100ng per 1 ml (mg of total recombinant DNA).
Текст научной статьи Разработка и получение ДНК-иммуногена на основе генов SARS-СоV-2
Возбудителем COVID-19 является бета-коронавирус SARS-СоV-2, распознанный в качестве патогена посредством секвенирования метагеномной РНК и выделения вируса из образцов жидкости бронхоальвеолярного лаважа пациентов с тяжелой пневмонией [10].
За последний год был достигнут огромный прогресс в создании эффективных вакцин против SARS-СоV-2. Согласно предварительному проекту ВОЗ по вакцинам, в настоящее время 172 вакцины-кандидата находятся в стадии доклинической разработки, 63 – в стадии клинической разработки, 6 из которых основаны на технологии плазмидной ДНК [1]. Эти вакцины могут легко производиться бактериями в больших количествах, их производство достаточно просто масштабируется и менее затратно по сравнению с иными вариантами вакцин [4].
На данный момент высказываются опасения по поводу безопасности и эффективности вакцин, разрабатываемых на основе различных технологических платформ. Важно, чтобы на введение вакцины не возникло аутоиммунной перекрестной реактивности за счет присутствия в активных агентах вакцины участков, гомологичных участкам генома человека [8]. Кроме того, предпочтительнее использование вакцин, которые также действенны против мутировавших штаммов нового коронавируса.
Разработанные на данный момент вакцины недостаточно эффективны от мутирующих штаммов, поскольку содержат в себе в том числе неконсервативные последовательности S белка [7]. Поэтому актуальна разработка ДНК-иммуногена, безопасного и активного против мутирующих штаммов SARS-СоV-2.
Цель работы – разработка и получение ДНК-иммуногена на основе плазмидной ДНК, кодирующей иммуногенные фрагменты структурных белков нового β-коронавируса SARS-СоV-2, вызывающего коронавирусную инфекцию 2019 (COVID-19).
Материалы и методы
Полноразмерная последовательность генома базового дикого типа SARS-СоV-2 была получена с сайта NCBI (NC_045512.2). Наиболее иммуногенные (клеточный иммунный ответ) фрагменты структурных белков M, S, N, E SARS-СоV-2 выбрали с помощью программы “СD4 T cell immunogenicity prediction” [2]. Участки белков, содержащие наибольшее количество иммуногенных фрагментов, объединили с помощью полиглициновых линкеров. Выровняли полученную последовательность с помощью BLAST против белков человека, чтобы убедиться в отсутствии сходства. Для экспрессии в эукариотических клетках к гибридной
Синтез гибридной последовательности с последующей вставкой в экспрессионный вектор рСМV-3Таg-3а был произведен на коммерческой основе в компании GenScript (США). Полученную плазмиду рСМV-3Таg-3а-СVVV3 нарабатывали в клетках E. coli DH5 . Подлинность плазмиды подтверждали методом ПЦР, рестрикцией по сайтам клонирования ВаmНI и ХhоI и секвенированием по Сэнгеру.
Выделение плазмидной ДНК из биомассы E. coli осуществляли методом щелочного лизиса. Осадок ДНК растворяли в воде и обрабатывали РНКазой А. Для последующей хроматографической очистки использовали последовательно анионообменную, гидрофобную и вновь анионообменную хроматографию.
Определение доли содержания суперспи-рализованных топоизомеров плазмидной ДНК производили методом высокоэффективной жидкостной хроматографии в градиенте натрия хлорида (Gen-Pak FAX, NP, AXC 4,6⋅100 мм 2,5 мкм, (Waters, США)). Отсутствие РНК проверяли по отсутствию диффузной полосы в области 200–500 пар нуклеотидов в 1% агарозном геле. Определение содержания бактериальных эндотоксинов проводили с помощью ЛАЛ-теста (Pyrotell) согласно рекомендациям производителя. Определение содержания остаточных белков осуществляли методом твердофазного ИФА с помощью набора Cygnus E. coli Host Cell Proteins (Cygnus, № F410, США) согласно инструкции к набору.
Суммарные кроличьи антитела из сывороток крови получали двукратной иммунизацией с интервалом в 2 недели 6 самок кроликов породы Советская Шиншилла внутримышечно (в бедро) 2 мл следующей смеси: плазмидная ДНК – 0,2 мг/мл, полиэтиленимин – 1,2 мг/мл, Sabowax – 2%, глюкоза – 10%, бензиловый спирт – 0,3%. Выделение и очистку антител проводили высаждением насыщенным раствором сульфата аммония.
Наличие специфических антител к гибридному белку СVVV3 определяли с помощью Вестерн-блоттинга с использованием белка СVVV3 в качестве антигена (был наработан в культуре эукариотических клеток НЕК293) и антител, выделенных из сыворотки кроликов. Использовали поликлональные антитела Goat Anti-Rabbit IgG conjugate (HRP) (EMD Millipore Corp, USA), специфичные к линейным участкам белковой молекулы. Образовавшиеся в месте локализации исследуемого белка иммунные комплексы проявлялись с помощью тетраметилбензидина (TMB). Как отрицательный контроль была использована сыворотка кроликов до иммунизации.
Созданная конструкция (рисунок 1), представляет собой ДНК-иммуноген, кодирующий гибридный белок, состоящий из фрагментов основных белков M, S, N и Е коронавируса SARS-СоV-2. Химерный белок, экспрессирующийся в клетках млекопитающих, содержит 424 аминокислоты, имеет прогнозируемую массу 46,5 кДа и рI 9,61, является стабильным и его период полураспада у млекопитающих составляет около 100 часов [3].
В результате лизиса и хроматографической очистки из 1 кг биомассы получили 100 мг ДНК-иммуногена рСМV-3Таg-3а-СVVV3 в растворе с концентрацией 1 мг/мл.
Полученный образец проанализировали согласно ряду критериев, указанных в Государственной Фармакопее РФ (ОФС.1.7.1.0013.18
ДНК-вакцины). Время выхода суперспирализо-ванной изоформы плазмидной ДНК составило 6,26 минут, площадь пика 85,64% (рисунок 2).
Концентрация эндотоксинов в растворе 1 мг/мл составила менее 25,0 ЕЭ на 1 мл, концентрация остаточных белков штамма-продуцента составила менее 100нг на 1 мл. Таким образом, по перечисленным критериям наш ДНК-иммуноген по перечисленным параметрам качества соответствует ГФ РФ.
Из кроличьих сывороток было получено 30 мл суммарных иммуноглобулинов с концентрацией 10 мкгр/мл. Антиген СVVV3, наработанный в линии эукариотических клеток НЕК293, специфически связывается с иммуноглобулинами IgG из кроличьих сывороток после иммунизации ДНК-иммуногеном рСМV-3Таg-3А-СVVV3 (рисунок 3).
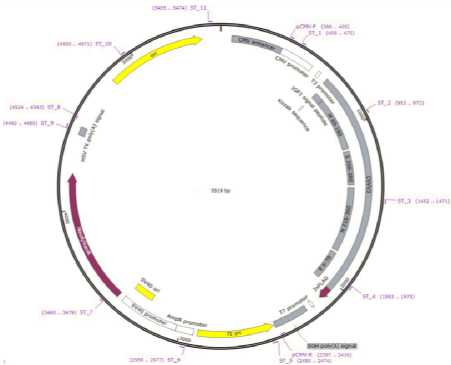
Рисунок 1. Структура плазмиды рСМV-3Таg-3а-СVVV3 с праймерами, необходимыми для секвенирования вектора вместе со вставкой
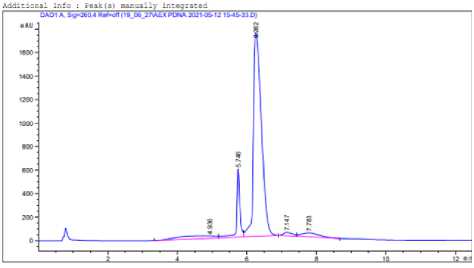
Рисунок 2. Анализ образца рСМV-3Таg-3А-СVVV3 с помощью ВЭЖХ. Суперспирализованная изоформа – пик на 6,26 мин
Figure 1. Structure of plasmid pCMV 3Tag 3a-CVVVV3 with primers required for sequencing the vector together with the insert
Figure 2. Analysis of the pCMV 3Tag 3A-CVVVV3 sample by HPLC. Superspiralized isoform - peak at 6.26 min
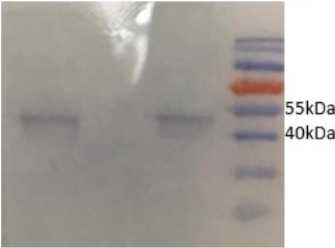
Рисунок 3. Проверка экспрессии гибридного белка методом Вестерн-блоттинга. Образец рекомбинантного белка СVVV3, наработанный в культуре клеток НЕК293, нанесен в двух нагрузках. Source: Составлено авторами
Figure 3. Verification of hybrid protein expression by Western blotting. A sample of recombinant CVVVV3 protein produced in HEK293 cell culture was plated in two loads. Source: Compiled by the authors
Обсуждение
В ходе работы был разработан и очищен ДНК-иммуноген для транзиентной экспрессии в клетках млекопитающих, содержащий иммуногенные участки структурных белков M, S, N, E β-коронавируса SARS-СоV-2.
Также была подтверждена экспрессия закодированного в нём рекомбинантного белка СVVV3 в клетках млекопитающих. Метод Ве-стерн-блоттинга позволил оценить формирование гуморального иммунного ответа на антиген СVVV3 и предварительно оценить его использование для разработки метода, аналогичного иммунофлуоресцентному анализу [4].
Кролики были двукратно иммунизированы рСМV-3Таg-3а-СVVV3 с адъювантным комплексом ПЭИ-Sabowax, поскольку существуют трудности в достижении достаточной иммуногенности ДНК-вакцин [5]. Также возможен вариант интраназальной иммунизации с добавлением адъюванта.
Разработанная технология получения ДНК-иммуногена приводит к выходу 0,1 мг/г, выходы зависят большей частью от процесса ферментации и производственных мощностей [9]. Для наработки большего количества ДНК-иммуногена процесс ферментации будет усовершенствован.
Разработана схожая ДНК-вакцина ZуСоV-D, кодирующая фрагменты S-белка SARS-СоV-2. Кандидатная ДНК-вакцина индуцирует в том числе нейтрализующие антитела и обеспечивает ответ Th-1, о чем свидетельствуют повышенные уровни IFN-γ (Momin, 2021). Дизайн нашего ДНК-иммуногена позволяет прогнозировать схожие данные исследований иммуногенности и безопасности.
post@vestnik-vsuet.ru Заключение
Разработана плазмида рСМV-3Таg-3а-СVVV3, кодирующая гибридный белок, содержащий иммуногенные участки структурных белков M, S, N, E β-коронавируса SARS-СоV-2, для транзиентной экспрессии в клетках млекопитающих. Данный ДНК-иммуноген рассматривается как перспективная кандидатная вакцина против SARS-СоV-2. Методом Вестерн-блоттинга подтверждена экспрессия гибридного белка СVVV3 в клетках млекопитающих. Усиление иммуногенных свойств ДНК-иммуногена рСМV-3Таg-3а-СVVV3 возможно изменением способа введения на интраназальный или внутрикожный. Созданный ДНК-иммуноген отвечает критериям кандидатной вакцины против COVID-19 нового поколений и в дальнейшей работе будет изучена иммуногенность и протективность.
Список литературы Разработка и получение ДНК-иммуногена на основе генов SARS-СоV-2
- Dey A. Immunogenic potential of DNA vaccine candidate, ZyCoV-D against SARS-CoV-2 in animal models // Vaccine. 2021. V. 39. № 30. P. 4108–4116.
- Dhanda S.K. Prediction of HLA CD4 immunogenicity in human populations // Front. Immunol. 2018. V. 9. P. 1369. Пат. № 2747762, RU, A61K 39/215, A61P 31/14, C12Q 1/6806, C07K 16/10, C12N 15/50.
- Вакцина для профилактики или лечения коронавирусной инфекции на основе генетической конструкции / Духовлинов И.В., Федорова Е.А., Колмаков Н.Н., Чирак Е.Л., Алексеев А.В. № 2020112937; Заявл. 05.04.2020; Опубл. 13.05.2021, Бюл. № 14.
- He Q. Development of a Western Blot Assay for Detection of Antibodies against Coronavirus Causing Severe Acute Respiratory Syndrome // Clin. Diagn. Lab. Immunol. 2004. V. 11. № 2. P. 417–422.
- Lee J. Engineering DNA vaccines against infectious diseases // Acta Biomater. 2018. V. 80. P. 31–47.
- Momin Т. Safety and Immunogenicity of a DNA SARS-CoV-2 vaccine (ZyCoV-D): Results of an open-label, non-randomized phase I part of phase I/II clinical study by intradermal route in healthy subjects in India // EClinicalMedicine. 2021. V. 38.
- Rodrigues João P.G.L.M. Insights on cross-species transmission of SARS-CoV-2 from structural modeling // PLoS Comput Biol. 2020. V. 16. № 12.
- Vojdania A., Kharrazianb D. Potential antigenic cross-reactivity between SARS-CoV-2 and human tissue with a possible link to an increase in autoimmune diseases // Clinical Immunology. 2020. V. 217. P. 1–2.
- Williams J.A. Generic plasmid DNA production platform incorporating low metabolic burden seed-stock and fed-batch fermentation processes // Biotechnol Bioeng. 2010. V. 103. № 6. P. 1129–1143.
- Zhao J. Antibody responses to SARS-CoV-2 in patients of novel Antibody responses to SARS-CoV-2 in patients of novel coronavirus disease 2019 // Clin. Infect. Dis. 2020. V. 71. № 16. P. 2027–2034.
- Чащин В.П., Гудков А.Б., Попова О.Н., Одланд Ю.О. и др. Характеристика основных факторов риска нарушений здоровья населения, проживающего на территориях активного природопользования в Арктике // Экология человека. 2014. №. 1. С. 3-12.
- Конторович А.Э., Коржубаев А.Г., Эдер Л.В. Прогноз глобального энергообеспечения: методология, количественные оценки, практические выводы // Минеральные ресурсы России. Экономика и управление. 2006. №. 5. С. 18-27.
- Раскина Т.А., Пирогова О.А., Зобнина О.В., Пинтова, Г.А. Показатели системы остеокластогенеза у мужчин с различными клиническими вариантами анкилозирующего спондилита // Современная ревматология. 2015. Т. 9. №. 2. С. 23-27. doi: 10.14412/1996-7012-2015-2-23-27
- Новиков А.А., Смоленский А.В., Михайлова А.В. Подходы к оценке показателей вариабельности сердечного ритма (обзор литературы) // Вестник новых медицинских технологий. Электронное издание. 2023. Т. 17. №. 3. С. 85-94.
- Абдурахманов Г.М., Лопатин И.К., Исмаилов Ш.И. Основы зоологии и зоогеографии. Москва: Академия, 2001. Кондратьев В.Б. Глобальная фармацевтическая промышленность // Отрасли и сектора глобальной экономики: особенности и тенденции развития. 2015. С. 226-249. URL: http://perspektivy.info/rus/ekob/ globalnaja_farmacevticheskaja_promyshlennost_2011-07-18.html ГОСТ 8.586.5-2005.
- Государственная система обеспечения единства измерений. Измерение расхода и количества жидкостей и газов с помощью стандартных сужающих устройств. М.: Стандартинформ, 2007. Ura T., Yamashita A., Mizuki N., Okuda K. et al. New vaccine production platforms used in developing SARS-CoV-2 vaccine candidates // Vaccine. 2021. V. 39. №. 2. P. 197-201.
- Chavda V.P., Pandya R., Apostolopoulos V. DNA vaccines for SARS-CoV-2: toward third-generation vaccination era // Expert Review of Vaccines. 2021. V. 20. №. 12. P. 1549-1560.
- Borgoyakova M.B., Karpenko L.I., Rudometov A.P., Shanshin D.V. et al. Immunogenic properties of the DNA construct encoding the receptor-binding domain of the SARS-CoV-2 spike protein // Molecular Biology. 2021. V. 55. P. 889-898.


