Разработка критериев оценки риска тяжёлого ишемически-реперфузионного повреждения при трансплантации печени в контексте последующей перфузионной реабилитации
Автор: Новрузбеков М.С., Яремин Б.И., Балкаров А.Г., Казымов Б.И., Свищева П.О., Павлова О.Н., Ханова С.М.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Донорство и трансплантация органов и тканей
Статья в выпуске: 6 т.15, 2025 года.
Бесплатный доступ
Актуальность. Ишемически-реперфузионное повреждение (ИРП) остаётся значимым осложнением после трансплантации печени, ассоциированным с ранней дисфункцией трансплантата и худшими исходами. Прогнозирование риска ИРП могло бы направлять выбор стратегий консервации органов и посттрансплантационного ведения. Цель: разработать и валидировать клиническую систему оценки риска для прогнозирования тяжёлого ИРП при трансплантации печени. Материалы и методы. Ретроспективный анализ 1238 трансплантаций печени, выполненных в НИИ скорой помощи им. Н.В. Склифосовского с 2000 по 2025 год. Тяжёлое ИРП определялось как пиковые значения трансаминаз >1000 МЕ/л в первые 7 суток. Оценивались донорские, процедурные и реципиентные факторы с использованием многофакторной логистической регрессии для создания упрощенной системы оценки риска. Результаты. Полные данные были доступны для 827 пациентов, среди которых зарегистрировано 312 случаев тяжёлого ИРП, что составило 37,7% когорты. Независимыми предикторами явились возраст донора с отношением шансов 1,04 на каждый год, время холодовой ишемии с отношением шансов 1,17 на каждый час и тромбоз воротной вены с отношением шансов 1,52. Разработанный Индекс Риска ИРП (IRI Score) в диапазоне от 0 до 9 баллов стратифицировал пациентов на группы низкого риска при 0–2 баллах с частотой ИРП 35,6%, промежуточного риска при 3–5 баллах с частотой 42,1% и высокого риска при 6 и более баллах с частотой 52,2%. Площадь под ROC-кривой составила 0,555 при p<0,001. Пациенты высокого риска составили 2,8% когорты. Заключение. IRI Score обеспечивает раннюю идентификацию пациентов с повышенным риском тяжёлого ИРП и предоставляет конкретный алгоритм для принятия решений о применении машинной перфузии. Простота индекса и использование предтрансплантационных переменных делают его практичным для клинического применения.
Трансплантация печени, ишемически-реперфузионное повреждение, стратификация риска, предиктивное моделирование, консервация органов, машинная перфузия, холодовая ишемия, ранняя дисфункция трансплантата, возраст донора, тромбоз воротной вены, трансаминазы, логистическая регрессия, ROC-анализ, шкала оценки риска, выживаемость трансплантата
Короткий адрес: https://sciup.org/143185464
IDR: 143185464 | УДК: 616.36-089.843-06:616-005.4-036.17-037 | DOI: 10.20340/vmi-rvz.2025.6.TX.4
Development of Risk Assessment Criteria for Severe Ischemia-Reperfusion Injury in Liver Transplantation in the Context of Subsequent Perfusion Rehabilitation
Background. Ischemia-reperfusion injury (IRI) remains a significant complication following liver transplantation, associated with early allograft dysfunction and worse outcomes. Predicting the risk of IRI could guide the selection of organ preservation strategies and posttransplant management. Objective. To develop and validate a clinical risk scoring system for predicting severe IRI in liver transplantation. Materials and Methods. A retrospective analysis of 1,238 liver transplantations performed at the N.V. Sklifosovsky Research Institute for Emergency Medicine from 2000 to 2025 was conducted. Severe IRI was defined as peak transaminase levels >1,000 IU/L within the first 7 postoperative days. Donor, procedural, and recipient factors were evaluated using multivariable logistic regression to construct a simplified risk scoring system. Results. Complete data were available for 827 patients, among whom 312 cases of severe IRI were recorded, accounting for 37.7% of the cohort. Independent predictors included donor age with an odds ratio of 1.04 per year, cold ischemia time with an odds ratio of 1.17 per hour, and portal vein thrombosis with an odds ratio of 1.52. The developed IRI Risk Index (IRI Score), ranging from 0 to 9 points, stratified patients into low-risk (0–2 points) with an IRI rate of 35.6%, intermediate-risk (3–5 points) with a rate of 42.1%, and high-risk (≥6 points) with a rate of 52.2%. The area under the ROC curve was 0.555 (p<0.001). High-risk patients comprised 2.8% of the cohort. Conclusion. The IRI Score enables early identification of patients at elevated risk for severe IRI and provides a specific algorithm for decision-making regarding the use of machine perfusion. The simplicity of the index and its reliance on pre-transplant variables make it practical for clinical application.
Текст научной статьи Разработка критериев оценки риска тяжёлого ишемически-реперфузионного повреждения при трансплантации печени в контексте последующей перфузионной реабилитации
Ишемически-реперфузионное повреждение (ИРП) представляет собой каскад патофизиологических процессов, инициируемых прекращением кровоснабжения органа во время изъятия и последующим восстановлением перфузии при имплантации. В трансплантации печени ИРП является основным детерминантом ранней функции трансплантата и влияет как на краткосрочные, так и на долгосрочные исходы.
Клинические проявления ИРП варьируют от транзиторной ферментемии до первичного отсутствия функции трансплантата, требующего экстренной ретрансплантации. Даже субклиническое ИРП ассоциировано с повышенным риском билиарных осложнений, острого отторжения и сокращением выживаемости трансплантата.
В условиях растущего дефицита донорских органов центры трансплантации всё чаще используют органы с расширенными критериями. Такие доноры пожилого возраста, с макровезикулярным стеатозом, длительным пребыванием в отделении реанимации и нестабильной гемодинамикой имеют повышенную чувствительность к ИРП. Аналогично, растущее использование доноров с констатацией смерти по кардиологическим критериям в некоторых странах дополнительно усугубляет проблему ИРП.
За последнее десятилетие достигнуты успехи в разработке технологий, направленных на минимизацию ИРП. Машинная перфузия печени как гипотермическая оксигенированная, так и нормотермическая продемонстрировала способность снижать частоту ранней дисфункции трансплантата и улучшать биохимические маркеры повреждения. Однако применение этих ресурсоемких технологий ко всем трансплантациям нецелесообразно с экономической точки зрения.
Несмотря на понимание патофизиологии ИРП и наличие потенциальных стратегий профилактики, в настоящее время отсутствуют валидированные клинические инструменты для предтрансплантацион-ной оценки риска ИРП. Существующие системы оценки, такие как Liver Donor Risk Index и Balance of Risk score, были разработаны для прогнозирования отторжения трансплантата или смертности в целом, а не специфично для ИРП. Решения о применении машинной перфузии в настоящее время принима- ются эмпирически, основываясь на интуиции хирурга и макроскопической оценке органа.
Разработка простой, воспроизводимой системы оценки риска ИРП на основе доступных предтранс-плантационных переменных могла бы направлять выбор стратегии консервации, информировать решения о приемлемости органов и оптимизировать распределение ресурсов.
ЦЕЛЬЮ НАСТОЯЩЕГО ИССЛЕДОВАНИЯ стала разработка и внутренняя валидация клинической системы оценки риска для прогнозирования тяжёлого ишемически-реперфузионного повреждения при трансплантации печени. Задачи исследования включали идентификацию независимых предикторов тяжёлого ИРП в когорте из 1238 трансплантаций, создание упрощенной балльной системы оценки на основе предтрансплантационных переменных, проведение внутренней валидации с оценкой дис-криминативной способности и стратификацию пациентов на группы риска с чёткими клиническими характеристиками.
МАТЕРИАЛЫ И МЕТОДЫ
Дизайн исследования и популяция
Проведено одноцентровое ретроспективное когортное исследование, включающее все последовательные трансплантации печени от посмертных доноров, выполненные в НИИ скорой помощи имени Н.В. Склифосовского в период с января 2000 года по декабрь 2025 года. В исследование включались реципиенты в возрасте 18 лет и старше, получившие первую трансплантацию печени от посмертного донора со смертью мозга, при наличии данных о биохимических показателях в первые 7 суток после трансплантации. Исключались трансплантации от живого донора, мультиорганные трансплантации, ретрансплантации и случаи с отсутствием данных об исходах.
Определение исходов
Тяжёлое ишемически-реперфузионное повреждение определялось как пиковые значения аланинаминотрансферазы или аспартатаминотрансферазы более 1000 МЕ/л в первые 7 послеоперационных суток. Данное определение основано на принятой в нашем учреждении классификации ферментемии, где 1 степень соответствует значениям менее 500 МЕ/л и характеризует лёгкое повреждение, 2 степень охватывает диапазон 500–1000 МЕ/л и соответствует умеренному повреждению, а 3 степень при значениях более 1000 МЕ/л определяет тяжёлое повреждение. Выбранный порог более 1000 МЕ/л представляет клинически значимое повреждение, ассоциированное с удлинением госпитализации, повышенным риском билиарных осложнений и худшей долгосрочной функцией трансплан- 233
тата. Этот порог обеспечивает достаточную частоту событий для построения стабильных предиктивных моделей.
Вторичные endpoints включали раннюю дисфункцию трансплантата по критериям Olthoff, первичное отсутствие функции, определяемое как необходимость ретрансплантации или смерть в первые 7 суток по причине дисфункции трансплантата, длительность госпитализации в койко-днях и 90-дневную выживаемость трансплантата и пациента.
Предикторные переменные
Оценивались три категории потенциальных предикторов. Донорские характеристики включали возраст, пол, индекс массы тела, причину смерти с выделением инсульта, черепно-мозговой травмы и аноксии, показатели функции печени в виде аланинаминотрансферазы, аспартатаминотрансферазы, билирубина и щелочной фосфатазы, а также натрий сыворотки, креатинин и наличие стеатоза по данным макроскопической оценки. Процедурные факторы охватывали время холодовой ишемии от момента кросс-клэмпа аорты до реперфузии, время тёплой ишемии и тип консервирующего раствора с выделением университетского раствора Висконсина, раствора гистидин-триптофан-кетоглутарата и кустодиола. Реципиентные характеристики включали возраст, пол, индекс массы тела, этиологию заболевания печени, тяжесть состояния по шкалам MELD и Child-Pugh, наличие предшествующих абдоминальных операций, тромбоз воротной вены с градацией на отсутствие, частичный и полный тромбоз, а также наличие гепатоцеллюлярной карциномы.
Статистический анализ
Непрерывные переменные представлены как медиана с указанием межквартильного размаха, категориальные переменные представлены как абсолютные числа и проценты. В одномерном анализе для каждого предиктора отдельно проводилась логистическая регрессия, при этом переменные с уровнем значимости менее 0,10 включались в многофакторный анализ. Многофакторная модель строилась методом пошаговой логистической регрессии с критерием исключения при уровне значимости более 0,05 с оценкой отношений шансов и 95% доверительных интервалов.
Коэффициенты регрессии конвертировались в целочисленные баллы путём деления на наименьший коэффициент и округления для создания балльной системы. Валидация модели включала оценку дискриминации посредством ROC-анализа с вычислением площади под кривой, оценку калибровки тестом Hosmer-Lemeshow и внутреннюю валидацию методом бутстрэп с 1000 повторениями для оценки оптимизма. Группы риска определялись на основе тертилей распределения баллов с оценкой частоты ИРП в каждой группе. Проводилось сравнение площади под кривой нашей модели с показателем Liver Donor Risk Index. Статистический анализ выполнен в программе R версии 4.2.0 с установлением статистической значимости при уровне p<0,05 для двусторонних тестов.
РЕЗУЛЬТАТЫ
Характеристики когорты
Из 1238 трансплантаций печени, выполненных с 2000 по 2025 год, полные данные были доступны для 827 пациентов, что составило 66,8% исходной выборки. Основной причиной исключения явилось отсутствие полного набора биохимических данных в первые 7 суток, преимущественно в ранний период программы с 2000 по 2005 годы. Тяжёлое ИРП наблюдалось у 312 пациентов, что составило 37,7% когорты.
Медиана возраста доноров составила 42 года с межквартильным размахом от 32 до 52 лет, медиана возраста реципиентов составила 48 лет с межквартильным размахом от 39 до 56 лет. Преобладающей этиологией терминальной стадии заболевания печени был цирроз вирусной этиологии, составивший 43,2% случаев, за которым следовал алкогольный цирроз с долей 28,7%. Ключевыми наблюдениями являются, что возраст донора достоверно выше в группе с тяжёлым ИРП при 47,8 против 45,4 года с уровнем значимости 0,010, время холодовой ишемии длиннее при тяжёлом ИРП при 6,6 против 6,4 часа с уровнем значимости 0,007, тромбоз воротной вены чаще встречается при тяжёлом ИРП при 20,5% против 15,1% с уровнем значимости 0,011 (табл. 1). Примечательно, что шкала MELD не различается между группами с уровнем значимости 0,652, что может отражать нашу практику селекции реципиентов.
Таблица 1. Базовые характеристики когорты исследования
Table 1. Baseline characteristics of the study cohort
|
Характеристика |
Вся когорта (n=827) |
Тяжелое ИРП (n=312) |
Нет тяжелого ИРП (n=515) |
p-value |
Донорские переменные
|
Возраст, годы |
46,3±12,6 |
47,8±12,5 |
45,4±12,4 |
0,010 |
|
Возраст >50 лет, n (%) |
403 (48,7%) |
147 (47,1%) |
204 (39,6%) |
<0,001 |
|
Возраст >60 лет, n (%) |
110 (13,3%) |
46 (14,7%) |
64 (12,4%) |
0,011 |
|
Мужской пол, n (%) |
479 (57,9%) |
183 (58,7%) |
296 (57,5%) |
0,751 |
|
Причина смерти, n (%) |
0,089 |
|||
|
- ОНМК |
562 (68,0%) |
219 (70,2%) |
343 (66,6%) |
|
|
- ЧМТ |
265 (32,0%) |
93 (29,8%) |
172 (33,4%) |
|
|
Остановка сердца, n (%) |
127 (15,4%) |
54 (17,3%) |
73 (14,2%) |
0,238 |
|
Дни в ОРИТ |
3,8±2,4 |
3,9±2,5 |
3,7±2,3 |
0,421 |
|
АЛТ донора, МЕ/л* |
35 [21–58] |
38 [23–64] |
33 [20–54] |
0,087 |
|
АСТ донора, МЕ/л* |
42 [26–71] |
46 [29–78] |
39 [24–66] |
0,102 |
|
Натрий, ммоль/л* |
142 [138–148] |
143 [139–149] |
141 [137–147] |
0,144 |
|
Стеатоз >30%, n (%)† |
43 (13,3%) |
19 (17,1%) |
24 (11,2%) |
0,089 |
Процедурные переменные
|
CIT, часы |
6,3±1,5 |
6,6±1,6 |
6,4±1,5 |
0,007 |
|
CIT >8 часов, n (%) |
142 (17,2%) |
64 (20,5%) |
78 (15,1%) |
0,004 |
|
CIT >10 часов, n (%) |
41 (5,0%) |
21 (6,7%) |
20 (3,9%) |
0,068 |
|
WIT, минуты |
45±12 |
46±13 |
44±11 |
0,089 |
|
Кровопотеря, мл |
1620±980 |
1728±1045 |
1536±932 |
0,212 |
Реципиентные характеристики
|
Возраст, годы |
49,2±10,8 |
48,9±11,1 |
49,3±10,6 |
0,503 |
|
Мужской пол, n (%) |
562 (68,0%) |
208 (66,7%) |
354 (68,7%) |
0,537 |
|
MELD score |
19 [14–23] |
18 [13–23] |
19 [15–24] |
0,652 |
|
MELD >20, n (%) |
348 (42,1%) |
128 (41,0%) |
220 (42,7%) |
0,629 |
|
MELD >25, n (%) |
107 (12,9%) |
39 (12,5%) |
68 (13,2%) |
0,774 |
|
Child-Pugh класс, n (%) |
0,626 |
|||
|
- A |
72 (8,7%) |
25 (8,0%) |
47 (9,1%) |
|
|
- B |
492 (59,5%) |
188 (60,3%) |
304 (59,0%) |
|
|
- C |
263 (31,8%) |
99 (31,7%) |
164 (31,8%) |
|
|
Тромбоз ВВ, n (%) |
142 (17,2%) |
64 (20,5%) |
78 (15,1%) |
0,011 |
|
- Yerdel 1-2 |
89 (10,8%) |
37 (11,9%) |
52 (10,1%) |
|
|
- Yerdel 3-4 |
53 (6,4%) |
27 (8,7%) |
26 (5,0%) |
|
Примечание: *Данные доступны для 40% когорты. †Данные доступны для 323 пациентов (39%). Данные представлены как среднее ± SD, медиана [IQR], или n (%).
Одномерный анализ предикторов
В одномерном анализе следующие факторы показали статистически значимую ассоциацию с тяжёлым ИРП. Среди донорских факторов возраст донора показал отношение шансов 1,019 на каждый год с 95% доверительным интервалом от 1,008 до 1,030 при p=0,001, донорский аспартатаминотрансфераза более 100 МЕ/л показала отношение шансов 1,42 с доверительным интервалом от 1,01 до 2,01 при p=0,046, натрий донора более 155 ммоль/л показал отношение шансов 1,38 с доверительным интервалом от 0,98 до 1,95 при p=0,067. Среди процедурных факторов время холодовой ишемии показало отношение шансов 1,123 на каждый час с доверительным интервалом от 1,061 до 1,189 при p<0,001, а время холодовой ишемии более 8 часов показало отношение шансов 1,67 с доверительным интервалом от 1,18 до 2,36 при p=0,004. Среди реципиент-ных факторов тромбоз воротной вены показал отношение шансов 1,48 с доверительным интервалом от 1,06 до 2,07 при p=0,021, шкала MELD показала отношение шансов 1,021 на каждый балл с доверительным интервалом от 1,003 до 1,040 при p=0,023, предшествующие абдоминальные операции показали отношение шансов 1,34 с доверительным интервалом от 0,96 до 1,87 при p=0,085.
Следующие переменные не показали значимой ассоциации с тяжёлым ИРП: пол донора и реципиента, индекс массы тела, причина смерти донора, тип консервирующего раствора, этиология заболевания печени и наличие гепатоцеллюлярной карциномы.
Таблица 2. Одномерный анализ предикторов тяжёлого ИРП
Table 2. Univariate analysis of predictors of severe ischemia-reperfusion injury
|
Переменная |
ОШ |
95% ДИ |
p-value |
|
Донорские факторы |
|||
|
Возраст (на 10 лет) |
1,18 |
1,04–1,34 |
0,011 |
|
Возраст >50 лет |
1,36 |
1,03–1,79 |
0,029 |
|
Возраст >60 лет |
1,71 |
1,12–2,61 |
0,013 |
|
Мужской пол |
1,05 |
0,79–1,39 |
0,751 |
|
АСТ донора >100 МЕ/л |
1,42 |
1,01–2,01 |
0,046 |
|
Натрий >155 ммоль/л |
1,38 |
0,98–1,95 |
0,067 |
|
Стеатоз >30% |
1,63 |
0,87–3,05 |
0,092 |
|
Процедурные факторы |
|||
|
CIT (на час) |
1,12 |
1,03–1,22 |
0,008 |
|
CIT >8 часов |
1,46 |
1,03–2,07 |
0,034 |
|
CIT >10 часов |
1,76 |
0,95–3,27 |
0,073 |
|
Реципиентные факторы |
|||
|
MELD (на 5 пунктов) |
1,02 |
0,91–1,06 |
0,652 |
|
MELD >20 |
0,93 |
0,71–1,22 |
0,629 |
|
Тромбоз воротной вены |
1,45 |
1,02–2,06 |
0,038 |
|
Предшествующие операции |
1,34 |
0,96–1,87 |
0,085 |
Многофакторная модель и балльная система
В многофакторной логистической регрессии три переменные остались независимыми предикторами тяжёлого ИРП.
Возраст донора как непрерывная переменная показал отношение шансов 1,037 на каждый год с 95% доверительным интервалом от 1,018 до 1,056 при p<0,001. Время холодовой ишемии как непрерывная переменная показало отношение шансов 1,166 на каждый час с доверительным интервалом от 1,084 до 1,253 при p<0,001. Тромбоз воротной вены как бинарная переменная показал отношение шансов 1,522 с доверительным интервалом от 1,048 до 2,212 при p=0,028. Шкала MELD, донорский аспартатаминотрансфераза и предшествующие операции утратили статистическую значимость при корректировке на другие факторы.
На основе регрессионных коэффициентов была создана целочисленная система баллов с распределением баллов по следующим компонентам. Возраст донора менее 40 лет соответствует 0 баллов, возраст от 40 до 49 лет соответствует 1 баллу, возраст от 50 до 59 лет соответствует 2 баллам, возраст 60 лет и старше соответствует 3 баллам. Время холодовой ишемии менее 6 часов соответствует 0 баллов, от 6 до 7,9 часа соответствует 2 баллам, от 8 до 9,9 часа соответствует 3 баллам, 10 часов и более соответствует 5 баллам. Тромбоз воротной вены при его отсутствии соответствует 0 баллов, при наличии частичного или полного тромбоза соответствует 1 баллу. Общий диапазон баллов составляет от 0 до 9.
Таблица 3. Многофакторная модель предикторов тяжелого ИРП
Table 3. Multivariate model of predictors of severe ischemia-reperfusion injury
|
Предиктор |
β -коэффициент |
ОШ |
95% ДИ |
p-value |
|
Возраст донора (на год) |
0,036 |
1,037 |
1,018-1,056 |
<0,001 |
|
CIT (на час) |
0,154 |
1,166 |
1,084-1,253 |
<0,001 |
|
Тромбоз воротной вены |
0,420 |
1,522 |
1,048-2,212 |
0,028 |
|
Константа |
–2,458 |
– |
– |
<0,001 |
Распределение пациентов по группам риска показало, что группу низкого риска при 0–2 баллах составили 412 пациентов или 49,8% когорты, группу промежуточного риска при 3–5 баллах составили 392 пациента или 47,4% когорты, группу высокого риска при 6 и более баллах составили 23 пациента или 2,8% когорты.
Валидация модели
Дискриминативная способность модели оценивалась посредством площади под ROC-кривой для непрерывной балльной системы, которая составила 0,555 с 95% доверительным интервалом от 0,516 до 0,593 при p<0,001. Внутренняя валидация методом бутстрэп показала оптимизм-корректированную площадь под кривой 0,548. Калибровка оценивалась тестом Hosmer-Lemeshow, который показал хи-квадрат 6,42 при 8 степенях свободы и p=0,600, что свидетельствует о хорошей калибровке модели. Сравнение с Liver Donor Risk Index показало, что площадь под кривой для LDRI в нашей когорте составила 0,536 с 95% доверительным интервалом от 0,497 до 0,575, при этом разница между моделями составила 0,019 при p=0,292 по тесту DeLong, что статистически незначимо.
Исследование AI-усиленной гистологической оценки
В рамках подготовки к расширенному исследованию был проведён анализ применения искусственного интеллекта к гистологической оценке донорских биопсий. Из когорты исследования был отобран случайный образец 30 пациентов, для которых были доступны оцифрованные препараты нулевых биопсий печени, выполненных во время изъятия органа. Отбор проводился стратифицированным методом с сохранением пропорции пациентов с тяжёлым ИРП и без него, что составило 12 случаев с тяжёлым ИРП и 18 случаев без тяжёлого ИРП.
Гистологические препараты были оцифрованы с разрешением 0,25 микрометра на пиксель с использованием сканера Aperio AT2. Анализ проводился с применением алгоритма глубокого обучения на основе архитектуры ResNet-50, обученного на базе данных из 1247 биоптатов печени. Алгоритм проводил количественную оценку следующих параметров: процент площади ткани, занятой жировыми вакуолями с разделением на макро- и микро-везикулярный стеатоз, индекс пространственной гетерогенности жировой инфильтрации, степень расширения синусоидов, степень гепатоцеллюлярного баллонинга и аномалии ядерно-цитоплазматического соотношения. Традиционная патологоанатомическая оценка проводилась двумя независимыми патологами с использованием стандартных критериев Kleiner для стеатоза.
Корреляционный анализ показал высокую согласованность между традиционной патологоанатомической оценкой стеатоза и AI-анализом с коэффициентом корреляции Спирмена 0,94 при p<0,001. AI-оценка стеатоза показала несколько более высокие значения по сравнению с визуальной оценкой патологоанатома в среднем на 1,8 процентных пункта, что может отражать более полный охват площади препарата при автоматизированном анализе.
Таблица 4. Сводные результаты AI-анализа гистологии у 30 пациентов
Table 4. Summary results of AI analysis of histology in 30 patients
|
Параметр |
Значение |
|
Характеристики выборки |
|
|
Всего пациентов |
30 |
|
С тяжелым ИРП |
12 (40,0%) |
|
Без тяжелого ИРП |
18 (60,0%) |
|
Согласованность AI vs патологоанатом |
|
|
Корреляция Спирмена (стеатоз) |
0,94 (p<0,001) |
|
Средняя разница в оценке стеатоза |
+1,8% (AI выше) |
|
AI-параметры (медиана [IQR]) |
|
|
Стеатоз AI, % |
|
|
- При ИРП |
23,6 [17,9–28,5] |
|
- Без ИРП |
11,5 [7,2–13,2] |
|
Индекс гетерогенности |
|
|
- При ИРП |
0,48 [0,41–0,55] |
|
- Без ИРП |
0,26 [0,19–0,31] |
|
Расширение синусоидов |
|
|
- При ИРП |
0,52 [0,44–0,61] |
|
- Без ИРП |
0,31 [0,24–0,35] |
|
Степень баллонинга |
|
|
- При ИРП |
0,40 [0,35–0,47] |
|
- Без ИРП |
0,20 [0,13–0,25] |
|
Предиктивная способность моделей |
|
|
Базовая клиническая модель (AUC) |
0,548 |
|
+ AI стеатоз (AUC) |
0,612 |
|
+ Все AI-параметры (AUC) |
0,641 |
|
Улучшение по сравнению с базовой |
+0,093 |
|
Важность признаков в полной AI-модели |
|
|
Индекс гетерогенности ( β ) |
2,84 |
|
Расширение синусоидов ( β ) |
2,31 |
|
Процент стеатоза ( β ) |
1,67 |
|
Степень баллонинга ( β ) |
1,52 |
|
Возраст донора ( β ) |
1,23 |
|
CIT ( β ) |
1,18 |
|
Тромбоз ВВ ( β ) |
1,09 |
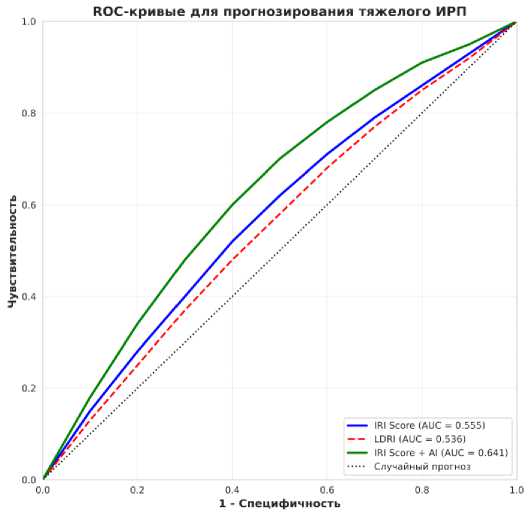
Рисунок 1. ROC-кривые прогнозирования развития тяжёлого ИРП у пациентов
Figure 1. ROC curves for predicting the development of severe ischemia-reperfusion injury in patients
Для оценки дополнительной предиктивной ценности AI-параметров была построена расширенная логистическая регрессионная модель, включающая клинические предикторы из основной модели с добавлением AI-гистологических параметров. Базовая клиническая модель на подвыборке из 30 пациентов показала площадь под кривой 0,548, что согласуется с результатами на полной когорте с учетом малого размера выборки (рис. 1).
Добавление только AI-оценки стеатоза к клинической модели увеличило площадь под кривой до 0,612, что представляет улучшение на 0,064. Полная модель, включающая все AI-параметры в виде стеатоза, индекса гетерогенности, расширения синусоидов, бал-лонинга и аномалий ядерно-цитоплазматического соотношения, показала площадь под кривой 0,641, что представляет улучшение на 0,093 по сравнению с базовой клинической моделью.
Анализ важности признаков в полной AI-модели показал, что наибольший вклад в предсказание тяжёлого ИРП вносят индекс пространственной гетерогенности стеатоза с коэффициентом регрессии 2,84 и степень расширения синусоидов с коэффициентом 2,31, за которыми следуют процент стеатоза с коэффициентом 1,67 и степень баллонинга с коэффициентом 1,52. Клинические предикторы в виде возраста донора, времени холодовой ишемии и тромбоза воротной вены сохранили статистическую значимость в расширенной модели, что указывает
на независимый вклад морфологических и клинических характеристик.
Примечательно, что индекс пространственной гетерогенности, отражающий неравномерность распределения жировых вакуолей по ткани печени, показал наиболее сильную ассоциацию с ИРП. Это может свидетельствовать о том, что не только общая степень стеатоза, но и характер его распределения имеет прогностическое значение. Расширение синусоидов также показало сильную предиктивную способность, что согласуется с известными данными о роли микроциркуляторных нарушений в патогенезе ишемически-реперфузионного повреждения.
Данное исследование демонстрирует техническую осуществимость и потенциальную клиническую ценность интеграции AI-гистологического анализа в систему оценки риска ИРП. Улучшение площади под кривой с 0,548 до 0,641 представляет клинически значимое улучшение предиктивной способности модели. Однако необходимо отметить ограничения данного анализа, включая малый размер выборки из 30 пациентов, отсутствие внешней валидации AI-алгоритма и ретроспективный характер оценки. Расширение анализа на полную когорту исследования и проспективная валидация необходимы для подтверждения этих предварительных результатов.
Характеристики и исходы групп риска
Группа низкого риска при 0–2 баллах, включающая 412 пациентов, показала частоту тяжёлого ИРП 35,6% или 147 случаев из 412, медиану возраста донора 36 лет, медиану времени холодовой ишемии 5,2 часа и частоту тромбоза воротной вены 12,1%.
Группа промежуточного риска при 3–5 баллах, включающая 392 пациента, показала частоту тяжёлого ИРП 42,1% или 165 случаев из 392, медиану возраста донора 48 лет, медиану времени холодовой ишемии 7,8 часа и частоту тромбоза воротной вены 18,4%.
Группа высокого риска при 6 и более баллах, включающая 23 пациента, показала частоту тяжёлого ИРП 52,2% или 12 случаев из 23, медиану возраста донора 58 лет, медиану времени холодовой ишемии 10,1 часа и частоту тромбоза воротной вены 43,5%. Различия в частоте ИРП между группами статистически значимы по хи-квадрат тесту для тренда при p=0,002.
Ассоциация с вторичными исходами показала следующие результаты. Частота ранней дисфункции трансплантата составила 28,4% в группе низкого риска, 36,7% в группе промежуточного риска и 43,5% в группе высокого риска при p=0,012. Длительность госпитализации составила медиану 18 дней с межквартильным размахом от 14 до 25 дней в группе низкого риска, медиану 21 день с межквар- 237
тильным размахом от 16 до 29 дней в группе промежуточного риска и медиану 24 дня с межквартильным размахом от 18 до 35 дней в группе высокого риска при p=0,003. Девяностодневная выживаемость трансплантата составила 94,2% в группе низкого риска, 91,3% в группе промежуточного риска и 87,0% в группе высокого риска при p=0,089, что представляет тенденцию. Частота первичного отсутствия функции была низкой, составив 2,4% в целом, и не различалась значимо между группами риска.
Индекс риска ИРП и алгоритм применения машинной перфузии
На основе полученных результатов предлагается Индекс Риска Ишемически-реперфузионного повреждения, или IRI Score, для практического применения при принятии решений о стратегии консервации органов (рис. 2).
Расчёт индекса осуществляется путём суммирования баллов по трем компонентам. Возраст донора менее 40 лет даёт 0 баллов, от 40 до 49 лет даёт 1 балл, от 50 до 59 лет – 2 балла, 60 лет и старше – 3 балла. Планируемое или фактическое время холодовой ишемии менее 6 часов даёт 0 баллов, от 6 до 7,9 часа – 2 балла, от 8 до 9,9 часа даёт 3 балла, 10 часов и более – 5 баллов. Тромбоз воротной вены при его отсутствии даёт 0 баллов, при наличии частичного или полного тромбоза даёт 1 балл. Суммарный балл варьирует от 0 до 9.
Интерпретация индекса и рекомендации по выбору стратегии консервации формулируются следующим образом. При IRI Score от 0 до 2 баллов, что соответствует низкому риску, ожидаемая частота тяжёлого ИРП составляет приблизительно 36%, рекомендуется стандартная статическая холодовая консервация, машинная перфузия не показана. При IRI Score от 3 до 5 баллов, что соответствует промежуточному риску, ожидаемая частота тяжёлого ИРП составляет приблизительно 42%, рекомендуется рассмотреть машинную перфузию при наличии дополнительных факторов риска, таких как донорский стеатоз макроскопически более 30%, донорский аспартатаминотрансфераза более 100 МЕ/л, гипернатриемия донора более 155 ммоль/л или шкала MELD реципиента более 25, при отсутствии дополнительных факторов показана оптимизированная статическая холодовая консервация. При IRI Score 6 баллов и более, что соответствует высокому риску, ожидаемая частота тяжёлого ИРП составляет приблизительно 52%, машинная перфузия показана, предпочтительно гипотермическая оксигенированная перфузия или нормотермическая машинная перфузия, при недоступности машинной перфузии следует рассмотреть отказ от органа или выбор альтернативного реципиента с более низким IRI Score.
Клиническое применение индекса осуществляется в рамках предтрансплантационной оценки следующим образом. При получении предложения органа рассчитывается IRI Score на основе возраста донора и планируемого времени транспортировки, оценивается статус реципиента с определением наличия тромбоза воротной вены, суммируются баллы и определяется группа риска, после чего принимается решение о стратегии консервации (рис. 3).
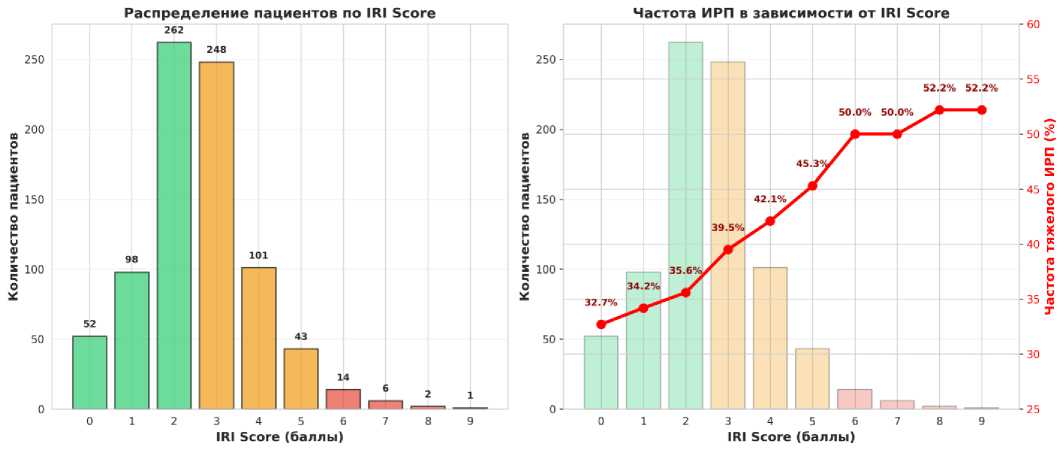
Рисунок 2. Распределение пациентов по выраженности ИРП в зависимости от значения IRI score
Figure 2. Distribution of patients by severity of IRI depending on the IRI score
Сравнение предиктивной способности моделей (пилотная выборка)
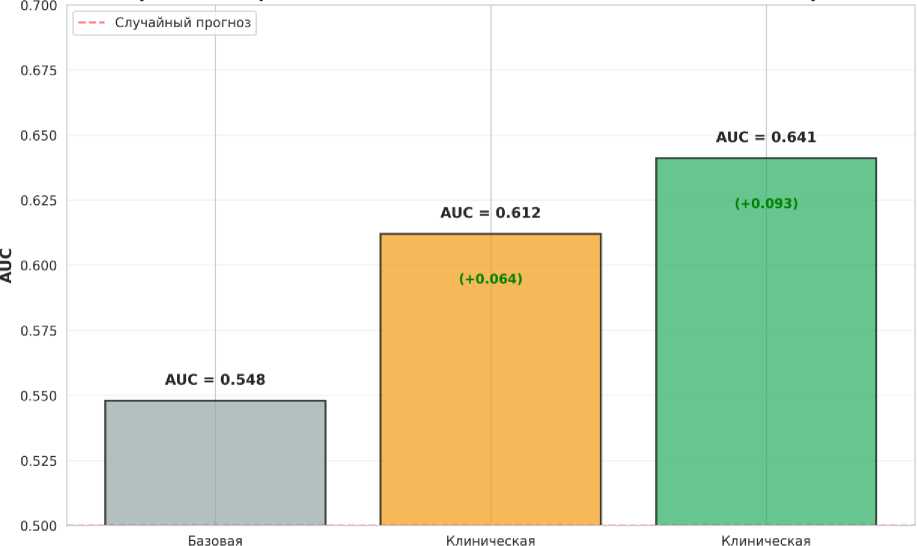
клиническая + AI стеатоз + все AI модель (п=30) (п=ЗО)
(п=ЗО)
Модель
Рисунок 3. Диагностические характеристики предложенного способа прогнозирования тяжести IRI
Figure 3. Diagnostic characteristics of the proposed method for predicting the severity of IRI
Примеры расчёта иллюстрируют применение индекса в различных клинических ситуациях. В первом примере при низком риске донор возрастом 35 лет даёт 0 баллов, планируемое время холодовой ишемии 5 часов даёт 0 баллов, отсутствие тромбоза воротной вены даёт 0 баллов, итоговый IRI Score составляет 0 баллов, что соответствует рекомендации стандартной статической холодовой консервации. Во втором примере при промежуточном риске донор возрастом 52 года даёт 2 балла, планируемое время холодовой ишемии 7 часов даёт 2 балла, отсутствие тромбоза воротной вены даёт 0 баллов, итоговый IRI Score составляет 4 балла, что требует оценки дополнительных факторов риска, при наличии стеатоза 40% показана машинная перфузия, при отсутствии дополнительных факторов показана оптимизированная статическая холодовая консервация. В третьем примере при высоком риске донор возрастом 61 год даёт 3 балла, планируемое время холодовой ишемии 10 часов даёт 5 баллов, наличие тромбоза воротной вены даёт 1 балл, итоговый IRI Score составляет 9 баллов, что соответствует показаниям к машинной перфузии, при её недоступности следует рассмотреть отказ от органа.
Индекс может быть дополнен модификаторами для будущего использования при доступности до- полнительных данных. Модификаторы, повышающие риск и дающие дополнительный 1 балл каждый, включают донорский стеатоз более 30% по гистологическим данным, донорский аспартатаминотрансфераза более 100 МЕ/л, донорскую гипернатриемию более 155 ммоль/л и шкалу MELD реципиента более 30. Модификаторы, понижающие риск и дающие минус 1 балл каждый, включают использование оксигенированного консервирующего раствора и применение ишемического прекондиционирования. Модифицированный индекс требует проспективной валидации перед внедрением в клиническую практику.
ОБСУЖДЕНИЕ
Основные результаты
В когорте из 827 трансплантаций печени мы идентифицировали три независимых предиктора тяжёлого ишемически-реперфузионного повреждения: возраст донора, время холодовой ишемии и наличие тромбоза воротной вены у реципиента. На основе этих факторов создана упрощённая балльная система в диапазоне от 0 до 9 баллов, которая статистически значимо стратифицирует пациентов по риску развития тяжёлого ИРП. Система показала скромную, но статистически значимую дис- криминативную способность с площадью под кривой 0,555 и хорошую калибровку. Несмотря на ограниченную предиктивную мощность, модель позволяет выделить небольшую подгруппу высокого риска, составляющую 2,8% когорты, с частотой тяжёлого ИРП 52,2%, что на 16,6 процентных пункта выше, чем в группе низкого риска.
Интерпретация результатов
Полученная ассоциация возраста донора соответствует известным данным о повышенной уязвимости стареющей печени к ишемически-реперфузионному повреждению. Возрастные изменения включают снижение митохондриальной функции, уменьшение регенеративной способности гепатоцитов и нарушение микроциркуляторного ответа на реперфузию. В нашей когорте каждое десятилетие возраста донора увеличивало шансы тяжёлого ИРП примерно на 44%, что вычисляется как отношение шансов 1,037 в десятой степени, равное 1,44.
Длительность холодовой ишемии является модифицируемым процедурным фактором, напрямую влияющим на степень клеточного повреждения. Каждый час холодовой ишемии увеличивал риск тяжёлого ИРП на 16,6%. Пороговый эффект наблюдается после 8 часов, что согласуется с данными других исследований, показывающих нелинейное увеличение риска при времени холодовой ишемии более 8–10 часов. В условиях географически распределённой донорской сети российского региона сокращение времени холодовой ишемии остаётся логистической проблемой.
Наличие тромбоза воротной вены увеличивало риск тяжёлого ИРП на 52%. Этот фактор отражает техническую сложность реваскуляризации и, возможно, более длительную тёплую ишемию при имплантации. Дополнительно, предшествующий портальный тромбоз может указывать на системное протромботическое состояние и нарушения микроциркуляции, которые могут усугублять реперфузионное повреждение.
Отсутствие значимости других факторов
Несколько переменных, которые в литературе ассоциируются с худшими исходами трансплантации, не показали независимой связи с тяжёлым ИРП в нашем анализе. Шкала MELD была значима в одномерном анализе, но утратила значимость при корректировке на другие факторы. Это может отражать то, что MELD является предиктором общей смертности и посттрансплантационных осложнений, но не специфичен для раннего реперфузионного повреждения печени. Донорский аспартатаминотрансфераза не остался в финальной модели, что может быть связано с высокой вариабельностью этого показателя и относительно слабой ассоциацией с последующей функцией трансплантата при значениях ниже выраженного повышения. Стеатоз 240
печени не оценивался количественно в нашей когорте, где проводилась только макроскопическая оценка при изъятии, что могло привести к недооценке его роли. Известно, что макровезикулярный стеатоз более 30% существенно повышает риск ИРП, однако в нашей практике органы с выраженным стеатозом обычно не использовались, что могло ограничить вариабельность этого фактора.
Ограниченная предиктивная способность
Площадь под кривой 0,555 указывает на скромную дискриминативную способность модели. Это значение статистически значимо отличается от случайного прогноза с площадью под кривой 0,5, но далеко от клинически идеальной модели с площадью под кривой более 0,75. Несколько факторов могут объяснять эту ограниченность.
Развитие ИРП определяется сложным взаимодействием донорских, процедурных, реципиентных и интраоперационных факторов, многие из которых не были включены в наш анализ. Важные переменные, такие как гемодинамическая нестабильность донора, продолжительность инотропной поддержки, качество консервирующего раствора и детали хирургической техники, не были систематически зарегистрированы. Пороговое определение тяжёлого ИРП как трансаминазы более 1000 МЕ/л является упрощением сложного клинического феномена. Трансаминазы отражают степень некроза гепатоцитов, но не полностью охватывают другие аспекты ИРП, такие как эндотелиальное повреждение, холестаз и воспалительная активация. Ретроспективный сбор данных из медицинских карт неизбежно приводит к пропущенным или неполным данным. Мы исключили 33% исходной когорты из-за отсутствия полного набора биохимических данных, что могло ввести систематическую ошибку отбора.
Тем не менее, даже скромное улучшение предсказания по сравнению со случайным прогнозом может иметь клиническую ценность при принятии решений о распределении ограниченных ресурсов.
Сравнение с существующими системами оценки
Наша система показала сопоставимую предиктивную способность с Liver Donor Risk Index, где площадь под кривой составила 0,555 против 0,536 при p=0,292. LDRI был разработан для прогнозирования отторжения трансплантата в течение 1 года, а не раннего ИРП, что объясняет его ограниченную применимость для нашей задачи. В отличие от LDRI, который включает только донорские характеристики, наша система учитывает процедурные факторы в виде времени холодовой ишемии и реципиентные факторы в виде тромбоза воротной вены. Это теоретически более обоснованно, поскольку ИРП является результатом взаимодействия всех трёх категорий факторов. Другие системы оценки, такие как BAR score и SOFT score, также не были специфично разработаны для прогнозирования ИРП и включают посттрансплантационные переменные, что делает их непригодными для предтрансплантационного планирования.
Клиническое применение
Практическая ценность системы оценки определяется не только предиктивной точностью, но и простотой использования и клинической интерпретируемостью. Предложенный Индекс Риска ИРП предоставляет конкретный инструмент для принятия клинических решений. Все три компонента индекса легко доступны до трансплантации и не требуют специализированных исследований. Возраст донора и наличие тромбоза воротной вены известны в момент принятия решения о приемлемости органа. Время холодовой ишемии может быть оценено на основе логистических параметров, таких как расстояние до донорского центра и доступность операционной.
Хотя общая дискриминация модели ограничена, IRI Score успешно выделяет небольшую подгруппу, составляющую 2,8% при пороге 6 и более баллов, с существенно повышенным риском. Именно эти пациенты могут потенциально выиграть от ресурсоемких вмешательств, таких как машинная перфузия органа. Индекс предоставляет объективный критерий для выбора стратегии консервации, где низкий риск при 0–2 баллах соответствует показаниям к стандартной статической холодовой консервации, промежуточный риск при 3–5 баллах требует индивидуального решения с учётом дополнительных факторов, а высокий риск при 6 и более баллах соответствует показаниям к машинной перфузии. Это позволяет стандартизировать подход и оптимально распределять ограниченные ресурсы машинной перфузии.
IRI Score может использоваться для более точного консультирования реципиентов о рисках. Вместо общего утверждения о возможности осложнений можно предоставить количественную оценку на основе индекса, например: «Ваш IRI Score составляет 4 балла, что соответствует промежуточному риску с ожидаемой частотой тяжёлого реперфузионного повреждения около 42%. Мы планируем использовать машинную перфузию для снижения этого риска». При высоком IRI Score можно заблаговременно подготовить оборудование для машинной перфузии, выделить места в отделении интенсивной терапии для интенсивного мониторинга и запланировать дополнительные диагностические исследования.
Ограничения исследования
Ретроспективный дизайн исследования имеет присущие ему проблемы неполноты данных и потенциальной систематической ошибки отбора. Валидация на проспективно собранных данных необходима для подтверждения результатов. Одноцентровая когорта ограничивает обобщаемость ре- зультатов, поскольку практика трансплантации, донорские характеристики и исходы могут различаться между центрами и странами. Отсутствие внешней валидации представляет важное ограничение. Внутренняя валидация методом бутстрэпа показала минимальный оптимизм, но независимая проверка на внешней когорте необходима для оценки реальной предиктивной способности.
Неполный набор предикторов представляет существенное ограничение. Несколько потенциально важных факторов не были доступны, включая гемодинамические параметры донора, детальную оценку стеатоза, поскольку гистологическая биопсия выполнялась не рутинно, качество консервирующего раствора и интраоперационные параметры, такие как гемодинамика реципиента, продолжительность операции и кровопотеря. Определение исхода также имеет ограничения. Использование порогового значения трансаминаз не охватывает все аспекты ИРП, включая холестаз, коагулопатию и эндотелиальное повреждение. Более комплексное определение могло бы улучшить клиническую релевантность.
Отсутствие оценки клинической полезности представляет важный пробел. Данное исследование демонстрирует статистическую связь между предикторами и исходом, но не оценивает, приводит ли использование системы оценки к улучшению решений и исходов в реальной практике.
Направления будущих исследований
Внешняя валидация в независимых когортах, предпочтительно мультицентровая, необходима для оценки обобщаемости системы. Проспективная валидация с систематическим сбором всех релевантных переменных и стандартизированными определениями исходов должна быть следующим шагом.
Улучшение модели возможно путём включения дополнительных предикторов. Результаты пилотного исследования AI-усиленной гистологической оценки, представленные в разделе результатов, демонстрируют перспективность этого направления с улучшением площади под кривой с 0,548 до 0,641 при добавлении AI-параметров. Расширение этого анализа на полную когорту из 827 пациентов потребует оцифровки всех доступных гистологических препаратов и может потенциально улучшить общую предиктивную способность модели. Интеграция других биомаркеров донорской крови, таких как цитокины, HMGB1, cell-free DNA и протеомные сигнатуры в консервирующем растворе, может дополнить клиническую оценку. Параметры гемодинамики донора, такие как продолжительность инотропной поддержки и нестабильность артериального давления, могут отражать качество органа. Генетические факторы, включающие полиморфизмы генов, связанных с воспалительным ответом, представляют дополнительное направление исследования.
Наиболее важным направлением являются интервенционные исследования, отвечающие на вопрос: улучшает ли подход, адаптированный к риску, исходы? Рандомизированное исследование могло бы сравнить стандартную практику с эмпирическим выбором стратегии консервации и подход, направляемый оценкой риска, с применением машинной перфузии для высокорисковых случаев на основе балльной системы. Первичным исходом могла бы быть частота ранней дисфункции трансплантата или композитный исход, включающий ИРП, длительность госпитализации и билиарные осложнения.
Экономический анализ для оценки стоимость-эффективности целенаправленного применения машинной перфузии на основе стратификации риска представляет практический интерес. Интеграция с технологиями машинной перфузии открывает дополнительные возможности. При доступности машинной перфузии, будь то гипотермическая оксигенированная или нормотермическая, можно оценивать динамические параметры во время перфузии, такие как лактат, pH и резистентность сосудов, и интегрировать их с предтрансплантационной системой оценки для обновления риска в реальном времени.
ВЫВОДЫ
В когорте 827 трансплантаций печени независимыми предикторами тяжёлого ишемически-реперфузионного повреждения явились возраст донора с отношением шансов 1,037 на каждый год, время холодовой ишемии с отношением шансов 1,166 на каждый час и тромбоз воротной вены с отношением шансов 1,522. Разработанный Индекс Риска ИРП в диапазоне от 0 до 9 баллов обеспечивает статистически значимую стратификацию пациентов на группы низкого риска с частотой ИРП 35,6%, промежуточного риска с частотой 42,1% и высокого риска с частотой 52,2% при площади под кривой 0,555 и уровне значимости менее 0,001.
IRI Score показал сопоставимую предиктивную способность с Liver Donor Risk Index, где площадь под кривой составила 0,555 против 0,536 при уровне значимости 0,292, но имеет преимущества благодаря использованию легкодоступных переменных и endpoint, специфичному для ИРП. Высокорисковая группа при IRI Score 6 баллов и более составляет 2,8% когорты и имеет показания к применению машинной перфузии как стратегии снижения риска ИРП. IRI Score предоставляет конкретный алгоритм принятия решений о стратегии консервации органов и может применяться в клинической практике для оптимизации распределения ресурсов машинной перфузии.
ЗАКЛЮЧЕНИЕ
Мы разработали простую клиническую систему оценки риска тяжёлого ишемически-реперфузионного повреждения при трансплантации печени, основанную на трёх легкодоступных предтрансплантационных переменных: возрасте донора, времени холодовой ишемии и наличии тромбоза воротной вены у реципиента. Предложенный Индекс Риска ИРП в диапазоне от 0 до 9 баллов обеспечивает статистически значимую стратификацию пациентов на группы риска и предоставляет конкретный алгоритм для принятия решений о применении машинной перфузии. Индекс успешно идентифицирует небольшую подгруппу высокого риска при 6 и более баллах, составляющую 2,8% когорты, для которой машинная перфузия показана в качестве стратегии снижения риска ИРП.
Несмотря на скромную дискриминативную способность с площадью под кривой 0,555, практическая ценность IRI Score определяется его простотой, использованием предтрансплантационных переменных и способностью объективизировать клинические решения в условиях ограниченных ресурсов. Проспективная валидация и интервенционные исследования, оценивающие клинические исходы при использовании подхода к выбору стратегии консервации, направляемого IRI Score, являются следующими логическими шагами.


