Разработка методики определения хлорамфеникола в мясных продуктах
Автор: Уланова Т.С., Карнажицкая Т.Д., Пшеничникова Е.О., Нахиева Э.А.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Экспериментальные модели и инструментальные исследования
Статья в выпуске: 4 (4), 2013 года.
Бесплатный доступ
Представлены результаты исследований по разработке методики определения хлорамфеникола в мясной продукции с использованием жидкостной хроматографии в сочетании с масс-селективным детектированием (ЖХ/МС). В ходе проведенных исследований отработаны оптимальные условия проведения анализа хлорамфеникола на жидкостном хроматографе Agilent серии 1200 в сочетании с масс-спектрометрическим детектором с тройным квадруполем LC/MS 6460 Agilent Technologies. Изучены условия эффективного извлечения хлорамфеникола из образцов мяса. В качестве оптимального варианта выбран метод жидкостной экстракции этилацетатом с последующей очисткой экстракта гексаном. Степень извлечения антибиотика из матрицы достигает 70–100 % в зависимости от содержания хлорамфеникола в мясопродуктах. Выполнены исследования по установлению метрологических характеристик разработанной методики, в ходе которых определены значения следующих показателей: точность – не превышает 26 %, воспроизводимость – не более 10 %, повторяемость – не более 5 %. Анализ образцов мясной продукции с помощью разработанной методики выявил присутствие антибиотика в 17,6 % проб.
Хлорамфеникол, ветеринарный лекарственный препарат, остатки ветеринарных лекарственных препаратов, мясные продукты, метод жх/мс
Короткий адрес: https://sciup.org/14237848
IDR: 14237848 | УДК: 613.2/3
The development of a method for chloramphenicol determination in meat products
This paper presents the findings of a study on the development of a method for chloramphenicol determination in meat products using liquid chromatography-mass selective detection (LC/MSD). The study determined optimum conditions for chloramphenicol analysis using an Agilent 1200 liquid chromatograph and an Agilent Technologies 6460 triple quadrupole liquid chromatograph/mass spectrometer. The conditions for an efficient extraction of chloramphenicol from meat samples were investigated. The optimum technique was found to be liquid extraction with ethyl acetate followed by further purification with hexane. The values of recovery were in the range of 70 to 100% in the matrix, depending on the levels of chloramphenicol in the meat products. The metrological characteristics of the developed method were evaluated and the values of the following parameters were calculated: the deviation between the mean value and the actual value, which is the measure of accuracy, did not exceed 26%, reproducibility was at most 10% and repeatability was no more than 5%.The analysis of meat product samples carried out using the developed method found that 17.6% of the samples contained the antibiotic.
Текст научной статьи Разработка методики определения хлорамфеникола в мясных продуктах
Хлорамфеникол (левомицетин) является антибиотиком широкого спектра действия. В ветеринарной медицине хлорамфеникол используют для лечения и профилактики возникновения у сельскохозяйственных животных инфекций, вызванных анаэробными бактериями или устойчивых к другим противомикробным средствам. Хлорамфеникол хорошо всасывается при пероральном и парентеральном поступлении, медленно выводится из организма животных и сравнительно долго сохраняет свою активность при хранении продуктов [13]. Для лечения человека хлорамфеникол используют с большой осторожностью. При исследовании токсичных свойств препарата выявлены ге- нотоксичность хлорамфеникола и его метаболитов, эмбриотоксичность, канцерогенный риск для человека и отсутствие корреляции в системе «доза–реакция» в случаях апластической анемии, вызванной лечением хлорамфениколом [8, 10, 11].
При употреблении продуктов животного происхождения, содержащих остатки ветеринарных лекарственных препаратов, в организме человека вырабатывается резистентность к антибиотикам, могут развиваться дисбактериоз, аллергические реакции, снижается иммунитет. При постоянном употреблении пищи с остатками ветеринарных лекарственных препаратов повышается нагрузка на системы и органы, от-
ветственные за выведение чужеродных соединений из организма (печень, почки) [2].
В странах ЕЭС в отношении ряда ветеринарных лекарственных препаратов, в том числе хлорамфеникола, действует запрет на их содержание в пищевых продуктах. Так, в регламенте стран европейского экономического союза (ЕЭС) № 2377/90 от 1990 г. представлены вещества, содержание которых недопустимо в продуктах в сыром и готовом виде, в их числе присутствует хлорамфеникол. В документе Комиссии Codex Alimentarius, утвержденном в июле 2012 г. на 35-й сессии Комиссии, перечислены запрещенные ветеринарные лекарственные препараты, для которых не может быть установлено никакое допустимое остаточное содержание в продуктах, так как остатки в любом количестве создают риск здоровью человека. В данном перечне присутствует хлорамфеникол [7]. В Российском законодательстве действует технический регламент Таможенного союза, в соответствии с которым не допускается присутствие хлорамфеникола в продуктах убоя, предназначенных для производства мясной продукции (примечание: < 0,0003 мг/кг) [6].
Действующие методические указания МУК 4.1.1912-04 устанавливают порядок определения хлорамфеникола в продуктах животного происхождения двумя методами – жидкостной хроматографией, обеспечивающей селективность определения, но имеющей низкую чувствительность – 0,01 мг/кг (арбитражный метод), и иммуноферментным анализом с высокой чувствительностью определения – 0,000012 мг/кг, но недостаточной специфичностью и воспроизводимостью результатов [4]. В соответствии с ГОСТ Р ИСО 13493-2005 «Метод определения содержания хлорамфеникола (левомицетина) с помощью жидкостной хроматографии» минимально определяемая концентрация хлорамфеникола в мясе составляет 0,0065 мг/кг.
В целях обеспечения контроля безопасности продуктов питания необходимо совершенствовать существующие и разрабатывать новые более высокочувствительные и селективные методики анализа. В настоящее время максимальную чувствительность и наиболее точную идентификацию сложных органических соединений в продуктах питания и других биологических образцах обеспечивают современные инструментальные методы газовой и жидкостной хроматографии в сочетании с масс-спектрометрией (ГХ/МС и ЖХ/МС) [1, 5, 13].
Цель исследования – разработка методики определения хлорамфеникола в мясной продукции с использованием жидкостной хроматографии в сочетании с масс-селек-тивным детектированием (ЖХ/МС).
Материалы и методы. Исследования проведены в лаборатории методов жидкостной хроматографии ФБУН «ФНЦ медикопрофилактических технологий управления рисками здоровью населения» на жидкостном хроматографе Agilent серии 1200 с масс-спектрометрическим детектором с тройным квадруполем LC/MS 6460 Agilent Technolo-giesи с ионизацией электростатическим распылением (ESI). В качестве стандартного образца использовали хлорамфеникол чистотой ≥98 % (пр-во SIGMA-ALDRICH).
Разработка методики определения хлорамфеникола в продуктах питания включала следующие этапы:
-
– оптимизация условий масс-спектрометрического анализа;
-
– извлечение хлорамфеникола из образца и очистка извлеченной пробы;
-
– количественное определение и качественное подтверждение наличия остатков хлорамфеникола в пробе.
Оптимизацию параметров масс-спектрометрического детектора для качественного определения хлорамфеникола проводили в автоматическом режиме при использовании программы «Optimizer». По литературным данным в условиях ионизации распылением в электрическом поле (ESI) регистрируются отрицательно заряженные частицы хлорамфеникола, в связи с этим исследования проведены в режиме отрицательной ионизации.
При отработке оптимальных условий хроматографического разделения стандартного образца хлорамфеникола с компонентами матрицы предварительно определили оптимальную длину волны диодно-матричного детектора.
Изучение разделения хлорамфеникола с компонентами матрицы проводили на колонках для обращено-фазной хроматографии: Poroshel 120 EC-C18 длиной 50 мм и внутренним диаметром 3,0 мм, размер частиц 2,7 мкм; Eclipse XDB-C18 длиной 150 мм и внутренним диаметром 2,1 мм, размер частиц 5 мкм; Bonus RP длиной 50 мм и внутренним диаметром 4,6 мм, размер частиц 1,8 мкм.
Для выявления мешающего влияния матричных компонентов анализировали образцы мясного фарша с добавлением и без добавления хлорамфеникола в оптимальном режиме элюирования на колонке Bonus RP.
Следующий этап разработки методики анализа хлорамфеникола в мясных продуктах включал отработку способа подготовки проб к анализу. Подготовка пробы влияет на все последующие стадии анализа антибиотика и, следовательно, является критически важным для абсолютной идентификации, подтверждения и количественного определения аналита. Масс-спектрометрия позволяет использовать более простые универсальные методы очистки. Вместе с тем эффективная очистка матрицы является необходимой мерой, так как компоненты, присутствующие в матрице, могут повлиять на производительность масс-спектрометра, в частности, посредством снижения сигнала детектора [14].
Для выбора оптимального способа подготовки проб мясных продуктов к анализу методом ЖХ/МС проведены экспериментальные исследования по определению эффективности извлечения хлорамфеникола из матрицы с использованием подходов, рекомендуемых в научной и методической литературе, – жидкостной и твердофазной экстракции.
Исследования по определению степени экстракции хлорамфеникола из образцов мяса осуществляли методом «введено– найдено». В образец мясного фарша навеской 10 г вносили известное количество хлорамфеникола, задавая определенную концентрацию антибиотика в мясе (мг/кг). Степень экстракции считали как отношение извлеченного количества к общему (начальному) количеству хлорамфеникола в образце по формуле
„ A - 100 R =------ ,
N где R – степень экстракции хлорамфеникола, %; А – извлеченное количество вещества, мкг; N – общее (начальное) количество вещества, мкг.
Образцы анализировали в оптимальных условиях работы жидкостного хроматографа и масс-спектрометрического детектора.
Техника выполнения процедуры жидкостной экстракции анализируемого вещества из биологической матрицы включала гомогенизацию образца, извлечение аналита из образца подходящим органическим растворителем, разделение фаз, удаление белков, липидов и других соединений из экстракта. По литературным данным для извлечения хлорамфеникола из продуктов питания методом жидкостной экстракции использовались органические растворители: этилацетат, ацетонитрил, смесь этилацетата с ацетонитрилом, смесь хлороформа и ацетона, смесь ацетонитрила и ацетатного буфера (рН 5,0). Среди перечисленных растворителей наибольшее применение в практике анализа хлорамфеникола нашел этилацетат.
Исследования по определению эффективности извлечения хлорамфеникола из мяса этилацетатом проводили по схеме: в образец мясного фарша массой 10 г вносили хлорамфеникол в количестве 0,192 мкг и экстрагировали дважды 20 см3 этилацетата в течение 10 мин; объединенный экстракт высушивали в токе воздуха при температуре 45 °С до образования маслянистого остатка. Образец очищали от белков и жира, добавляя в пробу метанол (для осаждения белков), соль хлорид натрия и 20 см3 гексана (для удаления жиров). После перемешивания и центрифугирования гексановый слой отбрасывали и повторно очищали. Оставшийся раствор дважды экстрагировали этилацетатом. Высушенный экстракт пере-растворяли в смеси метанол:вода и анализи- ровали аликвоту на приборе. Приведенная процедура подготовки проб обеспечивает получение надежных и высокочувствительных результатов анализа хлорамфеникола. Эффективность экстракции данным способом составила 70–99,9 %.
Согласно действующим методическим указаниям МУК 4.1.1912-04 извлечение хлорамфеникола проводится этилацетатом в присутствии буферного раствора. Этилацетатный экстракт очищается от примесей петролейным эфиром и анализируется методом ВЭЖХ.
Изучена возможность применения в качестве пробоподготовки для анализа хлорамфеникола метода QuEChERS, технически представляющего метод дисперсионной твердофазной экстракции, успешно применяющегося в аналитической химии для извлечения пестицидов, антибиотиков и других загрязняющих веществ из продуктов питания растительного и животного происхождения. Пробоподготовка основана на экстракции контаминантов ацетонитрилом из гомогенизированной пробы в присутствии солей, в основном MgSO 4 и NaCl, в условиях оптимального значения рН среды, задаваемого с помощью буферных растворов, и очистке экстракта насыпными полимерными сорбентами. В ходе исследований изучены два варианта пробоподготовки по методу QuEChERS.
Для количественного определения хлорамфеникола использовали метод внешнего стандарта – устанавливали зависимость интенсивности сигнала детектора от концентрации анализируемого соединения в мясе и рассчитывали градуировочный коэффициент.
Важной особенностью анализа химических соединений в биологических субстратах, к которым относятся пищевые продукты, является влияние многокомпонентной матрицы на конечный результат. Для получения достоверных результатов анализа необходимо учитывать мешающее влияние компонентов матрицы, степень извлечения анализируемого вещества, а также погрешность всех этапов подготовки образца к анализу [1, 3]. В связи с этим при построении градуировочной зависимости пробы с содержанием стандартного образца хлорамфеникола в диапазоне концентраций 0,00005–0,02 мг/кг подвергались обработке аналогично исследуемым пробам – экстракцией этилацетатом с последующей очисткой гексаном. Подготовленные пробы анализировали в оптимальных условиях ЖХ/МС анализа.
Градуировочный коэффициент рассчитывали по формуле
n
∑ C i/ S i
K= i=1 , n где Ci – массовая концентрация хлорамфеникола в градуировочном растворе, мг/кг; Si – среднее значение трех измерений площади пика хлорамфеникола i-й концентрации, усл. ед; n – количество градуировочных растворов.
Для расчета метрологических показателей методики (точности, правильности, повторяемости, внутрилабораторной прецизионности) применяли методы математической статистики.
Метрологические показатели методики определения хлорамфеникола в мясных продуктах устанавливали в соответствии с рекомендациями по межгосударственной стандартизации РМГ 61-2010 «Показатели точности, правильности, прецизионности методик количественного химического анализа. Методы оценки» и ГОСТ Р ИСО 5725-1÷6-2002 «Точность (правильность и прецизионность) методов и результатов измерений». Для получения экспериментальных данных готовили серию стандартных образцов хлорамфеникола в мясном фарше (мг/кг) с концентрациями вблизи нижнего, среднего и верхнего значений диапазона измеряемых концентраций
Результаты и их обсуждение. При сканировании дочерних отрицательных ионов в режиме грубой настройки зарегистрированы родительский ион с отношением массы к заряду (m/z) 321 и 4 дочерних иона с соотношением m/z 152, 257, 151,2 и 121. Максимальный отклик детектора получен для до-
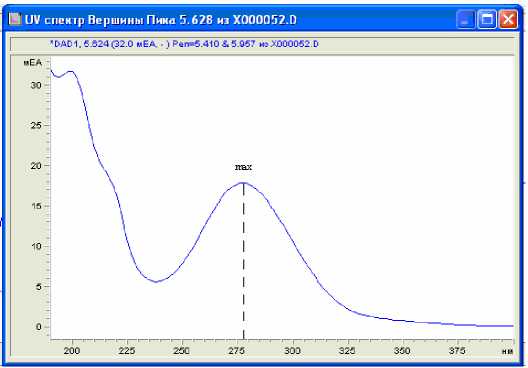
Рис. 1. Спектр поглощения хлорамфеникола в 50%-ном водном растворе метанола, λ max = 278 нм
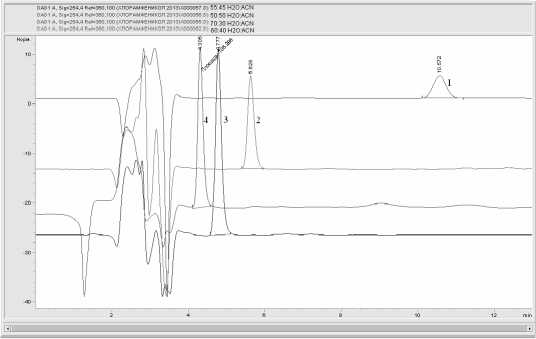
Рис. 2. Хроматограммы стандартного раствора хлорамфеникола, полученные на колонке Bonus RP при соотношении воды и ацетонитрила 70:30 (1), 60:40 (2), 55:45 (3), 50:50 (4)
черних ионов с m/z 152 и 257. На основании полученных результатов в качестве основного иона выбран фрагмент с m/z=152, подтверждающего иона – фрагмент с m/z=257. В режиме тонкой настройки детектора уточнено образование дочерних ионов с соотношением m/z 152,1 и 257,1. При этом значение оптимального напряжения фрагментатора составило 126 V, значения энергии ячейки соударения для дочерних ионов (СЕ) 12 и 4 V. Полученные значения согласуются с приведенными в литературе данными [9, 12].
На основании спектральной характеристики поглощения хлорамфеникола в ультрафиолетовой области света в диапазоне длин волн 190-400 нм в качестве оптимальной для селективного детектирования хлорамфеникола выбрана длина волны 278 нм (рис. 1).
Установлены времена удерживания и интенсивность сигнала хлорамфеникола для каждой колонки в различных режимах элюирования, варьирующихся по соотношению растворителей (вода/ацетонитрил) в подвижной фазе при скорости элюирования 0,2 см3/мин и температуре колонки 25 °С. В ходе исследований установлено, что на колонке Poroshel 120 EC-C18 при соотношениях ацетонитрила и воды 80:20, 75:25, 70:30 и 60:40 анализируемое вещество практически не удерживается, время выхода менее 1 минуты. На колонке Eclipse XDB-C18 оптимальный режим элюирования достигается при соотношении ацетонитрила и воды 55:45, время выхода хлорамфеникола 3,08 мин. На колонке Bonus RP оптимальное элюирование стандартного раствора хлорамфеникола с учетом времени выхода, высоты и симметрии пика протекает при соотношении воды и ацетонитрила 60:40 (рис. 2).
В дальнейших исследованиях использовали колонку Bonus RP. Оптимальные условия элюирования на колонке Bonus RP длиной 50 мм и внутренним диаметром 4,6 мм с размером частиц 1,8 мкм: элюент – смесь воды и ацетонитрила в соотношении 60:40, скорость элюирования 0,2 см3/мин, температура колонки 25 °С. При данных условиях время выхода хлорамфеникола составляет 6,1±0,3 мин. Установлено, что в выбранном режиме элюирования компоненты матрицы полностью разделяются с хлорамфениколом (рис. 3).
Проведенные нами экспериментальные исследования показали, что степень экстракции хлорамфеникола из образцов мяса этилацетатом с очисткой петролейным эфиром составляет 56,4 %.
В первом варианте пробоподготовки по методу QuEChERS экстракция хлорамфеникола этилацетатом проводилась в нейтральной среде, степень извлечения составила 33,2 %. Во втором варианте экстракция протекала в кислой среде (рН=3), степень извлечения хлорамфеникола этилацетатом составила 41,0 %. Результаты изучения
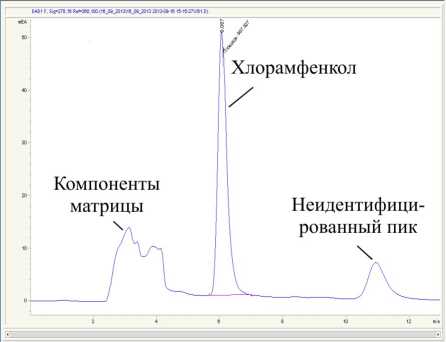
а
Рис. 3. Хроматограммы мясного образца с добавкой ( а ) и без добавки ( б ) стандартного раствора хлорамфеникола, полученные на колонке Bonus RP в оптимальном режиме элюирования
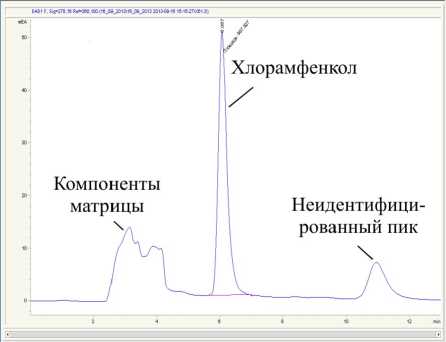
б
степени экстракции хлорамфеникола различными способами пробоподготовки представлены в табл. 1.
При сравнении различных способов пробоподготовки установлено, что максимальная степень экстракции антибиотика из образцов мясного фарша достигается с использованием в качестве растворителя-экстрагента этилацетата с последующей очисткой экстракта гексаном (см. табл. 1). При этом степень экстракции увеличивается от 70 до 99,9 % в зависимости от уменьшения концентрации хлорамфеникола в образце в диапазоне изучаемых концентраций (от 0,00005 до 0,02 мг/кг).
Результаты исследований по определе- нию метрологических характеристик представлены в табл. 2.
Таблица 1
Эффективность извлечения хлорамфеникола из мясной матрицы различными способами пробоподготовки
|
№ п/п |
Способ пробоподготовки |
Степень экстракции, % |
|
|
с учетом матричного эффекта |
без учета матричного эффекта |
||
|
1 |
Жидкостная экстракция этилацетатом и очистка экстракта гексаном |
70–99,9 |
101,3 |
|
2 |
Экстракция по методу QuEChERS в нейтральной среде |
33,2 |
91,0 |
|
3 |
Экстракция по методу QuEChERS в кислой среде (рН = 3) |
41,0 |
77,5 |
|
4 |
Экстракция этилацетатом и очистка экстракта петролейным эфиром |
56,4 |
70,5 |
Таблица 2
Значения показателей точности, повторяемости, воспроизводимости
|
Точка диапазона измерений хлорамфеникола, мг/кг |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σ r , % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости) σ R , % |
Показатель точности (границы относительной погрешности при вероятности р = 0,95), ±δ, % |
|
0,000086 |
4,49 |
9,95 |
25,55 |
|
0,0019 |
2,84 |
4,41 |
10,98 |
|
0,018 |
1,22 |
1,81 |
4,64 |
На основании результатов, представленных в табл. 2, можно заключить, что максимальная погрешность измерения хлорамфеникола в мясных продуктах не превышает 26 % в диапазоне измерений от 0,00005 до 0,02 мг/кг включительно.
В ходе апробации методики определения хлорамфеникола в мясных продуктах ( n =17) антибиотик обнаружен в 17,6 % всех проанализированных проб в диапазоне концентраций от 0,00005 до 0,0019 мг/кг (максимальное содержание 0,0019 мг/кг).
Выводы:
– разработана высокочувствительная и селективная методика хромато-масс-спектрометрического определения хлорамфеникола (левомицетина) в мясных продуктах питания с нижним пределом определения 0,00005 мг/кг, позволяющая контролировать остаточное содержание антибиотика в мясной продукции в соответствии с требованиями технического регламента Таможенного союза «О безопасности мяса и мясной продукции» [6];
– анализ остаточных количеств хлорамфеникола в образцах мясной продукции (говядина, свинина, птица, n = 17) посредством данной методики показал присутствие хлорамфеникола в 17,6 % проб;
– методика может быть рекомендована к применению в лабораториях, осуществляющих контроль качества и безопасности продовольственного сырья и пищевых продуктов.
Список литературы Разработка методики определения хлорамфеникола в мясных продуктах
- Другов Ю.С., Родин А.А. Анализ загрязненных биосред и пищевых продуктов: практическое руководство. -М.: БИНОМ, Лаборатория знаний, 2010. -294 с.
- Егоров Н.С. Основы учения об антибиотиках: учебник для студентов биологических специальностей университетов. -4-е изд. -М.: Высшая школа, 1986. -448 с.
- Онищенко Г.Г., Зайцева Н.В., Уланова Т.С. Контроль содержания химических соединений и элементов в биологических средах: руководство. -Пермь: Книжный формат, 2011. -520 с.
- МУК 4.1.1912-04. Определение остаточных количеств левомицетина (хлорамфеникола, хлормицетина) в продуктах животного происхождения методом высокоэффективной жидкостной хроматографии и иммуноферментного анализа: методические указания. -М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004. -26 с.
- Панин А.Н., Комаров А.А. Проблемы аналитического контроля безопасности кормов и продукции животноводства//Журнал Российского химического общества им. Д.И. Менделеева. -2005. -Т. XLIX, № 3. -С. 71-82.
- Технический регламент Таможенного союза «О безопасности мяса и мясной продукции» ТР ТС 034/2013/утвержден решением Совета Евразийской экономической комиссии № 68 9 октября 2013 г. -URL: http://socialvet.ru/blog/vetrinarni_meri_tsouz/3270.html (дата обращения: 10.09.2013).
- Codex Alimentarius Commission Maximum Residue Limits for Veterinary Drugs in Foods Updated as at the 35th Session of the Codex Alimentarius Commission (July 2012) CAC/MRL 2-2012. -URL: http://www.codexalimentarius.org/input/download/standards/45/MRL2_e.pdf (дата обращения: 10.09.2013).
- European Committee for Veterinary Medicinal Products. Chloramphenicol summary report. 1994. -European Agency for the Evaluation of Medicinal Products. -URL: http://www.emea.eu.int/pdfs/vet/mrls/chloramphenicol.pdf (дата обращения: 18.05.2004).
- Heidi R., James S., Hurlbut J. LC/MS/MS Analysis of Chloramphenicol in Crab Meat/U.S. Food and Drug Administration, Pacific Regional Lab Northwest, 22201 23rd Drive SE, Bothell, WA 98021//Laboratory Information Bulletin. -2003, April. -Vol. 19, № 4. -URL: http://www.fda.gov/Food/FoodScienceResearch/LaboratoryMethods/ucm113380.htm (дата обращения: 21.08.2013).
- IARC Monographs on the evaluation of carcinogenic risk of chemicals to humans//Chloramphenicol. -Lyon: IARCPress, 1990. -Vol. 50. -P. 169-193.
- Interaction of chloramphenicol and metabolites with colony stimulating factors: possible role in chloramphenicol-induced bone marrow injury/J.J. Jimenez, J.G. Jimenez, D. Daghistani and A.A. Yunis//Am. J. Med. Sci. -1990. -Vol. 300. -P. 350-353.
- Neuhaus В., Hurlbut J., Hammack W. LC/MS/MS Analysis of Chloramphenicol in Shrimp//Laboratory Information Bulletin. -2002. -№ 4290.
- Plumb D.C. Veterinary Drug Handbook. -Ames: Iowa State Press, 2002. -4th Ed. -P. 166-169.
- Wang J., Macneil J.D., Kay J.F. Chemical analysis of antibiotic residues in food. -Wiley, 2012. -353 p.


