Разработка микробиологического метода снижения вредоносности фузариоза на сое
Автор: Маслиенко Л.В., Курилова Д.А.
Рубрика: Защита и иммунитет
Статья в выпуске: 2 (151-152), 2012 года.
Бесплатный доступ
Представлены результаты ступенчатого скрининга коллекционных штаммов лаборатории биометода ВНИИМК к патогенному изоляту гриба Fusarium sporotrichiella Bilai var. poae (Pk.) Wr. emend Bilai. В результате отобраны два наиболее эффективные штаммы антагонистов Xk-1 Chaetomium olivaceum Cook et Ellis и 14-3 Pseudomonas chlororaphis. Установлена высокая биологическая эффективность лабораторных образцов микробиопрепаратов на фоне искусственного заражения возбудителем фузариоза и положительное влияние на культуру сои. Изучены физиологические признаки перспективного бактериального штамма-продуцента 14-3 Pseudomonas chlororaphis. Установлена совместимость перспективных штаммов Xk-1 Ch. olivaceum и 14-3 P. chlororaphis с рекомендованными к применению на сое фунгицидами с целью возможного совместного применения в интегрированной системе защиты.
Фузариоз, соя, антагонисты, грибы, бактерии, микробиопрепараты, скрининг, штаммы, ростостимуляция, антибиотическая активность, периодическое культивировоние
Короткий адрес: https://sciup.org/142151083
IDR: 142151083 | УДК: 632.937:633.853.52
Development of the microbiological method of decreasing the fusarium harmfulness in soybean
The article gives the results of stepped screening of strains from the collection of VNIIMK’s biomethods laboratory to the pathogenic isolate of fungus Fusarium sporotrichiella Bilai var. poae (Pk.) Wr. emend Bilai. Consequently, two the most effective strains of antagonists were selected: Xk-1 Chaetomium olivaceum Cook et Ellis and 14-3 Pseudomonas chlororaphis. There was established the high biological efficiency of laboratory samples of microbiological products against the background of the artificial infection by fusarium agent and positive effect on soybean crop. The physiological signs of promising bacterial producer strain of 14-3 Pseudomonas chlororaphis were studied. For the purpose of possible joint application in the integrated protection system, there was established the compatibility of promising strains of Xk-1 Ch. olivaceum and 14-3 P. chlororaphis with fungicides recommended for application to soybean.
Текст научной статьи Разработка микробиологического метода снижения вредоносности фузариоза на сое
Введение. Соя поражается грибными, бактериальными и вирусными болезнями. В нашей стране особой вредоносностью отличаются болезни всходов и увядания растений, одним из возбудителей которых является Fusarium spp. [1; 2; 3]. На посевах сои фузариоз встречается повсеместно. Согласно литературным данным использование живых культур микроорганизмов в борьбе с фузариозными заболеваниями растений является наиболее интересным подходом. Этот метод микробиозащиты не только менее опасен с точки зрения защиты окружающей среды, но и более обоснован с позиции эволюционного осмысления соотношения паразитических и сапрофитных свойств фузариев. Поскольку грибы рода Fusarium являются почвообитающими факультативными паразитами, способными длительное время вести сапрофитное существование, то интродукция антагонистов должна создавать дополнительное давление в сторону элиминирования агрессивных рас [4; 5].
Стратегия биологического метода защиты растений от болезней не ставит задачу полного уничтожения вредных организмов, а ориентируется на регулирование популяции патогена на уровне ниже экономического порога вредоносности [6]. Грамотное и своевременное применение микробиологических средств защиты растений на фоне высокой агротехники может значительно улучшить фитосанитарную обстановку посевов и значительно увеличить урожай, поскольку микробиологические средства защиты растений оказывают положительное влияние на растения и других членов агроценозов.
Целью данной работы являлась разработка эффективного и экологически допустимого микробиологического метода снижения вредоносности фузариоза на сое.
Материалы и методы. Объектом исследований служили: штаммы грибов и бактерий-антагонистов возбудителей болезней масличных культур, тест-культура возбудителя фузариоза сои, лабораторные образцы микробиопрепаратов. Грибы и бактерии, проявляющие антагонизм в отношении патогенных фузариозных грибов, были взяты из коллекции микроорганизмов лаборатории биометода ВНИИМК. В качестве тест-объекта для испытания антагонистической активности штаммов грибов и бактерий был выбран наиболее патогенный и агрессивный для сои изолят гриба Fusarium sporotrichiella Bilai var. poae (Pk.) Wr. emend Bilai, выделенный из корневой системы сои.
Определение антагонистической активности грибных и бактериальных штаммов проводили методом двойных (встречных) культур [7; 8] на картофель-но-сахарозном агаре (КСА) или среде Кинга В, при двух температурных режимах: 25 и 10 оС. Изучали характер взаимоотношений антагониста и патогена: наличие или отсутствие стерильных зон, их размер, изменение цвета, плотности, толщины и направления роста мицелия патогена. Все активные штаммы грибов при совместном культивировании с возбудителем фузариоза изучали по пяти типам взаимоотношений [9]. Взаимоотношения бактерий с возбудителем фуза-риоза изучали по образованию стерильных зон антибиотического действия или обладающих высоким показателем подвижности [10].
Определение фитотоксичности штаммов проводили методом обработки семян сои опытными партиями микробиопрепаратов и методом погружения подрезанной корневой системы здоровых 7-дневных проростков сои в суспензию штаммов антагонистов. Для изучения ростостимулирующего влияния перспективных штаммов на проростки сои, семена обрабатывали опытными партиями микробиопрепаратов и помещали на проращивание в рулоны из фильтровальной бумаги (в течение 7 дней при температуре 25 оС). Параметрами для последующего анализа служили длина и масса корня и побега.
Защитный эффект жидких культур (ЖК) и водных суспензий (ВС) штаммов антагонистов прорастающего семени и подбор оптимальных норм их применения определяли на фоне искусственного заражения семян сои F. sporotrichiella var. poae в лабораторных условиях во влажной камере методом агаровых блоков [11]. Контроль – чистые семена без нанесения инфекции и с нанесением инфекции. Опыт проводился при 25 оС. Активные штаммы антагонистов наращивали на подобранных средах. Перед обработкой семян определяли титр микробиопрепаратов. Титр ЖК и ВС во всех опытах определяли методом Коха [12].
Биологическую эффективность биопрепарата определяли по формуле [13]:
1 О О x (а - b ) C = , где C – биологическая эффективность;
a – количество больных растений в контроле;
b – количество больных растений в варианте.
Для определения колонизирующей активности и защитного эффекта штаммов антагонистов корней проростков сои использовали методические рекомендации по оценке и отбору растений подсолнечника на устойчивость к фузариозной корневой гнили [14]. Оценку степени поражения проростков возбудителем фу-зариоза производили согласно разработанной нами 6-балльной шкале.
Для создания искусственного фона заражения почвы фузариозом в лабораторных условиях на основе общепринятых методик [15; 16] нами были испытаны различные способы и нормы внесения инфекционного начала фитопатогена [17]. Учеты производили на 7 и 10-й день после посева.
Изучение физиологических особенностей перспективного штамма антагониста 14-3 Pseudomonas sp. проводили на жидкой питательной среде Кинга В. Культивирование микроорганизма осуществляли глубинным способом на качалке со скоростью вращения 195 об./мин, в колбах Эрленмейера (750 мл) при объеме среды 150 мл. Оптимальные параметры физиологических признаков определяли по количеству колониеобразующих единиц (КОЕ) в 1,0 мл жидкой культуры (титр). Повторность в каждом опыте – 3-кратная. Для определения оптимальной температуры культивирования, штамм бактерии выращивали при температурах 20, 25, 30 и 35 °С. Для определения оптимальной кислотности среды, pH устанавливали в пределах 3, 5, 6, 7, 8, и 10, добавляя лимонную кислоту или щелочь (4Н раствор NaOH). Устанавливали оптимальные источники углеродного и азотного питания. Источниками углеродного питания служили глюкоза, сахароза, глицерин и меласса. Источниками азотного питания служили азотнокислый натрий, пептон, дрожжевой и кукурузный экстракты. При подборе оптимальных питательных сред для выращивания перспективного штамма бактерии испытывали ряд сложных питательных сред: мясо-пептонный бульон (МПБ), Кинга В, Чапека для бактерий, пептонодрожжевая, в состав которых вхо- дят минеральные соли, сахара, микроэлементы, кукурузный и дрожжевой экстракты.
Для изучения динамики периодического роста, глубинное культивирование штамма бактерии осуществляли при оптимальных условиях в течение 4 суток, с предварительным внесением посевной (маточной) культуры (2 % от объема питательной среды). Для выращивания культуры использовали питательную среду Кинга В. Пробы для анализа брали через 8, 16, 24, 36, 48 и 72 часа после начала культивирования.
Антибиотическую активность определяли методом диффузии в агар [8].
Определение совместимости штаммов-продуцентов микробиопрепаратов с перспективными пестицидами проводили, используя модифицированный метод диффузии в агар, разработанный для определения антибиотической активности микроорганизмов [18; 19].
Результаты и обсуждения. На первом этапе скрининга тестировали 20 грибных штаммов из коллекции перспективных штаммов антагонистов фитопатогенов масличных культур лаборатории биометода ВНИИМК, представленных родами Trichoderma , Penicillium , Chaetomium , Trichothecium , Sordaria , Talaromyces и классом Basidiomycetes ; и 26 бактериальных штаммов, представленных родами Bacillus и Pseudomonas .
В результате первичного скрининга штаммов грибов и бактерий антагонистов к возбудителю фузариоза сои F. sporo-trichiella var. poae при двух температурных режимах 25 и 10 ºС наибольшую эффективность показали 12 штаммов антагонистов, среди которых 5 штаммов грибов: Tk-1 Trichoderma koningii , T-4 Trichoderma sp ., Sm-1 Sordaria macro-spora, A-1 Basidiomycetes , Хk-1 Chaetomi-um olivaceum , и 7 штаммов бактерий: 12-2 Pseudomonas sp . , 14-3 Pseudomonas sp. , Sgrc-1 P. fluorescens , Far 8 Bacillus sp ., 111 Bacillus sp ., Б-5 B. liche-niformis , Б-12 B. licheniformis [20].
Следующим этапом скрининга стало исследование возможного токсического воздействия активных штаммов антагонистов на культуру сои. Анализ данных показал, что тестируемые штаммы не оказывают негативного влияния на всхожесть семян и не вызывают увядания проростков. Более того, отмечено повышение всхожести семян по сравнению с контролем на 9,0–20,0 % [21].
Изучение ростостимулирующего влияния перспективных штаммов антагонистов на проростки сои показало, что наиболее сильное влияние штаммы оказывали на длину и массу корня. Максимальное увеличение длины корня (на 22,0–25,2 %) наблюдалось у штаммов грибов Xk-1 Ch. olivaceum , Tk-1 T. konin-gii. Максимальное увеличение массы корня (на 13,3–20,0 %) наблюдалось в вариантах с грибом Xk-1 Ch. olivaceum и бактериями 12-2 и 14-3 Pseudomonas sp . Влияние штаммов антагонистов на длину и массу стебля также отмечено, но в меньшей степени (2,6–11,5; 8,5–9,8 % соответственно) [21].
Определение защитного эффекта перспективных штаммов антагонистов прорастающего семени сои от фузариоза, а также отработку оптимальных норм расхода опытных образцов биопрепаратов проводили во влажной камере, используя метод агаровых блоков. Для бактериальных штаммов испытывались нормы от 0,5 до 3,0 л/т, для грибных штаммов от 2,0 до 4,0 л/т. Оптимальными были признаны: для бактериальных штаммов рода Pseudomonas 12-2 и Sgrc-1 – 1,0 л/т, для 14-3 – 2,0 л/т; для грибных штаммов Хk-1 Ch. oli-vaceum и Pv-3 P. verrucosum – 3,0 л/т; для Sm-1 S. macrospora, Tk-1 Tr. koningii и А-1 Basidiomycetes – 4,0 л/т. Максимальная биологическая эффективность на фоне поражения фузариозом в контроле 58,6 % установлена у штаммов: 12-2 Pseudomonas sp . (65,9 %), Хk-1 Ch. olivaceum (59,0 %), 14-3 Pseudomonas sp . (52,2 %), Tk-1 T. koningii (49,8 %), Sm-1 S. macrospora и Sgrc-1 Pseudomonas sp . (47,6 %).
Изучение колонизирующей активности, а одновременно и защитного эффекта, показало, что на жестком (100 %) фоне заражения F. sporotrichiella var. poae максимальную эффективность проявили штаммы: 14-3 Pseudomonas sp., Pv-3 P. verru- cosum, Б-5 B. licheniformis, Sgrc-1 P. fluo-rescens, 12-2 Pseudomonas sp., Sm-1 S. macrospora и Xk-1 Ch. olivaceum. В этих вариантах от 40,0 до 100 % проростков оказались жизнеспособными, тогда как в контрольном варианте жизнеспособных проростков не обнаружено.
Максимальная биологическая эффективность на фоне искусственного заражения семян сои фузариозом в почве отмечена у штаммов Xk-1 Ch. olivaceum (33,9 %), Tk-1 T. koningii (27,2 %) и 14-3 Pseudomonas sp . (20,3 %), при поражении в контроле 79,7 % [17].
Принимая во внимание положение о том, что успешный биоагент должен обладать комплексом положительных свойств на растение [22; 23], мы объединили весь спектр данных, полученных по скринингу активных штаммов антагонистов (рис. 1).
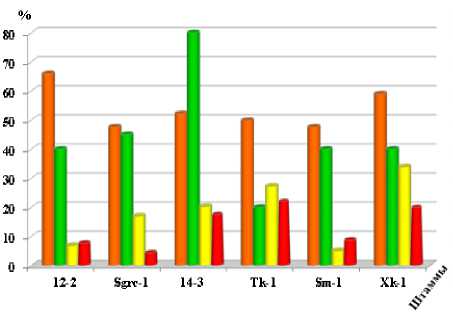
Рисунок 1 – Защитный эффект и колонизирующая активность на фоне искусственного заражения Fusarium sporotrichi-ella var. poae , а также ростостимулирующее действие микробиопрепаратов на основе перспективных штаммов антагонистов при обработке семян сои: – защитный эффект во влажной камере;
■ – колонизирующая активность во влажной камере;
– защитный эффект в почве;
■ – ростостимулирующее действие перспективных штаммов антагони- стов на проростки сои.
В результате анализа полученных экспериментальных данных в качестве продуцентов микробиопрепаратов для защиты растений сои от фузариоза были отобраны штаммы Xk-1 Chaetomium olivaceum Cook et Ellis и 14-3 Pseudomonas sp. Данные штаммы не только обеспечивали эффективную защиту семян и проростков сои на жестком фоне искусственного заражения возбудителем фуза-риоза, но и активно колонизировали корень, одновременно оказывая ростостимулирующее действие на культуру сои.
Согласно видовой идентификации штамма 14-3 Pseudomonas sp., проведённой в Центре «Биоинженерия» (г. Москва), изолят 14-3 является штаммом вида Pseudomonas chlororaphis.
Так как гриб Ch. olivaceum является продуцентом микробиопрепарата Хетомин, разработанного ранее в лаборатории биометода , основная часть дальнейших исследований проводилась по изучению бактериального штамма 14-3 P. chlororaphis.
Существенное значение для роста микроорганизмов имеет такой фактор внешней среды, как температура (табл. 1).
Таблица 1
Влияние температуры на рост штамма бактерии-антагониста 14-3 P. chlorora-phis в процессе периодического культивирования
|
Штамм |
Титр ЖК, КОЕ/мл |
||||
|
маточная культура |
температура, °С |
||||
|
20 |
25 |
30 |
35 |
||
|
14-3 P. chloro-raphis |
6,2х1010 |
1,4х109 |
2,9х1012 |
5,7х1012 |
2,3х1010 |
Максимальный титр клеток отмечен при 25 и 30 °С (2,9–5,7 × 1012). Следовательно, данный температурный диапазон является оптимальным для роста штамма 14-3 P. chlororaphis.
Одним из важных факторов, определяющих нормальный рост бактерий, является реакция рН среды. При изменении ее в неблагоприятную сторону микроорганизм перестает расти даже в тех случаях, если все остальные условия окружающей среды будут оптимальными [25].
Максимальный титр штамма 14-3 отмечался при рН среды 5,0 (5,3 × 1014), достаточно высокий при рН 6,0–10,0 (от 3,2 × 1012 до 2,1 × 1013) (табл. 2). Лимитирующим оказалось значение реакции среды 3,0, при котором выживали лишь единичные клетки. Следовательно, для штамма 14-3 P. chlororaphis оптимальным является достаточно широкий диапазон реакции среды – 5,0–10,0.
Таблица 2
Влияние реакции рН среды на рост штамма бактерии-антагониста 14-3 P. chlororaphis в процессе периодического культивирования
|
Штамм |
Титр ЖК, КОЕ/мл |
||||||
|
маточная культура |
рН |
||||||
|
3,0 |
5,0 |
6,0 |
7,0 |
8,0 |
10,0 |
||
|
14-3 P. chlorora-phis |
4,7 × 1014 |
8,0 × 103 |
5,3 × 1014 |
2,1 ×1013 |
6,0 × 1012 |
8,4 ×1012 |
3,2 ×1012 |
Для определения оптимальных источников углеродного и азотного питания штамм 14-3 P. chlororaphis выращивали при температуре 25,0 °С и рН среды 5,0. Максимальный титр штамма-продуцента отмечен в вариантах с добавлением глюкозы, глицерина и сахарозы (2,8–8,3 ×
1012 КОЕ/мл). Также хорошее развитие культура бактерии получила в варианте с мелассой (2,1 × 1010 КОЕ/мл) (табл. 3).
Таблица 3
Влияние источников углерода на рост штамма бактерии-антагониста 14-3 P. chlororaphis в процессе периодического культивирования
|
Штамм |
Титр ЖК, КОЕ/мл |
||||
|
маточная культура |
источник углерода |
||||
|
глицерин |
глюкоза |
сахароза |
меласса |
||
|
14-3 P. chloro-raphis |
4,9×1014 |
4,0×1014 |
2,8×1014 |
8,3×1014 |
2,1×1012 |
При испытании источников азота установлено, что добавление кукурузного экстракта в среду приводит к полной гибели клеток. На питательной среде с добавлением азотнокислого натрия отмечен низкий титр штамма (3,5 × 103 КОЕ/мл). Тогда как высокий титр штамма 14-3 наблюдался при использовании пептона и дрожжевого экстракта (2,1–4,4 × 1012 КОЕ/мл) (табл. 4).
Таблица 4
Влияние источников азота на рост штамма бактерии-антагониста 14-3 P. chlororaphis в процессе периодического культивирования
|
Штамм |
Титр ЖК, КОЕ/мл |
||||
|
маточная культура |
источник азота |
||||
|
пептон |
дрожже -вой экс тракт |
азотнокислый натрий |
кукурузный экстракт |
||
|
14-3 P. chloro-raphis |
2,9×1014 |
2,1×1014 |
4,4×1014 |
3,5×105 |
0 |
Определение оптимальных питательных сред для культивирования штамма 14-3 P. chlororaphis проводили на сложных синтетических и органосинтетических средах (табл. 5).
Таблица 5
Влияние питательных сред на рост штамма бактерии-антагониста 14-3 P. chlororaphis в процессе периодического культивирования
|
Штамм |
Титр ЖК, КОЕ/мл |
||||
|
маточная культура |
с |
еда |
|||
|
Кинга В |
Чапека для бактерий |
пептоно-дрожжевая |
мясо-пептонный бульон |
||
|
14-3 P. chloro-raphis |
3,2×1014 |
3,5×1012 |
2,2×1010 |
4,8×1012 |
2,9×107 |
Максимальный титр отмечен при культивировании бактериального штамма на пептон-дрожжевой и среде Кинга В (3,5– 4,8 × 1012 КОЕ/мл). Также хорошее развитие культура получила на среде Чапека для бактерий (2,2 × 1010 КОЕ/мл). На МПБ был получен низкий титр (2,9 × 107 КОЕ/мл). При этом, принимая во внимание титр маточной культуры (3,2 × 1014 КОЕ/мл) и посевной объем (3,0 мл на 150 мл стерильной питательной среды), можно сделать вывод о том, что бактерии не размножались, а находились в состоянии покоя, сохраняя жизнеспособность.
Изучение кинетики роста штамма 14-3 P. chlororaphis показало, что лучшими сроками культивирования данной бактерии являются 36–48 часов. Образцы жидкой культуры биопрепарата в этот период характеризовались высоким титром (1,6– 1,7 × 1013 КОЕ/мл) (табл. 6).
Таблица 6
Рост штамма бактерии-антагониста 14-3 P. chlororaphis в процессе периодического культивирования
|
Время культивирования, час |
Титр жидкой культуры штамма, КОЕ/мл |
|
8 |
3,0 × 10 6 |
|
16 |
4,2 × 10 9 |
|
24 |
7,8 × 10 12 |
|
36 |
1,6 × 10 13 |
|
48 |
1,7 × 10 13 |
|
72 |
1,8 × 10 12 |
|
96 |
4,3 × 10 10 |
Антибиотическую активность штамма-продуцента определяли в зависимости от срока периодического культивирования методом диффузии в агар. Установлено, что максимальная антибиотическая активность штамма 14-3 P. chlororaphis к возбудителю фузариоза сои, которая оказывала стойкое сдерживающее действие на патоген, наблюдалась через 72–96 часов культивирования (табл. 7).
Таблица 7
Антибиотическая активность штамма бактерии-антагониста 14-3 P. chlororaphis к возбудителю фузариоза F. sporotrichiella var. poae при периодическом культивировании
|
Вариант |
Срок культи-вирования штамма, час |
Срок выращивания Fusarium sporotrichiella var. poae , сут. |
|||||||
|
рост мицелия патогена, балл |
|||||||||
|
2 |
3 |
4 |
5 |
6 |
7 |
10 |
15 |
||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Контроль 14-3 P. chlor-oraphis |
8 |
2 2 |
5 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
|
Контроль 14-3 P. chlo- roraphis |
16 |
2 2 |
5 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
|
Контроль 14-3 P. chloro-raphis |
24 |
2 2 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
|
Контроль 14-3 P. chloro-raphis |
36 |
2 3 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
6 6 |
Продолжение таблицы 7
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Контроль 14-3 P. chloro- |
48 |
2 |
5 |
6 |
6 |
6 |
6 |
6 |
6 |
|
raphis |
2 |
6 |
6 |
6 |
6 |
6 |
6 |
6 |
|
|
Контроль 14-3 P. chloro- |
72 |
3 |
6 |
6 |
6 |
6 |
6 |
6 |
6 |
|
raphis |
2 |
4 |
5 |
5 |
5 |
5 |
5 |
5 |
|
|
Контроль 14-3 P. chloro- |
96 |
3 |
6 |
6 |
6 |
6 |
6 |
6 |
6 |
|
raphis |
2 |
4 |
4 |
5 |
5 |
5 |
5 |
5 |
Примечание: 2 балла – рост мицелия патогена на 15,0–25,0 % площади питательной среды; 3 балла – рост мицелия патогена на 30,0–40,0 % площади питательной среды; 4 балла – рост мицелия патогена на 45,0–60,0 % площади питательной среды; 5 баллов – рост мицелия патогена на 65,0–80,0 % площади питательной среды; 6 баллов – рост мицелия патогена на 85,0–100,0 % площади питательной среды.
Таким образом, для штамма 14-3 P. chlororaphis установлены оптимальные условия (t – 25–30 оС, рН – 5–10) и сроки культивирования (с учетом синтеза максимальной концентрации антибиотических веществ) – 72 часа.
Для установления возможности совместного применения грибного штамма Xk-1 Ch. olivaceum и бактериального штамма 14-3 P. chlororaphis определяли их совместимость методом встречных культур (рис. 2).
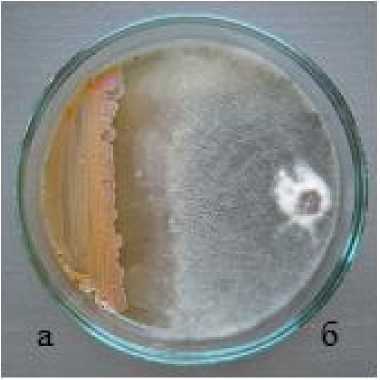
Рисунок 2 – Совместимость перспективных штаммов-продуцентов микробиопрепаратов на 10 сутки инкубации:
а – штамм 14-3 P. chlororaphis ;
б – штамм Xk-1 Ch. olivaceum.
На 7-е сутки инкубации наблюдалась явная антагонистическая активность штамма 14-3 P. chlororaphis по отношению к штамму Хk-1 Ch. olivaceum , которая выражалась в образовании антибиотической зоны (14 мм), тогда как в чистой культуре гриб занял всю площадь питательной среды чашки Петри. На 10-е сутки совместного культивирования расстояние между штаммами сократилось до 8 мм, однако вблизи зоны мицелий штамма Xk-1 был тонкий, паутинистый, плодовые тела отсутствовали. На 14-е сутки инкубации изменений не произошло. Таким образом, нами установлено, что штаммы Xk-1 и 14-3 несовместимы между собой, что исключает их совместное применение.
Следующим этапом исследований стало определение совместимости разработанных лабораторных образцов микробиопрепаратов и химических фунгицидов, разрешённых к применению на сое, с целью определения возможности их совместного применения в интегрированной системе защиты сои от комплекса болезней. Установлено, что штамм 14-3 P. chlororaphis совместим со всеми фунгицидами, рекомендуемыми в настоящее время для обработки семян сои: ТМТД, ВСК (тирам, 400 г/л), Максим, КС (флу-диоксонил, 25 г/л), Фундазол, СП, (бено-мил, 500 г/кг). Это делает возможным его применение в сложных композиционных составах для обработки семян сои. Грибной штамм Xk-1 Ch. olivaceum оказался совместим только с ТМТД, ВСК (тирам, 400 г/л), который оказывал на него незначительное ингибирующее действие. Такие препараты, как Максим, КС (флу-диоксонил, 25 г/л) и Фундазол, СП, (беномил, 500 г/кг) существенно задерживали рост гриба, что исключает их совместное применение [26].
Выводы. По итогам ступенчатого скрининга отобраны перспективные штаммы-продуценты микробиопрепаратов: Хк-1 Ch. olivaceum и 14-3 P. chloro-raphis, обеспечивающие эффективную защиту семян и проростков сои на жёстком фоне искусственного заражения фу-зариозом во влажной камере и в почве, активно колонизирующие корень, одновременно оказывающие стимулирующее влияние на культуру сои.
Для штамма 14-3 P. chlororaphis установлены оптимальные условия (температура 25,0–30,0 оС, рН 5–10) и сроки культивирования (с учетом синтеза максимальной концентрации антибиотических веществ) – 72 часа, элементы питания (источники углерода – глюкоза, глицерин, сахароза и меласса; источники азота – пептон и дрожжевой экстракт), питательные среды (пептон-дрожжевая и Кинга В).
При изучении совместимости лабораторных образцов микробиопрепаратов и химических фунгицидов была определена возможность их совместного применения в интегрированной системе защиты сои от комплекса болезней (14-3 P. chloro-raphis – с ТМТД, ВСК, Максим, КС, Фундазол, СП; Хк-1 Chaetomium olivaceum – с ТМТД, ВСК). Совместное же применение штаммов Xk-1 и 14-3 не представляется возможным.
Работа выполнена при финансовой поддержке гранта РФФИ № 09-08-00726-а и программы У.М.Н.И.К., государственный контракт №14046.


