Разработка неинвазивного метода оценки функционального состояния остаточной паренхимы печени и эффективность его применения у пациентов с очаговыми образованиями печени
Автор: Тарасенко С.В., Жучкова У.В., Копейкин А.А., Натальский А.А.
Журнал: Хирургическая практика @spractice
Статья в выпуске: 3, 2017 года.
Бесплатный доступ
В ходе исследования разработан и внедрен в клиническую практику неинвазивный морфо-функциональный индекс, с помощью которого обследовано 46пациентов с очаговыми образованиями печени. Показана выраженная корреляционная взаимосвязь биохимических показателей, достоверно отража- ющих изменение функций печени, и значений разработанного «индекса резектабельности», рассчитанного на дооперационном этапе. Проведен анализ послеоперационных осложнений, определено значение «индекса резектабельности», превышение которого статистически значимо увеличивало риск раз- вития послеоперационной печеночной недостаточности.
Очаговые образования печени, неинвазивный метод оценки
Короткий адрес: https://sciup.org/142221812
IDR: 142221812 | УДК: 616.36-006
The development of noninvasive method of assessment the functional state of the residual parenchymathe liver and the efficiency of its use in patients with focal lesions of the liver
During the study was developed and introduced into clinical practice a non-invasive morpho-functional index, using which were examined 46 patients with focal liver formations. The study demonstrated pronounced correlation biochemical indicators, authentically reflecting changes in liver function, and meanings of "resectional index", developed by the authors, defined at the preoperative stage. Was analyzed postoperative complications, defined value of the "resectional index", the excessing of which statistically significantly increased the risk of severe postoperative hepatic failure.
Текст научной статьи Разработка неинвазивного метода оценки функционального состояния остаточной паренхимы печени и эффективность его применения у пациентов с очаговыми образованиями печени
Актуальность
Послеоперационная печеночная недостаточность (ППН) – одно из наиболее тяжелых осложнений в гепатобилиарной хирургии, занимающее лидирующее место в структуре смертности послевыполнения обширных резекций печени (ОРП) (по данным разных авторов от 0 до 32%) [1]. В последнее десятилетие ППН привлекала все больше и больше внимания разных авторов и исследователей. В 2006 году для стандартизации понятия и четкого стадирования Международной исследовательской группой по хирургии печени (ISGLS) было дано определение и классификация ППН [2]. Так, ППН – недостаточность одной или более функций печени (секреторной, дезинтоксика-ционной, синтетической и т.д.).
Обычное течение реабилитации печени после ОРП проявляется типичными лабораторными изменениями в виде тран-зиторной гипербилирубинемии, повышением уровня мембранозависимых и цитоплазматических ферментов, являющихся маркерами цитолиза и холестаза, снижением биосинтетической функции печени – гипопротеинемией и гипокоагуляцией (снижение синтеза фибриногена, протромбина и иных прокоагулянтов) [3]. По истечению срока интенсивных регенераторных процессов, признаки печеночной недостаточности должны купироваться, в противном случае речь идет о прогрессирующей ППН, основными предикторами которой является низкий дооперационный функциональный резерв печени или недостаточный объем остаточной паренхимы [4]. Одним из факторов риска развития ППН является длительная ишемия печени и артериальная гипотония вследствие массивной интраоперационной кровопотери [5].
Уровень гипербилирубинемии выше 50 мкмоль/л и ПТИ менее 50% (выраженного в МНО, в норме >1,7) являются важными диагностическими маркерами в развитии ППН и входят в состав критерия 50-50 [6]. В соответствии с рекомендациями ISGLS, ППН разделяют на 3 класса: А-класс– с незначительными отклонениями от стандартного послеоперационного течения, В-класс – пациенты, которым требуется медикаментозная коррекция без проведения экстракорпоральных методов детоксикации, С-класс – необходимо проведение экстракорпоральных методов детоксикации [2].
Для оценки функциональных показателей используют ряд тестов, отражающих способность печени транспортировать органические анионы: клиренс бромсульфталеина и индоцианина зеленого, клиренс галактозы, кофеина и лидокаина, дыхательные тесты – аминопириновый и 13С-метацетиновый [4]. Разными авторами предлагается к использованию новые способы ранней диагностики ППН, основанные на вычислении комплексных индексов - PLFEI (индекс печеночной функции) [7], комплексном применении 13С-метацетинового дыхатель- ного теста и сцинтиграфии [8], критерия прогноза клинически значимых (класс В и С) форм ППН [9]. Разработка и внедрение в клиническую практику новых доступных методов оценки пострезекционного потенциала, позволяющих прогнозировать развитие ППН, по-прежнему остается крайне актуальной.
Целью исследования является разработка неинвазивного метода оценки функционального состояния остаточной паренхимы печени для прогнозирования послеоперационной печеночной недостаточности у пациентов с очаговыми образованиями печени.
Материалы и методы
Проведено проспективное когортное исследование. Дизайн исследования открытый. Анализированы результаты обследования и хирургического лечения 46 пациентов с очаговыми образованиями печени, находившихся на лечении в ГБУ РО «ГКБСМП» в период с 2011по 2017 год включительно. Из 46 пациентов, включенныхв исследование,было 17 мужчин (36,96%) и 29 женщин (63,04%), средний возраст – 54,04+10,45 лет. Этим пациентам при планировании оперативного лечения проводилась оценка функционального состояния остаточной паренхимы печени с определением «индекса резектабельности» (IR), разработанного в ходе клинического исследования.
Пациенты с доброкачественными новообразованиями печени составили 32,61% (n=15), с верифицированным холангио-целлюлярным раком (ХЦР) внепеченочных желчных протоков – 23,91% (n=11), метастазами колоректального рака (КРР) в печень – 43,48% (n=20).
Пациенты с очаговыми образованиями доброкачественной этиологии были представлены следующими нозологическими группами: эпителиальные опухоли (гепатоцеллюлярная аденома, фибронодулярная гиперплазия), неэпителиальные опухоли (гемангиома), паразитарные и непаразитарные кисты печени. Пациенты с ХЦР были распределены по классификации Bismuth-Corlette: тип I составил 18,18%, II – 18,18%, IIIa– 45,46%, IIIb – 9,09%, IV – 9,09%. По классификации Gennary пациенты с метастазами КРР в печень распределились следующим образом: I стадия – 35%, II –50%, III–10%, IVa – 5%. Результаты лабораторно-биохимического исследования пациентов при до-операционном исследовании имели нормальное распределение (анализ по Шопиру-Уилксу, W<0,948882, p<0,042476). Согласно интегральной оценке клинико-биохимических показателей по классификации Child-Plug, пациенты с классом А составили 69,57% (n=32), В – 30,43% (n=14).
Результаты исследования
Основным методом для определения объема было выбрано УЗИ, как метод, рекомендованный в качестве альтернативного СКТ и МРТ для расчета объемов резекции печени до операции [4]. Ультразвуковое сканирование печени проводилосьв трех плоскостях: сагиттальной, поперечной и косой (включая срезы по субкостальным пространствам в положении больного лежа на спине и левом боку). Правая и левая доли визуализировались путем определения на продольном срезе с наклоном датчика нижней полой вены (VCI) и проекции впадения в нее срединной печеночной вены (MHV). Локализация MHV соответствует главной портальной борозде и является границей разделения печени на правую и левую доли, согласно анатомии печени по C.Couinaud. Проводилось определение трех параметров: длина, высота, толщина (t – толщина, h – высота, d – длина) [заг]. По данной методике вычислялись размеры объемного образования, правой и левой долей печени, которые в последующем принимались за «условные» сферы. Объем сферы определяется по формуле: Vhep = 4/3πR3(см3), где R-радиус (или D/2, где D-диаметр). Вычисление «непораженной» паренхимы печени определялось по формуле: Vint = Vhep – Vtum (см3), где Vhep – объем печени. Определение объема остаточной паренхимы проводилось по следующей формуле: (Vres) = Vint–Vint.rem (см3), где Vint. rem – объем удаляемой неизмененной части (или доли) печени.
Принимаем за утверждение, что функционирующий объем паренхимы печени вырабатывает условное количество общего белка, эквивалентное тому объему, который он занимает. Т.о., IR определяется по следующей формуле:
где Vres – объем остаточной паренхимы печени (см3,%); ОБ – общий белок сыворотки крови (г/л).
IR=V /ОБ (Ед) int
Значение IR (M+Sd) в основной группе пациентов очаговыми образованиями печени составило 16,9+5,049 Ед и имело нормальное распределение в выбранной совокупности данных (p = 0,003998) (рисунок 1).
Б-ГТ^У, Ь'ЛГ.ЗГ. Т! Я VW **-*6 .'<3-- 1€ 902351 Лео-У* 1516К<0 ллгхг** 9 59С«О Лак".-^- 29 5KGX БУ Dev - 5 0*9252 Бгз*сзпз Erry- 07**4?2
Значения IR
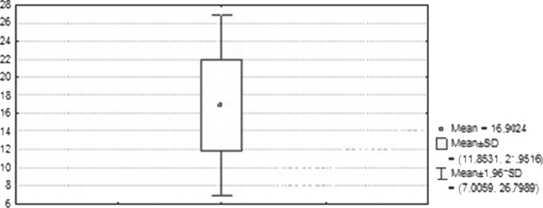
Рис. 1. Значения IR, рассчитанные по результатам УЗИ при дооперационном исследовании пациентов с очаговыми образованиями печени
Для оценки диагностической значимости разработанного неинвазивного метода оценки функционального резерва остаточной паренхимы печени, были использованы параметрические методы статистической обработки. Корреляционный анализ с определением коэффициента корреляции Пирсона значений IR и лабораторно-биохимических показателей, достоверно отражающих исследуемые функции печени, выявило-трицательную статистически значимую корреляционную взаимосвязь между значениями IR и показателями, отражающими биосинтетическую способность печени: альбумин (r=-0,7857), протромбиновый индекс (r=-0,7257) (рисунок 2), фибриноген (r=-0,7491).
Была выявлена выраженная положительная корреляционная взаимосвязь значений IR и уровня конъюгированного и не-конъюгированного билирубина плазмы крови, отражающего способность печени транспортировать органические анионы (r=0,86922) (рисунок 3).
При проведении корреляционного анализа c определением коэффициента корреляции Пирсона, была выявлена выраженная положительная корреляционная взаимосвязь значений IR и цитоплазматических ферментов – маркеров цитолиза: АСТ (r=0,89801), АЛТ (r=0,92243) (рисунок 4); уровнем мембраноза- висимых ферментов – маркеров холестаза – ЩФ (r=0,92243) и ГГТП (r=0,89801) (рисунок 5).
При исследовании взаимосвязи дооперационного значения IR и тяжести течения заболевания печени согласно интегральной клинико-биохимической шкале Child-Plug, выявлена выраженная положительная корреляционная связь (коэффициент корреляции Пирсона, r=0,86175).
Для оценки прогностической значимости разработанного метода неинвазивной оценки остаточной паренхимы печени, были проанализированы ранние послеоперационные осложнения, возникшие у пациентов, перенесших резекции печени. Для обработки данных был использован межгрупповой статистический анализ (t-критерий Стьюдента, односторонний вариант), анализ таблиц сопряженности (Пирсон Хи-квадрат, точный двусторонний критерий Фишера).
ОРП выполнены 26 (56,52%) пациентам. Объем остаточной паренхимы (М+sd) составил 648,158+227,3 см3 (52,226+25,342 %). Объем интраоперационной кровопотери составил 1137,609+701,45 мл. При оценке объема остаточной паренхимы, определяемого по результатам УЗИ, полученные результаты соответствовали общепринятым требованиям – объем остающейся части печени не менее 20% для нормальной паренхимы, не менее 30% - для цирротически измененной (рисунок 7).
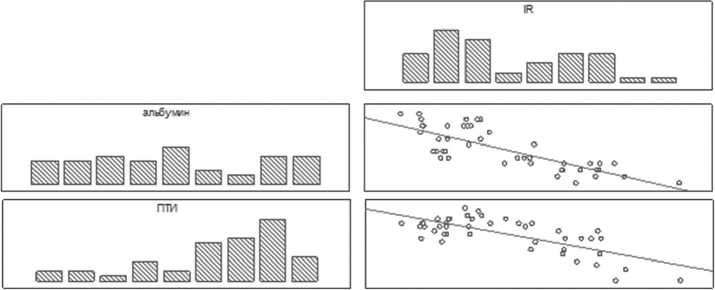
Рис. 2. Корреляционная взаимосвязь значений индекса резектабельности и альбумина, протромбинового индекса у пациентов с очаговыми образованиями печени
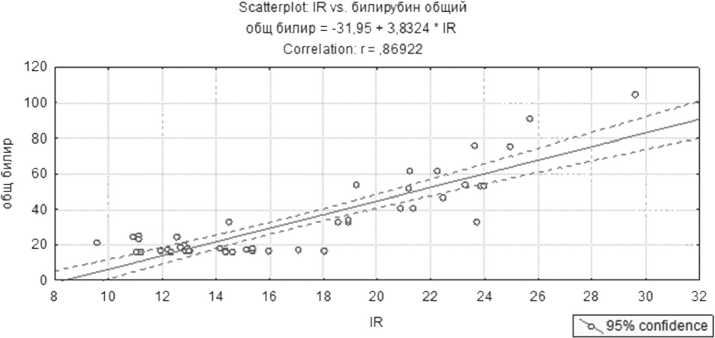
Рис. 3. Корреляционная взаимосвязь значений индекса резектабельности и общего билирубина плазмы крови у пациентов с очаговыми образованиями печени

Рис. 4. Корреляционный анализ по методу Пирсона (IR и АСТ, АЛТ) у пациентов с очаговыми поражениями печени
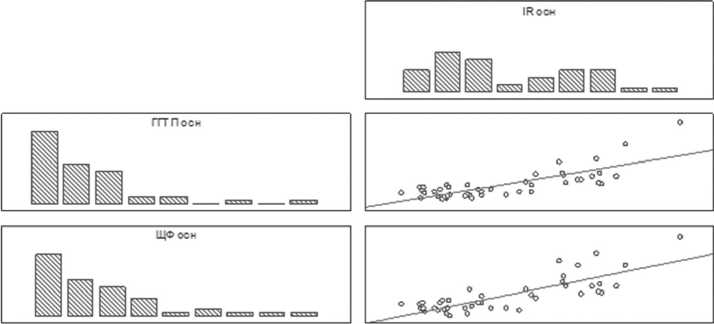
Рис. 5. Корреляционный анализ по методу Пирсона (IR и ГГТП, ЩФ) у пациентов с очаговыми поражениями печени
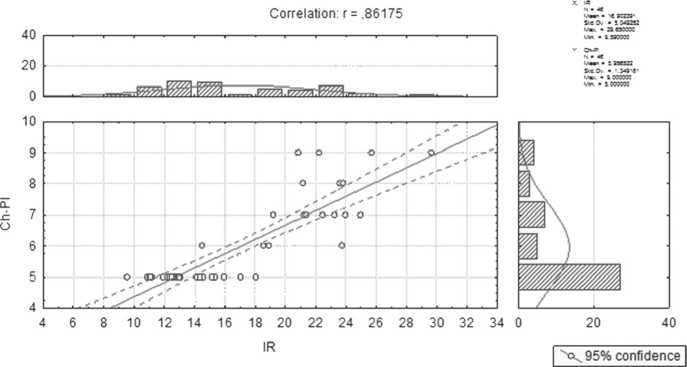
Рис. 6. Взаимосвязь значений IR и тяжести течения заболевания по шкале Child-Plug (баллы)
Осложнения были распределены по классификационной шкале Dindo-Clavien, в соответствии с которой частота жизнеугрожающих осложнений составила 8,7 %, средней тяжести -6,52 % (рисунок 8).
Тяжелая послеоперационная печеночно-клеточная недостаточность была выявленау 2,17%. Специфические осложнения развились у 23,33% (n=7) Билиарные осложнения были выявлены у 3 (6,52%) (таблица 1).
Для оценки прогностической значимости разработанного в ходе исследования «индекса резектабельности» все пациенты были распределены на две подгруппы в зависимости от величины значения IR. При сравнении числа и тяжести после-
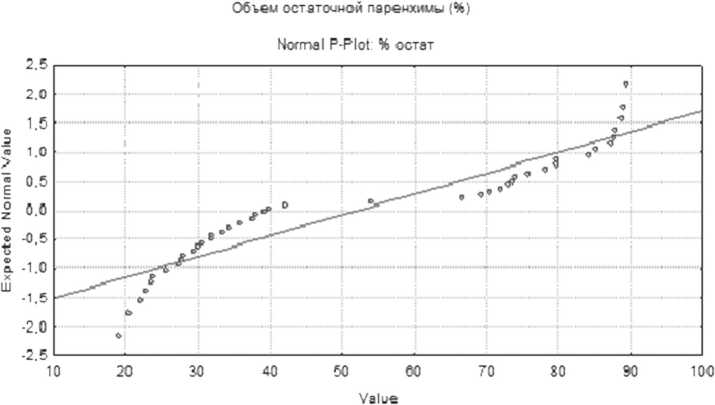
Рис. 7. Объем остаточной паренхимы у пациентов с очаговыми образованиями печени (в % соотношении к общему объему «непораженой паренхимы печени»)
частота развившихся послеоперационных осложнений по классификации Dindo-Clavien
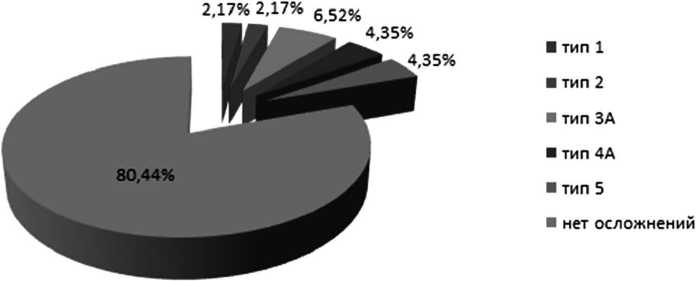
Рис. 8. Распределение осложнений по степени их тяжести у пациентов с очаговыми образованиями печени
Таблица 1
Билиарные осложнения в исследуемых группах (по классификации International Study Group of Liver Surgery, 2011 г.)
Обсуждение результатов
В ходе исследования был разработан и внедрен в клиническую практику неинвазивный морфо-функциональный индекс, основанный на измерении объема остаточной паренхимы печени на дооперационном этапе по заключению УЗИ и уровня общего белка сыворотки крови. Проведен корреляционный анализ полученных значений «индекса резектабельности» и значений лабораторно-биохимических показателей, которые достоверно отражают изменение функций печени: альбумин сыворотки крови, протромбиновый индекс (биосинтетическая функция печени), билирубин сыворотки крови (конъюгированная экскреция), АСТ, АЛТ, ГГТП, ЩФ (мембранозависимые
Таблица 2
Частота и тяжесть послеоперационных осложнений при значении IR более и менее 20 гл/см3
|
Осложнения |
IR<20 Ед,n(%) |
IR>20 Ед,n(%) |
р, точный двусторонний критерий Фишера |
|
легкие |
1(3,125) |
1(7,14) |
0,3913 |
|
средней тяжести |
1(3,125) |
3(21,43) |
0,2158 |
|
жизнеугрожающие |
0(0) |
4(28,57) |
0,0061 |
|
нет осложнений |
30(83,33) |
6(16,67) |
0,004 |
|
всего, n |
32 |
14 |
и цитоплазматические ферменты, изменение уровня которых свидетельствует о наличии гепатоцитолиза и холестаза). Выраженные корреляционные взаимоотношения показывают способность разработанного метода отражать изменение исследуемых функций и давать количественную оценку остаточной паренхимы печени на основании исследования ее синтетической функции.
Анализирована частота развившихся послеоперационных осложнений, в частности послеоперационной печеночной недостаточности. Выявлены критические значения (более 20 Ед), превышение которых соответствовало увеличению частоты и тяжести послеоперационных осложнений, в том числе специфических, наиболее грозным из которых является ОПН. По нашему мнению, рекомендуемый критический объем остаточной паренхимы печени не всегда является залогом благоприятного исхода оперативного лечения и не способен в ряде случаев восполнить функциональный дефицит в послеоперационном периоде, что может спровоцировать развитие острой пострезекционной печеночной недостаточности. Полученные результаты демонстрируют необходимость комплексной оценки функционального состояния печеночной паренхимы при планировании резекции с целью улучшения результатов хирургического лечения.
Выводы
-
1. Разработанный метод оценки функционального состояния остаточной паренхимы достоверно отражает изменение биосинтетической функций и коньюгированной экскреции, наличие некротического и холестатического процессов в печени.
-
2. Показана высокая эффективность применения неинвазивного дооперационного метода оценки функционального состояния остаточной паренхимы печенив отношении прогнозирования развития пострезекционной печеночной недостаточности.
-
3. Выявлены значения разработанного «индекса резекта-бельности», превышение которых достоверно увеличивает риск развития жизнеугрожающихпослеоперационных осложнений.
-
4. Применение «индекса резектабельности» может быть ре-
- комендовано с целью улучшения ближайших результатов хирургического лечения пациентов с очаговыми образованиями печени с целью предупреждения развития ОПН.
Список литературы Разработка неинвазивного метода оценки функционального состояния остаточной паренхимы печени и эффективность его применения у пациентов с очаговыми образованиями печени
- Вишневский В.А., Коваленко Ю.А., Андрейцева О.И., Икра- мов Р.З., Ефанов М.Г., Назаренко Н.А., Тупикин К.А. Пострезекционная печеночная недостаточность: современные проблемы определения, эпидемиологии, патогенеза, оценки факторов риска, профилактики и лечения // Украинский журнал хирургии. 2013. 22 (3). С. 172-182.
- N.N. Rahbari, O.J. Garden, R. Padbury [et al.] Posthepatectomy liver failure: a definition and grading by the International Study Group of Liver Surgery (ISGLS) // Surgery. - 2011. - Vol. 149. - P. 713-724.
- Готье С.В., Филин А.В., Цирульникова О.М. Обширные анатомические резекции в лечении очаговых поражений печени // Анналы РНЦХ РАМН, 2000, с. 12-18.
- Новрузбеков М. С. Оценка функциональных резервов печени и методы прогнозирования печеночной недостаточности при операциях на печени// кандид. диссер., Москва. 2008.
- Козырин И.А. Профилактика интраоперационной кровопотери при обширных резекциях печени. Автореф. дис.. канд. мед.наук.- М., 2011.- с. 12-46.
- S.Balzan, J. Belghiti, O. Farges. The «50-50 criteria» on postoperative day 5: an accurate predictor of liver failure and death after hepatectomy // Ann. Surg. - 2005. - № 242. - Р. 824-828.
- Li J.1., Lei B., Nie X., et al. A Comprehensive Method for Predicting Fatal Liver Failure of Patients With Liver Cancer Resection // Medicine. 2015. 94 (17). P. e784.
- Каприн А.Д., Сидоров Д.В., Рубцова Н.А.[etal.] Прогнозирование и профилактика острой печеночной недостаточности после обширных резекций печени по поводу первичных и метастатических опухолей // Исследования и практика в медицине. - 2016. - том 3 (№2). Р. 13
- К.А. Тупикин, Ю.А. Коваленко, А.А. Олифир, М.Д. Байдарова, В.А. Вишневский. Новые возможности диагностики и прогнозирования пострезекционной печеночной недостаточности в раннем послеоперационном периоде// Практическая медицина. - 2016. - '5(97). - Р. 50.
- Рябова Е.Н. Прогнозирование результатов портосистемного шунтирования у пациентов с синдромом портальной гипертензии // Автореф. дис. … канд. мед.наук. - Н.Новгород. 2014. - S. 12-46.


