Разработка пищевых продуктов на основе циклодекстринов
Автор: Грибкова В. А., Митрошина Д. П., Славянский А. А., Николаева Н. В., Литвяк В. В., Шилов В. В.
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Рубрика: Биотехнология продуктов питания и биологически активных веществ. Пищевые системы
Статья в выпуске: 2 т.28, 2025 года.
Бесплатный доступ
Производство нового поколения продуктов питания с заранее установленными требованиями к их качеству относится к приоритетным направлениям развития современной пищевой индустрии. Следует отметить необходимость более полного использования для этих целей социально значимых продуктов питания, к которым относится белый сахар. Кристаллический белый сахар является не только энергетически важным компонентом питания, но и сырьем для целого ряда отраслей пищевой промышленности. К ним, например, можно отнести кондитерское производство, где годовая потребность в нем составляет около 1 млн т. Придание сахару новых пищевых свойств позволит расширить линейку продуктов на его основе. Актуальным в этом направлении может быть использование йода, поскольку проблема йододефицита в России не потеряла своей актуальности. Тем не менее реализация подобного подхода сопряжена с технологическими особенностями, в том числе при создании йодированных продуктов. Расширение представлений по решению данной проблемы потребовало соответствующего анализа и проведения обоснованных исследований для более глубокого ее понимания. Причем особое внимание было обращено на механизм инкапсулирования йода при создании на его основе новых сахарсодержащих продуктов. Предварительные подходы к этой задаче показали возможность использования с этой целью продуктов крахмального производства – циклодекстринов (ЦД). В статье рассмотрены не только их основные свойства и особенности, но также предпринята попытка разобраться в осуществлении механизма комплексообразования ЦД с йодом. Полученные результаты доказали перспективность использования β-ЦД в пищевой промышленности для расширения линейки новых сахарсодержащих продуктов и, в частности, их значимость в решении проблемы дефицита йода.
Циклодекстрины, йод, комплекс "хозяин – гость", сахар, йодированные сахарсодержащие продукты, cyclodextrins, iodine, host – guest complex, sugar, iodized sugar-containing products
Короткий адрес: https://sciup.org/142244502
IDR: 142244502 | УДК: 612.396.111 | DOI: 10.21443/1560-9278-2025-28-2-151-163
Текст статьи Разработка пищевых продуктов на основе циклодекстринов
DOI:
e-mail: , ORCID:
Грибкова В. А. и др. Разработка пищевых продуктов на основе циклодекстринов. Вестник МГТУ. 2025. Т. 28, № 2. С. 151–163. DOI:
Gribkova, V. A. et al. 2025. Development of food products based on cyclodextrins. Vestnik of MSTU, 28(2), pp. 151–163. (In Russ.) DOI:
Стратегические основы и подходы, сформированные к качеству и безопасности пищевой продукции в Российской Федерации до 2030 г.1, как и производство новых видов продуктов питания, тесно увязаны с улучшением здоровья населения и профилактикой их дефицитных состояний. Поэтому йодирование пищевых продуктов представляется весьма актуальной и вполне обоснованной задачей современности. Использование с этой целью социально значимых продуктов питания позволит ускорить ее положительное решение2. Известно, что йод является одним из важнейших микроэлементов, необходимых для обеспечения нормальной жизнедеятельности человека. В настоящее время более 60 % населения РФ проживает в регионах с природно-обусловленным дефицитом йода. Особенно остро данная проблема ощущается в горных и предгорных районах Северного Кавказа, Урала, Алтая, Дальнего Востока, а также в Поволжье ( Цыплихин и др., 2025 ). Поэтому в этих регионах имеют место риски йододефицитных заболеваний.
Одним из перспективных методов устранения или снижения подобных заболеваний является преднамеренное добавление в пищевые продукты жизненно необходимых нутриентов ( Борисова и др., 2021 ). Вместе с этим, несмотря на значительные преимущества такого подхода, процесс обогащения продуктов питания сталкивается с рядом технологических затруднений. Последние, как правило, обусловлены сохранностью добавляемых нутриентов в производстве и процессе хранения готовой продукции. Причем одной из важнейших проблем является обеспечение минимизации контакта используемых добавок с одним из самых сильных природных окислителей – кислородом воздуха. Невзирая на то что кислород жизненно необходим для обеспечения процессов дыхания у растительных и животных организмов, выступающих в качестве источников продовольственного сырья, он также является ключевым фактором, инициирующим окислительные процессы ( Фролова и др., 2024 ). Известно также, что последние могут быть причиной деградации вводимых пищевых добавок. Причем наблюдается не только ухудшение органолептических характеристик пищевой продукции, но и снижение ее пищевой ценности.
Следует отметить, что повышение стабильности и сохранности различных биологически активных веществ (БАВ) при их использовании как добавок в продукты питания является довольно новым направлением в пищевой науке. Одним из возможных перспективных способов защиты вводимых нутриентов от агрессивного воздействия окружающей среды является гранулирование ( Славянский и др., 2021 ). Ранее было установлено, что этот процесс препятствует диффузии кислорода к вводимым нутриентам, например, в технологии гранулирования сахара. Помимо кислорода воздуха данная технология может защитить используемый нутриент от таких способствующих деградации факторов, как влага, свет и температурное воздействие. При этом молекулы БАВ в процессе гранулирования могут быть дополнительно защищены на молекулярном уровне покрытием на основе сахарных спиртов.
Технология инкапсулирования (способ введения пищевых добавок в обогощаемый ими пищевой продукт), с одной стороны, хорошо известна и уже используется в пищевых технологиях с разными целями, а с другой – наукоемка и позволяет разрабатывать или улучшать инновационные продукты для различных отраслей промышленности. Существующие сегодня методы инкапсулирования довольно широко применяются в медицине и фармацевтической промышленности ( Do Nascimento Cavalcante et al., 2019 ). Причем они позволяют решать множество задач, связанных с защитой, высвобождением и сохранением лекарственных веществ. Один из перспективных подходов их решения в фармацевтике основывается на использовании циклодекстринов (ЦД) – циклических олигосахаридов, получаемых из крахмала. Известно, что ЦД способны на молекулярном уровне образовывать комплексы "гость – хозяин" с широким спектром разнообразных продуктов ( Amiri et al., 2017; Crini, 2014 ). Так, в фармацевтике они необходимы для улучшения свойств лекарственных препаратов, особенно когда возникают проблемы с их растворимостью, стабилизацией протекания процесса или биодоступностью. ЦД относят к перспективному классу крахмалопродуктов, используемых в производстве лекарств. Вместе с тем потенциальные возможности их обогащения или придания им дополнительных пищевых свойств в продуктах питания еще до конца не исчерпаны.
Материалы и методы
Строение молекул циклодекстринов
Наиболее известные ЦД – это α-, β- и γ-ЦД, которые представляют собой циклические олигосахариды. Они могут содержать в своих структурах соответственно 6, 7 или 8 остатков D-глюкопиранозы3 (Jambhekar et al., 2016; Mura, 2015). При этом в основе их соединений связующими являются α-1-4-гликозидные связи. Молекулам циклодекстринов характерна форма усеченного конуса. Стабильность подобной формы молекул обусловлена наличием водородных связей между OH-группами. Все OH-группы располагаются на внешней поверхности молекулы, в результате чего внутренняя полость ЦД является гидрофобной (Zhang et al., 2013). Центральная их полость имеет определенный размер, который зависит от количества молекул глюкозы в цикле (рис. 1). Наличие атомов водорода на внутренней поверхности молекулы ЦД обусловливает ее гидрофобные свойства. В свою очередь, внешняя поверхность, напротив, проявляет гидрофильные свойства, что обусловлено присутствием гидроксильных групп (ОН-групп). Данные группы классифицируются по положению: первичные ОН-группы локализованы у узкого края молекулы ЦД, в то время как вторичные ОН-группы расположены у более широкого края (Das et al., 2020; Raffaini et al., 2019). На рис. 2 приведено схематическое изображение молекулы β-ЦД.
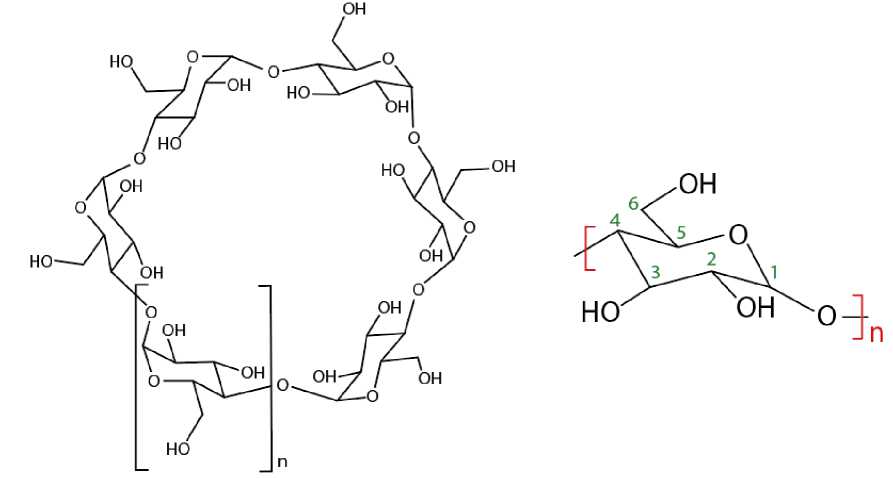
Рис. 1. Химическая структура ЦД ( n = 6 – α-ЦД, n = 7 – β-ЦД, n = 8 – γ-ЦД)
Fig. 1. Chemical structure of cyclodextrin (CD): n = 6 – α-CD, n = 7 – β-CD, n = 8 – γ-CD
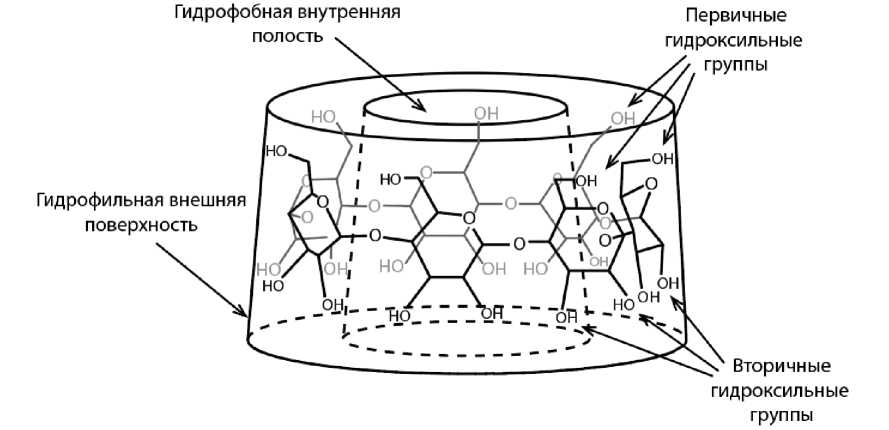
Рис. 2. Схематическое расположение первичных и вторичных гидроксильных групп в молекуле β-ЦД Fig. 2. Schematic arrangement of primary and secondary hydroxyl groups in the β-CD molecule
ЦД способны формировать молекулярные комплексные включения, известные как клатраты, с разнообразными веществами по принципу "гость – хозяин". В клатратах молекулы ЦД благодаря своей внутренней гидрофобной полости выступают в роли "хозяев", а молекулы включаемых субстанций играют роль "гостя". В результате подобного взаимодействия возможно достигнуть существенного улучшения физических и биологических свойств гостевых молекул ( Kavetsou et al., 2021 ). Такая ситуация объясняет повышенное внимание к ЦД в современных исследованиях.
Комплексообразование ЦД по схеме "хозяин – гость"
Способность ЦД образовывать и формировать на молекулярном уровне комплексные включения с разнообразными веществами разного назначения считается основой, определяющей их значимость и практическое применение ( Mashaqbeh et al., 2021; Minns et al., 2002 ). Так, например, благодаря их способности к комплексообразованию ЦД могут на молекулярном уровне образовывать особые включения по типу "хозяин – гость". При этом последние могут быть разного химического состава и структуры: твердыми, жидкими и газообразными химическими соединениями. В этих соединениях полость молекулы "хозяина" ЦД служит местом хранения молекулы "гостя".
Прочность и стабильность образуемого комплексного соединения зависят от соответствия размеров молекул "хозяина" и "гостя", а также от специфических локальных взаимодействий между их атомами, молекулами, а также соответствующими химическими и поверхностными связями.
Стериохимическое строение комплексов "хозяин – гость" может быть описано двумя возможными вариантами ( Natural…, 2016 ):
-
1) комбинация 1 : 1 молекула-хозяин (ЦД)/молекула-гость (МХ/МГ (К1:1)), следующее уравнение дает стехиометрию комплекса включения: МХ + МГ → МХ/МГ (К 1:1 ), при МХ = ЦД уравнение примет вид ЦД + МГ → ЦД/МГ (К1:1);
-
2) комбинация 2 : 1 молекула-хозяин (ЦД)/молекула-гость (МХ 2 /МГ (К 2:1 )), следующее уравнение дает стехиометрию комплекса включения: 2МХ + МГ → МХ 2 /МГ (К 2:1 ), при МХ = ЦД уравнение примет вид 2ЦД + МГ → ЦД 2 /МГ (К 2:1 ).
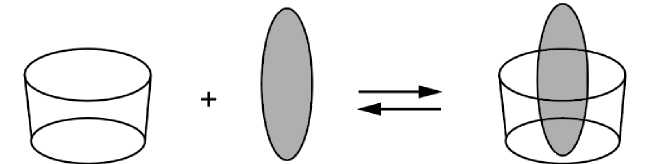
Равновесное связывание гостевой молекулы и ЦД с образованием комплекса в комбинации 1 : 1 и с комбинацией 2 : 1 показаны на рис. 3 и 4.
Молекула ЦД Молекула Комплекс
"хозяин" "гость" 1 : 1 "хозяин – гость"
Рис. 3. Схема образование комплекса включения "хозяин – гость" при равновесном связывании гостевой молекулы и ЦД с образованием комплекса 1 : 1
Fig. 3. Scheme of formation of the host – guest inclusion complex upon equilibrium binding of the guest molecule and CD with formation of a 1 : 1 complex
Молекула ЦД "хозяин"
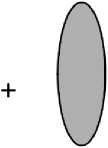
Молекула "гость"
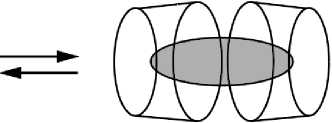
Комплекс
2 : 1 "хозяин – гость"
Рис. 4. Схема образование комплекса включения "хозяин – гость" с равновесным связыванием гостевой молекулы и ЦД с образованием комплекса 2 : 1
Fig. 4. Scheme of formation of the host – guest inclusion complex with equilibrium binding of the guest molecule and CD to form a 2 : 1 complex
Комбинация ЦД/МГ (1 : 1) является наиболее распространенным типом комплекса ЦД ( Leclercq, 2016 ). Она возникает, когда размер вводимого "гостя" соответствует размеру полости ЦД и одна молекула "гостя" оптимально заполняет полость. Предположительно, комплексы включения типа 2 : 1 образуются путем взаимодействия второй молекулы ЦД с ранее сформированным комплексом 1 : 1 ( Li et al., 2022 ).
Размеры полости ЦД и гостевой молекулы считаются определяющими и оказывают существенное влияние на комплексообразование (Mohammed-Saeid et al., 2019; Maniam et al., 2022). Однако механизм протекания этого процесса еще до конца не уточнен и исследования в этом направлении продолжаются. Так, например, до настоящего времени остается открытым вопрос о природе сил, удерживающих вводимые в ЦД молекулы, как и характер образующихся при этом связей. Известно также, что важную роль в образовании соответствующих связей могут играть Ван-дер-Ваальсовы силы и межмолекулярные связи, формирующиеся за счет гидрофобной внутренней полости циклодекстринов (Saokham et al., 2018; Venuti et al., 2019). В этой полости может быть сформирована особая среда и в нее могут проникать наиболее активные гидрофобные гостевые молекулы. При этом происходит вытеснение молекул воды из внутренней полости ЦД. Схема механизма подобного процесса с образованием комплексного соединения "гость – хозяин" показана на рис. 5.
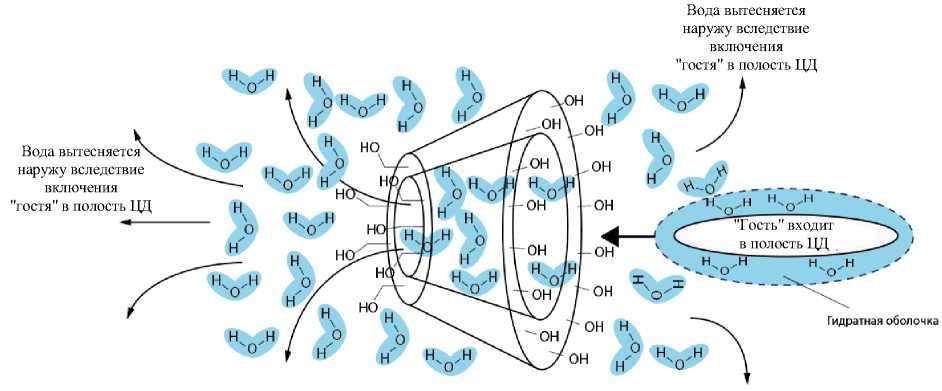
Циклодекстрин (ЦД)
Рис. 5. Схема механизма образования комплекса "хозяин – гость" Fig. 5. Scheme of the mechanism of formation of the host – guest complex
Движущей силой процесса образования комплексных соединений является способность молекулы "гостя" внедряться внутрь гидрофобной полости ЦД ( Zhu et al., 2015 ). Предполагается, что в этот период между гостевой молекулой и внутренней поверхностью полости ЦД могут иметь место некоторые силы (например, Ван-дер-Ваальсовы). При этом они стабилизируют молекулярное состояние образуемого комплекса. Характерной особенностью гидрофобных молекул "гостя" является отсутствие у них способности образовывать водородные связи с молекулами воды ( Adamiak et al., 2019 ). Поэтому количество водородных связей между молекулами воды с формированием более упорядоченной структуры вокруг поверхности гостевой молекулы возрастает. При этом как бы формируется гидратная оболочка вокруг "гостя". Следует также отметить, что внутренняя полость ЦД не является абсолютно свободной, так как внутри нее находится молекулы воды. Последние связаны с выстилающими полость ЦД атомами кислорода и водорода посредством слабых водородных связей и диполь-дипольных взаимодействий ( Jia et al., 2022 ). К тому же на внешней поверхности ЦД присутствуют гидроксильные группы, которые конкурируют за взаимодействие с молекулами воды из окружающего ЦД раствора. Все это ограничивает подвижность молекул воды внутри полости ЦД и влияет на их ориентацию в его полости. Когда гидрофобная молекула "гостя" инкапсулируется в гидрофобную полость ЦД, его гидратная оболочка разрушается. Молекулы воды, которые ранее были ограничены в своей подвижности и строго расположены в гидратной оболочке, в этой ситуации получают возможность свободно двигаться и взаимодействовать с другими молекулами воды окружающего их раствора. При инкапсуляции во внутренюю полость ЦД молекулы воды вытесняются из нее. При этом следует отметить то, что при этом наблюдается разрушение связей между молекулами воды и атомами, выстилающими полость ЦД. Высвобождение молекул воды из полости ЦД в свою очередь приводит к повышению энтропии сформированной системы ( Ali et al., 2021; Mohammed-Saeid et al., 2019 ). Возрастает ее неупорядоченность и подвижность молекул. Увеличение энтропии при высвобождении молекул воды вокруг гидрофобной молекулы "гостя" и внутри полости ЦД стабилизирует сформированный комплекс. Причем его образование становится термодинамически выгодным.
Методы получения комплексов с ЦД
Существует множество различных подходов к комплексообразованию. Их разнообразие обусловлено широким спектром молекул-гостей и соединений, компонентов рецептур, производственных процессов и конечных продуктов ( Janicka et al., 2022 ). В настоящее время известен ряд методов получения комплексов ЦД с "гостями": сорастирание, соосаждение, сухое вымешивание, герметичное нагревание, комплексообразование в пастообразном состоянии, нейтрализация, распылительная сушка, замораживание, испарение растворителя ( Sbârcea et al., 2019 ).
Производные ЦД с измененными свойствами
Целью модификации природных ЦД является получение на их основе производных ЦД, т. е. превращение в аморфные или кристаллические формы с различными свойствами ( Topuz et al., 2022 ). После подобных превращений ЦД должны обладать высокой растворимостью в воде. Это необходимо, чтобы обеспечить микробиологическую и физико-химическую стабильность в течение определенного периода времени. Поскольку все ЦД (α-, β- и γ-) имеют взаимозаменяемые гидроксильные группы, то существует много вариантов их потенциальных производных.
Выделяют следующие типы модифицированных ЦД:
-
1. Метилированные циклодекстрины (МЦД) представляют собой модифицированные формы циклодекстринов, в которых гидроксильные группы (–OH) на внешней стороне молекулы заменены на метильные (–CH3), что приводит к изменению их свойств ( Christoforides et al., 2022 ). Например, растворимость в воде метилированного β-ЦД выше, чем у нативного β-ЦД. Это объясняется тем, что немодифицированные ЦД имеют множество гидроксильных групп на внешней стороне молекулы. Последние способны образовывать межмолекулярные водородные связи с другими молекулами ЦД. Подобное взаимодействие является причиной формирования относительно крупных труднорастворимых агрегатов ЦД. Метилирование ЦД препятствует образованию межмолекулярных водородных связей между молекулами ЦД ( Aiassa et al., 2023 ). Это объясняется тем, что метильные группы не способны образовывать водородные связи. Таким образом, метилирование циклодекстринов повышает их растворимость, главным образом за счет разрушения межмолекулярных водородных связей между молекулами ЦД. Высокая растворимость МЦД расширяет сферы их применения, особенно в фармацевтике и пищевой промышленности, где необходимо работать с водными растворами.
-
2. Гидроксилированные производные ЦД – это ЦД, у которых гидроксильные группы (–OH) на внешней поверхности молекулы модифицированы путем добавления гидроксиалкильных групп. Наиболее распространенными являются гидроксипропил-циклодекстрины (ГП-ЦД) и гидроксиэтил-циклодекстрины (ГЭ-ЦД) ( Kato et al., 2009 ). Реакция гидроксилирования заключается в присоединении гидроксиалкильных групп к гидроксильным группам на внешней поверхности молекулы ЦД. Это обычно достигается путем взаимодействия ЦД с пропиленоксидом для ГП-ЦД и этиленоксидом для ГЭ-ЦД, соответственно. Как и МЦД, данные модифицированные формы ЦД обладают значительно более высокой растворимостью в воде по сравнению с нативными ЦД. Кроме того, гидроксилирование может оказывать влияние на способность ЦД к комплексообразованию. Так, гидроксиалкильные группы, присоединенные к гидроксильным группам на внешней стороне ЦД, являются более объемными, чем простые гидроксильные группы ( Matencio et al., 2016 ). Несмотря на то что эти группы не находятся внутри полости ЦД, они создают некоторое пространственное препятствие на входе в полость ЦД, которое может в некоторой степени изменить размер полости ЦД. В результате этих изменений гидроксилированные ЦД приобретают селективность в процессе комплексообразования, т. е. если гостевые молекулы не совпадают с размерами полости, то эффективность их включения существенно ниже.
-
3. Сульфоалкилированные производные ЦД (САЦД) – под ними понимают модифицированные ЦД, в которых к молекуле ЦД присоединены сульфоалкильные группы. Эти группы представляют собой алкильные цепи, на конце которых находится сульфонатная группа ( - SO - ), имеющая отрицательный заряд ( Qu et al., 2002 ). Отличительной особенностью САЦД является их пониженная способность к образованию комплексов с молекулами-гостями. Это может быть объяснено тем, что сульфонатные группы отрицательно заряжены, и если молекула-гость также имеет отрицательный заряд (или несет частично отрицательный заряд в определенной части своей структуры), то между ними может возникать электростатическое отталкивание, что в свою очередь может затруднять или препятствовать образованию комплекса. Помимо этого, в случае если "гость" имеет положительный заряд, то сульфонатные группы САЦД могут вступать в ионные взаимодействия. Однако эти взаимодействия могут связывать молекулу-гостя не внутри полости, а, скорее, на поверхности САЦД, что также снижает эффективность образования комплексов.
-
4. Серосодержащие производные ЦД (ССЦД) – это производные, в которых в молекулу ЦД введены атомы серы. Они могут включать различные серосодержащие функциональные группы, такие как тиолы (–SH), сульфиды (–S–), сульфоксиды (–SO–), сульфоны (–SO 2 –), сульфонаты (–SO 3 –) и тиоэфиры (–C–S–C–) ( Mohandoss et al., 2019 ). Благодаря введению атомов серы в структуру ЦД данные модификации могут образовывать координационные связи с ионами металлов, что позволяет использовать серосодержащие ЦД в качестве хелатирующих агентов. Это связано с тем, что эти функциональные группы способны отдавать свои неподеленные электронные пары и образовывать координационные (донорно-акцепторные) связи с ионами металлов. Эта особенность позволяет использовать ССЦД, например, для удаления тяжелых металлов и других загрязнений из окружающей среды ( Mura, 2014 ).
Факторы, влияющие на комплексообразование ЦД с гостевыми молекулами
На образование комплекса ЦД/гостевая молекула влияет ряд факторов:
-
1. Тип ЦД и размер его полости. Различные типы ЦД имеют разное количество глюкозных звеньев в кольцевой структуре, что напрямую определяет размер внутренней гидрофобной полости. "Гость" должен быть расположен внутри ЦД, следовательно, размер его полости должен быть соответствующим. ЦД имеют различный диаметр центральной полости, поэтому они способны образовывать комплексы с молекулами соответствующего размера ( Adamiak et al., 2019 ).
-
2. Влияние методов приготовления. Известны различные методы образования комплексных соединений с гостевыми молекулами, причем от выбранного способа зависит протекание процесса комплексообразования ( Araújo et al., 2021 ).
-
3. Связь между pH и состоянием ионизации. Если гостевая молекула при определенном pH становится более гидрофильной из-за ионизации (т. е. в результате процесса образования ионов из нейтральных атомов или молекул), ее сродство к гидрофобной полости ЦД снижается, что приводит к уменьшению стабильности комплекса. Оптимальное pH для комплексообразования часто соответствует pH, при котором гостевая молекула находится в наименее ионизированной форме (т. е. наиболее гидрофобна) ( Da Rocha Neto et al., 2018 ).
-
4. Температура. На процесс образования комплексов между ЦД и молекулами-гостями заметное влияние оказывает температура. Так, стабильность комплексного включения может уменьшаться с повышением температуры ( Xiao et al., 2019 ).
-
5. Степень замещения. Тип, количество и расположение заместителя в исходной молекуле ЦД может оказывать заметное влияние на физико-химические свойства молекулы, такие как ее комплексообразующая способность. Например, различия в физико-химических свойствах образцов ГП-ЦД, имеющих одинаковый уровень замещения в разных условиях, может быть результатом нерегулярности в размещении гидроксипропильных групп в различных местах исходной молекулы ЦД. Это обусловлено тем, что чистота ЦД может оказывать существенное влияние на конечное качество гостевой молекулы и его товарность ( Guendouzi et al., 2020 ).
Таким образом, на эффективность процесса формирования комплексов между ЦД и гостевыми молекулами, а также их стабильность влияет множество факторов, понимание которых критически важно для оптимизации комплексообразования и инкапсулирования различных незаменимых нутриентов. В рамках настоящего исследования особое внимание было уделено комплексообразованию β-ЦД с йодом.
Результаты и обсуждение
Получение комплексов йод-ЦД
По данным ВОЗ дефицит йода считается одной из причин заболевания щитовидной железы человека4. Это объясняется тем, что в его организме йод является неотъемлемой частью гормонов щитовидной железы. В мировой практике дефицит йода наблюдается почти у двух миллиардов человек ( Zimmerman, 2012; O’Kane et al., 2018 ). По существующим рекомендациям для решения проблемы йодосодержания детям рекомендуется в сутки потреблять 70–150 мкг йода, тогда как взрослым его требуется – 150 мкг5. Одним из важнейших мероприятий профилактики йододефицита является йодирование пищевых продуктов ( Iodine…, 2017 ). Добавление йода в продукты питания, особенно социально значимые, позволит обеспечить необходимое потребление этого важного микроэлемента.
К категории социально значимых продуктов питания относится белый сахар6 ( Николаева и др., 2021 ). Вследствие его широкого использования в рационе питания, экономической доступности и востребованности в различных отраслях пищевой промышленности (включая производство кондитерских изделий, хлебобулочных изделий и напитков) он может быть перспективной основой для обогащения йодом7 ( Славянский и др., 1984 ). В соответствии с действующими рекомендациями, взрослому населению рекомендуется употреблять примерно 25 г сахара в сутки3. Хорошо известно, что йод является весьма летучим элементом. Поэтому повышение его устойчивости к условиям окружающей среды является критически важным фактором. Это обусловлено тем, что последний определяет эффективность профилактики йододефицитных состояний.
Благодаря своей уникальной циклической структуре и наличию гидрофобной полости ЦД способны захватывать в нее различные молекулы. Например, включать в себя микроэлементы, которые часто имеют низкую стабильность и растворимость. При этом ЦД способны увеличить физическую и химическую стабильность этих компонентов ( Bednarek et al., 2019; Neoh et al., 2006 ). Получение комплексов ЦД с йодом – весьма перспективно для создания новых йодированных пищевых продуктов.
Вместе с тем известно, что йод весьма нестабилен и чувствителен к факторам окружающей его среды. Поэтому при его инкапсулировании в ЦД, а также при разработке йодированных сахарсодержащих продуктов, могут потребоваться дополнительные исследования в этом направлении ( Wang, 2011; Moini et al., 2020 ).
На основе ранее выполненных работ установлено, что α-ЦД образует комплекс со смесью йодида калия и йода ( Minns et al., 2002; Lechat et al., 1992 ). Проведенные в этом направлении эксперименты показали на стабильность разработанного соединения – после 16 месяцев его хранения. Кроме того отмечена его пригодность для промышленного использования.
Отмечено, что основой для включения и формирования комплексов с йодом могут быть как α-ЦД, так и β-ЦД. При этом уточнено то, что β-ЦД способен к образованию более стабильного комплекса с йодом, чем с α-ЦД. Причем этот тип комплексообразования в целом увеличивает растворимость йода в воде ( Polumbryk et al., 2019; Sharipov et al., 2017 ).
В ходе дальнейших исследований были получены комплексы ЦД с йодом (α-ЦД-I 2 и β-ЦД-I 2 ) путем смешивания концентрированных растворов ЦД и КI с последующим выпадением осадка, его промыванием и сушкой под разрежением ( Литвяк и др., 2024 ). Результаты этих экспериментов представлены на рис. 6 и 7. На рис. 8 показана схема образования комплексного соединения между β-ЦД и KI.

Комплекс α-ЦД с йодом
Рис. 6. Сканирующие электронные микрофотографии комплекса ЦД с йодом Fig. 6. Scanning electron micrographs of the CD complex with iodine

Комплекс β-ЦД с йодом

Рис. 7. Сканирующие электронные микрофотографии комплекса β-ЦД с йодом Fig. 7. Scanning electron micrographs of the β-CD complex with iodine
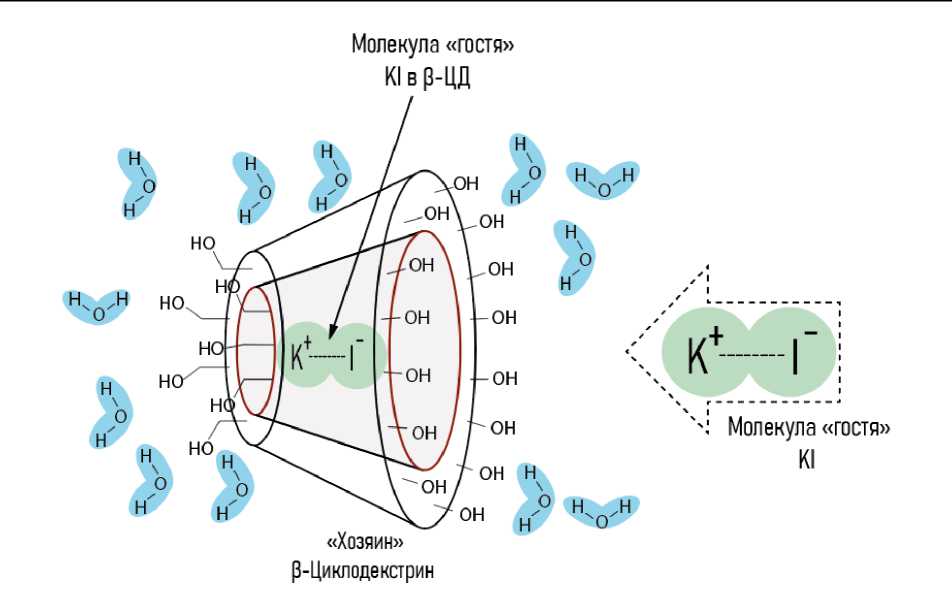
Рис. 8. Схема образования комплексного соединения между β-ЦД и KI Fig. 8. Scheme of formation of the complex compound between β-CD and KI
Таким образом, ЦД обеспечивает защиту молекулы йода от взаимодействия с кислородом и влагой из воздуха, которые могут вызывать деградацию "гостя" или химические реакции между ним и компонентами окружающей среды. Помимо этого включенные в полость β-ЦД молекулы йода становятся менее доступными для перехода в газовую фазу, так как полость β-ЦД препятствует высвобождению молекул йода. В ходе работы сканирующей электронной микроскопией и йодометрическим титрованием было установлено, что содержание йода в комплексе β-ЦД-I 2 составляет 16,82–16,90 %.
Заключение
Способность ЦД к образованию комплексных соединений открывает новые перспективные возможности их использования, например, для разработки новых видов обогащенных пищевых продуктов. При выборе последних в первую очередь следует ориентироваться на социально значимые продукты питания. В результате проведенных исследований в этом направлении отмечена важность понимания особенностей взаимодействий ЦД и гостевых молекул и новых подходов к их использованию. Особое внимание в данной работе уделено проблеме инкапсулирования и формирования комплексов йода с β-ЦД. Показано, что дальнейшие исследования в этой области могут стать основой разработки уточненных условий инкапсуляции с защитой их от факторов внешней среды. При этом данная проблема является не только актуальной в контексте йододефицита, но и перспективной, так как она ориентирована на создание нового поколения социально значимых пищевых продуктов с заданными или строго персонализированными характеристиками.


