Разработка технологии переработки пшеницы на спирт и белковый продукт
Автор: Романюк Т.И., Агафонов Г.В., Фролова Н.Н.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 1 (63), 2015 года.
Бесплатный доступ
В спиртовой отрасли актуально создание безотходной технологии переработки зерна на спирт. Целью исследований явилась разработка технологии переработки пшеницы на этанол и белковый продукт. Изучили процесс ферментативного гидролиза крахмала глюкоамилазой препарата Глюкогам. Подобрана оптимальная дозировка фермента - 8 ед. ГлС/г крахмала, температура 55 оС. При исследовании гидролиза белка сопутствующей глюкоамилазе протеазой ферментного препарата Глюкогам установлено накопление аминного азота 4,5 мг/см 3 за 7 ч биоконверсии. Проводили разделение полученной осахаренной массы с помощью центрифугирования на фильтрат и белковую массу. Центрифугирование проводили при частоте вращения 2500 об/мин в течение 8 мин. Белок высушивали до влажности 5 % при температуре не выше 35 оС, измельчали и исследовали свойства в сравнении с нативной клейковиной пшеницы. Полученный продукт обладал следующим характеристиками: растворимость 10 %, влагоудерживающая способность 1,53 г/г, жиросвязывающая способность 1,9 г/г. Исследовали процесс сбраживания осветленного сусла с концентрацией сухих веществ 14 %. Использовали дрожжи Saccharomyces cerevisiae расы XII и Saccharomyces cerevisiae расы IMB Y-5007 из расчета 120 млн клеток на 1 см 3 сусла. Подобрали оптимальный состав минеральных солей. Для дрожжей расы XII и IMB Y-5007 необходима подкормка в виде диаммоний фосфата в дозировке 1,5 г/дм 3. Выход спирта при использовании дрожжей расы IMB Y-5007 составил 60,7 дал/т условного крахмала, при внесении дрожжей расы XII - 60,6 дал/т условного крахмала.
Пшеница, этанол, биоконверсия, безотходная переработка
Короткий адрес: https://sciup.org/14040359
IDR: 14040359 | УДК: 663.5
Development of technology for wheat processing into alcohol and protein product
Creating a waste-free technology of processing of grain into alcohol is a topical issue in the alcohol industry. The purpose of this study was to develop a technology for the processing of wheat into ethanol and protein product. Studied the process of enzymatic hydrolysis of starch by glucoamylase preparation Glycogen. Obtained optimal dosage of enzyme - 8 units unit/g starch, the temperature of 55°C. In the study of the hydrolysis of protein, protease enzyme preparation glycogen accompanying glucoamylase found accumulation of amino nitrogen of 4.5 mg/cm 3 for 7 hours of bioconversion. Was made dividing the sugar mass to the filtrate and the protein masses by centrifugation. Centrifugation was done with the speed of rotation 2500 rpm for 8 min. Protein was dried to a moisture content of 5 % at a temperature not above 35 ° C, grinded and checked properties in comparison with native wheat gluten. The resulting product had the following characteristics: solubility of 10 %, the water-holding capacity of 1.53 g/g, adeps binding ability to 1.9 g/year. Investigated the process of fermentation of clarified wort with concentration of solids 14 %. Used the yeast Saccharomyces cerevisiae race XII and Saccharomyces cerevisiae race IMB Y-5007 based on 120 million cells per 1 cm3 of the wort. Obtained optimal composition of mineral salts. For yeast race XII and IMB Y-5007 needed nutrition in the form of diammonium phosphate at a dose of 1.5 g/dm 3. The output of the alcohol using yeast race IMB Y-5007 60.7 dal/t of starch, when making yeast race XII - 60,6 dal/ton of starch.
Текст научной статьи Разработка технологии переработки пшеницы на спирт и белковый продукт
Одно из перспективных направлений в данной области – создание технологии получения этилового спирта и белкового продукта при переработке злаков на спирт [2].
Учитывая количество перерабатываемого зернового сырья на этанол в спиртовом производстве России при утилизации белковой составляющей, можно дополнительно получить 370-600 тыс. т белка в год в виде белкового концентрата [3].
Целью проведенных исследований явилась разработка технологии переработки зерна пшеницы на этиловый спирт и белковый продукт.
На первом этапе изучали процесс ферментативного гидролиза крахмала пшеницы глюкоамилазой препарата Глюкогам (производитель Novozymes, Дания, активность 2000 ед/см3). Активность препарата определяли глюкозоксидаз-ным методом. Одним из основных факторов, оказывающих значительное влияние на процесс гидролиза крахмала, является дозировка ферментного препарата. При изучении влияния дозировки препарата Глюкогам на степень осахаривания крахмалистого сырья гидролиз осуществляли при оптимальных условиях действия [1] фермента (температура 58-60 оС, рН=5,0). Препарат вносили в количестве 6, 8 и 10 ед. ГлС/г крахмала. Количество образующихся редуцирующих сахаров определяли по методу Сомоджи-Нельсона. Результаты экспериментов представлены на рисунке 1.
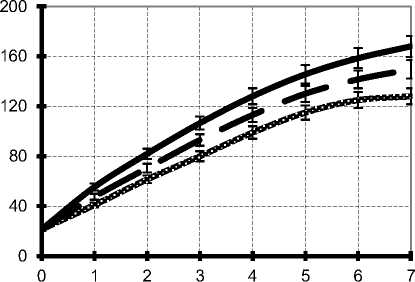
Продолжительность осахаривания, ч
^^J^J^J^J^J^J^J^Jti 6 ед. ГлС/г крахмала
^^^^e 8 ед. ГлС/г крахмала
^^^^^w 10 ед. ГлС/г крахмала
Рисунок 1. Накопление сахаров в процессе гидролиза крахмала при различной дозировке глюкоамилазы препарата Глюкогам
Анализ экспериментальных данных (рисунок 1) показал, что с увеличением концентрации глюкоамилазы возрастало накопление редуцирующих углеводов, что согласуется с традиционными представлениями о кинетике ферментативных реакций. Наиболее эффективно осахаривание проходило при внесении 10 ед. глюко- амилазы, однако большой расход ферментного препарата может привести к удорожанию конечного продукта. В связи с этим оптимальной дозировкой считали 8 ед. ГлС/г крахмала. На графике видно, что за 7 ч биоконверсии крахмала количество накопленных сахаров составляло 150 мг/см3. Внесение же ферментного препарата в количестве 6 ед. ГлС/г крахмала позволяет получить гидролизат с меньшим содержанием редуцирующих веществ (130 мг/см3).
Поскольку для нормального протекания процесса брожения необходимо наличие аминного азота в сусле [4], а в состав ферментного препарата Глюкогам в качестве сопутствующего фермента входит протеаза, то в процессе осахаривания исследовали интенсив- ность протеолиза по уменьшению количества белка, определяемому биуретовым методом.
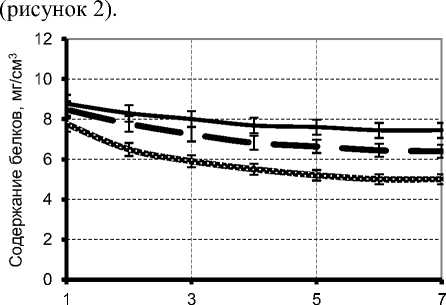
Продолжительность осахаривания, ч
10 ед. ГлС/мл ^^^^^^^^^ 6 ед. ГлС/мл
^^^^e 8 ед. ГлС/мл
Рисунок 2. Изменение количества белков в зависимости от дозировки ферментного препарата глюкоамилазы
Как видно из данных, представленных на рисунке 2, с увеличением дозировки глюкоамилазы увеличивалось накопление продуктов протеолиза, содержание аминного азота к 7 ч биоконверсии крахмала при внесении глюкоамилазы 8 ед. ГлС/г составило 4,5 мг/см3.
Затем изучали влияние температуры на процесс ферментативного гидролиза пшеничного крахмала. Осахаривание проводили при температурах 45, 50 и 55 оС при дозировке глюкоамилазы 8 ед/г крахмала. Результаты исследований представлены на рисунке 3.
На рисунке 3 видно, что кривые гидролиза имеют схожий вид. При проведении процесса осахаривания крахмала при температуре 45 0С количество накопленных редуцирующих сахаров составляло 130 мг/см3, при 50 оС – 150 мг/см3 и при 55 оС – 160 мг/см3 соответственно. Следовательно, рациональной является температура 55 оС.
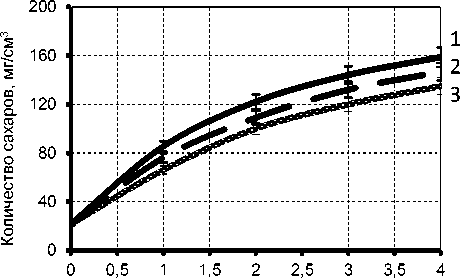
Продолжительность осахаривания, ч
1 – 55 оС 2 – 50 оС 3 – 45 оС
Рисунок 3. Влияние температуры на процесс ферментативного гидролиза крахмала
Далее исследовали процесс расщепления белка в процессе осахаривания сусла при различной температуре. Количество белка определяли биуретовым методом. Результаты
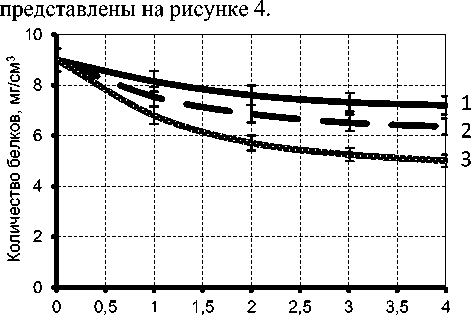
Продолжительность осахаривания, ч
1 - 450С 2 - 500С 3 - 550С
Рисунок 4. Влияние температуры на протеолиз белка пшеницы
Из полученных данных видно, что наиболее интенсивно процесс протекал первые 3 ч, что согласовывается с традиционными представлениями о кинетике ферментативных реакций – в первые часы биоконверсии расщепление субстрата идет интенсивнее, чем в последующие [5]. Количество белка за 4 ч гидролиза при 55 оС составляло 5 мг/см3 и являлось минимальным, что подтверждает данные об оптимальной температуре действия ферментного препарата.
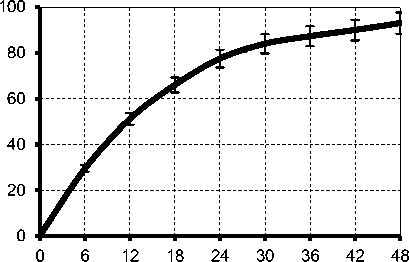
Так как известно, что полный гидролиз крахмала завершается за 48-72 ч, то представляло интерес изучить динамику биоконверсии крахмала при подобранных условиях на протяжении 48 ч (рисунке 5).
На графике видно, что первые 24 ч биодеструкция пшеничного крахмала проходила наиболее интенсивно, степень его гидролиза составила 78 %. В дальнейшем процесс проходил менее интенсивно, и к концу вторых суток степень осахаривания крахмала составляла 95 % от максимального.
Продолжительность осахаривания, ч
Рисунок 5. Динамика гидролиза крахмала в процессе осахаривания при 55 оС
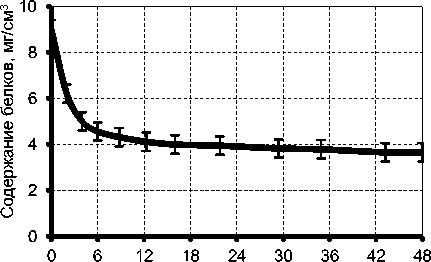
В производстве спирта наличие аминного азота при сбраживании имеет большое значение [4]. С одной стороны, аминокислоты служат важнейшим источником азота для осуществления жизнедеятельности дрожжевых клеток, а с другой – являются исходным материалом для образования побочных продуктов при спиртовом брожении высших спиртов. Поэтому исследовали динамику распада белков в процессе осахаривания зернового сырья (рисунок 6).
Продолжительность осахаривания, ч
Рисунок 6. Динамика гидролиза белков при 55 оС
Как видно из данных, представленных на рисунке 6, процесс накопления аминного азота наиболее интенсивно протекал в течение первых 4 ч, количество белков составляло 5 мг/см3. В дальнейшем скорость распада белков сократилась, и за последующие 36 ч содержание белков в гидролизате снизилось до 3,5 мг/см3.
На следующем этапе работы проводили разделение полученной осахаренной массы с помощью центрифугирования на фильтрат и белковую массу. Центрифугирование проводили при частоте вращения 2500 об/мин в течение 8 мин.
Белковую массу высушивали в сушильном шкафу до влажности 5 % при температуре не выше 35 0С во избежание денатурации белков, измельчали на лабораторной мельнице и исследовали ее свойства в сравнении с нативной клейковиной пшеницы.
По результатам анализа построили график зависимости водоудерживающей способности от продолжительности набухания полученного белкового продукта и товарной сухой клейковины пшеницы (рисунок 7).
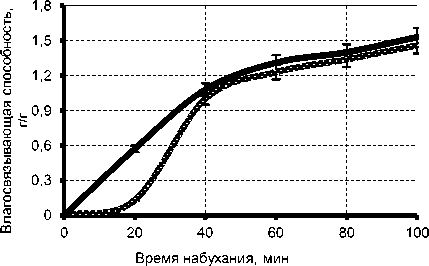
Белковый продукт ^^^^Сухая клейковина
Рисунок 7. Изменение влагосвязывающей способности клейковины
Как видно на рисунке 7, обе кривые имеют схожий вид, но полученный белковый продукт связывает влагу лучше, чем нативная пшеничная клейковина.
Были изучены физико-химические показатели полученного белкового продукта общепринятыми методами. Результаты представлены в таблице 1.
Т а б л и ц а 1
Физико-химические показатели клейковины
|
Наименование показателя |
Пшеничная клейковина |
Полученный продукт |
|
Растворимость, % |
7,0 |
10,0 |
|
Влагоудерживающая способность, г/г |
1,40 |
1,53 |
|
Жиросвязывающая способность, г/г |
1,45 |
1,90 |
Как выяснилось, полученный белковый продукт не только не уступает по показателям товарной пшеничной клейковине, но и превосходит ее. По внешнему виду полученный продукт представлял собой порошок без комков и посторонних примесей светло-кремового цвета со слабым мучным запахом.
Далее проводили исследование процесса сбраживания полученного после центрифугирования осветленного сусла на этанол. В осветленном сусле доводили концентрацию сухих веществ до 14% и вносили спиртовые дрожжи Saccharomyces cerevisiae расы XII и Saccharomyces cerevisiae расы IMB Y-5007 из расчета 120 млн клеток на 1 см3 сусла. Брожение вели в течение 48 ч при температуре 28 оС.
Поскольку гидролизат пшеничной муки несбалансирован по минеральному составу, необходимому для нормальной жизнедеятельности дрожжевой клетки, в опытные пробы вносили минеральные соли в различных дозировках, принятых в спиртовой отрасли.
В таблицах 2 и 3 представлены основные показатели процесса брожения сусла (методы исследований бражки стандартные, принятые в спиртовой отрасли), полученного из осветленного сусла с добавлением солей диаммоний фосфата в дозировках от 0,5 до 1,5 г/дм3 и сульфата аммония в количестве 0,5 г/дм3 при сбраживании различными расами дрожжей.
Т а б л и ц а 2
Показатели процесса брожения дрожжами Saccharomyces cerevisiae расы XII
|
Наименование показателя |
s о о к го И |
o' О & К к & |
о, О & К к & |
о к к & |
чО о и О & S ^i <> к |
|
рН |
4,6 |
4,8 |
5,2 |
5,15 |
5,05 |
|
Титруемая кислотность, град. |
0,3 |
0,3 |
0,4 |
0,5 |
0,3 |
|
Действительная массовая доля сухих веществ, % |
5,0 |
1,5 |
2,5 |
1,0 |
2,0 |
|
Видимый отброд, град. |
0,0 |
+0,1 |
+0,2 |
+0,3 |
+0,2 |
|
Выход спирта, дал из 1т сухих веществ крахмала |
39,3 |
53,6 |
57,1 |
60,6 |
53,6 |
Из полученных данных видно, что наиболее эффективно процесс брожения проходил при добавлении в качестве питания для дрожжей диаммоний фосфата в дозировке 1,5 г/дм3. В других случаях брожение проходило менее интенсивно, что было обусловлено недостаточным количеством минеральных солей.
Исследования показали, что при применении дрожжей Saccharomyces cerevisiae IMB Y-5007 процесс брожения проходил не менее интенсивно. Однако полученные результаты свидетельствуют о неудовлетворительном протекании процесса брожения при небольших дозировках солей, что, вероятно, связано с несбалансированностью минерального состава гидролизата. С другой стороны, при дозировке диаммоний фосфата в количестве 1,5 г/дм3 накопилось максимальное количество спирта.
Т а б л и ц а 3
Показатели процесса брожения дрожжами Saccharomyces cerevisiae расы IMB Y-5007
|
Наименование показателя |
s ЬЙ л о ЬЙ о со И |
о О & К |
-§ CD О & |
-§ о |
-§ cd" к о |
|
рН |
4,5 |
4,7 |
5,1 |
5,0 |
4,8 |
|
Титруемая кислотность, град. |
0,35 |
0,4 |
0,5 |
0,5 |
0,4 |
|
Действительная массовая доля сухих веществ, % . |
4,0 |
1,5 |
2,0 |
1,0 |
2,5 |
|
Видимый отброд, град. |
0,0 |
+0,1 |
+0,2 |
+0,4 |
+0,2 |
|
Выход спирта, дал из 1т сухих веществ крахмала |
42,9 |
53,6 |
57,1 |
60,7 |
53,6 |
Таким образом, для сбраживания полученного сусла пригодны обе культуры дрожжей.
Из представленных данных видно, что минеральное питание благоприятно влияет на выход спирта. Однако теоретический выход спирта из 1 т сухих веществ в пересчете на
Список литературы Разработка технологии переработки пшеницы на спирт и белковый продукт
- Фурсова Т. И. Получение сиропов путем биоконверсии зерна кукурузы и их сбраживание: дис. канд. тех. наук: 05. 18. 07. Воронеж: ВГТА, 2010. 169 с.
- Романюк Т.И., Чусова А.Е., Агафонов Г.В. Получение осветленного сусла из зерна ржи и его сбраживание на этанол//Производство спирта и ликероводочных изделий. 2013. №4. С. 13-16.
- Фурсова Т.И., Борисова И.В. Перспективы получения белка из зерна пшеницы//Успехи современного естествознания. 2011. №7. С. 228а.
- Фурсова Т.И., Корнеева О.С., Востриков С.В. Исследование процесса брожения гидролизатов крахмала различного углеводного состава. Часть 2.//Производство спирта и ликероводочных изделий. 2008. №4. С. 13-16.
- Фурсова Т.И., Корнеева О.С., Востриков С.В. Использование ферментных препаратов для получения гидролизатов крахмала различного углеводного состава. Часть 1//Производство спирта и ликероводочных изделий. 2008. №3. С. 18-21.
- Пат. 2006/119386 A2 US, IPC7 C12P 7/06 Способы производства этанола из крахмалсодержащего сырья и фракционирование/Скуг М., № 2006017041; Заявл. 02.05.2006; Опубл. 09.11.2006.


