Реакции гексаметилентетрамина (уротропина) с этилендиаминтетрауксусной кислотой. Молекулярная структура тригидрата диаммоний этилендиаминтетраацетата (NH4)2H2L∙3H2O
Автор: Владимир Викторович Семёнов, Борис Иванович Петров, Татьяна Семёновна Почекутова, Николай Михайлович Лазарев, Наталья Вадимовна Золотарёва, Роман Валерьевич Румянцев, Евгений Николаевич Разов
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Взаимодействие этилендиаминтетрауксусной кислоты (H4L, ЭДТА) с гексаметилентетрамином (CH2)6N4 (ГМТА) в водной среде приводит к образованию моногидрата гексаметилентетраминий этилендиаминтетраацетата [(CH2)6N4H]+(H3L)‒∙H2O (1) и тригидрата диаммонийэтилендиаминтетраацетата (NH4)2H2L∙3H2O (2). Диаммонийная соль получается в реакции 2 молей водного раствора аммиака, образующегося в результате диссоциации ГМТА в водно-метаноловой среде до формальдегида и аммиака и реакцией последнего с ЭДТА с выходом после перекристаллизации 32 %. Реакция в соотношении NH3 : H4L в соотношении 4 : 1 не приводит к образованию чистых продуктов тетра- или триаммонийных солей (NH4)nH4-nL∙mH2O (n = 3, 4). Смесь представляет собой триаммонийную соль с непрореагирующей кислотой. Однако, перекристаллизация из водного метанола дает чистый образец диаммонийной соли (NH4)2H2L∙3H2O. Строение синтезированных комплексов исследовано методами ИК-спектроскопии и элементного анализа. Строение комплекса 2 доказано методом РСА. Анализ показал, что дианион этилендиаминтетераацетата в 2 представляет собой цвиттер-ион, в котором атомы водорода расположены на атомах азота, а все четыре карбоксильные группы депротонированны. Выявлены общие закономерности по взаимодействию четырёхосновных кислот ЭДТА и ОЭДФ с ГМТА и водным аммиаком и показана аналогия протекания этих реакций. Установлено, что диаммонийные соли могут быть синтезированы напрямую из кислот и водных растворов аммиака.
Гексаметилентетрамин, этилендиаминтетрауксусная кислота и ее диаммонийная соль, молекулярная структура
Короткий адрес: https://sciup.org/147252522
IDR: 147252522 | УДК: 547.233.3; 547.288.15; 547.32; 546.39 | DOI: 10.14529/chem250410
Reactions of hexamethylenetetramine (urotropine) with ethylenediaminetetraacetic acid. Molecular structure of diammonium ethylenediaminetetraacetate trihydrate (NH4)2H2L∙3H2O
The interaction of ethylenediaminetetraacetic acid (H4L, EDTA) with hexamethylenetetramine (CH2)6N4 (HMTA) in aqueous medium leads to formation of hexamethylenetetraminium ethylenediaminetetraacetate monohydrate [(CH2)6N4H]+(H3L)-∙H2O (1) and diammonium ethylenediaminetetraacetate trihydrate (NH4)2H2L∙3H2O (2). The diammonium salt is obtained by reaction of 2 moles of aqueous ammonia solution formed by dissociation of HMTA in aqueous methanol medium to formaldehyde and ammonia and reaction of the latter with EDTA, yielding 32% after recrystallization. The reaction with the ratio NH3 : H4L equaling 4 : 1 does not lead to formation of pure products of tetra- or triammonium salts (NH4)nH4-nL∙mH2O (n = 3,4). The mixture is a triammonium salt with an unreacted acid. However, recrystallization from aqueous methanol gives a pure sample of the diammonium salt (NH4)2H2L∙3H2O. The structure of the synthesized complexes was investigated by IR spectroscopy and elemental analysis. The structure of complex 2 was proved by the X-ray method. The analysis has shown that the dianion of ethylenediaminetetraacetate in 2 is a zwitterion in which hydrogen atoms are located on nitrogen atoms and all four carboxyl groups are deprotonated. General regularities concerning the interaction of quadruplebutyric acids EDTA and OEDP with HMTA and aqueous ammonia have been revealed, and the analogy of the course of these reactions has been shown. It is established that the diammonium salts can be synthesized directly from acids and aqueous ammonia solutions.
Текст научной статьи Реакции гексаметилентетрамина (уротропина) с этилендиаминтетрауксусной кислотой. Молекулярная структура тригидрата диаммоний этилендиаминтетраацетата (NH4)2H2L∙3H2O
Известно, что этилендиаминтетрауксусная кислота (ЭДТА) – это органическое соединение, содержащая в своём составе как четыре карбоксильные, так и две аминогруппы. Являясь широко известным комплексоном, способным образовывать хелатные соединения металлов, данная ки- слота в первую очередь используется в промышленности для удаления металлов. К примеру, следует выделить следующие отрасли: текстильная [1], кожевенная [2–5], бумажная [6–8], лакокрасочная [9]. Кроме этого данную кислоту используют при производстве металлов [10], а также при нефтедобыче [11, 12], очистке почвы от тяжёлых металлов [13] и в газовой промышленности (ингибиторы и промоторы гидратообразования) [14–17].
Другим направлением использования ЭДТА является медицина. Применение кислоты связано с лечением отравлений тяжёлыми металлами [18, 19]. ЭДТА имеет антимикробную [20] и ан-тикоагулятивную активности [21]. ЭДТА также играет важную роль в стоматологии [22] и фармацевтике [23]. Этилендиаминтетрауксусная кислота используется в сельском хозяйстве. Кроме упомянутой выше фиторемедиации (очистки сточных вод, грунтов с использованием зелённых растений) ЭДТА является известным веществом для питания растений и повышения плодородия почв [24]. Существуют два основных способа подкормки растений: внесение в почву и внекорневая подкормка. Второй способ дополнительного питания растения является преимущественным, так как отсутствует риск вымывание питательных веществ из почвы, нет угнетения почвенной микрофлоры из-за побочной реакции ЭДТА или Трилона Б с находящимися в почве тяжёлым металлами и, последнее, осуществляется более быстрый отклик растения на внесенное через листья удобрения. Как правило, в качестве подкормки чаще используют динатриевую соль этилен-диаминтетрауксусной кислоты (Трилон Б), которая лучше растворяется в воде, чем исходная кислота. Данная соль реагирует с нерастворимыми солями металлов и переводит их в растворимую форму, необходимую для усвоения растениями [25]. Кроме этого, добавляют различные соединения (к примеру, органические амины), которые играют роль промотров растворимости.
В работе [26] показана возможность применения гексаметилентетрамина (ГМТА, уротропина) в качестве промотора увеличения водорастворимости (1-гидроксиэтилиден)дифосфонатов металлов M(H 2 L)∙2H 2 O (где М = марганец(II), кобальт(II) и цинк(II)). Растворимость комплексов биометаллов связана с использованием их в качестве микроудобрений, увеличивающих рост растений. ГМТА реагировал с ОЭДФ в среде метанола с образованием дигидрата гексаметилентет-раминий (1-гидроксиэтилиден)дифосфоната [(CH 2 ) 6 N 4 H]+H 3 L ՛ 2‒∙2H 2 O. При нагревании в смеси метанола и воды соединение диссоциировало на кислоту и основание, а гексаметилентетрамин взаимодействовал с водой, давая аммиак и формальдегид, в результате кислота и аммиак генерировали диаммонийную соль (1-гидроксиэтилиден)дифосфоновой кислоты (NH 4 ) 2 H 2 L ՛ :
[(CH 2 ) 6 N 4 H]+H 3 L ՛ ‒ = (CH 2 ) 6 N 4 + H 4 L ՛ H 4 L ՛ + 2 H 2 O = 2 H 3 O+ + H 2 L ՛ 2‒ (CH 2 ) 6 N 4 + 4 H 3 O+ + 2 H 2 O = 6 СН 2 О + 4 NH 4 + H 2 L ՛ 2‒ + 2 NH 4 + = (NH 4 ) 2 H 2 L ՛
Кроме того, ранее нами были получены и охарактеризованы девять новых комплексов ЭДТА с аминами (моноэтаноламином, три(гидроксиметил)метанамином, диэтиламином, трет-бутиламином, триэтаноламином, гексаметилен-1,6-диамином, 2,2’-(этилендиокси)ди(этиламином), триэтилендиамин(диазабицикло-2,2,2-октаном) и тетраметилэтилендиамином) [27].
Целью настоящего исследования является изучение реакций (CH 2 ) 6 N 4 (ГМТА) с этилен-диаминтетрауксусной кислотой (H 4 L, ЭДТА), имеющей также как и ОЭДФ четыре кислотные группы:
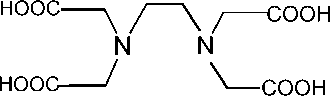
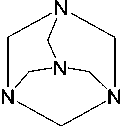
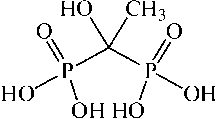
Этилендиаминтетрауксусная кислота H 4 L (ЭДТА)
Гексаметилентетрамин (CH 2 ) 6 N 4 (ГМТА)
(1-Гидроксиэтилиден) дифосфоновая кислота H 4 L ՛ (ОЭДФ)
В результате такое взаимодействие может привести к образованию новых индивидуальных комплексов или полимерных соединений. Кроме того, взаимодействие с протонными кислотами наряду с образованием аминиевых солей может сопровождаться разложением до аммиака и формальдегида. В водном растворе аммиак будет конкурировать с ГМТА и давать аммонийные производные (NH 4 ) n H 4-n L.
Экспериментальная часть
Реакция ЭДТА с ГМТА. К суспензии 3,00 г (1,03∙10–2 моль) ЭДТА в 30 мл Н 2 О приливали раствор 1,45 г (1,03∙10–2 моль) ГМТА в 20 мл Н 2 О, смесь нагревали до 50 °С. Через 20 мин суспензия ЭДТА растворилась. Прозрачный раствор упарили до объема 10 мл, добавили 15 мл метанола, нагрели до кипения. Из прозрачного водно-метанольного раствора при –8…–10 °С выпал осадок. Смесь фильтровали, осадок промывали метанолом, сушили в вакууме. Получили 1,50 г (3,94∙10–3 моль, 38%) кристаллов тригидрата диаммоний этилендиаминтетраацетата (NH 4 ) 2 H 2 L∙3H 2 O ( 2 ). ИК-спектр, ν/см–1: 3187, 2153, 1840 пл, 1629, 1459, 1444, 1399, 1379, 1352, 1325, 1230, 1203, 1093, 1078, 1060, 976, 956, 914, 860, 801, 720, 684, 634, 571, 497. Найдено, %: С 31,17; Н 7,39; N 14,64. C 10 H 28 N 4 O 11 . Вычислено, %: С 31,58, H 7,42, N 14,73. Фильтрат упарили, остаток в виде светло-желтой мягкой массы нагрели в вакууме до 110оС. Получили 2,63 г (5,84∙10–3 моль, 57 % гидрата гексаметилентетраминий этилендиаминтетраацетата [(CH 2 ) 6 N 4 H]+H 3 L‒∙H 2 O ( 1 ) в виде застывшей белой пены, легко размалывающейся до белого порошка. ИК-спектр, ν/см-1: 3175, 1918, 1665 пл, 1623, 1462, 1379, 1358, 1316, 1262, 1250, 1221, 1149, 1084, 1042, 1015, 991, 958, 905, 851, 824, 789, 717, 696, 649, 503. Найдено, %: С 42,63; Н 7,11; N 18,46. C 16 H 30 N 6 O 9 . Вычислено, %: С 42,65, H 6,72, N 18,66.
ИК-спектры поглощения регистрировали на ИК Фурье-спектрометре ФСМ 1201 в спектральном диапазоне от 400 до 4000 см–1 с разрешением 4 см–1; число сканов 32. Образцы готовили в виде суспензии в вазелиновом масле и помещали между окнами из бромистого калия.
Элементный анализ выполнен на автоматическом элементном анализаторе Vario EL cube (Elementar Analysensysteme GmbH) в конфигурации CHNS, газ-носитель – гелий марки 6.0.
Электронная микроскопия – на сканирующем электронном микроскопе Tescan VEGA II. Микрорельеф исследовали при увеличениях от 500 х до 50000 х . Съемку проводили при ускоряющем напряжении 20 кВ и рабочем расстоянии 2–8 мм, использовали детекторы вторичных электронов (SE) и обратно рассеянных электронов (BSE).
Рентгенофазовый анализ (РФА) проведён на рентгеновском дифрактометре Shimadzu XRD-7000.
Термогравиметрический анализ (ТГА) выполнен на приборе синхронного термического анализа TGA/DSC 3+ METTLER TOLEDO, скорость нагрева составляла 5 град. /мин, скорость подачи азота – 20 мл/мин.
Рентгеноструктурный анализ монокристалла тригидрата диаммонийэтилендиаминтетра-ацетата (NH4)2H2L∙3H2O (2) проводили на автоматическом дифрактометре Rigaku OD Xcalibur (графитовый монохроматор, МоКα-излучение, ω-сканирование, λ = 0,71073 Å) при температуре 100(2) К. Измерение и интегрирование экспериментальных наборов интенсивностей, а также учет поглощения проведены с использованием программного пакета CrysAlisPro [28]. Структура решена «dual-space» методом с использованием программы SHELXT [29]. Все неводородные атомы уточнены полноматричным МНК по Fhkl2 в анизотропном приближении с помощью программного пакета SHELXTL [30]. Атомы водорода, за исключением атомов водорода воды и аммонийных катионов, а также атомов H(1) и H(2), помещены в геометрически рассчитанные положения и уточнены с использованием модели наездника (Uiso(H) = 1,2Ueq(C)). В свою очередь все остальные атомы водорода локализованы объективно из разностного Фурье-синтеза и уточнены в изотропном приближении. Две из трёх молекул воды разупорядочены по двум положениям с соотношением 0,82:0,18. Для уточнения разупорядоченных атомов кислорода использовалась инструкция EADP, Кроме того, геометрия атомов водорода на разупорядоченных молекулах воды фиксировалась с использованием инструкции DFIX. Соединение (NH4)2H2L∙3H2O кристаллизуется в виде бесцветных пластинок. Для РСА был выбран кристалл с размерами 0,33 × 0,29 × 0,09 мм. Кристаллографические параметры и детали уточнения структуры 2 приведены в табл. 1. Структура задепонирована в КБСД (№ 2384278; .
Таблица 1
Кристаллографические параметры и детали уточнения структуры 2
|
Параметр |
Значение |
|
Брутто-формула |
C 10 H 28 N 4 O 11 |
|
М |
380,36 |
|
Сингония |
Моноклинная |
|
Пространственная группа |
P2 1 /c |
|
a , Å |
8,3593(5) |
|
b, Å |
28,3782(15) |
|
c, Å |
7,8036(6) |
|
β , град. |
109,514(7) |
|
V, Å3 |
1744,9(2) |
|
Z |
4 |
|
d calc , г·см–3 |
1,448 |
|
µ, мм–1 |
0,130 |
|
θ, град. |
2,585 < θ < 25,026 |
|
Число рефлексов |
|
|
измеренных |
18570 |
|
независимых |
3071 |
|
с I > 2σ I |
2263 |
|
R int |
0,0540 |
|
Число уточняемых параметров |
305 |
|
S(F2) |
1,042 |
|
R 1 ( I > 2σ( I )) |
0,0424 |
|
wR 2 (по всем отражениям) |
0,1113 |
|
Остаточная электронная плотность (Δρ min / Δρ max ), e ·Å–3 |
0,352/–0,292 |
Термическое разложение гидрата гексаметилентетраминий этилендиаминтетраацетата [(CH2)6N4H]+H3L‒ ∙ H2O ( 1 ). Нагревали в вакууме в трубке Шленка 0,90 г соединения 4 до температуры 255 °С. Желтый порошок при 220 °С поменял окраску на коричневую, при 250 °С потемнел, при 255 °С расплавился. Получили 0,65 г темно-коричневого остатка, быстро растворяющегося без остатка в воде, потери массы составили 28 % от первоначального веса. ИК-спектр, ν, см–1: 3700–2300 ш, 1718 пл, 1677, 1632, 1313, 1215, 1149, 1093, 973, 902, 720, 702, 634. В охлаждаемом жидким азотом отростке скопилось 0,09 г прозрачной желтоватой жидкости, ИК-спектр, ν, см–1: 3700–3000 ш, 2955, 2928, 2886, 2147, 1665, 1390, 1236, 1072, 1048, 1009, 812, 684, 613, 512; ГХ-МС: 11 летучих органических соединений, среди них идентифицированы N-метилформамид, 1,2,2-триэтилпиперидин, уротропин.
Обсуждение результатов
Реакция с ЭДТА протекала только в водной среде. ГМТА хорошо растворялся в хлороформе и в метаноле, в то время как ЭДТА плохо растворяется в воде и ещё хуже в МеОН. Попытки проведения реакции в среде МеОН и CHCl3 показали, что взаимодействия в этих растворителях не происходило. При соотношении компонентов 1:1 из реакционной смеси были выделены моногидрат гексаметилентетраминий этилендиаминтетраацетат [(CH 2 ) 6 N 4 H]+(H 3 L)‒∙H 2 O ( 1 ) и тригидрат диаммонийэтилендиаминтетраацетат (NH 4 ) 2 H 2 L∙3H 2 O ( 2 ). Соединение ( 1 ) умеренно растворялось в метаноле, плохо в ацетоне, ацетонитриле и хлороформе. При высыхании капель растворов в этих растворителях на подложке формировались аналогичные сетчатые фигуры, составленные из микрокристаллов. На рис. 1а представлена микрофотография осадка, высаженного из раствора соединения 1 в ацетоне. Диаммонийная соль 2 кристаллизовалась из пересыщенного раствора в Н 2 О/МеОН в виде тригидрата (NH 4 ) 2 H 2 L∙3H 2 O и была получена с выходом 32 %. СЭМ-изображение диаммонийной соли (рис. 1б) показывает, что соединение выпадает из раствора в виде крупных (до 0,50 мм) объемных кристаллов, на поверхности которых кристаллизуются мелкие поликристаллические частицы.
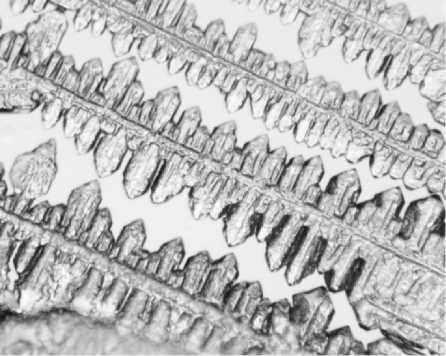
а)
Рис. 1. Оптическое (а, увеличение х100) и СЭМ (б) изображение кристаллов моногидрата гексаметилентетраминий этилендиаминтетраацетата [(CH 2 ) 6 N 4 H]+(H 3 L)‒ ∙H 2 O (а) и тригидрата диаммоний этилендиаминтетраацетата (NH 4 ) 2 H 2 L∙3H 2 O (б)

200 мкм
б)
Порошковые ре н тге н о граммы ( рис . 2) свидетельствуют о том, что соединения 1 и 2 существ у ю т в ра зли чн ых к ри с таллогр афических формах. Небольшая примесь аморфн ой фа зы в оз можно присутствует в 1. Ме лк и е ча с тицы на крупных кристаллах представляют с о б ой ми к ро к ри с талл ы соединения 2 .
На рис. 3 п ре д с та в л е н а мо лекулярная структура тригидрата диаммоний э ти ле н д и а ми н те тр а-ацетата (NH 4 ) 2 H 2 L∙3H 2 O ( 2 ). М онокристальный рентгеноструктурный анали з ( SC-XRD) показал, ч т о ди а н и он э ти л е н д и а м и н те тра а ц е та т а в 2 представляет собой цвиттер-ион, в котором атомы в одород а ра с п о лож е н ы на а томах азота, а все четыре карбоксильные группы д е п ротон и ров а ны.
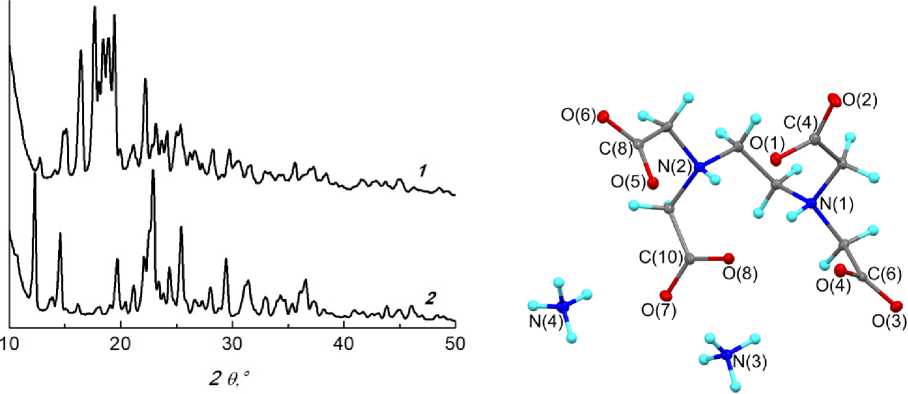
Рис. 2. Порошковые дифрактограммы моногидрата гексаметилентетраминий этилендиаминтетраацетата [(CH 2 ) 6 N 4 H]+H 3 L‒∙H 2 O (1) ( 1 ) и тригидрата диаммоний-этилендиаминтетраацетата (NH 4 ) 2 H 2 L∙3H 2 O (2) ( 2 )
Рис. 3. Молекулярная структура тригидрата диаммонийэтилендиаминтетраацетата (NH 4 ) 2 H 2 L∙3H 2 O (2). Молекулы воды не приведены для наглядности
Все расстояния C-O в о в с ех четырёх карбоксильных группах в значительн ой с те п е н и в ыровн ены межд у с о б ой и в арь иру ют ся в ди а п а зон е 1, 244(3)–1,262(3) Å (табл. 2). Ранее подобная геомет ри я ди а н и она э ти ле нд и а ми н те тра а це та та н а бл ю д а л а с ь в комплексах с двухвалентными металлами [31–32].
Таблица 2
|
Связь |
Длина, Å |
Угол |
ω, град |
|
O(1)-C(4) |
1,247(3) |
O(1)-C(4)-O(2) |
126,4(2) |
|
O(2)-C(4) |
1,258(3) |
O(3)-C(6)-O(4) |
127,2(2) |
|
O(3)-C(6) |
1,256(3) |
O(5)-C(8)-O(6) |
126,8(2) |
|
O(4)-C(6) |
1,244(3) |
O(7)-C(10)-O(8) |
127,2(2) |
|
O(5)-C(8) |
1,251(3) |
Σ ∠ @N(1) |
657(2) |
|
O(6)-C(8) |
1,248(3) |
Σ ∠ @N(2) |
656(2) |
|
O(7)-C(10) |
1,246(3) |
||
|
O(8)-C(10) |
1,262(3) |
Длины связей (Å) и углы (град) в структуре 2
Катионы аммония образуют короткие водородные связи с атомами кислорода карбоксильных групп и, вместе с молекулами воды, формируют в кристалле 2 3D-сеть водородных O-H…O и N-H…O связей (табл. 3).
Таблица 3
Геометрические характеристики, соответствующие N–H…O и O–H…O водородным связям в кристалле 2
|
D –H…O |
D –H, Å |
H…O, Å |
D …O, Å |
∠ D HO, град |
|
N(1)-H(1)...O(8) |
0,90(2) |
2,04(2) |
2,799(2) |
141(2) |
|
N(2)-H(2)…O(1) |
0,84(3) |
2,11(3) |
2,788(2) |
137(2) |
|
N(2)-H(2)…O(8) |
0,84(3) |
2,15(3) |
2,641(2) |
117(2) |
|
N(3)-H(3)…O(4)_$1* |
1,00(3) |
1,79(3) |
2,760(3) |
163(2) |
|
N(3)-H(4)…O(8)_$2 |
0,97(3) |
1,81(3) |
2,771(3) |
174(2) |
|
N(3)-H(5)…O(5)_$3 |
0,92(3) |
2,04(3) |
2,929(3) |
161(2) |
|
N(3)-H(5)…O(6)_$3 |
0,92(3) |
2,47(3) |
3,187(3) |
134(2) |
|
N(3)-H(6)…O(7) |
0,86(3) |
1,98(3) |
2,836(3) |
171(2) |
|
N(4)-H(7)…O(1)_$1 |
0,91(3) |
2,05(3) |
2,814(3) |
141(2) |
|
N(4)-H(8)…O(5)_$1 |
0,88(3) |
2,17(3) |
2,951(3) |
147(3) |
|
N(4)-H(9)...O(3)_$2 |
0,91(3) |
1,98(3) |
2,878(3) |
167(2) |
|
N(4)-H(10)...O(3)_$4 |
0,95(3) |
1,90(4) |
2,850(3) |
172(3) |
|
O(1S)-H(1S1)...O(2)_$4 |
1,00(4) |
1,68(4) |
2,675(2) |
173(3) |
|
O(1S)-H(1S2)...O(6) |
0,76(3) |
2,11(4) |
2,864(3) |
169(4) |
|
O(2S)-H(2S1)...O(3S)_$5 |
0,959(5) |
2,10(3) |
2,685(5) |
118(2) |
|
O(2S)-H(2S2)...O(2) |
0,962(5) |
1,767(10) |
2,711(3) |
166(3) |
|
O(3S)-H(3S1)...O(1S)_$5 |
0,958(5) |
1,791(9) |
2,741(3) |
171(3) |
|
O(3S)-H(3S2)...O(2S) |
0,961(5) |
1,76(2) |
2,644(4) |
152(4) |
|
O(2Q)-H(2Q1),,,O(2) |
0,958(5) |
2,45(15) |
2,941(13) |
112(11) |
|
O(3Q)-H(3Q1),,,O(1S) |
0,958(5) |
2,49(10) |
3,071(13) |
119(8) |
– Операции симметрии, используемые для генерации эквивалентных атомов:
|
$1 |
x, |
y, |
z–1; |
|
$2 |
–x+2, |
–y, |
–z+1; |
|
$3 |
x+1, |
y, |
z; |
|
$4 |
x–1, |
y, |
z–1; |
|
$5 |
x, |
–y+1/2, |
z+1/2. |
Интересно отметить, что кристалл 2 имеет слоистую структуру. В нём последовательно чередуются слои дианионов, катионов, дианионов и нейтральных молекул растворителя (рис. 4). При этом все четыре карбоксильные группы этилендиаминтетраацетата принимают участие в водородных связях с катионным слоем.
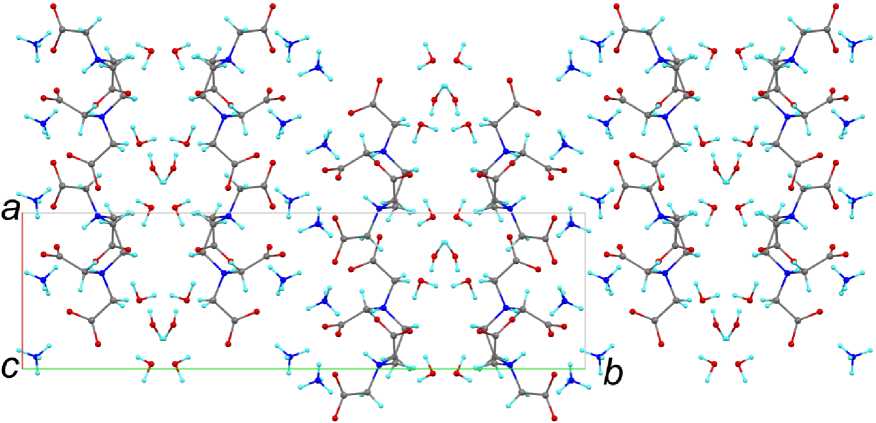
Рис. 4 . Фрагмент кристаллической упаковки (NH4)2H2L^3H 2 O ( 2 )
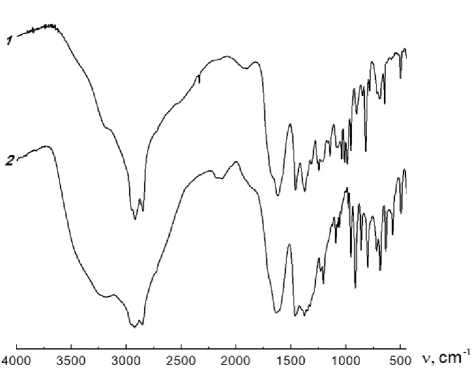
Рис. 5 . ИК-спектры моногидрата гексаметилентетраминий этилендиаминтетраацетата [(CH 2 ) 6 N 4 H]+H 3 L‒∙H 2 O (1) и тригидрата диаммонийэтилендиаминтетраацетата (NH 4 ) 2 H 2 L∙3H 2 O (2)
На рис. 5 представлены ИК-спектры соединений 1 и 2 . В характеристичной области спектра от 3700 до 1500 см–1 следу е т отме ти ть с ле д у ю щ ие ра зли чи я:
-
– в спектре соединения 2 высокое содержание связей N-H (восемь) в четвертичных аммонийных группах и связей О- Н (шесть) в молекулах кристаллизационной воды в ызв а ло и н те н с ивное поглощение в области 3 700–2500 см–1;
-
– деформа ц и онны е к ол е ба н и я с в яз ей N-H и валентные колебания связей С=О представлены н ера зд е л е н н ой оче н ь и н т е н с и в ной п ол ос ой с цен т р ом п ри 1629 с м–1;
-
– в соединении 1 т о ль к о од н а с в язь N-H в аминиевой группировке и две связи О-Н в молекул е кри с та л ли за ц и он н ой в од ы обе с п е чи ли н а мн о го ме н ее и н тенсивное поглощение в области 3700–2500 см–1;
-
– деформа ц и онны е к ол е ба н и я с в яз ей N-H и валентные колебания связей С=О представлены п л охо ра з д е ле н н ой и н тен с и в н ой п олос ой с мак си му мом п ри 1623 см–1 (С=О) и плечом при 1665 см–1 (N-H).
Обра зовани е д и а ммон и йной соли свидетельствовало о диссоциации ГМТА в водно-мет ан ольн ой сре де д о фо рма ль дегида и аммиака. Последний взаимодействов а л с ЭДТ А с об р а з ованием (NH 4 ) 2 H 2 L∙3H 2 O ( 2). Происходящие при этом реакции аналогичн ы п ре д с т а в ле н н ым на схеме 1 (L ՛ след у е т за мени ть н а L).
При термической обработке в отсутствие Н 2 О генерирование одновременно двух газообразных продуктов (формальдегида и аммиака) не представляется возможным. Однако выделение NH3 вполне может происходить, Изучение термических свойств соединения 1 методом ТГА (рис. 6) показало существенную разницу в его поведении при нагревании в инертной атмосфере по сравнению с аналогичным производным ГМТА с ОЭДФ [26]. Нагревание навески 1,5–2,0 мг комплекса на основе ОЭДФ [(CH 2 ) 6 N 4 H]+H 3 L‒ ∙2H 2 O до 170–200 °С приводило к расширению объема во время этого процесса с выделением газа, тогда как термическое разложение 1 протекало спокойно. При нагревании производного ЭДТА в вакууме не наблюдалось расширение объёма и образования пены, как это происходило в случае аналогичного производного ОЭДФ.
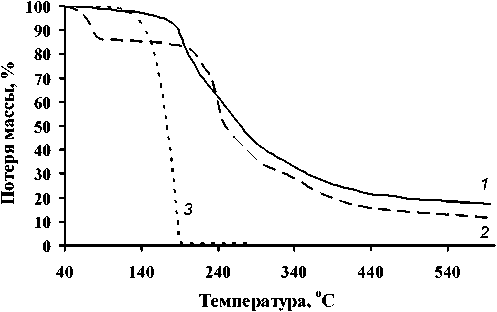
Рис. 6 . Термогравиметрический анализ соединений 1 ( 1 ), 2 ( 2 ) и ГМТА ( 3 )
Эксперимент по изучению термостабильности соединений 1 и 2 был проведён в температурном интервале 40–600 °С. На рис. 6 представлены соответствующие кривые потери массы при нагревании в инертной атмосфере, а также сведения о термическом поведении уротропина. Авторы статьи [33] предположили, что уротропин начинает сублимироваться при температуре 110 °С, что хорошо согласуется с нашими данными, полученными для уротропина в индивидуальном состоянии. Однако, если для соединения уротропина с п-нитрофенолом [33] при этой температуре наблюдается потеря массы (связанная с уротропином), то для изученного в этой работе комплекса 1 уменьшение массы не наблюдается до 180 °С, что связано с лучшей термической стабильностью. Соединение 1 , содержащее уротропин и ЭДТА начинает интенсивно теряет свою массу при 180 °С. Оно практически полностью переходит в газовую фазу. Окончательная потеря массы при 600 °С составляет ~ 83 %. Согласно литературным данным [34] основными конечными летучими продуктами термораспада уротропина являются аммоний, формальдегид и углекислый газ. Кроме того, в работе [35] отмечено, что одним из продуктов разложение уротропина может быть гидразин. Аналогично конечными продуктами пиролиза ЭДТА могут являться метан, этан, этилен, пропилен и азот в виде аминов [36].
В отличие от 1 , характер экспериментальной кривой для соединения 2 говорит о том, что вещество теряет массу с частичным разложением. На первой стадии при 60–100 °С происходит потеря молекул воды. Безводная соль теряет молекулы аммиака в интервале температур 200– 250 °С. Затем ЭДТА подвергается постепенному и полному разложению от 250 до 600 °С, поскольку, согласно работам [37, 38], свободная кислота термически стабильна до 240 °С. Авторами статьи [36] предположено, что при повышении температуры кислота теряет четыре –COOH группы. Затем при 260 °С образуются CO, формальдегид и ацетальдегид. При 600 °С вещество 2 теряет до 89 % своей массы. Конечные продукты разложения аналогичны 1 соединению. Подобный характер термического разложения вещества 2 опубликован в статье [39], где приводится анализ ТГА для амониевой соли циклогександиаминтетрауксусной кислоты.
Ожидалось, что образование и кристаллизация диаммонийной соли в смешанном растворителе вода-метанол даст возможность ее получения напрямую из аммиака и ЭДТА. Сведения о получении и свойствах солей лития, натрия и калия достаточно многочисленны. Динатриевая соль Na2H2L∙2H2O получена с целью исследования ее термических свойств в диапазоне темпера- тур 80–645оС [40], в [41] представлены ИК-спектры тетранатриевой соли Na4L. В [42] исследованы колебательные спектры полного ряда калиевых солей КnH4-nL (n = 1–4) в том числе дейтеро-замещенных КnD4-nL (n = 1–4). Рентгеноструктурные исследования выполнены для соединений лития [43], натрия [44], калия [45, 46] и рубидия [47]. Известно координационное соединение [Co(NH3)6][NaL] ∙3,5H2O, в котором аммиак входит в состав катиона [48]. Отметим, что в данном комплексе молекула ЭДТА непосредственно связана с катионом натрия, который координирует шесть донорных атомов ЭДТА (четыре атома кислорода и два атома азота) и нейтральную молекулу воды. В свою очередь, катион [Co(NH3)6]3+ взаимодействует с ЭДТА только за счёт водородных связей. При проведении реакции ЭДТА с гидразингидратом в аммиачной среде был получен комплекс (N2H5)H3L∙2NH3∙4H2O, содержащий молекулу аммиака, не связанную с молекулой кислоты [39, 49]. В этих же работах сообщалось о синтезе и строении дигидрата аммоний циклогександиаминтетрауксусной кислоты (NH4)H3L՛ ∙2H2O. В работе представлены люминесцентные свойства серии комплексов лития, натрия, калия и аммония Na2L∙2H2O, Na4L, Li2L, K2L, (NH4)2L [50]. Их структурные данные не приведены.
Осложнения, которые могут встретиться в экспериментах по синтезу (NH 4 ) n H 4–n L из H 4 L и NH 4 ОH, становятся понятными при сравнении свойств водных растворов NaOH, KOH с водными растворами аммиака. При синтезе NanH4–nL и KnH4–nL точная стехиометрия реакции щелочи и кислоты может быть вполне задана и выдержана на всем протяжении процесса выделения целевого соединения в чистом виде. Кислота и щелочь не могут быть потеряны из-за их малой летучести. В отличие от этого в аналогичном процессе с аммиаком его концентрация может существенным образом измениться при упаривании водного раствора, вследствие чего будет получена смесь аммонийной соли с пониженным значением n в (NH 4 ) n H 4–n L и непрореагировавшей ЭДТА. Для выяснения возможности получения ди- и тетрааммонийных солей к водной суспензии ЭДТА были добавлены 2 и 4 моля аммиака, полученные прозрачные растворы упарены, твердые продукты высушены на воздухе и перекристаллизованы из Н 2 О-МеОН в условиях, аналогичных выделению (NH 4 ) 2 H 2 L из реакционной смеси ГМТА с ЭДТА. Выделенные продукты были проанализированы методами элементного анализа, ИК-спектроскопии. Полученные результаты представлены в табл. 4 и на рис. 7.
Из результатов элементного анализ следовало, что продукт реакции, проведенной при соотношении NH3 : H4L = 2 : 1, сразу после синтеза и после перекристаллизации из Н2О-МеОН соответствовал формуле (NH 4 ) 2 H 2 L∙3H 2 O, В отличие от этого продукт реакции, проведенной при соотношении реагентов NH 3 : H 4 L = 4 : 1, заданной формуле (NH 4 ) 4 L не соответствовал, Наблюдалось пониженное содержание азота, 16,95 против 23,33 %, что явно указывало на потерю аммиака при синтезе, Несоответствие несколько сглаживалось, но не исчезало при расчете для формулы (NH 4 ) 3 HL, Добавление в расчетную формулу одной или нескольких молекул кристаллизационной воды не изменяло ситуацию, Наилучшее соответствие экспериментально определённого состава наблюдалось с расчетной формулой (NH 4 ) 3 HL∙H 4 L.
Таблица 4
Результаты элементного анализа (%) продуктов реакции аммиака с ЭДТА в молярных соотношениях 2:1 и 4:1 до перекристаллизации из Н 2 О-МеОН
|
Соотношение NH 3 :H 4 L |
С |
H |
N |
Соотношение NH 3 :H 4 L |
С |
H |
N |
|
2:1, найдено |
31,04 |
7,29 |
14,10 |
4:1, найдено |
36,42 |
7,22 |
16,95 |
|
(NH 4 ) 2 H 2 L∙3H 2 O, вычислено |
31,58 |
7,42 |
14,73 |
(NH 4 ) 4 L, вычислено |
33,32 |
7,83 |
23,33 |
|
(NH 4 ) 2 H 2 L∙3H 2 O ( 2 ), найдено |
31,17 |
7,48 |
14,64 |
(NH 4 ) 3 HL, вычислено |
34,38 |
7,34 |
20,40 |
|
(NH 4 ) 3 HL∙H 4 L, вычислено |
37,80 |
6,52 |
15,43 |
Данные рентгенофазового анализа свидетельствовали о том, что полученная соль формировалась в одной и той же кристаллографической модификации вне зависимости от использованного растворителя, На рис. 7 представлены дифрактограммы продукта, выделенного непосредственно при синтезе из воды (кривая 1), а также после перекристаллизации его из смеси раствори- телей Н2О-МеОН (кривая 2), Дифрактограмма продукта реакции, проведенной при соотношении реагентов NH3 : H4L = 4 : 1 и измеренная сразу после синтеза, кардинальным образом отличалась от дифрактограмм, представленных на рис. 7, кривые 1,2, Однако перекристаллизация этого продукта из смеси Н2О – МеОН (соотношение 1:1), привела к тригидрату диаммонийэтилендиамин-тетраацетата (NH4)2H2L∙3H2O, о чем свидетельствовала соответствующая дифрактограмма (см. рис. 7, кривая 3).
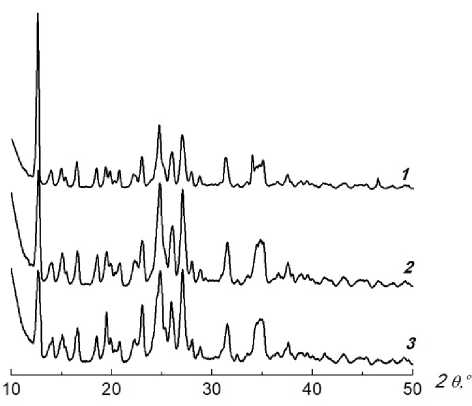
Рис. 7. РФА продуктов реакции аммиака с ЭДТА:
1 – NH 3 : H 4 L = 2 : 1, сразу после синтеза, (NH 4 ) 2 H 2 L∙3H 2 O,
2 – NH 3 : H 4 L = 2 : 1 после перекристаллизации из Н 2 О-МеОН, (NH 4 ) 2 H 2 L∙3H 2 O, 3 – NH 3 : H 4 L = 4 : 1 после перекристаллизации из Н 2 О-МеОН, (NH 4 ) 2 H 2 L∙3H 2 O
Отсутствие протекания реакции с образованием тетрааммонийной соли и неустойчивость продукта реакции с тремя эквивалентами аммония, вероятно, объясняется термодинамической устойчивостью структуры (NH 4 ) 2 H 2 L∙3H 2 O и летучестью аммиака. В присутствии воды вероятно протекание реакций с его потерей.
(NH 4 ) 4 L + 2H 2 O → (NH 4 ) 2 H 2 L + 2NH 4 ОН (NH 4 ) 3 HL + H 2 O → (NH 4 ) 2 H 2 L + NH 4 ОН NH 4 ОН → NH 3 + H 2 O
Ранее мы показали [26], что ГМТА взаимодействовал с (1-гидроксиэтилиден)дифосфоновой кислотой в метиловом спирте с образованием дигидрата гексаметилентетраминий (1-гидроксиэтилиден)дифосфоната [(CH 2 ) 6 N 4 H]+H 3 L ՛ ‒∙2H 2 O – продукта, аналогичного моногидрату гексаметилентетраминий этилендиаминтетраацетата [(CH 2 ) 6 N 4 H]+(H 3 L)‒ ∙H 2 O ( 1 ). Перекристаллизация из водного метанола привела к образованию диаммоний (1-гидроксиэтилиден)дифосфоната (NH 4 ) 2 H 2 L ՛ – продукту, аналогичному тригидрату диаммоний этилендиаминтетраацетата (NH 4 ) 2 H 2 L∙3H 2 O ( 2 ). Кислотно-основные свойства четырехосновных кислот ЭДТА и ОЭДФ вполне соизмеримы: ЭДТА, рК а 1–4 = 1,99, 2,67, 6,16, 10,26; ОЭДФ, рК а 1–4 = 1,70; 2,47; 7,28; 10,29 [51]. Большое подобие протекающих реакций с данными кислотами побудило к попытке синтеза диаммонийной соли из аммиака и ОЭДФ. В качестве метода идентификации полученных продуктов использовался рентгеновский фазовый анализ. Были выделены продукты из реакций NH3 : H4L ՛ = 2 : 1 и NH3 : H4L ՛ = 4 : 1, которые затем были перекристаллизованы из водного метанола. На рис. 8 представлены соответствующие рентгенограммы, из которых следует, что продукты реакций аммиака с ОЭДФ, произведенные в соотношениях 2:1 и 4:1, кристаллизуются в разных кристаллографических модификациях. Однако перекристаллизация продукта реакции 1:4 из водного метанола приводит к соединению, идентичному продукту реакции, проведенной в соотношении 2:1, т. е. к (NH 4 ) 2 H 2 L ՛ .
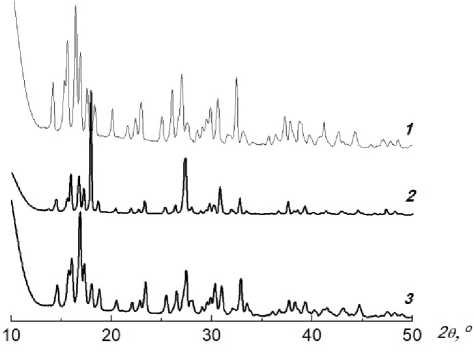
Рис. 8. РФА продуктов реакции аммиака с ОЭДФ:
1 – NH 3 : H 4 L ՛ = 2 : 1, сразу после синтеза, (NH 4 ) 2 H 2 L,
2 – NH 3 : H 4 L ՛ = 4 : 1 сразу после синтеза,
3 – NH 3 : H 4 L = 4 : 1 после перекристаллизации из Н 2 О-МеОН, (NH 4 ) 2 H 2 L ՛
Полученные данные находятся в хорошем соответствии с результатами аналогичных экспериментов, произведенных с ЭДТА и аммиаком.
Заключение
Таким образом, в результате проведенных экспериментов по взаимодействию четырехосновных кислот ЭДТА и ОЭДФ с ГМТА и водным раствором аммиака показана высокая аналогия в протекании этих реакций. В реакциях с ГМТА и в том, и в другом случае наблюдается образование ожидаемых гексаметилентетрааминиевых солей [(CH2)6N4H]+(H3L)‒∙H2O и [(CH 2 ) 6 N 4 H]+H 3 L ՛ ‒∙2H 2 O. Наряду с этим получаются диаммонийные соли (NH 4 ) 2 H 2 L∙3H 2 O и (NH 4 ) 2 H 2 L ՛ , что свидетельствует о генерировании в кислой среде аммиака из ГМТА. Диаммо-нийные соли могут быть синтезированы напрямую из кислот и водных растворов аммиака.


