Реакции хлоридов тетраорганилфосфония и тетраэтиламмония с гидратом гексахлороплатиноводородной кислоты в растворах ацетонитрила и диэтилсульфоксида
Автор: Ткачва Ална Романовна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.11, 2019 года.
Бесплатный доступ
Взаимодействием хлоридов тетраорганилфосфония и тетраэтиламмония с гидратом гексахлороплатиноводородной кислоты в растворе ацетонитрила в присутствии диэтилсульфоксида (deso), синтезированы комплексы [Ph4P][PtCl6]·CH3CN (1), [Ph3PEt][PtCl5(deso-S)] (2), [Et4N][PtCl5(deso-S)] (3). Соединения 1-3 охарактеризованы методом ИК-спектроскопии и рентгеноструктурным анализом. По данным РСА, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 QuestBruker (МоК α - излучение, λ = 0,71073 Å, графитовый монохроматор), атомы фосфора и азота в катионах комплексов 1-3 имеют искаженную тетраэдрическую конфигурацию [C52H46N2Cl6P2Pt (1), M 1168,64; сингония триклинная, группа симметрии P ; параметры ячейки: a = 10,200(10), b = 10,960(15), c = 12,160(11) Å; a = 73,65(4) град., β = 80,64(3) град., g = 77,48(4) град.; V = 1266(2) Å3; размер кристалла 0,48´0,39´0,13 мм; интервалы индексов отражений -12 ≤ h ≤ 12, -13 ≤ k ≤ 13,-15 ≤ l ≤ 15; всего отражений 27973; независимых отражений 5205; R int 0,0338; GOOF 1,028; R1 = 0,0470; wR2 = 0,1252; остаточная электронная плотность 6,33/-1,14 e/Å3, C24H30PCl5PtSO (2), M 769,85; сингония моноклинная, группа симметрии P21/n; параметры ячейки: a = 12,176(6), b = 14,522(9), c = 16,426(8) Å; a = 90,00 град., β = 95,365(16) град., g = 90,00 град.; V = 2892(3) Å3; размер кристалла 0,64´0,39´0,22 мм; интервалы индексов отражений -22 ≤ h ≤ 22, -26 ≤ k ≤ 26, -30 ≤ l ≤ 30; всего отражений 147427; независимых отражений 19324; R int 0,0674; GOOF 1,078; R 1 = 0,0642; w R 2 = 0,1019; остаточная электронная плотность 4,49/-2,72 e/Å3, C12H30NCl5PtSO (3), M 608,77; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 10,535(6), b = 15,206(7), c = 13,149(6) Å; a = 90,00 град., β = 94,12(2) град., g = 90,00 град.; V = 2101,0(19) Å3; размер кристалла 0,52 ´ 0,27 ´ 0,15 мм; интервалы индексов отражений -19 ≤ h ≤ 19, -28 ≤ k ≤ 28, -24 ≤ l ≤ 22; всего отражений 48540; независимых отражений 14161; R int 0,0537; GOOF 0,999; R 1 = 0,0447; w R 2 = 0,0648; остаточная электронная плотность 1,60/-1,26 e/Å3]. Валентные углы СРС и CNC в 1-3 составляют 107,9(3)°-113,2(3)°для 1, 108,7(2)°-111,2(3)°для 2, 108,6(2)°-111,2(2)°для 3, длины связей P-С близки между собой 1,785(6)-1,805(6) Å в 1; 1,789(4)-1,801(5) Å в 2, как и расстояния N-C 1,515(4)-1,524(4) Å в 3. В кристалле сольвата 1 в октаэдрических анионах [PtCl6]2- транс -углы ClPtCl равны 180,0º, длины связей 2,308(2)-2,327(3) Å. В несколько искаженных диэтилсульфоксидопентахлорплатинатных октаэдрических анионах [PtCl5(dmso-S)]- комплексов 2, 3 транс -углы SPtCl 175,12(5)°-176,23(3)°, транс -углы СlPtCl 177,12(3)-178,45(3)°, расстояния Pt-Cl и Pt-S2,3156(14)-2,3379(14) и 2,3363(14) в 1, 2,3219(12)-2,3459(12) и 2,3424(12) в 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1865783 для 1, 1854655 для 2,1854649 для 3, deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Этилтрифенилфосфоний хлорид, тетраэтиламмоний хлорид, тетрафенилфосфоний хлорид, ацетонитрил, диэтилсульфоксид, гексахлороплатиноводородная кислота, диэтилсульфоксидопентахлорплатинат-анион, рентгено, структурный анализ
Короткий адрес: https://sciup.org/147233114
IDR: 147233114 | УДК: 546.39+546.185+546.924+547.53.024+548.312.2 | DOI: 10.14529/chem190103
Reactions of tetraorganylphosphonium and tetraethylammonium chloride with hexachloroplatinic acid hexahydrate in solutions of acetonitrile and diethylsulphoxide
The interaction of hexachloroplatinic acid with tetraorganylphosphonium, tetraethylammonium chlorides in solutions of acetonitrile in the presence of diethylsulphoxide (deso) synthesized the following complexes: [Ph4P][PtCl6]·CH3CN (1), [Ph3PEt][PtCl5(deso-S)] (2), [Et4N][PtCl5(deso-S)] (3). The structures 1-3 were determined by XRDA and IR. The X-ray diffraction patterns of crystals 1-3 were obtained at 293 K on an automatic diffractometer D8 Quest Broker (MoK α radiation, λ = 0.71073 Å, graphite monochromator) the phosphorus and nitrogen atoms of complexes 1-3 have a distorted tetrahedral configuration in the cations. [C52H46N2Cl6P2Pt](1), M 1168.64; the triclinic syngony, the symmetry group P ; cell parameters: a = 10.200(10), b = 10.960(15), c = 12.160(11) Å; a = 73.65(4) degrees, β = 80.64(3) degrees, g = 77.48(4) degrees; V = 1266(2) Å3; the crystal size is 0.48´0.39´0.13 mm; intervals of reflection indexes -12 ≤ h ≤ 12, -13 ≤ k ≤ 13, -15 ≤ l ≤ 15; total reflections 27973; independent disclosures 5205; R int 0.0338; GOOF 1.028; R 1 = 0.0470; w R 2 = 0.1252; residual electron density 6.33/-1.14 e/Å3, C24H30PCl5PtSO (2), M 769.85; the monoclinic syngony, the symmetry group P21/n; cell parameters: a = 12.176(6), b = 14.522(9), c = 16.426(8) Å; a = 90.00 degrees, β = 95.365(16)degrees, g = 90.00 degrees; V = 2892(3) Å3; the crystal size is 0.64´0.39´0.22 mm; intervals of reflection indexes -22 ≤ h ≤ 22, -26 ≤ k ≤ 26,-30 ≤ l ≤ 30; total reflections 147427; independent disclosures 19324; R int 0.0674; GOOF 1.078; R 1 = 0.0642; w R 2 = 0.1019; residual electron density 4.49/-2.72 e/Å3, C12H30NCl5PtSO (3), M 608.77; the monoclinic syngony, the symmetry group P21/c; cell parameters: a = 10.535(6), b = 15.206(7), c = 13.149(6) Å; a = 90.00 degrees, β = 94.12(2) degrees, g = 90.00 degrees; V = 2101.0(19) Å3; the crystal size is 0.52´0.27´0.15 mm; intervals of reflection indexes -19 ≤ h ≤ 19, -28 ≤ k ≤ 28, -24 ≤ l ≤ 22; total reflections 48540; independent disclosures 14161; R int 0.0537; GOOF 0.999; R 1 = 0.0447; wR2 = 0.0648; residual electron density 1,60/-1,26 e/Å3]. The СРС and CNC valence angles are 107.9(3)°-113.2(3)° for 1, 108.7(2)°-111.2(3)° for 2, 108.6(2)°-111.2(2)° for 3, distance P-С 1.785(6)-1.805(6) Å in 1; 1.789(4)-1.801(5) Å in 2, and distance N-C 1.515(4)-1.524(4) Å in 3. In octahedral anions [PtCl6]2- trans-angles ClPtCl equal 180.0º, distance 2.308(2)-2.327(3) Å in a crystal solvate. In the [PtCl5(dmso-S)]- anions of complexes 2, 3 the SPtCl trans-angles are 175.12(5)°-176.23(3)°, the СlPtCl trans-angles equal 177.12(3)°-178.45(3)°, the distances Pt-Cl and Pt-S are 2.3156(14)-2.3379(14) and 2.3363(14) in 1, 2.3219(12)-2.3459(12) and 2.3424(12) in 2. Complete tables of coordinates of atoms, bond lengths and valence angles are deposited at the Cambridge Structural Data (No. 1865783 for 1, 1854655 for 2, 1854649 for 3, deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Текст научной статьи Реакции хлоридов тетраорганилфосфония и тетраэтиламмония с гидратом гексахлороплатиноводородной кислоты в растворах ацетонитрила и диэтилсульфоксида
Взаимодействием хлоридов тетраорганилфосфония и тетраэтиламмония с гидратом гексахлороплатиноводородной кислоты в растворе ацетонитрила в присутствии диэтилсульфоксида (deso), синтезированы комплексы [Ph4P][PtCl6]·CH3CN (1), [Ph3PEt][PtCl5(deso-S)] (2), [Et4N][PtCl5(deso-S)] (3). Соединения 1-3 охарактеризованы методом ИК-спектроскопии и рентгеноструктурным анализом. По данным РСА, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 QuestBruker (МоКα-излучение, λ = 0,71073 Å, графитовый монохроматор), атомы фосфора и азота в катионах комплексов 1–3 имеют искаженную тетраэдрическую конфигурацию [C52H46N2Cl6P2Pt (1), M 1168,64; сингония триклинная, группа симметрии P 1 ; параметры ячейки: a = 10,200(10), b = 10,960(15), c = 12,160(11) A; a = 73,65(4) град., в = 80,64(3) град., у = 77,48(4) град.; V = 1266(2) A3; размер кристалла 0,48x0,39x0,13 мм; интервалы индексов отражений -12 < h < 12, -13 < к < 13,-15 < l < 15; всего отражений 27973; независимых отражений 5205; Rint 0,0338; GOOF 1,028; R1 = 0,0470; wR2 = 0,1252; остаточная электронная плотность 6,33/-1,14 e/A3, C24H30PCl5PtSO (2), M 769,85; сингония моноклинная, группа симметрии P21/n; параметры ячейки: a = 12,176(6), b = 14,522(9), c = 16,426(8) A; a = 90,00 град., в = 95,3 65(16) град., у = 90,00 град.; V = 2892(3) A3; размер кристалла 0,64x0,39x0,22 мм; интервалы индексов отражений -22 < h < 22, -26 < к < 26, -30 < l < 30; всего отражений 147427; независимых отражений 19324; Rint 0,0674; GOOF 1,078; R1 = 0,0642; wR2 = 0,1019; остаточная электронная плотность 4,49/-2,72 e/A3, C12H30NCl5PtSO (3), M 608,77; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 10,535(6), b = 15,206(7), c = 13,149(6) A; a = 90,00 град., в = 94,12(2) град., у = 90,00 град.; V = 2101,0(19) A3; размер кристалла 0,52 x 0,27 x 0,15 мм; интервалы индексов отражений -19 < h < 19, -28 < к < 28, -24 < l < 22; всего отражений 48540; независимых отражений 14161; Rint 0,0537; GOOF 0,999; R1 = 0,0447; wR2 = 0,0648; остаточная электронная плотность 1,60/-1,26 e/A3]. Валентные углы СРС и CNC в 1-3 составляют 107,9(3)°-113,2(3)°для 1, 108,7(2)°-111,2(3)°для 2, 108,6(2)°-111,2(2)°для 3, длины связей P-С близки между собой 1,785(6)-1,805(6) A в 1; 1,789(4)-1,801(5) A в 2, как и расстояния N-C 1,515(4)-1,524(4) A в 3. В кристалле сольвата 1 в октаэдрических анионах [PtCl6]2- транс-углы ClPtCl равны 180,0º, длины связей 2,308(2)–2,327(3) Å. В несколько искаженных диэтил-сульфоксидопентахлорплатинатных октаэдрических анионах [PtCl5(dmso-S)]– комплексов 2,3 транс-углы SPtCl 175,12(5)°-176,23(3)°, транс-углы ClPtCl 177,12(3)-178,45(3)°, расстояния Pt-Cl и Pt-S2,3156(14)-2,3379(14) и 2,3363(14) в 1, 2,3219(12)-2,3459(12) и 2,3424(12) в 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1865783 для 1, 1854655 для 2,1854649 для 3, ; .
Комплексные соединения платины являются эффективными катализаторами многих химических процессов и удобными объектами для изучения реакций лигандного обмена. Особое внимание привлекают комплексы платины, имеющие в своём составе P, N-бидентатные системы. Эти координационные соединения зарекомендовали себя эффективными катализаторами ряда практически значимых процессов, например, гидрирования, гидроформилирования, гидросилилирования С=O и С=С связей, гидроборирования, аллильного алкилирования, кросс-сочетания [1–3]. Например, окисление алкинов кислородом воздуха по тройной связи до дикарбонильных соединений происходит в присутствии комплексов платины [4]. Обладая свойствами мягкого и жёсткого оснований, P, N-бидентатные лиганды способны к направленной организации координационной сферы металла, построению биметаллических и полиядерных систем [1]. Интерес к органическим диалкилсульфоксидам во многом определяется той ролью, которую они играют в химии как лиганды, реагенты и растворители [5, 6]. Диалкилсульфоксиды обладают способностью образовывать прочные комплексы с платиной. Как известно, при координации свойства лигандов значительно изменяются, и изучение реакционной способности координированных сульфоксидов, несомненно является актуальной задачей [7–10].
Реакции лигандного обмена хлоридов органилтрифенилфосфония с тетрахлороплатинатом или гексабромоплатинатом калия в диметилсульфоксиде приводят к замещению одного из атомов хлора на молекулу S-координированного диметилсульфоксида [11 - 13]. Также известны диэтилсульфоксидные комплексы платины(II) в литературе [14, 15], однако к настоящему времени практически не исследованы диэтилсульфоксидные комплексы платины(IV). Ранее мы установили, что реакция хлорида 2-бутенил- бис (трифенилфосфония) с гексахлороплатиновой кислотой в присутствии диэтилсульфоксида и триэтиламина приводит к образованию комплекса цис- [PtCl2(SOEt2)(PPh3)]. В продолжение исследования в этом направлении мы изучили взаимодействие хлоридов тетраорганилфосфония и тетраэтиламмония с гидратом гексахлороплатиноводородной кислоты (1:1) в растворе ацетонитрила в присутствии диэтилсульфоксида.
Экспериментальная часть
Синтез [Ph 4 P][PtCl 6 ]∙CH 3 CN (1). Раствор 0,037 г (0,1 ммоль) хлорида тетраэтилфосфония в 4 мл ацетонитрила приливали к раствору 0,05 г (0,1 ммоль) гексагидрата гексахлороплатиноводородной кислоты в 4 мл ацетонитрила. К полученной смеси добавляли 0,2 мл диэтилсульфоксида. Раствор концентрировали до объема 0,5 мл, образовавшиеся кристаллы фильтровали и сушили. Выход комплекса 1 0,030 г (76 %), оранжевые кристаллы, т. пл. 178 °С (с разл.). ИК-спектр, ν , см–1: 3060, 2976, 2360, 2255, 1829, 1584, 1482, 1437, 1403, 1377, 1314, 1254, 1189, 1165, 1108, 1027, 995, 935, 760, 720, 689, 613, 527. Найдено, %: С 37,58; Н 3,12. C 24 H 23 PCl 6 PtN. Вычислено, %: С 37,69; Н 3,01.
Синтез [Ph 3 PC 2 H 5 ][(PtCl 5 (deso- S )] (2). Раствор 0,033 г (0,1 ммоль) хлорида этилтрифенилфосфония в 4 мл ацетонитрила приливали к раствору 0,05 г (0,1 ммоль) гексагидратагексахлороплатиноводородной кислоты в 4 мл ацетонитрила. К полученной смеси добавляли 0,2 мл диэтилсульфоксида. Раствор концентрировали до объема 0,5 мл, образовавшиеся кристаллы фильтровали и сушили. Выход комплекса 2 0,069 г (86 %), желто-оранжевые кристаллы, т. пл. 164 ° С. ИК-спектр, ν , см–1: 3086, 3055,2981, 2950, 2908, 2360, 1976, 1586, 1484, 1432, 1392, 1380, 1319, 1262, 1189, 1160, 1140, 1071, 1032, 995, 977, 938, 754, 736, 718, 689, 530, 503, 490. Найдено, %: С 35,53; Н 3,84. C 24 H 30 PCl 5 PtSO. Вычислено, %: С 35,69; Н 3,72.
Аналогично синтезировали [(C 2 H 5 ) 4 N][PtCl 5 (deso- S )] (3). Выход 93 %, оранжевые кристаллы, т. пл. 151 °С. ИК-спектр, ν , см–1: 2987, 2940, 2908, 1717, 1654, 1557, 1455, 1406, 1374, 1309, 1280, 1183, 1144, 1068, 1003, 966, 783, 765, 700, 485. Найдено, %: С 23,57; Н 4,99. C 12 H 30 NCl 5 PtSO. Вычислено, %: С 23,66; Н 4,93.
ИК-спектры соединений 1 – 3 записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S; образцы готовили таблетированием с KBr (область поглощения 4000 - 400 см - 1).
Рентгеноструктурный анализ (РСА) кристаллов 1 – 3 проводили на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (MoK α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [16]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [17], OLEX2 [18]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структур приведены в табл. 1, основные длины связей и валентные
углы – в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1865783 для 1; 1854655 для 2,1854649 для 3, ; .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
1 |
2 |
3 |
|
М |
1168,64 |
769,85 |
608,77 |
|
Сингония |
Триклинная |
Моноклинная |
Моноклинная |
|
Пр. группа |
P 1 |
P2 1 /n |
P2 1 /c |
|
a , Å |
10,200(10) |
12,176(6) |
10,535(6) |
|
b , Å |
10,960(15) |
14,522(9) |
15,206(7) |
|
c, Å |
12,160(11) |
16,426(8) |
13,149(6) |
|
α , град. |
73,65(4) |
90,00 |
90,00 |
|
β, град. |
80,64(3) |
95,365(16) |
94,12(2) |
|
γ , град. |
77,48(4) |
90,00 |
90,00 |
|
V , Å3 |
1266(2) |
2892(3) |
2101,0(19) |
|
Z |
1 |
4 |
4 |
|
ρ (выч,), г/см3 |
1,533 |
1,768 |
1,925 |
|
- 1 µ , мм |
3,188 |
5,459 |
7,412 |
|
F (000) |
582,0 |
1504,0 |
1184,0 |
|
Размер кристалла, мм |
0,48 × 0,39 × 0,13 |
0,64 × 0,39 × 0,22 |
0,52 × 0,27 × 0,15 |
|
Область сбора данных по θ , град |
5,7 - 52,92 |
5,72 - 82,64 |
5,8 - 84,36 |
|
Интервалы индексов отражений |
–2 ≤ h ≤ 12, –13 ≤ k ≤ 13, –15 ≤ l ≤ 15 |
–22 ≤ h ≤ 22, –26 ≤ k ≤ 26, –30 ≤ l ≤ 30 |
–19 ≤ h ≤ 19, –28 ≤ k ≤ 28, –24 ≤ l ≤ 22 |
|
Измерено отражений |
27973 |
147427 |
48540 |
|
R int |
0,0338 |
0,0674 |
0,0537 |
|
Независимых отражений |
5205 |
19324 |
14161 |
|
Переменных уточнения |
287 |
302 |
197 |
|
GOOF |
1,028 |
1,078 |
0,999 |
|
R -факторы по F 2> 2 σ ( F 2) |
R 1 = 0,0470, wR 2 = 0,1252 |
R 1 = 0,0642, wR 2 = 0,1019 |
R 1 = 0,0447, wR 2 = 0,0648 |
|
R -факторы по всем отражениям |
R 1 = 0,0474, wR 2 = 0,1258 |
R 1 = 0,1224, wR 2 = 0,1197 |
R 1 = 0,1117, wR 2 = 0,0773 |
|
Остаточная электронная плотность (min/max), e/A3 |
6,33/–1,14 |
4,49/–2,72 |
1,60/–1,26 |
Таблица 2
Длины связей ( d ) и валентные углы ( ω ) в структурах 1 - 3
|
Связ |
ь, d, Å \ |
Угол, ω , |
град |
|
1 |
|||
|
Pt(1) - Cl(1) |
2,308(2) |
Cl(1)Pt(1)Cl(3) |
90,89(9) |
|
Pt(1) - Cl(3) |
2,319(2) |
Cl(1)Pt(1)Cl(1') |
180,0 |
|
Pt(1) - Cl(2) |
2,327(3) |
Cl(1)Pt(1)Cl(2) |
90,22(11) |
|
P(1) - C(11) |
1,805(6) |
Cl(3)Pt(1)Cl(3') |
179,999(1) |
|
P(1) - C(31) |
1,800(6) |
Cl(2)Pt(1)Cl(2') |
180,0 |
|
P(1) - C(1) |
1,802(6) |
Cl(1')Pt(1)Cl(2) |
89,78(11) |
|
P(1) - C(21) |
1,785(6) |
Cl(1)Pt(1)Cl(3') |
89,11(9) |
|
C(31)P(1)C(11) |
113,2(3) |
||
|
C(1)P(1)C(11) |
107,9(3) |
||
|
C(1)P(1)C(31) |
109,1(3) |
||
|
2 |
|||
|
Pt(1) - Cl(1) |
2,3156(14) |
Cl(1)Pt(1)Cl(5) |
89,54(5) |
|
Pt(1) - Cl(2) |
2,3164(14) |
Cl(1)Pt(1)Cl(3) |
91,14(5) |
|
Pt(1) - Cl(3) |
2,3285(14) |
Cl(1)Pt(1)Cl(2) |
178,68(5) |
Окончание табл. 2
|
Связь, d, Å |
Угол, ω , град |
||
|
Pt(1) - Cl(4) |
2,3226(14) |
Cl(1)Pt(1)Cl(4) |
90,02(5) |
|
Pt(1) - Cl(5) |
2,3379(14) |
Cl(3)Pt(1)Cl(4) |
178,02(5) |
|
Pt(1) - S(1) |
2,3363(14) |
S(1)Pt(1)Cl(1) |
85,59(5) |
|
S(1) - O(1) |
1,455(3) |
S(1)Pt(1)Cl(5) |
175,12(5) |
|
S(1) - C(17) |
1,765(6) |
S(1)Pt(1)Cl(4) |
89,52(6) |
|
S(1) - C(19) |
1,834(6) |
O(1)S(1)Pt(1) |
114,33(17) |
|
P(1) - C(21) |
1,795(5) |
O(1)S(1)C(17) |
108,8(3) |
|
P(1) - C(11) |
1,789(4) |
O(1)S(1)C(19) |
109,4(3) |
|
P(1) - C(7) |
1,801(5) |
C(17)S(1)Pt(1) |
113,0(2) |
|
P(1) - C(1) |
1,791(5) |
C(19)S(1)Pt(1) |
108,1(2) |
|
C(17) - C(18) |
1,505(9) |
C(7)S(1)C(8) |
102,5(3) |
|
C(19) - C(20) |
1,455(10) |
C(21)P(1)C(7) |
111,2(3) |
|
C(1)P(1)C(21) |
109,3(2) |
||
|
C(1)P(1)C(7) |
108,7(2) |
||
|
3 |
|||
|
Pt(1) - Cl(1) |
2,3219(12) |
Cl(1)Pt(1)Cl(4) |
89,00(4) |
|
Pt(1) - Cl(2) |
2,3305(12) |
Cl(1)Pt(1)Cl(5) |
90,48(3) |
|
Pt(1) - Cl(3) |
2,3414(14) |
Cl(1)Pt(1)Cl(2) |
178,45(3) |
|
Pt(1) - Cl(4) |
2,3235(14) |
Cl(1)Pt(1)Cl(3) |
89,76(4) |
|
Pt(1) - Cl(5) |
2,3459(12) |
Cl(4)Pt(1)Cl(3) |
177,12(3) |
|
Pt(1) - S(1) |
2,3424(12) |
S(1)Pt(1)Cl(1) |
93,00(3) |
|
N(1) - C(7) |
1,517(4) |
S(1)Pt(1)Cl(5) |
176,23(3) |
|
N(1) - C(1) |
1,521(4) |
S(1)Pt(1)Cl(5) |
90,24(4) |
|
N(1) - C(5) |
1,524(4) |
O(1)S(1)Pt(1) |
113,27(11) |
|
N(1) - C(3) |
1,515(4) |
O(1)S(1)C(9) |
109,93(16) |
|
S(1) - O(1) |
1,465(2) |
O(1)S(1)C(11) |
107,26(17) |
|
S(1) - C(11) |
1,792(3) |
C(11)S(1)Pt(1) |
113,04(12) |
|
S(1) - C(9) |
1,789(3) |
C(9)S(1)Pt(1) |
108,78(11) |
|
C(9) - C(10) |
1,520(4) |
C(9)S(1)C(11) |
104,14(16) |
|
C11 - C12 |
1,503(5) |
C(7)N(1)C(1) |
111,2(2) |
|
C(1)N(1)C(5) |
108,6(2) |
||
|
C(3)N(1)C(7) |
108,7(2) |
||
Обсуждение результатов
Синтез сольватного комплекса гексахлороплатината тетрафенилфосфония ( 1 ) осуществляли взаимодействием хлорида тетрафенилфосфония с гексахлороплатиновой кислотой в присутствии диэтилсульфоксида в ацетонитриле (мольное соотношение исходных реагентов 1:1:2) с выходом 76 %:
deso
[Ph 4 P]Cl+ H 2 [PtСl 6 ] → [Ph 4 P][PtCl 6 ]·CH 3 CN + 2 HCl.
Мы установили, что взаимодействие хлоридов этилтрифенилфосфония и тетраэтиламмония с гексахлороплатиноводородной кислотой в аналогичных условиях сопровождается образованием диэтилсульфоксидопентахлорплатинатов этилтрифенилфосфония ( 2 ) и тетраэтиламмония ( 3 ), в которых наблюдается замещение атома хлора в анионе [PtCl 6 ]2– на молекулу S -координированного диэтилсульфоксида:
deso
[Ph 3 PEt]Cl + H 2 [PtСl 6 ] → [Ph 3 PEt][PtCl 5 (deso- S )] + 2 HCl.
deso
[Et 4 N]Cl + H 2 [PtCl 6 ] ^ [Et 4 N][PtCl 5 (deso- 5 )] + 2 HCl.
Комплексы 2 и 3 представляют собой оранжевые кристаллы, которые выделяли из реакционной смеси с выходом 86 и 93 % соответственно.
Методом рентгеноструктурного анализа установлено строение комплексов 1 - 3 . По данным РСА, атомы фосфора и азота в катионах комплексов 1, 2, 3 имеют искаженную тетраэдрическую конфигурацию (рис. 1-3). Значения валентных углов СРС и CNC в 1 - 3 приближаются к идеальному значению (107,9(3) °- 113,2(3) ° для 1 , 108,7(2) °- 111,2(3) ° для 2 , 108,6(2) °- 111,2(2) ° для 3 ). Расстояния P - С близки между собой (1,785(6) - 1,805(6) А в 1 ; 1,789(4) - 1,801(5) А в 2 ), как и расстояния N - C(1,515(4) - 1,524(4) А в 3 ). В кристалле сольвата 1 в центросимметричных октаэдрических анионах [PtCl 6 ]2- транс -углы ClPtCl равны 180,0°. Длины связей Pt - Cl в анионах [PtCl 6 ]2-2,308(2)-2,327(3) Å.В несколько искаженных октаэдрических анионах [PtCl 5 (dmso-S)]– комплексов 2,3 транс -углы SPtCl изменяются в интервалах 175,12(5) - 176,23(3) ° , транс -углы ClPtCl 177,12(3) - 178,45(3) ° приближаются к 180 ° , расстояния Pt - Cl и Pt - S (2,3156(14) - 2,3379(14) и 2,3363(14) в 2 , 2,3219(12) - 2,3459(12) и 2,3424(12)) в 3 близки к суммам ковалентных радиусов указанных атомов 2,35 и 2,31 Å [18].
ОД
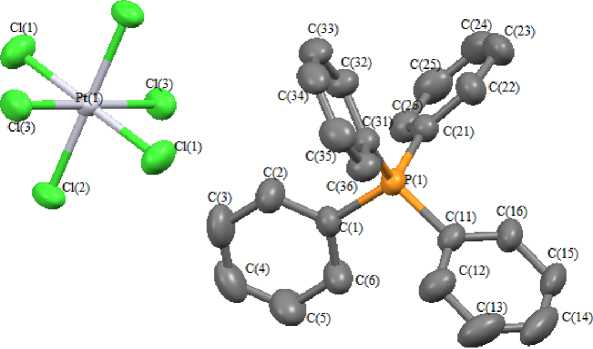
Рис. 1. Строение комплекса 1 (структура комплекса без молекулы растворителя)
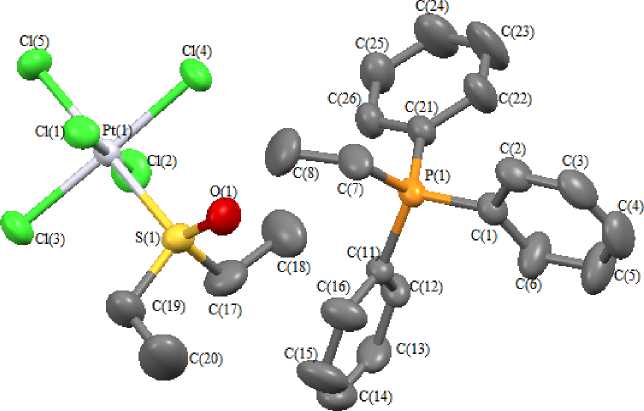
Рис. 2. Строение комплекса 2
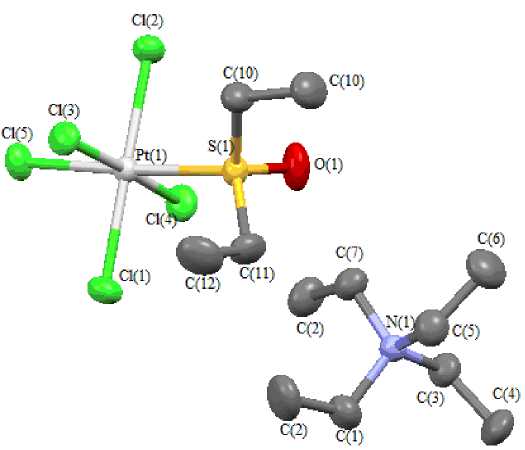
Рис. 3. Строение комплекса 3
Геометрия координированного диэтилсульфоксидного лиганда отлична от геометрии свободной молекулы диэтилсульфоксида [19 - 23]. Так, углы OSC равны 108,8(3) ° , 109,4(3) ° в 2 , 107,26(17) ° , 109,93(16) ° в 3 , в свободной молекуле диэтилсульфоксида аналогичные углы составляют 106,7(4)°, 106,8(4) ° . Углы CSC (102,5(3) ° в 2 , 104,14(16) ° в 3 ) также отличаются от значения этого угла в свободной молекуле 97,4°. Длины связей S–C (1,765(6), 1,834(6) Å в 2 , 1,792(3), 1,789(3) Å в 3 ) сопоставимы со значениями, наблюдаемые в свободной молекуле диэтилсульфоксида (1,795(5), 1,795(5) Å). Значения длин связей S–O в координированной молекуле диэтилсульфоксида (1,455(3) Å в 2 , 1,465(2) Å в 3 ) несколько меньше, чем в свободной молекуле диэтилсульфоксида (1,496(14) Å). Длины связей С–С в анионах составляют (1,505(9), 1,455(10) Å в 2 и 1,520(4), 1,503(5) Å в 3 ) близки по значению к аналогичным расстояниям в свободной молекуле (1,47(8) Å). В ИК-спектрах соединений 2, 3 наблюдается гипсохромный сдвиг сульфоксидной группы S=O(1140 ( 2 ) и 1144 ( 3 ) вместо 1050 см–1 в свободном лиганде), что свидетельствует о координации атома серы диэтилсульфоксидного лиганда на атом платины.
Выводы
Таким образом, взаимодействие хлоридов этилтрифенилфосфония и тетраэтиламмония с гидратом гексахлороплатиноводородной кислотой в растворе ацетонитрила с добавлением диэтилсульфоксида протекает с заменой одного из атомов хлора на диэтилсульфоксидный лиганд, в то время как продуктом подобной реакции с хлоридом тетрафенилфосфония является гексахлороплатинат тетрафенилфосфония.
Выражаю благодарность проф. В.В. Шарутину за проведенные рентгеноструктурные исследования.
Список литературы Реакции хлоридов тетраорганилфосфония и тетраэтиламмония с гидратом гексахлороплатиноводородной кислоты в растворах ацетонитрила и диэтилсульфоксида
- Салищева, О.В. Синтез комплексов платины (II) с аминокислотами / О.В. Салищева, Н.Е. Молдагулова // Успехи в химии и химической технологии. - 2008. - Т. 22, № 3. - С. 6-8.
- Cotton, F. Sulfoxides as Ligands. I. A Preliminary Survey of Methyl Sulfoxide Complexes / F. Cotton, R. Francis // J. Am. Chem. Soc. - 1960. - V. 82. - P. 2986-2091. DOI: 10.1021/ja01497a003
- Meek, D. Transition Metal Ion Complexes of Dimethyl Sulfoxide / D. Meek, D. Straub, R. Drago // J. Am. Chem. Soc. - 1960. - V. 82. - P. 6013-6016. DOI: 10.1021/ja01508a012
- Sharutin, V.V. Interaction of Diphenylacetylene with Platinum Diiodide in Dimethyl Sulfoxide in the Presence of Oxygen / V.V. Sharutin, O.K. Sharutina, V.S. Senchurin // Butlerov com. - 2013. - V. 36, № 11. - P. 98-99. DOI: jbc-01/13-36-11-98.
- Кукушкин, Ю.Н. О трансвлиянии диметилсульфоксида в комплексных соединениях платны(II) / Ю.H. Кукушкин, Ю.E. Вязьменский, Л.И. Зорина // Журн. неорган. хим. - 1968. - Т. 13, № 11. - С. 3052-3058.
- Кукушкин, Ю.Н. Новые дезоксигенирующие реагенты для диметилсульфоксидных комплексов платины / Ю.Н. Кукушкин, З.А. Хроменкова // Журн. общей химии. - 1996. - Т. 66, № 10. - С. 1752-1759.
- Спевак, В.Н. Синтез и исследование комплексных соединений платины с органическими сульфоксидами: автореф. дис.. канд. хим. наук / В.Н. Спевак. - М.: Изд-во МГУ, 1971. - 25 с.
- Кукушкин, Ю.Н. Вклад исследований диметилсульфоксидных комплексов в теории координационной химии / Ю.Н. Кукушкин // Коорд. хим. - 1997. - Т. 23, № 3. - С. 163-174.
- Кукушкин, Ю.Н. Различное поведение диметилсульфоксидной группы в комплексах платины(II) и (IV) по отношению к PCl3 / Ю.Н. Кукушкин, З.А. Хроменкова, В.А. Эсаулова // Журн. общей хим. - 1994. - Т. 64, № 9. - С. 1554-1558.
- Кукушкин, В.Ю. Дезоксигенирование диметилсульфоксида в комплексах платины / В.Ю. Кукушкин, Е.Ю. Панькова // Журн. общей хим. - 1987. - Т. 57, № 10. - С. 2391-2392.
- Синтез и строение комплексов платины с хлоридами органилтрифенилфосфонием и ДМСО / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журнал общей химии. - 2018. - Т. 88, № 7. - С. 80-86.
- Synthesis and Structure of Platinum Complexes [Ph4P] [PtCl3(DMSO)]-and [Ph4P] [PtCl5(DMSO)]-/ V.V. Sharutin, V.S. Senchurin, O.K. Sharutina et al. // Russ. J. Inorg. Chem. - 2013. -V. 58, N 1. - P. 33-38.
- DOI: 10.1134/S0036023613010191
- Synthesis and Structure of the Platinum Complexes [Bu4N] [PtBr5(DMSO)]-, [Ph4P] [PtBr5(DMSO)]-, and [Ph3(n_Am)P] [PtBr5(DMSO)]- /V.V. Sharutin, V.S. Senchurin, O.K. Sharutina et al. // Russ. J. Coord. Chem. - 2011. - V. 37, № 11. - P. 854-861.
- DOI: 10.1134/S1070328411100113
- X-ray Structure Determination of Cis-dibromo(dimethyl sulfoxide)(acetonitrile)platinum(II) / V.Yu. Kukushkin, V.K. Belsky, V.E. Konovalov, R.R. Shifrina, A.I. Moiseev, R.A. Vlasova // lnorg. Chim. Acta. - 1991. - V. 183. - P. 57-61.
- Amico, D. Antiproliferative Activity of Platinum(II) Complexes Containing Triphenylphosphine: Correlation Between Structure and Biological Activity / D. Amico, L. Via, A. García-Argáez // J. Polyhedron. - 2015. - V. 85. - P. 685-689. 10.1016@j.poly.2014.10.001.
- DOI: 10.1016/j.po1y.2014.10.001
- Bruker. SMART and SAINT-Plus Data Collection and Processing Software for the SMART System Versions 5.0, Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data Versions 5.10, Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov, O.V. OLEX2: a Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea // J. Appl. Cryst. - 2009. - V. 42. - P. 339-341.
- DOI: 10.1107/S0021889808042726
- Бацанов, С.С. Атомные радиусы элементов / С.С. Бацанов // Журн. неорган. химии. - 1991. - Т. 36, № 12. - С. 3015-3037.
- Thomas, R. The Molecular and Crystal Structure of Dimethylsulfoxide, (H3C)2SO / R. Thomas, C.B. Shoemaker, K. Eriks // ActaCryst. - 1966. - V. 21, № 1. - P. 12-20.
- DOI: 10.1107/S0365110X66002263
- Calligaris, M. Structure and Bonding in Metal Sulfoxide Complexes / M. Calligaris, O. Carugo // Coord. Chem. Rev. - 1996. - V. 153. - P. 83-154.
- DOI: 10.1016/0010-8545(95)01193-5
- Calligaris, M. Stereochemical Aspects of Sulfoxides and Metal Sulfoxide Complexes / M.Calligaris // Croatica Chemica Acta. - 1999. - V. 72, № 3. - P. 147-169.
- Calligaris, M. Structure and Bonding in Metal Sulfoxide Complexes: an update / M. Calligaris // Coord. Chem. Rev. - 2004. - V. 248, № 4. - P. 351-375.
- DOI: 10.1016/j.ccr.2004.02.005


