Реакции пентафенилфосфора с 2,6-дигидроксибензойной и янтарной кислотами
Автор: Шарутина Ольга Константиновна, Губанова Юлия Олеговна, Рыбакова Анастасия Владимировна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.11, 2019 года.
Бесплатный доступ
Взаимодействием пентафенилфосфора с 2,6-дигидроксибензойной и янтарной кислотами (мольное соотношение 2:1 и 1:1) в растворе ароматического углеводорода (бензол или толуол, запаянная ампула, 0,5 часа, 60 °С) синтезированы карбоксилаты тетрафенилфосфония в форме сольватов с растворителем [Ph4P]+ [OC(O)C6H3(OH)2-2,6]- × PhH (1) и [Ph4P]2+ [O2CCH2CH2CO2]2- × TolH (2). Соединения охарактеризованы методами ИК-спектроскопии и РСА. По данным РСА, кристаллы карбоксилатов тетрафенилфосфония 1 и 2 сформированы из тетраэдрических катионов [Ph4P]+ (углы СРС 106,4(3)°-113,5(3)° (1), 107,8(2)°-111,5(2)° (2), расстояния Р-C 1,771(6)-1,809(6) Å в 1, 1,791(4)-1,804(4) Å в 2), однозарядных (1) или двухзарядных (2) карбоксилатных анионов и молекул сольватного арена. В кристалле соединения 1 присутствуют по два типа кристаллографически независимых катионов и анионов ( а, б ). Анионы в соединении 2 центросимметричны. В карбоксилат-анионах связи С-О выровнены (1,263(9), 1,273(9) Å 1 а, 1,24(1), 1,257(9) Å 1 б, 1,254(6), 1,272(5) Å 2), углы при карбоксильном атоме углерода ОСО близки к теоретическому значению 120°. В анионах 1 имеют место внутримолекулярные водородные связи О-Н∙∙∙О-С между атомами кислорода карбоксильной группы и орто- гидроксильными группами (расстояния Н∙∙∙О 1,73-2,03 Å, О∙∙∙О 2,450(8)-2,484(8) Å). Структурная организация в кристаллах обусловлена слабыми водородными связями типа С-Н···О с участием карбоксилатных групп и атомов кислорода гидроксильных групп (в кристалле 1). В комплексе 2 наблюдаются короткие контакты карбоксилатных атомов кислорода с атомом водорода метильной группы сольватированной молекулы толуола.
Пентафенилфосфор, 6-диоксибензойная, янтарная кислота, карбоксилаты тетрафенилфосфония, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147233120
IDR: 147233120 | УДК: 546.185+547.29+547.46+547.53.024+548.312.2 | DOI: 10.14529/chem190108
Reactions of pentaphenylphosphorus with 2,6-dihydroxybenzoic and succinic acid
Tetraphenylphosphonium carboxylates as solvates of [Ph4P]+[OC(O)C6H3(OH)2-2,6]-×PhH (1) and [Ph4P]2+[O2CCH2CH2CO2]2-×TolH (2) types were synthesized by the reactions of pentaphenylphosphorus with 2,6-dihydroxybenzoic and succinic acids at the mole ratio of 2:1 and 1:1, respectively. The reactions were accomplished by heating the benzene or toluene solutions of the mixture of compounds inside an evacuated glass ampoule at 60 °С for 0.5 hour. The structure of compounds was characterized by IR spectroscopy and single-crystal X-ray diffraction study. According to X-ray diffraction data, the crystals of tetraphenylphosphonium carboxylates 1 and 2 consist of the [Ph4P]+ tetrahedral cations (the СРС angles are 106.4(3)-113.5(3)° (1), 107.8(2)-111.5(2)° (2), and the P-C bond lengths are 1.771(6)-1.809(6) Å (1), 1.791(4)-1.804(4) Å (2)), single charged (1) or double charged (2) carboxylate anions and solvate arene molecules. Two types of crystallographically independent cations and anions ( a, b ) exist in crystals 1. Anions of the compound 2 are centrosymmetric. In the carboxylate anions the C-O bonds are aligned (1.263(9), 1.273(9) Å 1 а, 1.24(1), 1.257(9) Å 1 b, 1.254(6), 1.272(5) Å 2), and the OCO angles at the carboxyl carbon atom are close to the theoretical value of 120°. The anions 1 are characterized by the presence of intermolecular short contacts О-Н∙∙∙О-С between oxygen atoms of the carboxyl group and o -hydroxyl groups; the Н∙∙∙О and О∙∙∙О distances are 1.73-2.03 Å and 2.450(8)-2.484(8) Å, respectively. Structural organization in the crystals is caused by weak hydrogen bonds of the С-Н···О type between the carboxylate groups and oxygen atoms of the hydroxyl groups (in crystal 1). Short contacts between the carboxylate oxygen atoms and a hydrogen atom of the methyl group of the solvated toluene molecule are observed in complex 2.
Текст научной статьи Реакции пентафенилфосфора с 2,6-дигидроксибензойной и янтарной кислотами
В литературе описаны методы получения и особенности строения органических соединений пятиковалентного фосфора [1 - 10]. Значительно меньше изучена реакционная способность таких соединений. Например, известны реакции пентафенилфосфора со спиртами, оксидами неметаллов и кислотами, протекающие с отщеплением фенильных лигандов от атома фосфора [10 - 12]. Кроме того, описаны способы получения карбоксилатов тетрафенилфосфония взаимодействием галогенидов тетрафенилфосфония с различными кислотами [13, 14] либо с солями кислот [15, 16]. Цианоформиат тетрафенилфосфония был получен при обработке углекислым газом концентрированного раствора [Ph 4 P]CN [17]. Изучены комплексы, в состав которых кроме катионов тетрафенилфосфония входят карбоксилат-анионы, содержащие атомы переходных металлов [18– 20]. На примере реакции трифторацетата трифенилфосфония с производным хинона осуществлен синтез карбоксилата 2,5,3,6-замещенного фенил(трифенил)фосфония [21].
Следует отметить, что полифункциональные карбоновые кислоты реагируют с солями фосфония не всегда однозначно. Так, при наличии сульфогруппы в составе карбоновой кислоты ожидаемо карбоксильная группа не принимает участия в реакции [12, 22]. Однако продуктом взаимодействия бромида тетрафенилфосфония с оксалатом серебра в мольном соотношении 2:1 является гидрооксалат тетрафенилфосфония [Ph 4 P]+ [HC 2 O 4 ]-, который, по мнению авторов, образуется в результате гидролиза оксалата тетрафенилфосфония [Ph 4 P] 2 +[C 2 O 4 ]2- [16]. 2-гидроксиизофталевая кислота реагирует с бромидом тетрафенилфосфония как замещенный фенол, образуя фенолят тетрафенилфосфония [14].
В настоящей работе нами изучены реакции пентафенилфосфора с полифункциональными кислотами (2,6-дигидроксибензойной и янтарной) и установлено строение выделенных продуктов методом рентгеноструктурного анализа (РСА).
Экспериментальная часть
Синтез сольвата 2,6-дигидроксибензоата тетрафенилфосфония с бензолом [Ph 4 P]+ [OC(O)C 6 H 3 (OH) 2 -2,6] - PhH (1). Смесь 0,200 г (0,44 ммоль) сольвата пентафенилфосфо-ра с бензолом (Ph 5 P • % PhH) и 0,134 г (0,44 ммоль) 2,6-дигидроксибензойной кислоты в 5 мл бензола выдерживали в стеклянной запаянной ампуле 0,5 ч при 60 ° С, охлаждали. После вскрытия ампулы медленно концентрировали раствор до объема 1 мл. Образовавшиеся светло-желтые кристаллы фильтровали и сушили. Выход 0,198 г (85 %), т. пл. 148 °С.
ИК-спектр (ν, см-1): 3556, 3482, 3418, 1643, 1618, 1128, 789, 735, 696, 623, 473.
Синтез сольвата сукцината бис(тетрафенилфосфония) с толуолом [Ph 4 P] 2 +[O 2 CCH 2 CH 2 CO 2 ]2 - ⋅ 2TolH (2) . Смесь 0,200 г (0,44 ммоль) сольвата пентафенилфосфора с бензолом (Ph 5 P • % PhH) и 0,051 г (0,22 ммоль) янтарной кислоты в 5 мл толуола выдерживали в стеклянной ампуле 0,5 ч при 60 ° С, охлаждали. После вскрытия ампулы медленно концентрировали раствор до объема 1 мл. Образовавшиеся бесцветные кристаллы фильтровали и сушили. Выход 0,280 г (76 %), т. пл. 204 °С.
ИК-спектр (ν, см–1): 3522, 3450, 3266, 2924, 2851, 1630, 1586, 1433, 1360, 1317, 1105, 993, 762, 727, 694, 527.
ИК-спектры соединений 1 , 2 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
РСА кристаллов 1 , 2 проведен на дифрактометре D8 Quest фирмы Bruker (Mo K α-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT- Plus [23]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [24] и OLEX2 [25]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структур 1 , 2 приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 и 2
|
Параметр |
Значение |
|
|
1 |
2 |
|
|
М |
1063,07 |
489,54 |
|
Сингония |
Триклинная |
Моноклинная |
|
Пр. гр. |
P1 |
P2 1 /c |
|
a , Å |
10,945(13) |
10,636(8) |
|
b , Å |
13,681(14) |
19,849(15) |
|
c , Å |
19,68(2) |
12,410(10) |
|
α, град. |
99,82(6) |
90,00 |
|
β, град. |
105,34(4) |
94,01(4) |
|
γ, град. |
91,78(6) |
90,00 |
|
V , Å3 |
2792(5) |
2614(3) |
|
Z |
2 |
4 |
|
ρ выч , г/см3 |
1,265 |
1,244 |
|
-1 μ, мм |
0,136 |
0,134 |
|
F (000) |
1116,0 |
1036,0 |
|
Размер кристалла, мм |
0,16 × 0,12 × 0,07 |
0,46 × 0,21 × 0,21 |
|
Область сбора данных по 2θ, град. |
3,88–59,08 |
6,38 - 50,04 |
|
Интервалы индексов отражений |
-14 ≤ h ≤ 14, -18 ≤ k ≤ 18, -27 ≤ l ≤ 27 |
-12 ≤ h ≤ 12, -23 ≤ k ≤ 23, -14 ≤ l ≤ 14 |
|
Измерено отражений |
101169 |
25481 |
|
Независимых отражений |
15223 ( R int = 0,3125) |
4593 ( R int = 0,1635) |
|
Переменных уточнения |
707 |
327 |
|
GOOF |
0,933 |
0,999 |
|
R -факторы по F 2> 2σ( F 2) |
R 1 = 0,1132, wR 2 = 0,2956 |
R 1 = 0,0678, wR 2 = 0,1628 |
Окончание табл. 1
|
Параметр |
Значение |
|
|
1 |
2 |
|
|
R -факторы по всем отражениям |
R 1 = 0,2878, wR 2 = 0,4300 |
R 1 = 0,1618, wR 2 = 0,2135 |
|
Остаточная электронная плотность (min/max), e/Å3 |
0,47/-0,72 |
0,42/-0,46 |
Таблица 2
|
Связь |
d , Å |
Угол 1 |
ω, град |
|
1 |
|||
|
P(1) - C(1) |
1,809(6) |
C(21)P(1)C(1) |
106,4(3) |
|
P(1) - C(21) |
1,776(6) |
C(21)P(1)C(11) |
110,2(3) |
|
P(1) - C(11) |
1,798(6) |
C(11)P(1)C(1) |
113,5(3) |
|
P(1) - C(31) |
1,771(6) |
C(31)P(1)C(1) |
109,0(3) |
|
P(2) - C(51) |
1,787(6) |
C(31)P(1)C(21) |
111,1(3) |
|
P(2) - C(61) |
1,803(6) |
C(31)P(1)C(11) |
106,7(3) |
|
P(2) - C(41) |
1,783(5) |
C(51)P(2)C(61) |
107,7(3) |
|
P(2) - C(71) |
1,784(6) |
C(41)P(2)C(51) |
111,5(3) |
|
О(1) - C(97) |
1,244(8) |
C(41)P(2)C(61) |
108,7(3) |
|
О(2) - C(97) |
1,256(8) |
C(41)P(2)C(71) |
108,0(2) |
|
О(4) - C(92) |
1,343(8) |
C(71)P(2)C(51) |
108,5(3) |
|
О(3) - C(96) |
1,363(8) |
C(71)P(2)C(61) |
112,5(3) |
|
О(8) - C(82) |
1,351(9) |
О(1)С(97)О(2) |
124,8(7) |
|
О(6) - C(87) |
1,273(9) |
О(1)С(97)С(91) |
119,1(7) |
|
2 |
|||
|
P(1) - C(31) |
1,801(4) |
C(31)P(1)C(1) |
109,9(2) |
|
P(1) - C(11) |
1,791(4) |
C(11)P(1)C(31) |
111,5(2) |
|
P(1) - C(1) |
1,804(4) |
C(11)P(1)C(1) |
107,8(2) |
|
P(1) - C(21) |
1,795(5) |
C(11)P(1)C(21) |
110,3(2) |
|
О(1) - C(7) |
1,254(6) |
C(21)P(1)C(31) |
108,5(2) |
|
О(2) - C(7) |
1,272(5) |
C(21)P(1)C(1) |
108,8(2) |
|
C(8) - C(7) |
1,515(7) |
О(1)С(7)О(2) |
122,9(5) |
Основные длины связей ( d ) и валентные углы (ω) в структурах 1 и 2
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1849657 (1), № 1849663 (2); ; .
Обсуждение результатов
Нами установлено, что дефенилирование пентафенилфосфора 2,6-дигидроксибензойной и янтарной кислотами независимо от соотношения исходных реагентов в растворе бензола или толуола приводит к практически количественному образованию карбоксилатов тетрафенилфосфония [Ph 4 P]+ [OC(O)C 6 H 3 (OH) 2 -2,6] - ⋅ PhH ( 1 ) и [Ph 4 P] 2 + [O 2 CCH 2 CH 2 CO 2 ]2 - ⋅ TolH( 2 ):
PhH
Ph 5 P + HOС(O)C 6 H 3 (OH) 2 -2,6 → [Ph 4 P]+ [OC(O)C 6 H 3 (OH) 2 -2,6] - ⋅ PhH + PhH
TolH
2 Ph 5 P + HOC(О)CH 2 CH 2 C(О)OH → [Ph 4 P] 2 + [O 2 CCH 2 CH 2 CO 2 ]2 -⋅ 2TolH + 2 PhH
Соединения 1 и 2 представляют собой растворимые в ароматических углеводородах, тетрагидрофуране и диоксане бесцветные кристаллические вещества, выделенные из реакционной смеси с выходом 85 и 76 % соответственно.
По данным РСА, карбоксилаты тетрафенилфосфония 1 , 2 являются соединениями ионного типа, которые кристаллизуются из бензола и толуола в виде сольватов. В кристалле соединения 1 присутствуют по два типа кристаллографически независимых катионов и анионов ( а, б ).
Катионы тетрафенилфосфония имеют мало искаженную тетраэдрическую конфигурацию (рис. 1, 2). Валентные углы СРС изменяются в интервалах 106,4(3) °- 113,5(3) ° ( 1 а ), 107,7(3) °- 112,5(3) ° ( 1б ), 107,8(2) °- 111,5(2) ° ( 2 ). Расстояния Р-C равны 1,771(6) - 1,809(6) А ( 1 а ), 1,783(5) - 1,803(5) А ( 1б ), 1,791(4) - 1,804(4) А ( 2 ).
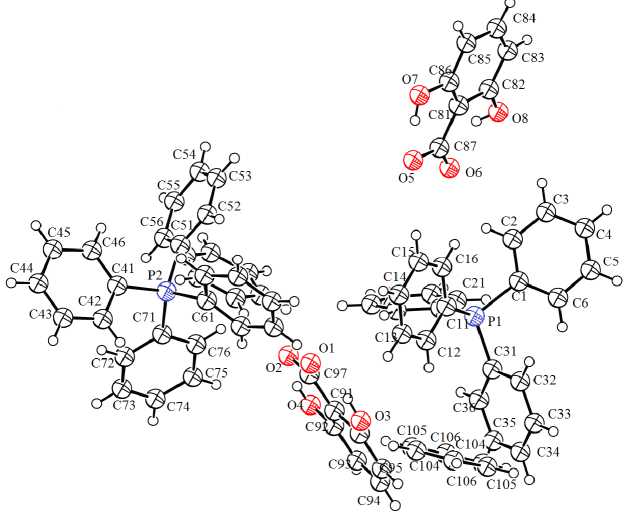
Рис. 1. Строение сольвата 2,6-дигидроксибензоата тетрафенилфосфония с бензолом [Ph 4 P]+ [OC(O)C 6 H 3 (OH) 2 -2,6] - ⋅ PhH (1)
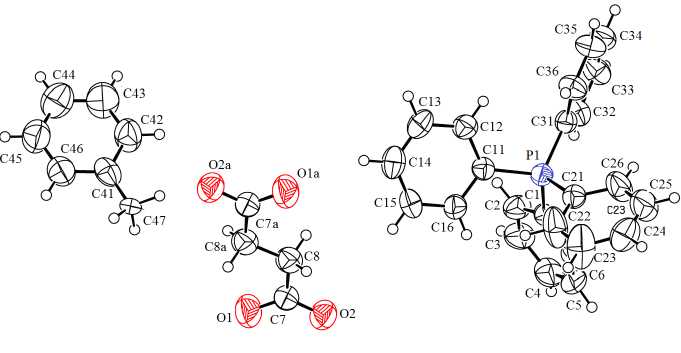
Рис. 2. Строение сольвата сукцината бис (тетрафенилфосфония) с толуолом [Ph 4 P] 2 + [O 2 CCH 2 CH 2 CO 2 ]2 - ⋅ 2 TolH (2)
В анионах 1 а, б плоскости бензольных колец и карбоксильных групп практически совпадают (углы между соответствующими плоскостями составляют 1,53° и 1,76° соответственно). Сук-цинат-дианион в кристалле 2 является центросимметричным, центр симметрии располагается на середине связи С(8)-С(8а).
В карбоксилат-анионах 1 и 2 связи С-О практически выровнены: С(87)-О(5) 1,263(9) Å, С(87)-О(6) 1,273(9) Å ( 1а ), (С(97)-О(1) 1,24(1) Å, С(97)-О(2) 1,257(9) Å ( 1б ), С(7)-О(1) 1,254(6) Å, С(7)-О(2) 1,272(5) Å ( 2 ). Валентные углы при карбоксильных атомах углерода О(1)С(97)О(2), О(5)С(87)О(6) ( 1 а, б ) и О(1)С(7)О(2) ( 2 ) равны 125,7(7)°, 124,8(7)°, 122,9(5)° соответственно.
В анионах 1 а, б ожидаемо имеют место внутримолекулярные водородные связи между атомами кислорода карбоксильной группы и орто- гидроксильными группами со следующими параметрами: Н(3)···О(1) 1,75 Å, Н(4)···О(2) 1,73 Å, Н(7)···О(5) 1,74 Å, Н(8)···О(6) 2,03 Å. Отметим, что аналогичное расстояние в остатке салициловой кислоты молекулы салицилата тетрафенил-сурьмы равно 1,82 Å [26].
Формирование кристаллических структур 1 и 2 обусловлено, в основном, слабыми водородными связями типа С-Н···О с участием карбоксилатных групп и кислорода гидроксильных групп (в кристалле соединения 1 ). Короткие (опорные) контакты в кристалле 1 представлены на проекции вдоль оси а на рис. 3. В комплексе 2 имеет место наличие короткого контакта карбоксилатных атомов кислорода с атомом водорода метильной группы сольватированной молекулы толуола (рис. 4), при этом расстояние О(2)···Н(47) составляет 1,59 Å, что меньше суммы ван-дер-ваальсовых радиусов данных атомов [27].
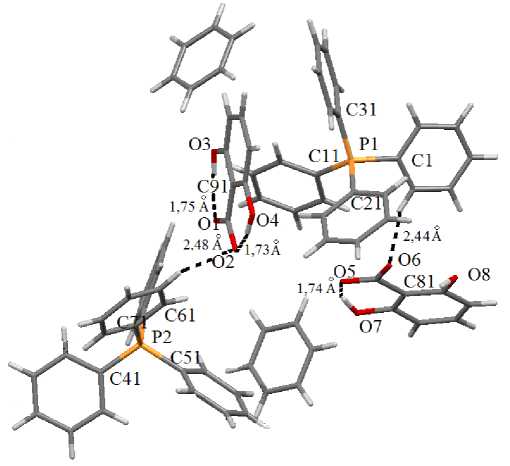
Рис. 3. Короткие (опорные) контакты в кристалле комплекса 1
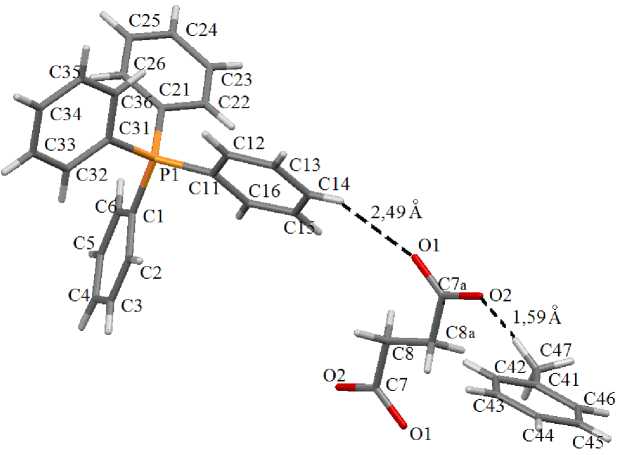
Рис. 4. Короткие (опорные) контакты в кристалле комплекса 2
Выводы
Таким образом, в реакции пентафенилфосфора с янтарной кислотой независимо от мольного соотношения реагентов участвуют обе карбоксильных группы. Гидроксигруппы 2,6-дигидроксибензойной кислоты остаются инертными даже при избытке пентафенилфосфора в реакционной среде. 2,6-Дигидроксибензоат тетрафенилфосфония [Ph 4 P]+ [OC(O)C 6 H 3 (OH) 2 -2,6] - ⋅ PhH и сукцинат бис(тетрафенилфосфония) [Ph 4 P] 2 + [O 2 CCH 2 CH 2 CO 2 ]2 - ⋅ TolH в кристаллах имеют ионное строение.
Список литературы Реакции пентафенилфосфора с 2,6-дигидроксибензойной и янтарной кислотами
- Wheatley, P.J. The Crystal and Molecular Structure of Pentaphenylphosphorus / P.J. Wheatley // J. Chem. Soc. - 1964. - P. 2206-2222.
- Carbodicarbenes: Unexpected π-Accepting Ability during Reactivity with Small Molecules / W.-Ch. Chen, W.-Ch. Shih, T. Jurca et al. // J. Am. Chem. Soc. - 2017. - V. 139. - P. 12830-12836.
- The Chemistry of Heteroarylphosphorus Compounds, Part 16. An X-Ray Structural Study of (2-Thienyl)bis(2,2′-biphenylylene)phosphorane. A Comparison with Related Methyl and Aryl bis(2,2′-biphenylylene)-spirophosphoranes / D.W. Allen, L.A. March, I.W. Nowell at al. // Z. Naturforsch. B. Chem. Sci. - 1983. - Bd. 38. - P. 465-469.
- Formation of a Dicyanotriorganophosphorane from the Reaction of Triphenylphosphane with Phenylselenocyanate / N.A. Barnes, S.M. Godfrey, R.T.A. Halton et al. // Angew. Chem. Int. Ed. - 2006. - V. 45. - P. 1272-1275.
- 5-Organyl-5-phosphaspiro[4.4]nonanes: A Contribution to the Structural Chemistry of Spirocyclic Tetraalkylphosphonium Salts and Pentaalkylphosphoranes / U. Monkowius, N.W. Mitzel, A. Schier et al. // J. Am. Chem. Soc. - 2002. - V. 124. - P. 6126-6132.
- Diphosphanylketenimines: New Reagents for the Synthesis of Unique Phosphorus Heterocycles / J. Ruiz, F. Marquínez, V. Riera et al. // Chem.-Eur. J. - 2002. - V. 8. - P. 3872-3878.
- Muller, G. Crystal and Molecular Structure of P(C6H5)5∙0.5 THF / G. Muller, U. J. Bildmann // Z. Naturforsch. B. Chem. Sci. - 2004. - Bd. 59, № 11-12. - P. 1411-1414.
- Day, R.O. Molecular Structure of the Methyl and Phenyl Derivatives of Bis (2,2'-biphenylylene)phosphorane / R.O. Day, S. Husebye, R.R. Holmes // Inorg. Chem. - 1980. - V. 19. - P. 3616-3622.
- A Facile Access to lλ5,3λ5-Benzodiphospholes / H.J. Bestmann, H.P. Oechsner, C. Egerer-Sieber et al. // Angew. Chem. Int. Ed. - 1995. - V. 34. - P. 2017-2020.
- Термолиз пентафенилфосфорана в присутствии диоксида углерода / В.В. Шарутин, В.Т. Бычков, В.А. Лебедев и др. // Журн. общ. химии. - 1986. - Т. 56, № 2. - С. 325-328.
- Alkyloxy- and Silyloxy-Derivatives of PV and SbV / G.A. Razuvaev, N.A. Osanova, T.G. Brilkina et al. // J. Organometal. Chem. - 1975. - V. 99, № 1. - P. 93-106.
- Карбоксилаты и сульфонаты тетрафенилфосфора. Синтез и строение / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина, Е.А. Бояркина // Журнал общей химии. - 2009. - Т. 79. - С. 80-89.
- Tetraphenylphosphonium 2,4,5-Tricarboxybenzoate / G.-D. Yang, J.-C. Dai, W.-S. Wu et al. // Acta Crystallogr. Sect. E: Struct. Rep. Online. - 2007. - V. E63. - P. o1010-o1011.
- 2-Hydroxyisophthalic Acid: Hydrogen-Bonding Patterns in the Monohydrate and the Tetraphenylphosphonium salt. An Instance of Dramatic Acidity Enhancement by Symmetric, Internally Hydrogen-Bonded Anion Stabilization / S. Bawa, M.L. Cole, P. Dubois et al. // Acta Crystallogr., Sect. B: Struct. Sci. - 2004. - V. 60. - P. 438-446.
- Synthesis and Structures of Perthio- and Polymeric Metal Complexes With the Tetrathio- and Dithioterephthalate Ligands / A.R. Paital, J. Zhan, R. Kim et al. // Polyhedron. - 2013. - V. 64. - P. 328-338.
- Tetraphenylphosphonium Hydrogen Oxalate / P.A.W. Dean, D.C. Craig, M.L. Scudder et al. // Acta Crystallogr., Sect. E: Struct. Rep. Online. - 2008. - V. 64. - P. o243.
- A Simple Complex on the Verge of Breakdown: Isolation of the Elusive Cyanoformate Ion / L.J. Murphy, K.N. Robertson, S.G. Harroun et al. // Science. - 2014. - V. 344. - P. 75-78.
- Rhenium and Molybdenum Oxo-Complexes Containing Ligands Related to N-Hydroxyiminodipropionic Acid / S.M. Harben, P.D. Smith, R.L. Beddoes et al. // J. Chem. Soc., Dalton Trans. - 1997. - № 16. - P. 2777-2784.
- Oxorhenium(V) and Oxotechnetium(V) Complexes of Cysteine / M. Chatterjee, B. Achari, S. Das et al. // Inorg.Chem. - 1998. - V. 37. - P. 5424-5430.
- Cationic Induced Assembly of Two 2D Zinc-Terephthalate Polymeric Networks / Y.-X. Lian, G.-D. Yang, Z.-Y. Fu et al. // Inorg. Chim. Acta. - 2009. - V. 362. - P. 3901-3909.
- Взаимодействие 1,4-бензохинонов с Р-Н-фосфониевыми солями / Н.Р. Хасиятуллина, А.М. Вазыхова, Ю.К. Воронина и др. // Журн. общ. химии. - 2017. - Т. 87, № 9. - P. 1451-1457.
- On a Novel Synthesis of 2-Sulfonatobenzoic Acid by Oxidation of Thiosalicylic Acid Catalyzed by Copper(II): a Structural Study / E. G. Ferrer, P. A. M. Williams, E. E. Castellano et al. // Z. Anorg. Allg. Chem. - 2002. - V. 628. - P. 1979-1984. (200209)628:9/103.0.co;2-v.
- DOI: 10.1002/1521-3749
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. - 2009. - V.42. - P. 339-341.
- Реакции пентаарилсурьмы с диацилатами триарилсурьмы / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Журн. общ. химии. - 1997. - Т. 67, вып. 9. - С. 1536-1541.
- Бацанов, С.С. Атомные радиусы элементов / С.С. Бацанов // Журн. неорган. химии. - 1991. - Т. 36, № 12. - С. 3015-3037.


