Реакции пентафенили пента(пара-толил)сурьмы с ферроцендикарбоновой кислотой
Автор: Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 3 т.15, 2023 года.
Бесплатный доступ
При взаимодействии пентафенил- и пента( пара -толил)сурьмы с ферроцендикарбоновой кислотой (мольные соотношения 1:1 и 2:1) в толуоле (20°С 24 ч) имеет место замещение водорода в одной или двух карбоксилатных группах и образование ферроценкарбоксилатов тетраарилсурьмы HOOCС5H4FeС5H4C(O)OSbPh4 (1), HOOCС5H4FeС5H4C(O)OSbTol4 (2), Ph4SbC(O)OС5H4FeС5H4C(O)OSbPh4 (3) и p -Tol4SbC(O)OС5H4FeС5H4C(O)OSbTol4 (4) с выходом до 83 %. Соединения 1-4 идентифицированы элементным анализом, методом ИК-спектроскопии и рентгеноструктурным анализом для 4. РСА комплекса 4 проводили на автоматическом четырехкружном дифрактометре D8 Quest Bruker (Мо К α -излучение, λ = 0,71073 Å, графитовый монохроматор) при 293 К. Кристаллографические характеристики 4: моноклинная сингония, пространственная группа P21/ c , a = 17,227(17), b = 11,064(9), c = 30,59(3) Å, β = 100,00(4) град., V = 5742(9) Å3, Z = 4, rвыч = 1,440 г/см3, 2q 6,02-49,08 град., всего отражений 124343, независимых отражений 9436, число уточняемых параметров 684, R int = 0,1051, GOOF 1,094, R 1 = 0,0536, wR 2 = 0,1309, остаточная электронная плотность (max/min), 0,88/-1,21 e/Å3. По данным рентгеноструктурного анализа в кристалле 4 координация атомов сурьмы - искаженная октаэдрическая вследствие того, что карбоксилатный лиганд является бидентатным хелатирующим. Диагональные углы в двух октаэдрах составляют 146,4(2), 154,0(3), 171,0(2)° и 147,4(2), 154,8(2), 166,9(2)°. Расстояния Sb-О равны 2,296(5), 2,502(5) Å и 2,289(5), 2,453(5) Å, связи Sb-С существенно различаются (2,146(7)-2,166(7) и 2,123(6)-2,165(7) Å). Структурная организация кристалла обусловлена в основном взаимодействиями С-Н···p-типа.
Реакция, пентафенилсурьма, пента(пара-толил)сурьма, ферроцендикарбоновая кислота, ферроценкарбоксилат тетраарилсурьмы, строение, ик-спектроскопия, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147241848
IDR: 147241848 | УДК: 549.242+547.53.024+546.722+547.514.721 | DOI: 10.14529/chem230303
Reactions of pentaphenyland penta(para-tolyl)antimony with ferrocene dicarboxylic acid
In reactions of pentaphenyl- and penta( para -tolyl)antimony with ferrocene dicarboxylic acid (molar ratios 1:1 and 2:1) in toluene (20 °С, 24 h), hydrogen in one or two carboxylate groups is replaced with formation of tetraarylantimony ferrocene carboxylates HOOС5H4FeС5H4C(O)OSbPh4 (1), HOOС5H4FeС5H4C(O)OSbTol4 (2), Ph4SbC(O)OC5H4FeС5H4C(O)OSbPh4 (3) and p -Tol4SbC(O)OC5H4FeС5H4C(O)OSbTol4 (4), yielding up to 83 %. Compounds 1-4 have been identified by elemental analysis, IR spectroscopy, and X-ray diffraction analysis for 4. X-ray diffraction analysis of complex 4 has been performed on a D8 Quest Bruker automatic four-circle diffractometer (Mo Kα radiation, λ = 0.71073 Å, graphite monochromator ) at 293 K. Crystallographic characteristics of compound 4: monoclinic system, space group P21/ c , a = 17.227(17), b = 11.064(9), c = 30.59(3) Å, β = 100.00(4) deg., V = 5742(9) Å3, Z = 4, rcalc = 1.440 g/cm3, 2 q 6.02-49.08 deg., total reflections 124343, independent reflections 9436, number of refined parameters 684, R int = 0.1051, GOOF 1.094, R 1 = 0.0536, wR 2 = 0.1309, residual electron density (max/min) 0.88/-1.21 e/Å3. According to the X-ray diffraction analysis data, in crystal 4 coordination of the antimony atoms is distorted octahedral due to the fact that the carboxylate ligand is a bidentate chelating ligand. The diagonal angles in the two octahedra are 146.4(2), 154.0(3), 171.0(2)° and 147.4(2), 154.8(2), 166.9(2)°. The Sb-O distances are 2.296(5), 2.502(5) Å and 2.289(5), 2.453(5) Å, the Sb-C bonds are significantly different (2.146(7)-2.166(7) and 2.123(6)-2.165(7) Å). The structural organization of the crystal is mainly due to the interactions of the С-Н··· p -type.
Текст научной статьи Реакции пентафенили пента(пара-толил)сурьмы с ферроцендикарбоновой кислотой
Известно, что арильные соединения сурьмы Ar3SbX2 могут быть использованы как прекурсоры для получения производных сурьмы несимметричного строения Ar4SbX по реакции перераспределения радикалов, в которых вторым реагентом является пентаарилсурьма [1 - 7]. В основе другого эффективного получения производных сурьмы общей формулы Ar4SbX (где Х – электроотрицательный лиганд) лежат реакции пентаарилсурьмы с соединениями, содержащими подвижный атом водорода (НХ). В этом случае синтез целевого продукта происходит в одну стадию, а его выделение не является трудоемким. Таким способом, например, получен ряд карбоксилатов тетраарилсурьмы как для моно-, так и дикарбоновых кислот [8 - 23]. Однако подобные реакции с участием карбоновой кислоты, содержащей металлоорганический фрагмент, известны на единственном примере [24].
Настоящая работа посвящена исследованию реакций пентафенилсурьмы и пента( пара -толил)сурьмы с ферроцендикарбоновой кислотой.
Экспериментальная частьРеакция ферроцендикарбоновой кислоты с пентафенилсурьмой.
-
А) Раствор 250 мг (0,50 ммоль) пентафенилсурьмы и 137 мг (0,50 ммоль) ферроцендикарбоновой кислоты в 40 мл толуола перемешивали при 20 °С 24 ч, удаляли в вакууме растворитель. Остаток перекристаллизовывали из смеси спирт–октан (5:1 объемн.). Получили 285 мг (81 %) светло-коричневых кристаллов соединения HOOCС 5 H 4 FeС 5 H 4 C(O)OSbPh 4 ( 1 ) c t разл = 226 °С.
ИК-спектр ( ν , см–1): 3585, 3049, 2984, 1587, 1572, 1547, 1479, 1462, 1429, 1377, 1350, 1323, 1175, 1063, 1018, 997, 920, 837, 797, 733, 692, 555, 513, 492, 471, 453, 420. Найдено, %: С 62,36; Н 4,27. C 36 H 29 O 4 FeSb. Вычислено, %: С 62,45; Н 4,13.
Аналогично получали соединения 2 - 4 .
Светло-коричневые кристаллы HOOCС 5 H 4 FeС 5 H 4 C(O)OSbTol 4 ( 2 ) ( t пл = 185°С, 76 %).
ИК-спектр ( ν , см–1): 3586, 3010, 2920, 1593, 1560, 1518, 1491, 1479, 1385, 1354, 1310, 1190, 1057, 1015, 799, 704, 573, 490, 422. Найдено, %: С 63,30; Н 4,94. C 40 H 37 O 4 FeSb. Вычислено, %: С 63,24; Н 4,87.
Светло-коричневые кристалы Ph 4 SbC(O)OС 5 H 4 FeС 5 H 4 C(O)OSbPh 4 ( 3 ) c t разл = 188°С, 83 %. ИК-спектр ( ν , см–1): 3049, 1574, 1558, 1477, 1429, 1381, 1346, 1333, 1182, 1059, 1020, 997, 926, 876, 839, 812, 799, 733, 692, 679, 542, 503, 468, 449, 420. Найдено, %: С 63,51; Н 4,32. C 60 H 48 O 4 FeSb. Вычислено, %: С 63,60; Н 4,24.
Светло-коричневые кристаллы p -Tol 4 SbC(O)OС 5 H 4 FeС 5 H 4 C(O)OSbTol 4 ( 4 ) ( t разл = 173°С, 72 %). ИК-спектр ( ν , см–1): 3011, 2916, 2864, 1520, 1479, 1385, 1354, 1310, 1188, 1055, 1015, 799, 704, 571, 554, 482, 420. Найдено, %: С 65,47; Н 5,25. C 68 H 64 O 4 FeSb 2 . Вычислено, %: С 65,57; Н 5,14.
ИК-спектры соединений 1 - 4 записывали на ИК-спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000–400 см–1.
Элементный анализ на С, Н проведен на анализаторе Carlo-Erba 1106.
Рентгеноструктурный анализ (РСА) кристалла соединения 4 проводили на дифрактометре D8 QUEST фирмы Bruker (Mo Kα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [25]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [26], OLEX2 [27]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структуры приведены в табл. 1. Основные длины связей и валентные углы – в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов для структуры депонированы в Кембриджском банке структурных данных (№ 2235292); ; .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 4
|
Параметр |
4 |
|
Формула |
C 68 H 64 O 4 FeSb 2 |
|
М |
1244,54 |
|
Сингония |
Моноклинная |
|
Пр. группа |
P 2 1 / с |
|
a , Å |
17,227(17) |
|
b , Å |
11,064(9) |
|
c , Å |
30,59(3) |
|
α, град. |
90,00 |
|
β, град. |
100,00(4) |
|
γ, град. |
90,00 |
|
V , Å3 |
5742(9) |
|
Z |
4 |
|
ρ (выч.), г/см3 |
1,440 |
|
µ, мм–1 |
1,232 |
|
F (000) |
2528,0 |
|
Размер кристалла, мм |
0,25 × 0,21 × 0,06 |
|
Область сбора данных по 2θ, град. |
6,02–49,08 |
|
Интервалы индексов отражений |
–20 ≤ h ≤ 20, –12 ≤ k ≤ 12, –35 ≤ l ≤ 35 |
|
Измерено отражений |
124343 |
|
Независимых отражений |
9436 ( R int = 0,1051) |
Окончание табл. 1
|
Параметр |
4 |
|
Переменных уточнения |
684 |
|
GOOF |
1,094 |
|
R -факторы по I>2σ(I) |
R 1 = 0,0536, wR 2 = 0,1309 |
|
R -факторы по всем отражениям |
R 1 = 0,0669, wR 2 = 0,1381 |
|
Остаточная электронная плотность (max/min), e/Å3 |
0,88/–1,21 |
Таблица 2
Основные длины связей ( d) и валентные углы ( го ) в структуре 4
|
Связь |
d, Å |
Угол |
го , град |
|
Sb(1)–O(1) |
2,296(5) |
C(11)Sb(1)C(1) |
154,0(3) |
|
Sb(1)–O(2) |
2,502(5) |
C(21)Sb(1)O(2) |
146,4(2) |
|
Sb(1)–C(11) |
2,148(7) |
C(21)Sb(1)C(11) |
102,3(3) |
|
Sb(1)–С(21) |
2,146(7) |
C(31)Sb(1)O(1) |
171,6(2) |
|
Sb(1)–C(31) |
2,160(7) |
C(31)Sb(1)O(2) |
117,0(2) |
|
Sb(1)–C(1) |
2,166(7) |
C(21)Sb(1)C(1) |
100,8(3) |
|
Sb(2)–O(3) |
2,289(5) |
C(41)Sb(2)C(61) |
154,8(2) |
|
Sb(2)–O(4) |
2,453(5) |
C(71)Sb(2)O(3) |
166,9(2) |
|
Sb(2)–C(41) |
2,161(7) |
C(71)Sb(2)O(4) |
111,7(2) |
|
Sb(2)–С(61) |
2,161(7) |
C(51)Sb(2)O(4) |
147,4(2) |
|
Sb(2)–C(71) |
2,165(7) |
C(51)Sb(2)C(41) |
102,6(3) |
|
Sb(2)–C(51) |
2,123(6) |
C(51)Sb(2)C(71) |
100,9(2) |
Обсуждение результатов
Известно, что эффективным способом получения ониевых соединений сурьмы Ar 4 SbX является метод, основанный на реакции деарилирования пентаарилсурьмы кислотами [8 - 23]. В случае, например, реакции пентаарилсурьмы с карбоновой кислотой единственным продуктом реакции являлся карбоксилат тетраарилсурьмы, выделяемый из реакционной смеси с выходом до 98 % [1]. Карбоксилаты тетраарилсурьмы привлекают внимание из-за своей биологической активности [28 - 30] и строения, поскольку для них известны три типа координации карбоксилатного лиганда на атом сурьмы: монодентатный, когда лиганд образует только одну связь Sb - O [22], анизобидентатный в случае внутримолекулярной координации карбонильного атома кислорода при условии, что расстояние Sb···O существенно меньше суммы ван-дер-ваальсовых радиусов атомов [5, 30, 31] и бидентатный с практически двумя равными расстояниями Sb - O [29, 32, 33]. Установлено, что способ координации зависит от заместителей как в органическом радикале кислоты, так и в арильном лиганде при атоме сурьмы. Однако карбоксилаты тетраарилсурьмы, содержащие металлоорганический фрагмент в карбоксилатном остатке, практически не изучены [24, 29], поэтому в качестве исходного реагента в реакциях деарилирования пентаарилсурьмы была выбрана ферроцендикарбоновая кислота.
Найдено, что эквимолярные количества пентаарилсурьмы и ферроцендикарбоновой кислоты в растворе толуола (24 ° С, 24 ч) реагируют с образованием кислого ферроценкарбоксилата тетраа-рилсурьмы ( 1 , 2 ) с выходом до 81 %.
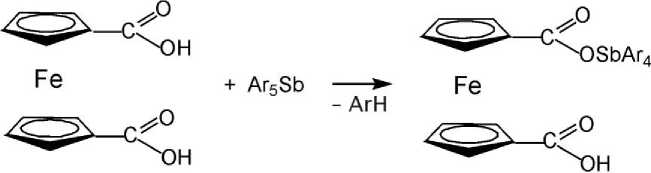
Ar = Ph (1), p-Tol (2)
Найдено, что увеличение количества пентаарилсурьмы в указанной реакции (мольное соотношение 1:2 соответственно) приводит к образованию биядерных производных сурьмы ( 3 , 4 ) с выходом до 83 %.
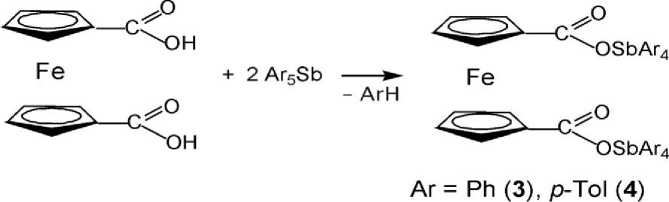
Соединения 1 - 4 , представляющие собой кристаллы светло-коричневого цвета, хорошо растворяются в ароматических углеводородах и полярных растворителях.
В ИК-спектрах соединений 1 - 4 в области 3049 - 3011 см-1 наблюдаются слабые полосы поглощения, отвечающие валентным колебаниям связей С - Н, а также полосы при 1479 - 1475 ( v as(C - C Ср-кольца)), 1120 - 1015 ( 8 as Ср-кольца), 505 - 482 v as(Fe - СрK o Л ьц O), что свидетельствует о наличии ферроценовой структуры в составе соединений [34, 35]. Полоса при 420 см–1 соответствует колебаниям связей Sb - C. Полосы при 571 - 542 см-1 отвечают колебаниям связей Sb - О в хелатном цикле. В спектрах соединений 1 - 4 в области 1574 - 1379 см-1 наблюдаются две полосы, характерные для карбонильных групп, относящиеся к асимметричным и симметричным колебаниям двух примерно равноценных связей C - O, что свидетельствует о бидентатном характере связывания карбоксилатного лиганда с атомом сурьмы [36]. Отметим, что положение перечисленных полос изменяется по сравнению с ИК-спектром чистой ферроцендикарбоновой кислоты, в котором наблюдаются полосы при 1680 и 1302 см–1, характеризующие колебания связей С=О и С - ОН в карбоксильной группе.
В целом молекула 4 представляет собой сочетание ферроценового фрагмента с обычной сэн-двичевой структурой [37], карбоксильной и тетра-( пара -толил)стибониевой групп. По данным РСА, в молекуле 4 атом сурьмы гексакоординирован за счет дополнительного взаимодействия Sb···O=C (рис. 1).
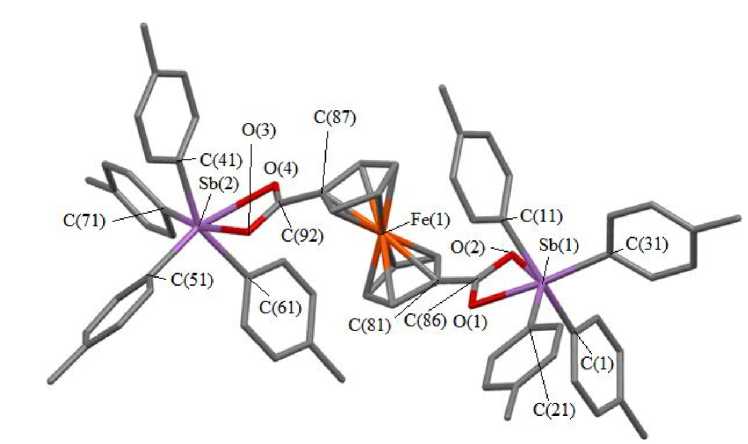
Рис. 1. Строение ферроцендикарбоксилата бис [тетра( пара -толил)сурьмы] (4) (атомы водорода не показаны)
Диагональные углы ОSb(1)C, CSb(1)C и ОSb(2)C, CSb(2)C в искаженных октаэдрах составляют 146,4(2); 171,6(2); 154,0(3)° и 147,4(2); 166,9(2); 154,8(2)°. Значения других углов при атоме сурьмы колеблются в интервале 55,19(16)-117,0(2)°. Максимально отклоняются от 90° углы 0(1)Sb(1)0(2) (54,66(16)°) и О(3)Sb(2)О(4) (55,19(16)°) в четырехчленных металлоциклах [SbO2C]. Интервал изменения связей Sb-C (2,123(6)-2,166(7) А) достаточно велик, при этом меньшие значение принимают связи Sb(1)-C(21) и Sb(2)-C(51) с арильным кольцом, плоскость которого практически совпадает с плоскостью карбоксильной группы, что обеспечивает минимальные стерические затруднения. Расстояния Sb(1)-0(2), Sb(1)-0(1) (2,296(5) и 2,502(5) А) и Sb(2)-O(3), Sb(2)-O(4) (2,289(5) и 2,453(5) А) различаются, как и в молекуле ферроценкарбокси-лата тетра(пара-толил)сурьмы (2,313(5) и 2,475(6) Å) [38], в отличие от молекулы ферроценкар-боксилата тетрафенилсурьмы [29], где координация карбоксилатного лиганда симметрична. Расстояния О(1)-С(86) (1,261(8) А), О(2)-С(86) (1,264(8) А), О(3)-С(92) (1,243(8) А), О(4)-С(92) (1,243(8) Å) примерно одинаковы и не соответствуют интервалу изменения длины ординарных связей С-О в карбоксильных группах монокарбоновых кислот (1,293-1,308 А [39]), но больше, чем указано в литературе для двойной связи (1,214-1,229 А), что свидетельствует о наличии дополнительного взаимодействия Sb···O. Атомы сурьмы Sb(1) и Sb(2) выходят из плоскости карбоксильной группы на 0,081 и 0,060 Å соответственно, плоскости металло-циклов [SbO2C] и цик-лопентадиенильных фрагментов практически совпадают (двугранный угол между ними составляет 4,47 и 4,35°). Среднее значение длин связей Fe-C равно 2,043(8) А, что близко к найденным значениям в других замещенных ферроцена [29, 33, 40, 41]. Циклы фрагмента CpFeCp’ почти параллельны друг другу, двугранный угол между плоскостями Cp и Cp’ равен 1,79°. Ферроцен может существовать как в заслонѐнной D5h (eclipsed), так и в заторможенной D5d (staggered) конформациях, которые различаются лишь углом поворота углеродных колец вокруг центральной оси молекулы [42]. В молекуле 4 конформация сэндвичей близка к заслоненной, которая чаще всего наблюдается в производных ферроцена и, как доказали авторы [43], характеризуется настоящим энергетическим минимумом, в то время как заторможенная конформация - лишь седлообразной точкой. Отметим, что структуры с симметрией D5h характерны для производных катиона ферри-цения [44] и, в общем случае, для ферроценильных лигандов, «отдавших» часть своей п-электронной плотности на ближайший акцепторный центр, в результате чего наблюдается значительное упрочение связи между ними, как, например, в диферроценилтитаноцене [45]. Структурная организация кристалла формируется в основном за счет межмолекулярных контактов С-Н • •п-типа (рис. 2).
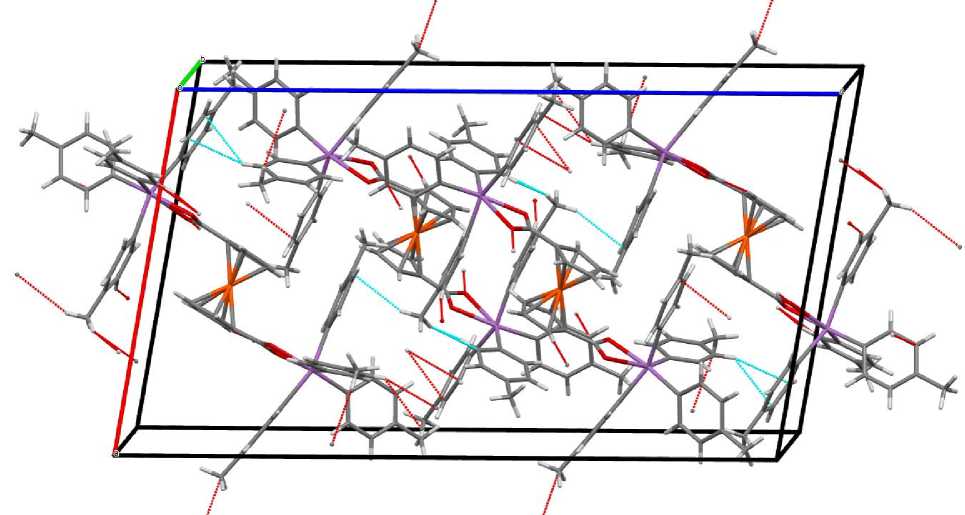
Рис. 2. Структурная организация кристалла 4 (проекция вдоль оси b )
Выводы
Таким образом, реакции пентафенилсурьмы и пента( пара -толил)сурьмы с ферроцендикарбоновой кислотой, в зависимости от мольного соотношения реагентов, приводит к образованию ферроценкарбоксилатов тетраарилсурьмы HOOCС 5 H 4 FeС 5 H 4 C(O)OSbPh 4 ( 1 ), HOOCС 5 H 4 FeС 5 H 4 C(O)OSbTol 4 ( 2 ), Ph 4 SbC(O)OС 5 H 4 FeС 5 H 4 C(O)OSbPh 4 ( 3 ), p -Tol 4 SbC(O)OС 5 H 4 FeС 5 H 4 C(O)OSbTol 4 ( 4 ) с выходом до 83 %. Соединения 1 - 4 идентифицированы элементным анализом, методом ИК-спектроскопии и рентгеноструктурным анализом для 4 . По данным РСА в кристалле 4 атомы сурьмы имеют искаженную октаэдрическую координацию из-за бидентатных свойств карбоксилатных лигандов.
Список литературы Реакции пентафенили пента(пара-толил)сурьмы с ферроцендикарбоновой кислотой
- Шарутин В.В., Поддельский А.И., Шарутина О.К. // Коорд. химия. 2020. Т. 46, № 10. С. 579. DOI: 10.31857/S0132344X20100011.
- Шарутин В.В., Сенчурин В.С., Шарутина О.К. и др. // Журн. общ. химии. 1996. Т. 66, № 10. С. 1755.
- Шарутин В.В., Шарутина О.К., Панова Л.П., Бельский В.К. // Коорд. химия. 1997. Т. 23, № 7. С. 513.
- Шарутин В.В., Шарутина О.К., Пакусина А.П., Бельский В.К. // Журн. общ. химии. 1997. Т. 67, № 9. С. 1536.
- Шарутин В.В., Сенчурин В.С., Шарутина О.К. и др. // Журн. общ. химии. 2009. Т. 79, № 10. С. 1636.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н., Артемьева Е.В. Журн. неорган. химии 2020. Т. 65, № 4. С. 482. DOI: 10.31857/S0044457X20040170.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. неорган. химии. 2013. Т.58, № 11. С. 1454.
- Губанова Ю.О., Шарутин В.В., Шарутина О.К., Петрова К.Ю. // Журн. общ. химии. 2020. Т. 90, № 9. С. 1407. DOI: 10.31857/S0044460X20090127.
- Шарутин В.В., Шарутина О.К., Хныкина К.А. // Журн. неорган. химии. 2016. Т. 61, № 2. С. 192.
- Шарутин В.В., Шарутина О.К., Котляров А.Р. // Журн. неорган. химии. 2015. Т. 60, № 4. С. 525.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. неорган. химии. 2014. Т. 59, № 9. С. 1182.
- Шарутин В.В., Шарутина О.К., Мельникова И.Г. и др. // Изв. Акад. наук. Сер. хим. 1996. № 8. С. 2082.
- Шарутин В.В., Сенчурин В.С., Шарутина О.К. // Журн. неорган. химии 2014. Т. 59. С. 247.
- Шарутин В.В., Шарутина О.К. // Коорд. химия 2014. Т. 40. № 9. С. 559. DOI: 10.1134/S1070328414090073.
- Sharutin V.V., Sharutina O.K, Gubanova Yu.O. // Bulletin of the South Ural State University. Ser. Chemistry. 2015. V. 7, No 4. P. 17. DOI: 10.14529/chem150403.
- Шарутин В.В., Шарутина О.К. // Журн. неорган. Химии. 2015. Т. 60, № 3. С. 340. DOI: 10.7868/S0044457X15030174.
- Sharutin V.V., Sharutina O.K., Gubanova Y.O. et al. // J. Organomet. Chem. 2015. V. 798. P. 41. DOI: 10.1016/j.jorganchem.2015.09.002.
- Sharutin V.V., Sharutina O.K., Senchurin V.S. // Russ. J. Coord. Chem. 2014. V. 40, No. 2. P. 109. DOI: 10.1134/S1070328414020109.
- Sharutin V.V., Sharutina O.K., Gubanova Y.O. et al. // Mendeleev Commun. 2018. V. 28. P. 621. DOI: 10.1016/j.mencom.2018.11.019.
- Шарутин В.В., Шарутина О.К., Губанова Ю.О. // Вестник ЮУрГУ. Серия «Химия». 2017. Т. 9, № 4. С. 56. DOI: 10.14529/chem170409.
- Sharutin V.V., Sharutina O.K., Gubanova Y.O., Eltsov O.S. // Inorg. Chim. Acta. 2019. V. 494. P. 211. DOI: 10.1016/j.ica.2019.05.029.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. // Журн. неорган. химии. 2022. Т. 67. № 3. С. 1151. DOI: 10.31857/S0044457X22080244.
- Шарутин В.В. // Вестник ЮУрГУ. Серия «Химия». 2023. Т. 15. № 2. С. 156. DOI: 10.14529/chem230215.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Display-ing Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726.
- Li J.-S., Ma Y.-Q., Cui J.-R. et al. // Appl. Organomet. Chem. 2001. V. 15, No. 7. P. 639. DOI: doi.org/10.1002/aoc.200.
- Liu R.-C., Ma Y.-Q., Yu L. et al. // Appl. Organomet. Chem. 2003. V. 17, No. 9. P. 662. DOI: 10.1002/aoc.491.
- Ma Y., Li J., Xuan Z. et al. // J. Organomet. Chem. 2001. V. 620, No. 1–2. P. 235. DOI: 10.1016/S0022-328X(00)00799-3.
- Quan L., Yin H.-D., Cui J.-C. et al. // J. Organomet. Chem. 2009. V. 694, No. 23. P. 3708. DOI: 10.1016/j.jorganchem.2009.07.040.
- Bone S.P., Sowerby D.B. // Phosphorus, Sulfur Silicon, Relat. Elem. 1989. V. 45, No. 1–2. P. 23. DOI: 10.1080/10426508908046072.
- Li J.-S., Liu R.-C., Chi X.-B. et al. // Inorg. Chim. Acta. 2004. V. 357, No. 7. P. 2176. DOI: 10.1016/j.ica.2003.12.012.
- Накамото К. ИК-спектры и спектры КР неорганических и координационных соединений. М.: Мир, 1991. 536 с.
- Lippincott E.R., Nelson R.D. // J. Amer. Chem. Soc. 1955. V. 77, No. 19. P. 4990. DOI: 10.1021/ja01624a012.
- Смит А. Прикладная ИК-спектроскопия / пер. с англ. к.х.н. Б.Н. Тарасевича. М.: Мир, 2001. 327 с.
- Takusagawa F.A., Koetzle T.F. // Acta Crystallogr. Sec. B. 1979. V. 35. No, 5. P. 1074. DOI: 10.1107/S0567740879005604.
- Шарутина О.К. // Вестник ЮУрГУ. Серия «Химия». 2021. Т. 13, № 4. С. 63. DOI: 10.14529/chem210404
- Orpen А.G., Brammer G., Allen F.H. et al. // J. Chem. Soc., Dalton Trans. 1989. P. S1. DOI: 10.1039/DT98900000S1.
- Васильев А.Д., Фабинский П.В., Сергеев Е.Е. и др. // Журн. структ. химии. 2011. Т. 52, № 5. С. 968.
- Васильев А.Д., Баюков О.А., Кондрасенко А.А. и др. // Журн. структ. химии. 2010. Т. 51, № 1. С. 120.
- Paliwoda D., Kowalska K., Hanfland M. et al. // J. Phys. Chem. Lett. 2013. V. 4, No. 23. P. 4032. DOI: 10.1021/jz402254b.
- Mohammadi N., Ganesan A., Chantler C.T. et al. // J. Organometal. Chem. 2012. V. 713, No. 15. P. 51. DOI: 10.1016/j.jorganchem.2012.04.009.
- Mammano N.J., Zalkin A., Landers A., Rheingold L. // Inorg. Chem. 1977. V. 16, No. 2. P. 297. DOI: 10.1021/ic50168a014.
- Zakharov L.N., Struchkov Yu.T., Sharutin V.V., Suvorova O.N. // Cryst. Struct. Comm. 1979. V. 8. P. 439.


