Реакции пентафенили пента(пара-толил)сурьмы с фумаровой кислотой
Автор: Шарутин Владимир Викторович, Семенова Арина Дмитриевна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.15, 2023 года.
Бесплатный доступ
Взаимодействием пентафенилсурьмы с фумаровой кислотой в бензоле (24 ч, 24 °С, мольное соотношение 4:3) получен сольват с бензолом Ph4SbOC(O)CH=CHC(O)OSbPh4 ∙ 2Ph4SbOC(O)CH=CHC(O)H ∙ 3PhH (1). При молярном соотношении исходных реагентов 2:1 имеет место образование биядерного производного фумаровой кислоты Ph4SbOC(O)CH=CHC(O)OSbPh4 (2). В аналогичных реакциях пента( пара -толил)сурьмы с фумаровой кислотой образуются аддукт p -Tol4SbOC(O)CH=СHC(O)OSbTol4 ∙ НOC(O)CH=CHC(O)OH ∙ 4PhH (3) и сольват биядерного производного фумаровой кислоты с бензолом p -Tol4SbOC(O)CH=СHC(O)OSbTol4 ∙ 3PhH (4) соответственно. По данным рентгеноструктурного анализа, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD-детектор, Мо К α-излучение, λ = 0,71073 Å, графитовый монохроматор), атомы сурьмы в кристаллах 1 [C63H53O6Sb2, M 1149,55; сингония триклинная, группа симметрии P1 ; параметры ячейки: a = 9,938(4), b = 14,999(8), c = 19,088(8) Å; a = 92,833(17), β = 102,148(16), g = 99,02(3) град.; V = 2737(2) Å3; размер кристалла 0,3 × 0,17 × 0,05 мм; интервалы индексов отражений -13 ≤ h ≤ 13, -20 ≤ k ≤ 20, -25 ≤ l ≤ 25; всего отражений 89119; независимых отражений 14039; Rint 0,0698; GOOF 1,070; R 1 = 0,0442, wR 2 = 0,0675; остаточная электронная плотность 0,47/-0,80 e/Å3], 2 [C26H21O2Sb, M 487,18; сингония моноклинная, группа симметрии С 2 /с ; параметры ячейки: a = 28,35(3), b = 10,453(15), c = 17,49(2) Å; β = 93,01(5) град.; V = 5176(12) Å3; размер кристалла 0,2 × 0,12 × 0,08 мм; интервалы индексов отражений -26 ≤ h ≤ 30, -11 ≤ k ≤ 11, -19 ≤ l ≤ 13; всего отражений 6329; независимых отражений 3283; Rint 0,1220; GOOF 1,318; R 1 = 0,1253 wR 2 = 0,3080; остаточная электронная плотность 2,09/-4,45 e/Å3], 3 [C88H86O8Sb2, M 1515,09; сингония триклинная, группа симметрии P1 ; параметры ячейки: a = 13,35(2), b = 13,50(2), c = 14,15(2) Å; a = 67,02(5), β = 62,29(6), g = 65,63(6) град.; V = 1994(5) Å3; размер кристалла 0,55 × 0,33 × 0,28 мм; интервалы индексов отражений -17 ≤ h ≤ 17, -17 ≤ k ≤ 17, -18 ≤ l ≤ 18; всего отражений 54923; независимых отражений 9183; Rint 0,0604; GOOF 1,069; R 1 = 0,0494 wR 2 = 0,1159; остаточная электронная плотность 1,83/-1,68 e/Å3], 4 [C39H38O2Sb, M 660,44; сингония триклинная, группа симметрии P1 ; параметры ячейки: a = 11,328(6), b = 12,416(7), c = 12,997(6) Å; a = 82,24(2), β = 72,87(2), g = 75,50(3) град.; V = 1687,5(15) Å3; размер кристалла 0,23 × 0,17 × 0,05 мм; интервалы индексов отражений -14 ≤ h ≤ 14, -15 ≤ k ≤ 15, -16 ≤ l ≤ 16; всего отражений 40178; независимых отражений 7469; Rint 0,2589; GOOF 1,029; R 1 = 0,0627, wR 2 = 0,1275; остаточная электронная плотность 0,95/-1,72 e/Å3], имеют искаженную тригонально-бипирамидальную координацию с атомами углерода и кислорода в аксиальных положениях (аксиальные углы составляют 173,65(10), 175,74(11)° для 1; 176,6(7)° для 2; 176,07(10)° для 3; 178,41(16)° для 4). Расстояния Sb-O составляют 2,253(2) и 2,240(2) Å для 1; 2,262(17) Å для 2; 2,302(3) Å для 3 и 2,234(4) Å для 4. Длины связей Sb-C изменяются в узком интервале значений (2,110(3)-2,176(3) Å для 1; 2,114(2)-2,18(3) Å для 2; 2,109(5)-2,188(4) Å для 3; 2,113(5)-2,184(5) Å для 4). Структурная организация в кристаллах обусловлена слабыми межмолекулярными контактами типа С=О···Н (1,83-2,71 Å для 1, 1,81-2,71 Å для 3, 2,69 Å для 4). В кристаллах 1, 3, 4 блоки двух дикарбоновых кислот связаны между собой через цепочки -С=О···НOC(O)- (1,83; 1,83; 1,81 Å соответственно). Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2217281 для 1, (№ 2214920 для 2, № 2220380 для 3, № 2217063 для 4; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Пентафенилсурьма, пента(пара-толил)сурьма, реакция, фумаровая кислота, продукты, строение сольватов карбоксилатов тетрафенил- и (пара-толил)сурьмы, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147240927
IDR: 147240927 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem230203
Reactions of pentaphenyland penta(para-tolyl)antimony with fumaric acid
The interaction of pentaphenylantimony with fumaric acid in benzene (24 h, 24 °С, molar ratio 4:3) gave a solvate with benzene Ph4SbOC(O)CH=CHC(O)OSbPh4 ∙ 2Ph4SbOC(O)CH=CHC(O)H ∙ 3PhH (1). At a molar ratio of the initial reagents of 2:1, the binuclear derivative of fumaric acid Ph4SbOC(O)CH=CHC(O)OSbPh4 (2) was formed. In similar reactions of penta( para -tolyl)antimony with fumaric acid, the adduct p-Tol4SbOC(O)CH=CHC(O)OSbTol4 ∙ HOC(O)CH=CHC(O)OH ∙ 4PhH (3) and the solvate of the binuclear derivative of fumaric acid with benzene p -Tol4SbOC(O)CH=СHC(O)OSbTol4 ∙ 3PhH (4) were formed, respectively. According to X-ray diffraction analysis performed at 293 K on a D8 Quest Bruker automatic four-circle diffractometer (two-coordinate CCD detector, Mo K α radiation, λ = 0.71073 Å, graphite monochromator), the antimony atoms in crystals 1 [C63H53O6Sb2, M 1149.55; triclinic syngony, symmetry group P-1; cell parameters: a = 9.938(4), b = 14.999(8), c = 19.088(8) Å; a = 92.833(17), β = 102.148(16), g = 99.02(3) degrees; V = 2737(2) Å3; crystal size 0.3 × 0.17 × 0.05 mm; reflection index intervals -13 ≤ h ≤ 13, -20 ≤ k ≤ 20, -25 ≤ l ≤ 25; total reflections 89119; independent reflections 14039; Rint = 0.0698; GOOF 1.070; R 1 = 0.0442, wR 2 = 0.0675; residual electron density 0.47/-0.80 e/Å3], 2 [C26H21O2Sb, M 487.18; monoclinic syngony, symmetry group С 2/ с ; cell parameters: a = 28.35(3), b = 10.453(15), c = 17.49(2) Å; β = 93.01(5) degrees; V = 5176(12) Å3; crystal size 0.2×0.12×0.08 mm; reflection index intervals -26 ≤ h ≤ 30, -11 ≤ k ≤ 11, -19 ≤ l ≤ 13; total reflections 6329; independent reflections 3283; R int = 0.1220; GOOF 1.318; R 1 = 0.1253 wR 2 = 0.3080; residual electron density 2.09-4.45 e/Å3], 3 [C88H86O8Sb2, M 1515.09; triclinic syngony, symmetry group P-1; cell parameters: a = 13.35(2), b = 13.50(2), c = 14.15(2) Å; a = 67.02(5), β = 62.29(6), g = 65.63(6) degrees; V = 1994(5) Å3; crystal size 0.55 × 0.33 × 0.28 mm; reflection index intervals -17 ≤ h ≤ 17, -17 ≤ k ≤ 17, -18 ≤ l ≤ 18; total reflections 54923; independent reflections 9183; R int = 0.0604; GOOF 1.069; R 1 = 0.0494, wR 2 = 0.1159; residual electron density 1.83-1.68 e/Å3], 4 [C39H38O2Sb, M 660.44; triclinic syngony, symmetry group P-1; cell parameters: a = 11.328(6), b = 12.416(7), c = 12.997(6) Å; a = 82.24(2), β = 72.87(2), g = 75.50(3) degrees; V = 1687.5(15) Å3; crystal size 0.23×0.17×0.05 mm; reflection index intervals -14 ≤ h ≤ 14, -15 ≤ k ≤ 15, -16 ≤ l ≤ 16; total reflections 40178; independent reflections 7469; Rint 0.2589; GOOF 1.029; R 1 = 0.0627, wR 2 = 0.1275; residual electron density 0.95/-1.72 e/Å3], have a distorted trigonal-bipyramidal coordination with the carbon and oxygen atoms in axial positions (axial angles are 173.65(10), 175.74(11)° for 1, 176.6(7)° for 2, 176.07(10)° for 3, 178.41(16)° for 4). The Sb-O distances are 2.253(2) and 2.240(2) Å for 1, 2.262(17) Å for 2, 2.302(3) Å for 3, and 2.234(4) Å for 4. The Sb-C bond lengths vary in a narrow range of values (2.110(3)-2.176(3) Å for 1, 2.114(2)-2.18(3) Å for 2, 2.109(5)-2.188(4) Å for 3, 2.113(5)-2.184(5) Å for 4). Structural organization in crystals is due to weak intermolecular contacts of the C=O···H type (1.83-2.71 Å for 1, 1.81-2.71 Å for 3, 2.69 Å for 4). In crystals 1, 3, 4 the blocks of two dicarboxylic acids are linked to each other via the -C=O···HOC(O)-chains (1.83, 1.83, 1.81 Å, respectively). Complete tables of atomic coordinates, bond lengths, and bond angles for the structures were deposited at the Cambridge Crystallographic Data Center (no. 2217281 for 1, (no. 2214920 for 2, no. 2220380 for 3, no. 2217063 for 4; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Текст научной статьи Реакции пентафенили пента(пара-толил)сурьмы с фумаровой кислотой
Взаимодействием пентафенилсурьмы с фумаровой кислотой в бензоле (24 ч, 24 °С, мольное соотношение 4:3) получен сольват с бензолом Ph4SbOC(O)CH=CHC(O)OSbPh4 ∙ 2Ph4SbOC(O)CH=CHC(O)H ∙ 3PhH (1). При молярном соотношении исходных реагентов 2:1 имеет место образование биядерного производного фумаровой кислоты Ph4SbOC(O)CH=CHC(O)OSbPh4 (2). В аналогичных реакциях пента(пара-толил)сурьмы с фумаровой кислотой образуются аддукт p-Tol4SbOC(O)CH=СHC(O)OSbTol4 ∙ НOC(O)CH=CHC(O)OH ∙ 4PhH (3) и сольват биядерного производного фумаровой кислоты с бензолом p-Tol4SbOC(O)CH=СHC(O)OSbTol4 ∙ 3PhH (4) соответственно. По данным рентгеноструктурного анализа, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD-детектор, Мо Кα-излучение, λ = 0,71073 Å, графитовый монохроматор), атомы сурьмы в кристаллах 1 [C63H53O6Sb2, M 1149,55; сингония триклинная, группа симметрии P1; параметры ячейки: a = 9,938(4), b = 14,999(8), c = 19,088(8) А; а = 92,833(17), в = 102,148(16), у = 99,02(3) град.; V = 2737(2) Å3; размер кристалла 0,3 × 0,17 × 0,05 мм; интервалы индексов отражений –13 ≤ h ≤ 13, –20 ≤ k ≤ 20, –25 ≤ l ≤ 25; всего отражений 89119; независимых отражений 14039; Rint 0,0698; GOOF 1,070; R1 = 0,0442, wR2 = 0,0675; остаточная электронная плотность 0,47/-0,80 e/А3], 2 [C26H21O2Sb, M487,18; сингония моноклинная, группа симметрии С2/с; параметры ячейки: a = 28,35(3), b = 10,453(15), c = 17,49(2) Å; β = 93,01(5) град.; V = 5176(12) Å3; размер кристалла 0,2 × 0,12 × 0,08 мм; интервалы индексов отражений –26 ≤ h ≤ 30, –11 ≤ k ≤ 11, –19 ≤ l ≤ 13; всего отражений 6329; независимых отражений 3283; Rint 0,1220; GOOF 1,318; R1 = 0,1253 wR2 = 0,3080; остаточная электронная плотность 2,09/-4,45 e/А3], 3 [C88H86O8Sb2, M 1515,09; сингония триклинная, группа симметрии P1; параметры ячейки: a = 13,35(2), b = 13,50(2), c = 14,15(2) А; а = 67,02(5), в = 62,29(6), у = 65,63(6) град.; V = 1994(5) А3; размер кристалла 0,55 х 0,33 х 0,28 мм; интервалы индексов отражений –17 ≤ h ≤ 17, –17 ≤ k ≤ 17, –18 ≤ l ≤ 18; всего отражений 54923; независимых отражений 9183; Rint 0,0604; GOOF 1,069; R1 = 0,0494 wR2 = 0,1159; остаточная электронная плотность 1,83/-1,68 e/А3], 4 [C39H38O2Sb, M 660,44; сингония триклинная, группа симметрии P1; параметры ячейки: a = 11,328(6), b = 12,416(7), c = 12,997(6) А; а = 82,24(2), в = 72,87(2), у = 75,50(3) град.; V = 1687,5(15) А3; размер кристалла 0,23 × 0,17 × 0,05 мм; интервалы индексов отражений –14 ≤ h ≤ 14, –15 ≤ k ≤ 15, –16 ≤ l ≤ 16; всего отражений 40178; независимых отражений 7469; Rint 0,2589; GOOF 1,029; R1 = 0,0627, wR2 = 0,1275; остаточная электронная плотность 0,95/-1,72 e/А3], имеют искаженную тригонально-бипирамидальную координацию с атомами углерода и кислорода в аксиальных положениях (аксиальные углы составляют 173,65(10), 175,74(11)° для 1; 176,6(7)° для 2; 176,07(10)° для 3; 178,41(16)° для 4). Расстояния Sb-O составляют 2,253(2) и 2,240(2) Å для 1; 2,262(17) Å для 2; 2,302(3) Å для 3 и 2,234(4) Å для 4. Длины связей Sb-C изменяются в узком интервале значений (2,110(3)-2,176(3) А для 1; 2,114(2)-2,18(3) А для 2; 2,109(5)-2,188(4) А для 3; 2,113(5)-2,184(5) А для 4). Структурная организация в кристаллах обусловлена слабыми межмолекулярными контактами типа С=О···Н (1,83–2,71 Å для 1, 1,81–2,71 Å для 3, 2,69 Å для 4). В кристаллах 1, 3, 4 блоки двух дикарбоновых кислот связаны между собой через цепочки -С=О···НOC(O)- (1,83; 1,83; 1,81 Å соответственно). Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2217281 для 1, (№ 2214920 для 2, № 2220380 для 3, № 2217063 для 4; ; .
К настоящему времени известны эффективные методы синтеза фенильных производных сурьмы общей формулы Ph4SbX, среди которых следует выделить их получение из пентафенил-сурьмы и кислоты НХ [1]. Так, описаны реакции пентафенилсурьмы с сульфоновыми кислотами [2 - 4], фенолами [5, 6], карбоновыми кислотами [7 - 10], р -дикетонами [11, 12], оксимами [13, 14]. При избытке кислоты (2 моль) могут образовываться аддукты, например, Ph 4 SbOC(O)CH 3 - CH s C(O)OH или Ph4SbONO 2 - HNO s [15].
Стоит отметить, что при взаимодействии пентафенилсурьмы и кислоты НХ, как правило, происходит отщепление только одной фенильной группы от атома сурьмы. В то же время показано, что взаимодействие диоксима метилендициклопентанона-2,2’ с пентафенилсурьмой в жестких условиях (90 ° С, 5 ч) при мольном соотношении исходных реагентов 1:2 соответственно приводит к образованию макроциклического сурьмаорганического соединения - бис - ц - [(метилендициклопентанон-2,2’-диоксимато)трифенилсурьмы], в молекулах которого симметричные диоксимные радикалы чередуются со структурными блоками Ph 3 Sb [16]. При взаимодействии оксима ацетофенона с пента( пара- толил)сурьмой и оксима циклогексанона с пентафенил-сурьмой (1:1 мольн.) при нагревании реакционной смеси в течение часа на водяной бане образовывался бис (ацетофеноноксимат) три( пара -толил)сурьмы (выход 89 %) и бис (циклогексаноноксимат) трифенилсурьмы (выход 66 %). Если же реакцию проводили при комнатной температуре, то выделяли соответственно бензофеноноксимат тетра( пара -толил)сурьмы (выход 93 %) и циклогексаноноксимат тетрафенилсурьмы (выход 70 %) [17]. Неожиданный результат был получен авторами [18] в реакции пентафенилсурьмы с 3,4-дифторбензойной кислотой в бензоле, когда в качестве основного продукта была выделена бис (3,4-дифторбензоато)трифенилсурьма Ph 3 Sb[OC(O)C 6 H 3 F 2 -3,4] 2 . Весьма эффективным методом синтеза карбоксилатов тетраарилсурь-мы является их получение по реакции перераспределения радикалов из пентаарилсурьмы и дикарбоксилата триарилсурьмы [19, 20].
Взаимодействием эквимолярных количеств пентафенилсурьмы и малоновой кислоты в толуоле получен кислый малонат тетрафенилсурьмы [21]:
О сн Phbsb Jz^CH2
НООС/ ^СООН ** Ph4Sb О 'соОН
-
- РКП
В то же время реакции других двухосновных карбоновых кислот (янтарной, яблочной и винной) с двумя молями пентафенилсурьмы (толуол, 48 ч) приводят к образованию биядерных производных сурьмы с выходом до 98 % [22]:
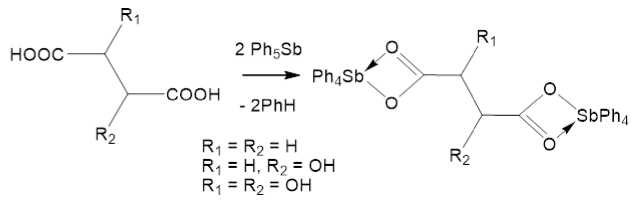
Продуктом реакции ацетилендикарбоновой кислоты с двумя молями пентафенилсурьмы (толуол, 24 ч, 23 ° С, 1:2 мольн.) является ацетилендикарбоксилат бис (тетрафенил)сурьмы [23]:
НООС
=—соон
-2PhH ph4Sb-O'
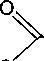
,0-SbPh

Отметим, что взаимодействие эквимолярных количеств ацетилендикарбоновой кислоты и пентафенилсурьмы сопровождалось элиминированием углекислого газа, при этом имело место образование пропиолата тетрафенилсурьмы, который синтезировали также из пентафенилсурьмы и пропиоловой кислоты [24].
Особенностью взаимодействия пентафенилсурьмы с тетрахлорфталевой кислотой является то, что даже при соотношении реагентов 1:1 продуктом реакции является биядерное соединение [25]:
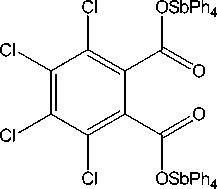
Если продуктом реакции пентафенилсурьмы с карборандикарбоновой кислотой при мольном соотношении исходных реагентов 2:1 (толуол, 24 ° С, 18 ч) является биядерное производное сурьмы (94 %), то взаимодействие эквимолярных количеств реагентов протекает с элиминированием углекислого газа и образованием монокарбоксилата тетрафенилсурьмы [26]:
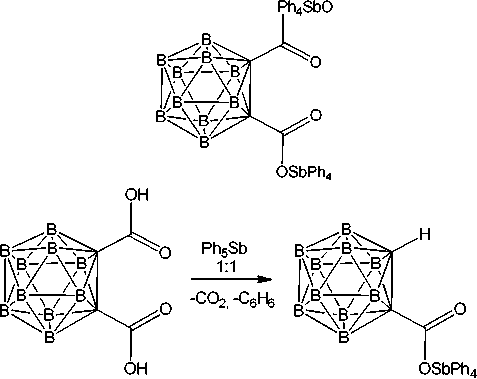
В то же время мета -карборандикарбоновая кислота реагирует в растворе бензола с пентафе-нилсурьмой независимо от соотношения исходных реагентов с образованием только биядерного дикарбоксилата [27]:
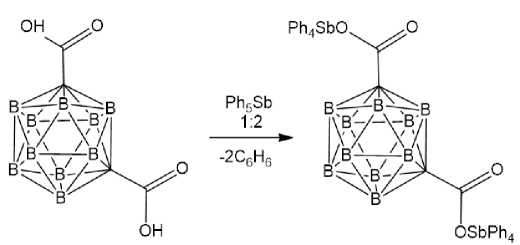
В продолжение исследования реакционной способности дикарбоновых кислот с пентафенил-и пента( пара -толил)сурьмой изучено взаимодействие последних с фумаровой кислотой в растворе бензола.
Экспериментальная часть
Реакции пентафенилсурьмы с фумаровой кислотой . Смесь 0,728 г (1,32 ммоль) пентафе-нилсурьмы и 0,116 г (0,99 ммоль) фумаровой кислоты в 15 мл бензола выдерживали при комнатной температуре 12 ч, добавляли 2 мл гептана и медленно удаляли растворитель (24 ч). Получили 0,674 г (88 %) неокрашенных кристаллов сольвата Ph 4 SbOC(O)CH=CHC(O)OSbPh 4 ∙ 2Ph 4 SbOC(O)CH=CHC(O)H • 3PhH ( 1 ) с бензолом с т. разл. 185 °С. ИК-спектр, ( v , см - 1): 3055, 3032, 1705, 1645, 1612, 1585, 1572, 1479, 1435, 1308, 1227, 1184, 1065, 1020, 997, 980, 797, 729, 691, 648, 579, 447, 420. Найдено: C 65,59; H 4,70. C 126 H 106 O 12 Sb 4 . Вычислено: C 65,77; H 4,61.
В аналогичных условиях при мольном соотношении исходных реагентов 2:1 из реакционной смеси выделяли Ph 4 SbOC(O)CH=CHC(O)OSbPh 4 ( 2 ), 90 %, т. разл. 208 °С. ИК-спектр, ( ν , см - 1): 3051, 1607, 1587, 1574, 1479, 1433, 1395, 1350, 1265, 1188, 1157, 1065, 1020, 997, 980, 800, 733, 694, 656, 571, 449, 419. Найдено: C 63,89; H 4,42. C 52 H 42 O 4 Sb 2 . Вычислено: C 64,07; H 4,31.
Реакции пента( пара -толил)сурьмы с фумаровой кислотой . Смесь 0,288 г (0,5 ммоль) пен-та( пара -толил)сурьмы и 0,058 г (0,5 ммоль) фумаровой кислоты в 15 мл бензола нагревали до образования прозрачного раствора, добавляли 2 мл гептана и выдерживали 24 ч при комнатной температуре. Получили 0,344 г (91 %) неокрашенных кристаллов аддукта p -Tol 4 SbOC(O)CH=СHC(O)OSbTol 4 ∙ НOC(O)CH=CHC(O)OH ∙ 4PhH ( 3 ), 91 %, с т. разл. 195 °С. ИК-спектр, ( ν , см - 1): 3017, 2918, 1622, 1493, 1445, 1393, 1298, 1188, 1063, 1015, 988, 951, 795, 677, 573, 482, 419. Найдено: C 69,62; H 5,73. C 88 H 86 O 8 Sb 2 . Вычислено: C 69,70; H 5,68.
В аналогичных условиях при мольном соотношении исходных реагентов 2:1 из реакционной смеси выделяли сольват p -Tol 4 SbOC(O)CH=СHC(O)OSbTol 4 ∙ 3PhH ( 4 ), 93 %, т. разл. 213 °С. ИК-спектр, ( ν , см - 1): 3015, 2957, 2920, 2862, 1622, 1491, 1445, 1393, 1298, 1211, 1188, 1063, 1015, 988, 951, 795, 677, 573, 482, 419. Найдено: C 70,67; H 5,83. C 78 H 76 O 4 Sb 2 . Вычислено: C 70,86; H 5,75.
Элементный анализ на C и H выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
ИК-спектры соединений 1–4 записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ ( РСА ) кристаллов проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор) при 293 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [28]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [29] OLEX2 [30]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника ( U изо (H) = 1,2 U экв (C)) . Кристаллографические данные и результаты уточнения структур приведены в табл. 1, геометрические характеристики координационного полиэдра атома сурьмы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 - 4
|
Параметр |
1 |
2 |
3 |
4 |
|
Формула |
C 63 H 53 O 6 Sb 2 |
C 26 H 21 O 2 Sb |
C 44 H 43 O 4 Sb |
C 39 H 38 O 2 Sb |
|
М |
1149,55 |
487,18 |
757,53 |
660,44 |
|
Сингония |
Триклинная |
Моноклинная |
Триклинная |
Триклинная |
|
Пр. группа |
P I |
С 2/ с |
P I |
PI |
|
a , Å |
9,938(4) |
28,35(3) |
13,35(2) |
11,328(6) |
|
b, Å |
14,999(8) |
10,453(15) |
13,50(2) |
12,416(7) |
|
c, Å |
19,088(8) |
17,49(2) |
14,15(2) |
12,997(6) |
|
α ,º |
92,833(17) |
90 |
67,02(5) |
82,24(2) |
|
β,º |
102,148(16) |
93,01(5) |
62,29(6) |
72,87(2) |
|
γ ,º |
99,02(3) |
90 |
65,63(6) |
75,50(3) |
|
V , Å3 |
2737(2) |
5176(12) |
1994(5) |
1687,5(15) |
|
Z |
2 |
8 |
2 |
2 |
|
ρ (выч.), г/см3 |
1,395 |
1,250 |
1,262 |
1,300 |
|
µ , мм–1 |
1,037 |
1,082 |
0,731 |
0,848 |
|
F (000) |
1162,0 |
1952,0 |
780,0 |
678,0 |
|
Размер кристалла, мм |
0,3 × 0,17 × 0,05 |
0,2 × 0,12 × 0,08 |
0,55 × 0,33 × 0,28 |
0,23 × 0,17 × 0,05 |
|
Область сбора данных по 2 θ , град. |
4,84 - 57,64 |
4,16 - 46,1 |
5,74 - 55,54 |
5,68 - 54,44 |
|
Интервалы индексов отражений |
- 13 ≤ h ≤ 13, - 20 ≤ k ≤ 20, - 25 ≤ l ≤ 25 |
- 26 ≤ h ≤ 30, - 11 ≤ k ≤ 11, - 19 ≤ l ≤ 13 |
- 17 ≤ h ≤ 17, - 17 ≤ k ≤ 17, - 18 ≤ l ≤ 18 |
- 14 ≤ h ≤ 14, - 15 ≤ k ≤ 15, - 16 ≤ l ≤ 16 |
Окончание табл. 1
|
Параметр |
1 |
2 |
3 |
4 |
|
Измерено отражений |
89119 |
6329 |
54923 |
40178 |
|
Независимых отражений |
14039 |
3283 |
9183 |
7469 |
|
R int |
0,0698 |
0,1220 |
0,0604 |
0,2589 |
|
Переменных уточнения |
643 |
262 |
447 |
383 |
|
GOOF |
1,070 |
1,318 |
1,069 |
1,029 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0442, wR 2 = 0,0675 |
R 1 = 0,1253, wR 2 = 0,3080 |
R 1 = 0,0494, wR 2 = 0,1159 |
R 1 = 0,0627, wR 2 = 0,1275 |
|
R-факторы по всем oтражениям |
R 1 = 0,0768, wR 2 = 0,0743 |
R 1 = 0,2155, wR 2 = 0,3972 |
R 1 = 0,0708, wR 2 = 0,1354 |
R 1 = 0,0998, wR 2 = 0,1439 |
|
Остаточная электронная плотность (max/min), e/A3 |
0,47/ - 0,80 |
2,09/ - 4,45 |
1,83/ - 1,68 |
0,95/ - 1,72 |
Таблица 2
Длины связей и валентные углы в соединениях 1–4
|
Связь |
d , Å |
Угол \ |
ω , град. |
|
1 |
|||
|
Sb(1) - О(1) |
2,253(2) |
O(1)Sb(1)C(1) |
173,65(10) |
|
Sb(1) - C(31) |
2,125(3) |
C(21)Sb(1)C(31) |
116,49(12) |
|
Sb(1) - C(21) |
2,110(3) |
C(21)Sb(1)C(11) |
118,47(12) |
|
Sb(1) - С(1) |
2,174(3) |
C(11)Sb(1)C(31) |
122,22(12) |
|
Sb(1) - С(11) |
2,116(3) |
C(31)Sb(1)O(1) |
79,86(10) |
|
Sb(2) - O(5) |
2,240(2) |
C(31)Sb(1)C(1) |
94,30(11) |
|
Sb(2)–С(51) |
2,120(3) |
C(21)Sb(1)O(1) |
87,49(10) |
|
Sb(2)–С(71) |
2,120(3) |
O(5)Sb(2)C(61) |
175,74(11) |
|
Sb(2)–С(41) |
2,128(3) |
C(51)Sb(2)O(5) |
85,72(11) |
|
Sb(2)–С(61) |
2,176(3) |
C(51)Sb(2)C(41) |
113,65(13) |
|
Sb(1)∙∙∙О(7) |
3,389(5) |
C(71)Sb(2)C(51) |
124,09(12) |
|
Sb(2)∙∙∙О(6) |
3,156(5) |
C(71)Sb(2)C(41) |
119,38(13) |
|
C=O(7)∙∙∙HО(3)C(O) |
1,84(10) |
O(5)Sb(2)C(41) |
83,20(11) |
|
Преобразования симметрии: 11–x, 1–y, 1–z; 22–x, 1–y, 1–z |
|||
|
2 |
|||
|
Sb(1) - О(1) |
2,262(17) |
O(1)Sb(1)C(31) |
176,6(7) |
|
Sb(1) - C(31) |
2,118(3) |
C(21)Sb(1)C(11) |
125,4(9) |
|
Sb(1) - C(21) |
2,11(2) |
C(21)Sb(1)C(1) |
117,3(8) |
|
Sb(1) - С(11) |
2,14(3) |
C(1)Sb(1)C(11) |
112,8(10) |
|
Sb(1) - С(1) |
2,14(2) |
C(1)Sb(1)O(1) |
79,3(8) |
|
Sb(1)∙∙∙О(2) |
3,196(5) |
C(37)O(1)Sb(1) |
119,0(14) |
|
Преобразования симметрии: 11–x, 1–y, 1–z |
|||
|
3 |
|||
|
Sb(1) - О(1) |
2,302(3) |
C(31)Sb(1)O(1) |
176,07(10) |
|
Sb(1) - C(31) |
2,188(4) |
C(1)Sb(1)C(21) |
118,27(16) |
|
Sb(1) - С(21) |
2,132(4) |
C(1)Sb(1)C(11) |
120,16(16) |
|
Sb(1) - С(1) |
2,109(5) |
C(21)Sb(1)C(11) |
117,74(17) |
|
Sb(1) - С(11) |
2,128(5) |
C(21)Sb(1)C(31) |
95,82(17) |
|
Sb(1)∙∙∙О(2) |
3,482(5) |
C(21)Sb(1)O(1) |
80,73(16) |
|
C=O(2)∙∙∙HО(4)C(O) |
1,81(10) |
C(1)Sb(1)C(31) |
96,79(18) |
|
C=O(3)∙∙∙H(Me)C(11-17) |
2,71(10) |
C(11)Sb(1)O(1) |
86,36(16) |
|
Преобразования симметрии: 11–x, 1–y, 1–z; 2–x,1–y, 2–z |
|||
|
4 |
|||
|
Sb(1) - О(2) |
2,234(4) |
C(31)Sb(1)O(2) |
178,41(16) |
|
Sb(1) - С(1) |
2,113(5) |
С(1)Sb(1)С(11) |
129,9(2) |
Окончание табл. 2
|
Связь |
d , Å |
Угол |
ω , град. |
|
Sb(1) - С(11) |
2,116(5) |
С(1)Sb(1)С(21) |
113,1(2) |
|
Sb(1) - С(21) |
2,117(5) |
С(11)Sb(1)С(21) |
115,3(2) |
|
Sb(1) - С(31) |
2,184(5) |
С(1)Sb(1)O(2) |
85,00(17) |
|
Sb(1)∙∙∙О(4) |
3,166(10) |
C(1)Sb(1)С(31) |
95,5(2) |
|
Преобразования симметрии: 1–x, 2–y, 1–z; 2–x, 1–y, 2–z |
|||
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2217281 для 1, № 2214920 для 2, № 2220380 для 3, № 2217063 для 4; ; .
Обсуждение результатов
Нами найдено, что продуктом реакции эквимолярных количеств пентафенилсурьмы с фумаровой кислотой в бензоле при комнатной температуре является аддукт фумарата бис (тетрафенилсурьмы) с кислым фумаратом тетрафенилсурьмы и бензолом, выделенным из реакционной смеси в виде сольвата Ph 4 SbOC(O)CH=CHC(O)OSbPh 4 ∙ 2Ph 4 SbOC(O)CH=CHC(O)OH ∙ 3PhH ( 1 ), выход которого при мольном соотношении исходных реагентов 4:3 повышался до 88 %:
PhH
4 Ph 5 Sb + 3 HOC(O)CH=CHC(O)OH
Ph 4 SbOC(O)CH=CHC(O)OSbPh 4 . 2Ph 4 SbOC(O)CH=CHC(O)OH . 3PhH
Показано, что увеличение концентрации пентафенилсурьмы в реакционной смеси (мольное соотношение реагентов 2:1) в аналогичных условиях приводит к образованию биядерного производного сурьмы Ph 4 SbOC(O)CH=CHC(O)OSbPh 4 ( 2 ) с выходом 90 %:
2 Ph 5 Sb + HOC(O)CH=CHC(O)OH Ph 4 SbOC(O)CH=CHC(O)OSbPh 4
Проведение реакции между эквимолярными количествами пента( пара -толил)сурьмы и фумаровой кислоты в аналогичных условиях был получен аддукт фумарата бис [(тетра( пара -толил)сурьмы] с фумаровой кислотой и бензолом, выделенным из реакционной смеси в виде сольвата ( p -Tol) 4 SbOC(O)CH=CHC(O)OSb( p -Tol) 4 ∙ HOC(O)CH=CHC(O)OH ∙ 4PhH ( 3 ) с выходом 91 %:
-
2 (p-Tol) 5 Sb + 2 HOC(O)CH=CHC(O)OH
(p-Tol) 4 SbOC(O)CH=CHC(O)OSb(p-Tol) 4 . HOC(O)CH=CHC(O)OH . 4PhH 3
В то же время увеличение количества пента(пара-толил)сурьмы (мольное соотношение исходных реагентов 2:1) привело к образованию биядерного производного фумаровой кислоты, которое было выделено из реакционной смеси в виде сольвата фумарата бис [(тетра( пара -толил)сурьмы] с бензолом ( p -Tol) 4 SbOC(O)CH=CHC(O)OSb( p -Tol) 4 ∙ 3PhH ( 4 ) с выходом 93 %:
2 (p-Tol)5Sb + HOC(O)CHCHC(O)OH (p-Tol) 4 SbOC(O)CHCHC(O)OSb(p-Tol) 4 . 3 PhH
Прозрачные бесцветные кристаллы 1 - 4 , устойчивые к действию влаги и кислорода воздуха, растворимы в ацетоне, ароматических углеводородах, хлороформе и диоксане.
В ИК-спектрах соединений 1–4 наблюдаются полосы поглощения средней интенсивности, относящиеся к валентным колебаниям связей Sb–C при ∼420 см–1 соответственно. Наличие карбонильной группы характеризуется присутствием полосы поглощения валентных колебаний связи С=О высокой интенсивности при 1705-1607 см–1, которые смещены в низкочастотную область спектра по сравнению с полосой поглощения карбонильной группы фумаровой кислоты (1670 см–1). Полосы поглощения, характеризующие колебания ν(С–О) в карбоксилатных лигандах, наблюдаются при 1308-1298 см–1. Полосы поглощения валентных колебаний метильных групп расположены в ИК-спектрах при ∼2950 см–1 (асимметричные колебания). ИК-спектры соединений также содержат характерные полосы валентных колебаний углеродного скелета ароматических фрагмен- тов: 1435-1184 см–1. Валентным колебаниям связей CAr–H отвечает полоса поглощения средней интенсивности при ∼3050 см–1 [31–33].
По данным РСА, в кристалле 1 на одну центросимметричную молекулу биядерного производного фумаровой кислоты (центр инверсии - середина двойной связи С=С) приходятся две молекулы кислого фумарата тетрафенилсурьмы и три молекулы сольватного бензола (рис. 1).
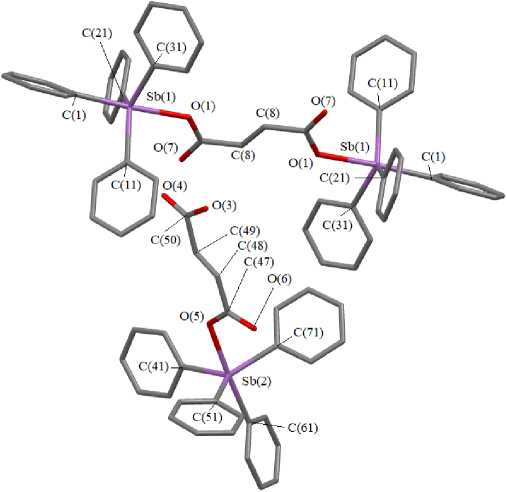
Рис. 1. Строение соединения 1
(атомы водорода и сольватные молекулы бензола не приведены)
Кристалл 2 состоит из центросимметричных молекул фумарата бис (тетрафенил)сурьмы (центр инверсии - посередине двойной связи С=С), геометрические характеристики которых весьма близки к наблюдаемым в аналогичных молекулах комплекса 1 (рис. 2).
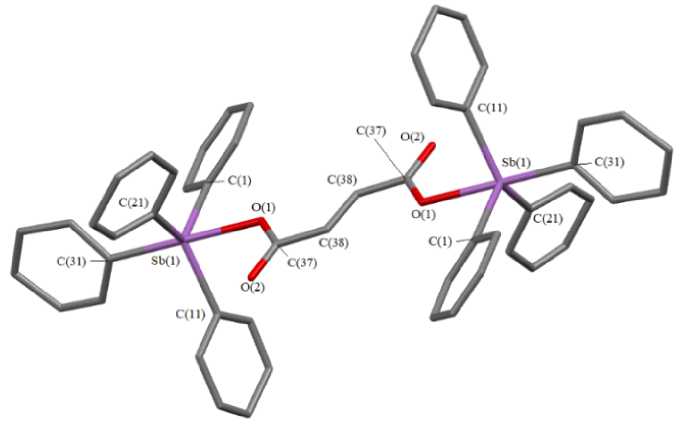
Рис. 2. Строение соединения 2 (атомы водорода не приведены)
В кристалле 3 на одну центросимметричную молекулу фумарата бис [тетра-( пар а-толил)сурьмы] приходится одна центросимметричная молекула фумаровой кислоты и четыре молекулы бензола (рис. 3).
В кристалле 4 на одну молекулу фумарата бис [тетра-( пар а-толил)сурьмы] приходится три молекулы бензола (рис. 4).
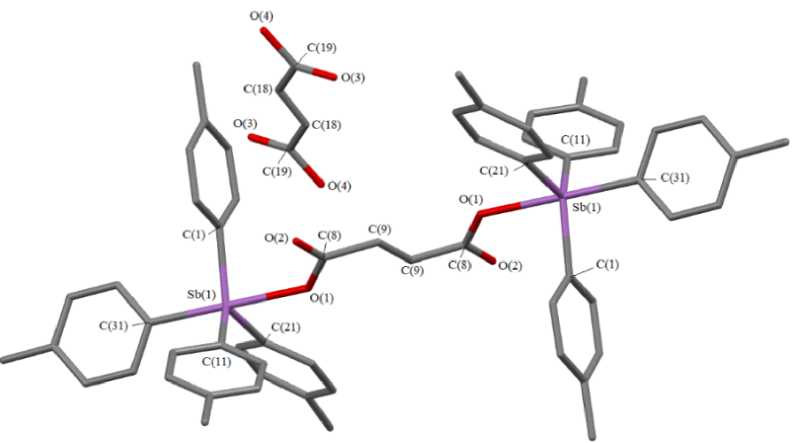
Рис. 3. Строение соединения 3
(атомы водорода и сольватные молекулы бензола не приведены)
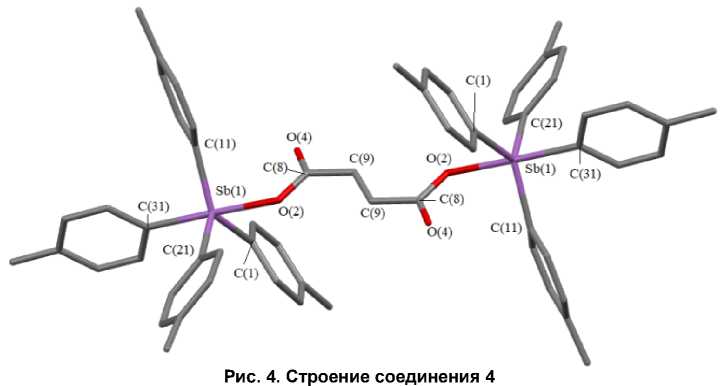
(атомы водорода и сольватные молекулы бензола не приведены)
В кристаллах 1 - 4 атомы сурьмы имеют тригонально-бипирамидальную координацию с различной степенью искажения с атомами углерода и кислорода в аксиальных положениях (аксиальные углы составляют 173,65(10), 175,74(11) ° для 1 , 176,6(7)° для 2 , 176,07(10)° для 3 , 178,41(16)° для 4 ). Расстояния Sb - O составляют 2,253(2) и 2,240(2) А для 1 , 2,262(17) А для 2 , 2,302(3) А для 3 и 2,234(4) А для 4 . Длины связей Sb - C изменяются в узком интервале значений (2,110(3) - 2,176(3) А для 1 , (2,114(2) - 2,18(3) А для 2 , 2,109(5) - 2,188(4) А для 3 , 2,113(5) - 2,184(5) А для 4 ). Структурная организация в кристаллах обусловлена слабыми межмолекулярными контактами типа С=О···Н (1,83–2,71 Å для 1 , 1,81–2,71 Å для 3 , 2,69 Å для 4 ). В кристаллах 1 , 3 , 4 блоки двух дикарбоновых кислот связаны между собой через цепочки -С=О···НOC(O)- (1,83, 1,83, 1,81 Å соответственно).
Выводы
Установлено, что взаимодействием пентафенилсурьмы с фумаровой кислотой в бензоле (24 ч, 24 °С, мольное соотношение 4:3) получен сольват с бензолом Ph4SbOC(O)CH=CHC(O)OSbPh4 • 2Ph4SbOC(O)CH=CHC(O)H ∙ 3PhH (1). При молярном соотношении исходных реагентов 2:1 имеет место образование биядерного производного фумаровой кислоты Ph4SbOC(O)CH=CHC(O)OSbPh4 (2). В аналогичных реакциях пента(пара-толил)сурьмы с фумаровой кислотой образуются аддукт p-Tol4SbOC(O)CH=СHC(O)OSbTol4 ∙ НOC(O)CH=CHC(O)OH ∙ 4PhH (3) и сольват биядерного производного фумаровой кислоты с бензолом p-Tol4SbOC(O)CH=СHC(O)OSbTol4 ∙ 3PhH (4) соответ- ственно. Строение полученных соединений охарактеризовано элементным анализом, методами ИК-спектроскопии и рентгеноструктурного анализа.
Список литературы Реакции пентафенили пента(пара-толил)сурьмы с фумаровой кислотой
- Шарутин В.В., Поддельский А.И., Шарутина О.К. Синтез, реакции и строение арильных соединений пятивалентной сурьмы // Коорд. химия. 2020. Т. 46, № 10. С. 579-648. DOI: 10.31857/S0132344X20100011.
- Сульфонаты тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, Л.П. Панова, В.К. Бельский // Журн. общ. химии. 1997. Т. 67, вып. 9. С. 1531-1535.
- Синтез и строение органосульфонатов тетра- и трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Коорд. химия. 2004. Т. 30, № 1. С. 15-24.
- Синтез и строение сурьма- и висмуторганических производных 4-сульфофенола и 2,4-дисульфофенола / В.В. Шарутин, И.В. Егорова, А.П. Пакусина, О.К. Шарутина, М.А. Пушилин // Коорд. химия. 2007. Т. 33, № 3. С. 176-183.
- Реакции пентаарилсурьмы с орто-замещенными фенолами / В.В. Шарутин, О.К. Шарутина, П.Е. Осипов, М.А. Пушилин, Д.В. Муслин, Н.С. Ляпина, В.В. Жидков, В.К. Бельский // Журн. общ. химии. 1997. Т. 67, вып. 9. С. 1528-1530.
- Арокситетраарильные соединения сурьмы. Синтез, строение и термическое разложение / В.В. Шарутин, О.К. Шарутина, П.Е. Осипов, Е.В. Воробьева, Д.В. Муслин, В.К. Бельский // Журн. общ. химии. 2000. Т. 70, № 6. С. 931-936.
- Синтез и термическое разложение производных ацилокситетрафенилсурьмы / O.K. Шарутина, B.B. Шарутин, B.C. Сенчурин, Г.К. Фукин, Л.Н. Захаров, А.И. Яновский, Ю.Т. Стручков // Изв. РАН. Сер. хим. 1996. № 1. С. 194-198.
- Reactions of Pentaphenylantimony with Dicarboxyclic Adds / V.V. Sharutin, O.K. Sharutina, A.P. Pakusina, V.K. Belsky // J. Organometal. Chem. 1997. Vol. 536, no. 1. P. 87-92.
- Синтез и строение кислого фталата тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, И.Г. Мельникова и др. // Изв. АН. Сер. хим. 1996. № 8. С. 2082-2085.
- Синтез и строение пентафторбензоата тетрафенилсурьмы и нитрата тетра-и-толилсурьмы / B.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др. // Коорд. химия. 2001. Т. 27, № 6. С. 423-427.
- Синтез р-дикетонатов тетраарилсурьмы из пентаарилсурьмы и р-дикетонов / В.В. Шарутин, О.К. Шарутина, О.П. Задачина и др. // Журн. общ. химии. 2000. Т. 70, № 5. С. 746-747.
- Синтез и строение хлорацетилацетоната тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, О.П. Задачина и др. // Журн. общ. химии. 2000. Т. 70, № 10. С. 1672-1674.
- Синтез и строение оксиматов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др. // Журн. общ. химии. 2001. Т. 71, № 8. С. 1317-1321.
- Синтез и строение оксиматов тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др. // Журн. общ. химии. 2000. Т. 70, № 12. С. 1990-1996.
- Синтез и строение аддуктов нитрата тетрафенилсурьмы с азотной кислотой и ацетата тетрафенилсурьмы с уксусной кислотой / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина, Л.П. Панова // Журн. неорган. химии. 2008. Т. 53, № 7. С. 1194-1198.
- Синтез и строение бис-ц-[(метилендициклопентанон-2,2'-диоксимато)трифенилсурьмы] / B.В. Шарутин, О.К. Шарутина, О.В. Молокова, Е.А. Алябьева // Коорд. химии. 2005. Т. 31, № 3. C.172-176.
- Синтез и строение диоксиматов триарилсурьмы / В.В. Шарутин, О.В. Молокова, О.К. Шарутина и др. // Журн. общ. химии. 2004. Т. 74, № 10. С. 1600-1607.
- Шарутин В.В., Ефремов А.Н. Трифенилсурьма и пентафенилсурьма - исходные соединения в синтезе фенильных производных пятивалентной сурьмы. Строение трифенилсурьмы, бис(3,4-дифторбензоато)трифенилсурьмы и карбоната тетрафенилсурьмы // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 2. С. 14-24. DOI: 10.14529/chem220202
- Способ получения солей тетрафенилстибония общей формулы Ph4SbX [X=Cl, Br, OC(O)Ph, SCN] / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина, А.П. Пакусина // Журн. общ. химии. 1996. Т. 66, № 10. С. 1755-1756.
- Реакции пентаарилсурьмы с диацилатами триарилсурьмы / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина, В.К. Бельский // Журн. общ. химии. 1997. Т. 67, № 9. С. 1536-1541.
- Шарутин В.В., Сенчурин В.С., Шарутина О.К. Синтез и строение кислого малоната тетрафе-нилсурьмы // Журн. неорган. химии. 2014. Т. 59. С. 247-250. DOI: 10.1134/S003602361402017X.
- Шарутин В.В., Шарутина О.К. Синтез и строение сукцината, малата и тартрата бис(тетрафенилсурьмы) // Коорд. химия 2014. Т. 40. № 9. С. 559-563. DOI: 10.1134/S1070328414090073.
- Sharutin V.V., Sharutina O.K., Gubanova Yu.O. Interaction of Pentaphenylantimony with Ace-tylenedicarboxylic Acid. Molecular Structure of Bis(tetraphenylantimony) Acetylenedicarboxilate // Bulletin of the South Ural State University. Ser. Chemistry. 2015. Vol. 7, no. 4. P. 17-22. DOI: 10.14529/chem150403.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. Синтез и строение пропиолатов три- и тет-рафенилсурьмы // Коорд. химия. 2014. Т. 40, № 2. С. 108-112. DOI: 10.1134/S1070328414020109.
- Шарутин В.В., Шарутина О.К. Синтез и строение тетрахлорфталата бис(тетрафенилсурьмы) // Журн. неорган. химии 2015. Т. 60, № 3. С. 340-342. DOI: 10.1134/S0036023615030171.
- Sharutin V.V., Sharutina O.K., Gubanova Y.O. et al. Interaction of pentaphenylantimony with carboranedicarboxylic acid // J. Organomet. Chem. 2015. Vol. 798. P. 41-45. DOI: 10.1016/j .jorganchem.2015.09.002
- Sharutin V.V., Sharutina O.K., Gubanova Y.O. et al. Synthesis and structure of ¿«(tetraphenyl-A5-stibanyl)-1,7-carborane-1,7-dicarboxylate // Mendeleev Commun. 2018. Vol. 28. P. 621-622. DOI: 10.1016/j .mencom.2018.11.019.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. 2009. Vol. 42. P. 339-341. DOI: 10.1107/S0021889808042726.
- Тарасевич Б.Н. ИК-спектры основных классов органических соединений. М.: МГУ, 2012. 54 с.
- Васильев А.В., Гриненко Е.В., Щукин А.О., Федулина Т.Г. Инфракрасная спектроскопия органических и природных соединений: учебное пособие. СПб.: СПбГЛТА, 2007. 54 с.
- Spectral Database for Organic Compounds, SDBS. Release 2021. National Institute of Advanced Industrial Science and Technology. [Электронный ресурс]. URL: https://sdbs.db.aist.go.jp (дата обращения: 25.03.2022).


